血栓弹力图参数联合INR D-D水平对脓毒血症伴DIC早期诊断的价值分析
闫冬梅, 汪 辉
(哈尔滨医科大学附属第二医院输血科, 黑龙江 哈尔滨 150086)
弥散性血管内凝血(DIC)是一种以全身凝血系统激活、纤维蛋白沉积、微血栓形成或多脏器功能障碍等为特征的凝血功能紊乱综合征,凝血异常作为脓毒血症的常见并发症之一,这种凝血系统的失调是导致DIC发生的重要诱发因素[1]。大约有35%的脓毒血症患者继发DIC,DIC的发生可引起微血管血栓、低灌注、器官功能障碍等损伤,据不完全统计[2],每年世界范围内大约有数百万的人因脓毒血症死亡,而伴有DIC的患者死亡率至少增加2倍。虽然国际血栓与止血委员会(ISTH)于2001年已经提出DIC的诊断标准,但这些标准被认为并不适用于DIC的早期发现[3]。因此寻找早期诊断DIC的特异性指标对降低患者死亡风险具有重要意义,鉴于DIC凝血特点,既往多依赖于凝血功能指标国际标准化比值(INR)、D-二聚体(D-D)等诊断,具有一定诊断价值,但整体准确性并不高[4]。血栓弹力图可通过检测少量全血反映各种组织细胞主要成分,分析它们之间的相互作用,快速、全面地评估凝血全貌,虽然目前已经证实适用于DIC的早期诊断,但具体诊断阈值尚不清楚[5]。因此本研究在常规凝血指标INR、D-D的基础上联合血栓弹力图参数,以期望早期识别脓毒血症伴DIC,改善患者预后。
1 资料与方法
1.1临床资料:选取2021年1月至2023年1月我院收治的脓毒血症患者179例作为研究对象,根据是否伴DIC分为非DIC组87例、DIC组92例,两组基础资料见表1。诊断标准:①脓毒血症诊断标准:符合Sepsis 3.0关于脓毒血症的诊断标准[6],即有明确感染,意识改变,体温>38.3℃或<36℃,心率>90次/min或高于正常值2个标准差,呼吸频率>30次/min,有持续24h以上的明显水肿或液体正平衡>20mL/kg,白细胞增多,伴或不伴多器官功能衰竭。②DIC诊断标准:符合2017年版中国专家共识[7]关于DIC的诊断,以出血、休克或微循环衰竭、微血栓栓塞为主要表现,DIC评分≥5分,并根据ISTH积分标准,将脓毒血症伴DIC患者分为显性DIC(DIC评分≥5分)、DIC前期(虽DIC评分<5分,但在未来一周内发展为显性DIC)两个分级。纳入标准:①非DIC组符合脓毒血症诊断标准,DIC组符合脓毒血症及DIC相关诊断标准;②所有研究对象均自愿参与本次研究,签署知情同意书,且获得我院伦理委员会批准。排除标准:①良恶性瘤变史;②免疫障碍性疾病史;③年龄<18岁;④精神或沟通障碍者;⑤既往血液系统病史。
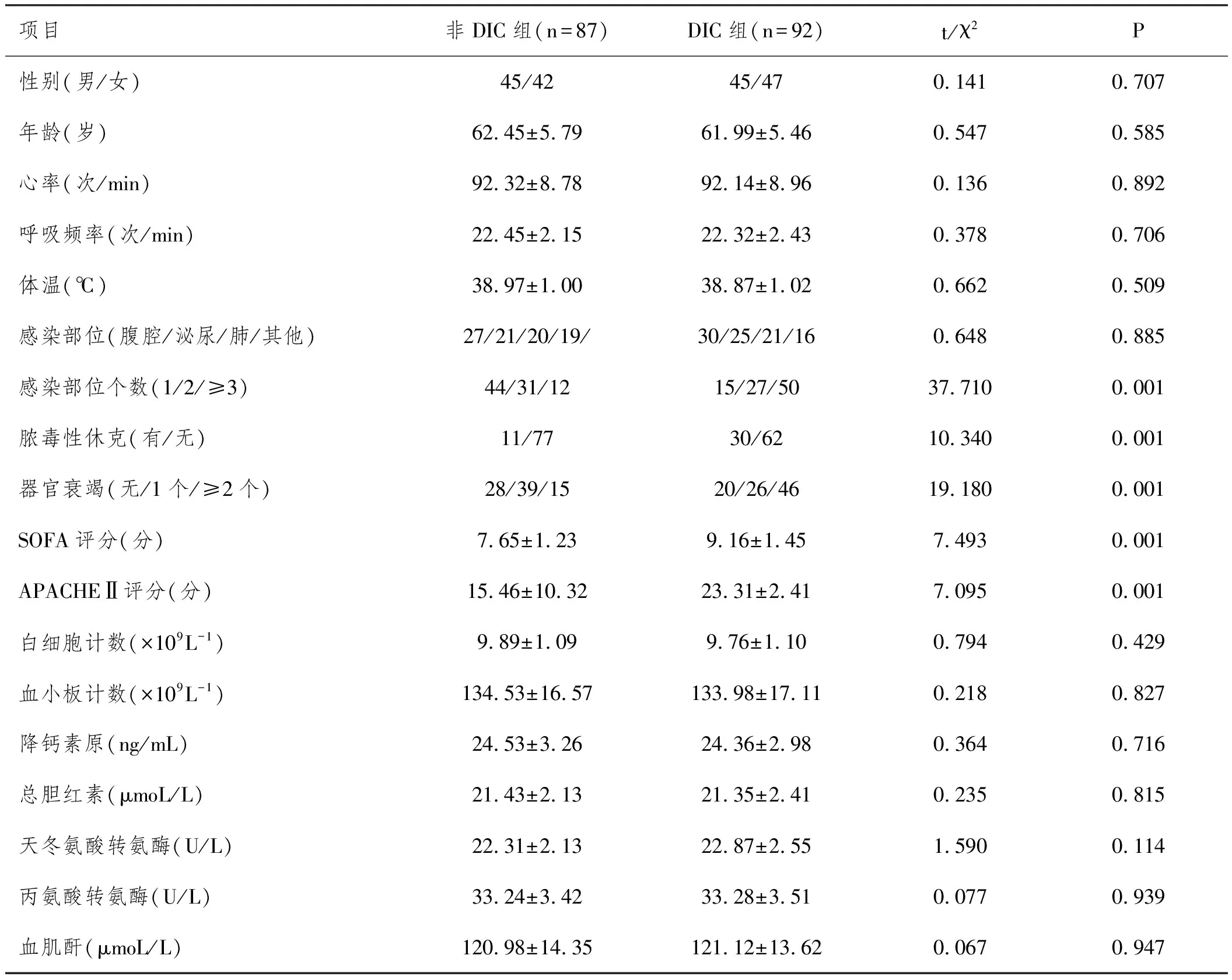
表1 两组基本资料比较
1.2方 法
1.2.1资料采集:采集非DIC组与DIC组临床资料,包括心率、呼吸频率、体温、感染部位(腹腔/泌尿/肺/其他)、感染部位个数(1/2/≥3)、脓毒性休克(有/无)、器官衰竭(无/1个/≥2个)、序贯器官衰竭评分(SOFA)、急性生理学与慢性健康状况评分Ⅱ(APACHEⅡ)评分、白细胞计数、血小板计数、降钙素原、总胆红素、天冬氨酸转氨酶、丙氨酸转氨酶、血肌酐。
1.2.2血栓弹力图参数测定:采集所有研究对象3mL静脉血,加3.2%枸橼酸钠1∶9抗凝,使用美国TEG 5000血栓弹力图仪行血栓弹力图检测,获得凝血反应时间(R值)、凝血形成时间(K值)、凝固角(α角)、最大振幅(MA值)及综合凝血指数(CI值)。①R值:开始检测样本到纤维蛋白形成时间,参考范围为5~10min;②K值:凝血开始到描记图振幅达到20mm的时间,参考范围为1~3min;③α角:参考范围为53~72度;④MA值:参考范围为50~70mm;⑤CI值:参考范围为-3~3。>3表示高凝,<-3表示低凝。
1.2.3INR、D-D检测:抽取3mL静脉血,加3.2%枸橼酸钠1∶9抗凝,离心获得血浆,使用凝血分析仪获得凝血酶时间(PT),使用免疫比浊法检测D-D水平。根据患者与正常对照PT水平计算INR,INR=(患者PT/正常对照PT)ISI参考范围为0.8~1.5,D-D参考范围为0~0.5mg/L。
1.2.4预后随访:对脓毒血症伴DIC患者行28d的预后随访,评价预后情况。
1.3指标观察:①比较非DIC组与DIC组基本资料;②比较非DIC组与DIC组血栓弹力图参数、INR、D-D水平及在不同分级、不同分期DIC组中的表达差异;③分析脓毒血症伴DIC的影响因素;④明确血栓弹力图参数与INR、D-D的相关性;⑤分析血栓弹力图参数联合INR、D-D对脓毒血症伴DIC的诊断价值;⑥根据随访结果,分析脓毒血症伴DIC预后转归情况。

2 结 果
2.1两组基本资料比较:非DIC组与DIC组在感染部位个数、有无脓毒性休克、器官衰竭、SOFA评分、APACHEⅡ评分等资料中比较,差异具有统计学意义(P<0.05);其余资料比较,差异无统计学意义(P>0.05)。见表1。
2.2两组血栓弹力图参数、INR、D-D比较:与非DIC组比较,DIC组R值[9.09±2.31(min)vs7.56±1.21(min)]、K值[5.12±0.97(min)vs3.54±0.68(min)]、INR[1.82±0.29vs1.21±0.14]、D-D[7.89±1.08(mg/L)vs3.54±0.78(mg/L)]高于非DIC组,α角[50.43±5.46(度)vs59.97±6.11(度)]、MA值[40.98±3.42(mm)vs58.65±4.98(mm)]、CI值[0.45±0.06vs2.00±0.21]低于非DIC组,差异具有统计学意义(t=5.504、12.550、17.760、30.740、11.030、27.800、67.930,P<0.05)。见图1。

图1 两组血栓弹力图参数、INR、D-D比较
2.3不同分级脓毒血症伴DIC患者血栓弹力图参数、INR、D-D比较:显性DIC患者R值[9.98±1.00(min)vs8.70±0.76(min)]、K值[5.79±0.57(min)vs4.68±0.65(min)]、INR[1.98±0.21vs1.76±0.19]、D-D[8.54±1.13(mg/L)vs7.10±0.65(mg/L)]高于DIC前期患者,α角[48.39±5.54(度)vs53.11±7.32(度)]、MA值[38.98±4.53(mm)vs42.11±5.46mm)]、CI值[0.21±0.03vs0.76±0.08]低于DIC前期患者,差异具有统计学意义(t=6.836、8.728、5.240、7.354、3.512、3.004、44.700,P<0.05)。见图2。
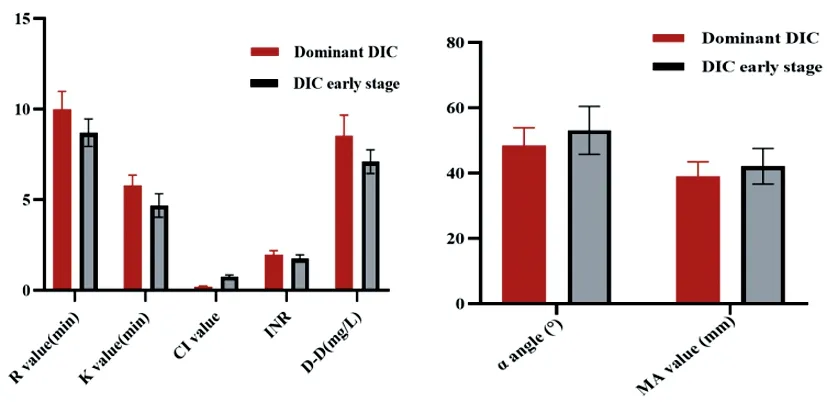
图2 不同分级脓毒血症伴DIC患者血栓弹力图参数、INR、D-D比较
2.4不同分期脓毒血症伴DIC患者血栓弹力图参数、INR、D-D比较:纤溶期患者R值[10.23±1.27(min)vs9.04±0.93(min)vs8.00±0.76(min)]、K值[6.01±0.98(min)vs5.12±0.54(min)vs4.21±0.25(min)]、INR[0.22±0.04vs0.45±0.10vs0.80±0.23]、D-D[9.32±1.09(mg/L)vs8.10±0.54(mg/L)vs6.56±0.75(mg/L)]高于低凝期、高凝期患者,α角[47.65±4.56(度)vs50.68±5.46(度)vs55.46±6.11(度)]、MA值[37.65±3.42(mm)vs42.32±5.46(mm)vs45.65±4.35(mm)]、CI值[0.22±0.04vs0.45±0.10vs0.80±0.23]低于低凝期、高凝期患者,差异具有统计学意义(F=6.341、6.830、7.683、8.678、3.414、5.679、16.335,P<0.05)。见图3。
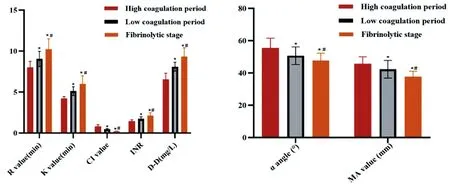
图3 不同分期脓毒血症伴DIC患者血栓弹力图参数、INR、D-D比较
2.5脓毒血症伴DIC发生的影响因素分析:以脓毒血症患者是否伴DIC作为因变量,伴DIC=1,未伴DIC=0,行Logistic回归分析,结果显示,感染部位个数、脓毒性休克、器官衰竭、SOFA评分、APACHEⅡ评分、R值、K值、α角、MA值、CI值、INR、D-D均是影响脓毒血症伴DIC发生的危险因素(P<0.05)。见表2。

表2 脓毒血症伴DIC发生的影响因素分析
2.6血栓弹力图参数与INR、D-D的相关性分析:Pearson检验显示,R值与INR、D-D正相关(r=0.453、0.476,P<0.05);K值与INR、D-D正相关(r=0.447、0.389,P<0.05);α角与INR、D-D负相关(r=-0.512、-0.553,P<0.05);MA值与INR、D-D负相关(r=-0.498、-0.589,P<0.05);CI值与INR、D-D负相关(r=-0.500、-0.476,P<0.05)。见图4。

图4 血栓弹力图参数与INR、D-D的相关性分析图
2.7血栓弹力图参数联合INR、D-D对脓毒血症伴DIC的诊断价值分析:ROC曲线分析显示,血栓弹力图参数联合INR、D-D诊断脓毒血症伴DIC的效能优于单项诊断,诊断AUC为0.943,灵敏度、特异度分别为92.30%、87.93%。见表3、图5。


图5 血栓弹力图参数联合INR、D-D对脓毒血症伴DIC的诊断价值分析
2.8脓毒血症伴DIC预后随访:对92例脓毒血症伴DIC患者行28d预后随访,结果发现,36例患者28d内死亡,死亡率为39.79%,预后死亡率较高,其余患者经临床相关措施干预,均存活,病情稳定。见图6。

图6 脓毒血症伴DIC生存曲线图
3 讨 论
炎症与凝血功能障碍是脓毒血症患者继发DIC的重要原因,由于DIC的发生涉及凝血、抗凝、纤溶、内皮细胞等多个系统,影响临床转归。INR、D-D常用于脓毒血症患者凝血功能状态的评价,其中INR是通过分析患者PT与正常血浆PT比值和所用试剂标出的ISI值获得的参数,其与凝血功能有关[6]。D-D源于纤溶酶溶解的交联纤维蛋白凝块,是凝血过程中所形成而二聚体复合物,与纤溶系统活性有关,其值升高往往提示着机体纤维蛋白血栓的产生和继发性纤溶事件的发生[8-9]。在本研究中比较发生DIC的患者与未发生DIC的患者INR、D-D变化,结果发现,与脓毒血症患者比较,伴有DIC的脓毒血症患者INR、D-D均显著升高,提示着DIC患者凝血异常,且随着疾病的进展,INR、D-D升高更显著,此结果说明,在DIC发生后持续激活纤溶系统,凝血功能障碍逐渐加剧,最终导致凝血功能指标INR、D-D水平升高。
但研究发现,INR值高低受凝血活酶试剂的影响,且D-D在肺栓塞、血栓形成等非DIC疾病中亦增高[10]。因此对脓毒血症伴DIC的诊断价值有待提高。血栓弹力图是利用血栓弹力仪经传感器对不同状态的血液样本所产生的信号进行反应,而描绘出的一种特殊图形,可客观反映凝血物质激活、纤维蛋白形成,经血块收缩、纤维蛋白交互链接至最终的血块溶解凝血全过程,用血量少,操作简便,短时间内即可获得结果,近年来随着临床上血栓弹力图检测技术的发展,逐渐广泛应用于临床。血栓弹力图参数主要包括R值、K值、α角、MA值、CI值等,其中R值提示血液样本中尚未形成纤维蛋白,其值延长多提示着凝血功能障碍。K值表示血液样本中开始形成纤维蛋白,α角是反映纤维蛋白与血小板在凝血块开始形成时的结果,与K值有关,均可反映凝块聚集速率[11]。MA值与血凝块稳定性有关,CI值可反映凝血综合指数[12]。综上认为,R值、K值升高说明患者凝血、纤维蛋白功能降低,机体处于高纤溶状态,α角、MA值、CI值降低说明血栓活性异常,机体处于低度凝血状态。本研究发现,伴有DIC的脓毒血症患者血栓弹力图参数R值、K值升高,α角、MA值、CI值降低,且显性DIC和处于纤溶期的患者R值、K值升高,α角、MA值、CI值降低更显著,从此结果可以看出,脓毒血症伴DIC患者血液黏滞度明显低于单独脓毒血症患者,推测其原因可能与脓毒血症早期血小板活化血液处于高凝状态,随着凝血因子消耗和继发纤溶系统亢进转为血液低凝状态,提示检测脓毒血症患者血栓弹力图参数可提示DIC的发生,并有效区分脓毒血症及所伴随的DIC。
本研究分析血栓弹力图参数与INR、D-D的关系,结果显示,血栓弹力图参数与INR、D-D存在一定关联,且经绘制ROC曲线发现,将血栓弹力图参数与INR、D-D联合用于脓毒血症伴DIC的诊断,诊断效能更优,此结果提示着,血栓弹力图联合INR、D-D可综合性的从血小板功能、血栓坚固性等方面予以评价,临床可通过监测脓毒血症患者血栓弹力图参数、INR、D-D水平变化对DIC发生风险早期作为诊断。另外本研究对脓毒血症伴DIC患者预后随访,结果发现,39.79%的患者在28d内死亡,死亡率较高,此结果提示着临床需尽早对脓毒血症伴DIC作为正确诊断和治疗,以改善患者预后,促进疾病转归。
综上所述,脓毒血症伴DIC患者血栓弹力图参数R值、K值升高,α角、MA值、CI值降低,INR、D-D水平升高,血栓弹力图与INR、D-D联合可准确诊断脓毒血症伴DIC,从而为临床正确诊治提供支持,降低预后死亡率。

