左室压力-应变环定量评估肥厚型心肌病患者心肺运动试验前后左室功能变化
侯淑红 林瑜芬 吴 波 孙林林 李章静 张 力 陈东平
肥厚性心肌病(hypertrophic cardiomyopathy,HCM)是最常见的遗传性心肌病,其特征是心肌细胞肥大、心室壁厚度增加,并伴有心肌纤维紊乱和间质纤维化,从而引起左室形变受损。该病起病隐匿,部分患者可长期无明显症状,临床较难发现。常规超声心动图是目前临床诊断HCM 的重要检查手段。左室整体纵向应变(GLS)较左室射血分数(LVEF)能够更敏感地检出HCM 患者早期亚临床收缩功能受损[1],且与心脏MRI评估的心肌纤维化显著相关[2]。但由于其未考虑后负荷的影响,临床应用受限。左室压力-应变环(left ventricular pressure-strain loop,LVPSL)将无创测量的动脉血压和超声心动图斑点追踪分析获得的GLS 结合起来,同时考虑了左室形变和后负荷,可无创评估心肌做功。HCM 猝死风险高,尤其是运动后,故早期发现运动后心肌功能变化,对预防不良事件发生至关重要。心肺运动试验(cardiopulmonary exercise test,CPET)是一项客观、定量、无创评估心肺功能的检查方法,在心血管疾病鉴别诊断、效果评估、运动个性化制定等方面均具有重要的临床价值。本研究应用LVPSL 定量评估HCM 患者CPET 前后左室功能变化,探讨其临床应用价值,为临床早期干预、了解适应病理相关的运动限制提供参考依据。
资料与方法
一、研究对象
选取2022 年1 月至2023 年3 月我院经超声心动图或心脏MRI 确诊的非梗阻性HCM 患者55 例,其中男40例,女15例,年龄22~66岁,平均(44.67±9.79)岁。纳入标准:符合2017 年《中国成人肥厚型心肌病诊断与治疗指南》[3]制定的HCM 诊断标准,即二维超声心动图测量室间隔或任意室壁厚度≥15 mm,或有明确家族史且左室室壁厚度≥13 mm。排除标准:①高血压、主动脉瓣狭窄和先天性主动脉瓣下隔膜等引起的左室室壁增厚;②NYHA 心功能Ⅳ级;③静息状态血压≥180/100 mm Hg(1 mm Hg=0.133 kPa),药物控制不佳;④合并急性心肌梗死;⑤不能耐受运动;⑥既往行左室流出道疏通术或室间隔酒精消融术。另选同期年龄、性别与之匹配且12导联心电图及超声心动图检查未发现异常的健康志愿者55 例作为对照组,其中男38 例,女17 例,年龄25~63 岁,平均(46.98±10.97)岁。本研究经我院医学伦理委员会批准,所有受试者均签署知情同意书。
二、仪器与方法
1.常规超声心动图检查及LVPSL 图像分析:使用GE Vivid E 95彩色多普勒超声诊断仪,M5Sc相控阵探头,频率1.4~4.6 MHz;配备EchoPAC 203 脱机图像分析工作站。先行常规超声心动图获取左室舒张末期内径(LVEDd)、左室收缩末期内径(LVEDs)、左房收缩末期内径(LAD)、舒张末期室壁厚度(MWT)、二尖瓣口舒张早期血流峰值速度与二尖瓣环舒张早期运动峰值速度比值(E/e’)、左室射血分数(LVEF);采集心尖四腔心、三腔心、两腔心切面常规超声图像,采用EchoPAC 203 软件进行分析,输入患者血压,依据主动脉瓣和二尖瓣开闭时间,判断左室等容舒张和射血期时间,勾勒心内膜及左室壁轮廓,获取GLS、纵向应变达峰时间离散度(PSD),以及左室整体心肌做功参数,包括左室心肌整体做功指数(GWI)、整体有用功(GCW)、整体无用功(GWW);如患者存在心房颤动可手动选择心率相近的图像进行LVPSL分析。
2.CPET 方法:在安静和具备完整复苏设施的房间中进行,试验由经验丰富的心脏病专家、高级护士和高级技术员监督。输入受试者性别、年龄、身高及体质量指数(BMI)。所有受试者均进行脚踏车运动,运动过程中佩戴面罩,与容量传感器相连,并通过气体采样管连续自动采集分析呼出气,连续监测患者心率、血压、12 导联心电图及血氧饱和度。由心内科专家根据受试者的年龄和运动能力选择15~30 W/min 逐步增加工作速率,以达到最大耐受。受试者以55~65 r/min的恒定速度循环,直至疲劳或症状受限。正常的血压反应定义为从静息到运动峰值时收缩压增加≥20 mm Hg。CPET 的终点:①患者出现胸痛、呼吸困难、头晕、心悸、下肢疼痛、站立不稳或感到疲劳要求终止;②出现室性心动过速、多源性室性早搏、二度或三度房室传导阻滞及窦性停搏等严重心律失常。CPET前及CPET后即刻应用LVPSL 获取GLS、PSD 及心肌做功参数,观察运动对左室功能的影响。
3.一般资料获取:包括受试者年龄、性别、BMI、体表面积、心率及血压。
三、统计学处理
结果
一、两组基线资料比较
HCM 组MWT、LAD、E/e’均较对照组增大,差异均有统计学意义(均P<0.05);两组性别、年龄、BMI、心率、体表面积、血压(收缩压和舒张压)、LVEDd、LVEDs、LVEF 比较差异均无统计学意义。见表1。
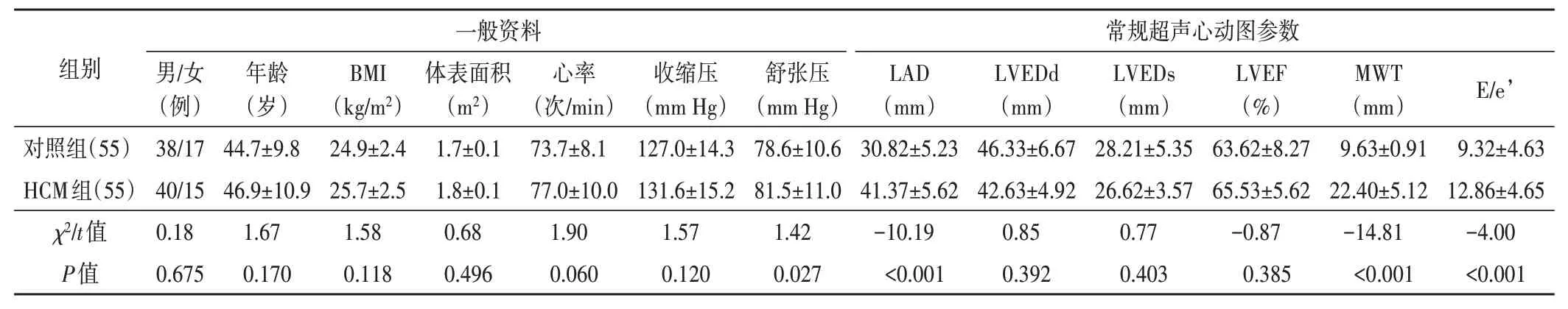
表1 两组基线资料比较
二、两组CPET 前后GLS、PSD 及左室心肌做功参数比较
CPET 前,HCM 组GLS、GCW、GWI 均较对照组减低,GWW、PSD 均较对照组增加,差异均有统计学意义(均P<0.05);CPET 后,HCM 组GLS、GCW、GWI 均较对照组减低,GWW、PSD 均较对照组增加,差异均有统计学意义(均P<0.05)。HCM 组CPET 后GLS 较CPET前减低,PSD较CPET前增加,差异有统计学意义(均P<0.05);HCM 组CPET 前后GCW、GWW、GWI 比较差异均无统计学意义。对照组CPET 后GCW、GWW、GWI 均较CPET 前增加,差异均有统计学意义(均P<0.05);CPET 前后GLS、PSD 比较差异均无统计学意义。见表2和图1,2。
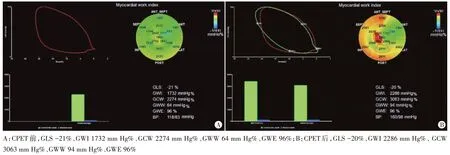
图1 对照组一健康志愿者(男,46岁)CPET前后LVPSL图

图2 HCM组一患者(男,42岁)CPET前后LVPSL图
表2 两组CPET前后GLS、PSD及左室心肌做功参数比较()
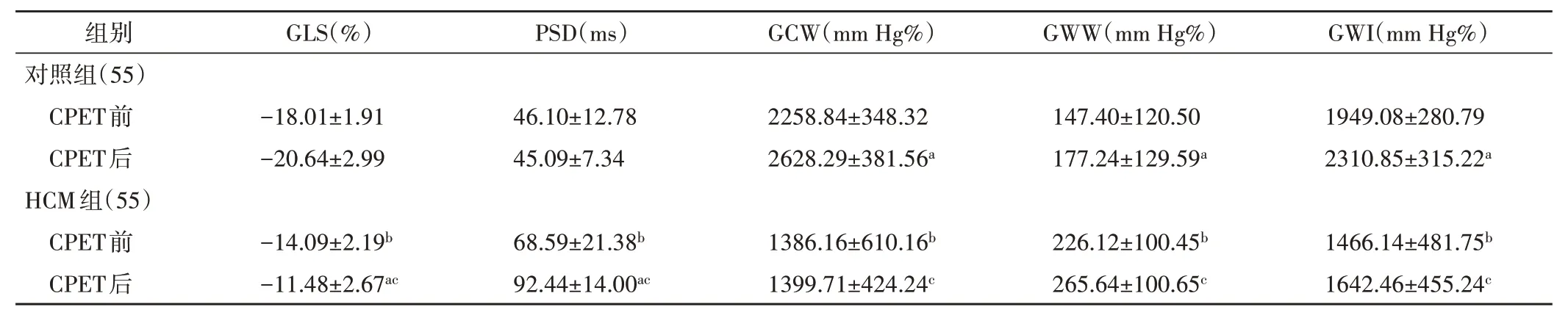
表2 两组CPET前后GLS、PSD及左室心肌做功参数比较()
与同组CPET 前比较,aP<0.05;与对照组CPET 前比较,bP<0.05;与对照组CPET 后比较,cP<0.05。GLS:整体纵向应变;PSD:纵向应变达峰时间离散度;GCW:整体有用功;GWW:整体无用功;GWI:整体做功指数
?
讨论
HCM 是最常见的遗传性心肌病,编码肌小节蛋白质成分的基因致病性变异是主要原因,因基因表达差异和区域壁应力差异引起左室壁不同部位的心肌肥厚[4]。HCM 患者可引起劳力性呼吸困难、胸痛、心悸、晕厥甚至猝死等。因此早期识别、诊断HCM 有利于及时进行相关干预,降低患者猝死风险。超声心动图是目前诊断HCM 最常用方法,LVEF 用于评估HCM 患者左室收缩功能应用广泛。但HCM 患者早期LVEF常在正常范围内,而一旦出现LVEF 明显下降,心功能损害往往已不可逆。本研究两组LVEDd、LVEDs、LVEF 比较差异均无统计学意义,表明常规超声心动图无法敏感识别HCM 患者左室收缩功能异常。而HCM 组MWT、LAD、E/e’均高于对照组,差异均有统计学意义(均P<0.05),表明HCM 引起左室结构性重构,出现心室充盈功能障碍及左房压力增高。这可能与HCM 患者室壁增厚、心肌僵硬度增加导致心肌组织顺应性降低有关。既往研究[5]发现LVEF 保留的HCM患者心肌应变值减低,斑点追踪技术可以较早反映HCM 患者心肌收缩功能及心肌形变受损。本研究结果也显示HCM 组GLS低于对照组,差异有统计学意义(P<0.05),表明HCM 患者左室整体收缩功能及心肌形变能力明显受损。本研究结果还显示HCM 组PSD 较对照组增加,差异有统计学意义(P<0.05),提示HCM患者应变达峰时间不一致,心肌收缩不同步使得左室心肌不能有效收缩[6]。
LVPSL 将无创测量的动脉血压和超声心动图斑点追踪分析获得的GLS 结合起来,同时考虑了左室形变和后负荷,可早期敏感地评估左室收缩功能受损情况,具有快速、便捷、无创、客观的优点。CPET 是在运动状态下综合评估患者心脏、肺部及骨骼肌功能的无创检查方法,可用于评估HCM患者心肺功能并进行危险分层[6-8]。HCM 患者运动后心脏不良事件发生率明显升高,HCM 运动后心肌做功参数如何变化,目前研究甚少。本研究应用LVPSL定量评估HCM患者CPET前后左室心肌做功情况,结果显示,CPET 前,HCM 组GCW、GWI 均较对照组减低,GWW 较对照组增加,差异均有统计学意义(均P<0.05)。表明HCM 患者在LVEF 保留时,左室整体心肌做功已经受损,表现为有用功的减低和无用功的增加。其中,GCW 减低是反映左室心肌纤维化的敏感指标[9],说明LVPSL 较常规超声心动图可更敏感地评估左室收缩功能受损情况,并可预测左室纤维化情况。分析原因可能为心肌纤维紊乱和间质纤维化引起左室形变,导致左室功能障碍[10]。而肥厚心肌内冠状动脉微血管功能障碍、壁内小动脉内侧肥大导致供氧量降低,加重了心肌同步性的损害,机电运动的异常降低了左室射血的机械效率,增加了能量损失和无效功,降低了心肌有效做功[11]。
为了进一步分析HCM 组运动后左室功能变化,本研究将HCM组与对照组在CPET前后应变及心肌做功参数进行比较发现,HCM组CPET后GLS较CPET前减低,PSD较CPET前增加,差异均有统计学意义(均P<0.05);对照组CPET 后GCW、GWW、GWI 均较CPET 前增加,差异均有统计学意义(均P<0.05);CPET 后,HCM 组GLS、GCW、GWI 均较对照组减低,GWW、PSD 均较对照组增加,差异均有统计学意义(均P<0.05)。表明HCM患者在静息状态下LVEF保留时已经出现了心肌做功的变化,随着运动时后负荷即血压的升高,心肌耗氧量明显增加,HCM患者因摄氧量降低,心肌内血管压力增加和心肌血液供应相对减少,心肌氧供需失衡,引起心肌同步性受损加剧,即PSD延长,使得心肌未能有效收缩,GCW、GWI均未有效升高,这可能是HCM患者运动受限的根本原因。而对照组在运动后负荷增加时通过有效功GCW 的增加来满足运动需要。分析HCM患者上述参数变化的原因可能为:HCM 患者因室壁肥厚,心肌耗氧量和需氧量增加,左房储存期应变减低[12],使每搏量不能有效增加,同时心肌肥厚引起冠状动脉血流储备有限[13],进一步加重心肌缺氧,引起HCM 患者心肺功能降低。本研究有3 例CPET 前无明显临床症状的HCM 患者在CPET 时出现峰值血压下降,血压异常反应,GLS、PSD 均明显升高,收缩压随着心力衰竭严重程度的增加而下降,考虑与运动诱导的左室舒张功能障碍、心搏出量锐减,引起血流动力学不稳定有关,这也是心源性猝死的高风险因素[14]。表明部分静息状态下无明显症状的HCM 患者运动后可出现严重的心肌做功改变,诱发心脏不良事件发生。
本研究的局限性:①以患者受检时的瞬时袖带压作为左室内压力,可能导致结果存在一定误差;②未根据患者心肌肥厚部位及运动强度进行亚组分析;③为单中心研究,样本量小,待今后扩大样本量进行多中心研究深入验证。
综上所述,LVPSL 可定量评估HCM 患者CPET 前后左室心肌做功变化,有助于早期发现静息状态下常规超声心动图无法检出的HCM患者隐匿性心肌损伤,为临床早期干预,优化治疗策略,个体化运动指导提供参考依据。

