弓形虫病的治疗研究进展
邱燕华,董 朕,张吉丽,白玉彬,陈 晨,张继瑜
(中国农业科学院兰州畜牧与兽药研究所 农业农村部兽用药物创制重点实验室 甘肃省新兽药工程重点实验室,兰州 730050)
弓形虫病是一种由刚地弓形虫引起的专性胞内寄生原虫病。刚地弓形虫能感染包括人在内的所有温血动物,甚至是一些冷血动物,并且能寄生于动物机体的所有有核细胞内[1-2]。而且弓形虫病的传播途径广泛,宿主主要可通过饮食、垂直传播、器官移植和输血等方式感染[3]。在免疫力强的个体中,弓形虫病通常不表现出症状,或者是轻度的自限性感染。然而,在免疫系统不发达的胎儿和新生儿或在HIV和其它具有细胞免疫力下降的疾病使免疫系统受损的情况下,弓形虫病可能会危及生命[4]。弓形虫病能严重影响人类、家畜和野生动物的健康,被视为一种严重威胁[5]。
近年来,国内外虽然在弓形虫病诊断、流行病学和病原学研究等方面取得了显著进步,但在治疗技术方面几乎没有取得新的进展。由于弓形虫生命周期的复杂性、发病机制的多样性和生物学特性的独特性,目前还没有预防和特异性的治疗药物[6]。本文从弓形虫病、临床用药及新型抗弓形虫药物的研究方面进行综述。
1 现有临床用药
针对弓形虫病,目前还没有有效的疫苗,临床治疗多采用化学疗法。弓形虫病的经典化学疗法通常采用抗菌药物磺胺嘧啶、螺旋霉素和克林霉素或抗疟疾药物乙胺嘧啶和阿托伐醌[7]。用于治疗弓形虫病的药物具有不同的作用机制(表1),它们通过抑制寄生虫的复制而保护器官免受损害,但不能将其从宿主体中完全清除。

表1 目前用于弓形虫病治疗的主要临床药物及作用机理[8, 10-11]Table 1 Main clinical drugs used in the treatment of toxoplasmosis and their mechanism
目前,乙胺嘧啶联合磺胺嘧啶(PS)和甲氧苄啶联合磺胺甲恶唑(TMP-SMX)以及螺旋霉素(Spiramycins,SPI)是弓形虫病临床治疗的首选,二线治疗药物由阿托伐醌和克林霉素等组成[8]。尽管这些方案对急性感染有效,但不能最终治愈。临床上,几乎所有的治疗方案都离不开磺胺类药物,由于这类药物经常引起过敏并伴有血液毒性。其中80%的患者在没有长期治疗的情况下会复发,约有40%的患者因发生严重的不良反应而终止治疗,目前还没有高效低毒的替代药物[9]。治疗上存在的另一个问题是这些药物不能穿越血脑屏障有效治疗由弓形虫引起的中枢神经系统疾病[6]。
2 弓形虫病的临床治疗
2.1 先天性弓形虫病的治疗先天性弓形虫病(CT)是孕妇感染刚地弓形虫,并经胎盘传播给胎儿的结果。怀孕期间感染可能导致严重后果,除死产、子宫内发育迟缓、早产或胎儿畸形外,还可能发生流产[12](图1)。通常只有怀孕期间或受孕期的急性感染才能导致CT,在慢性感染的免疫功能低下的孕妇中或在孕妇再感染南美和非洲的高毒力(非典型虫株)的情况下很少见[13]。CT的临床治疗包括产前治疗和产后治疗。从治疗目标上,产前治疗旨在预防弓形虫的母胎传播(MFTP)或减少对胎儿损伤,而产后治疗则是为了减轻感染新生儿的临床表现或预防其后遗症[6]。然而,文献中对产前治疗的益处有不同的认识,因为治疗的前提是要知道孕妇感染的准确时间,但这只有在有孕妇血清学筛查方案的国家,即数量有限的欧洲国家才能实现。产后治疗的效益/风险比率也受到质疑,特别是在无症状或亚临床感染患者中,对治疗效果的评估仍然存在争议[14]。
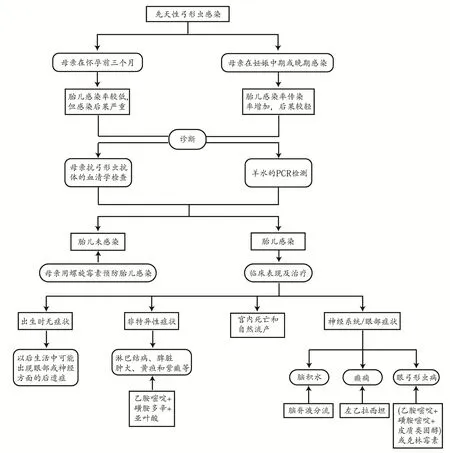
图1 先天性弓形虫感染[15-16]Fig.1 Congenital Toxoplasma infection
2.1.1 产前治疗 垂直传播随着孕龄的增加而增加,而胎儿症状的严重程度与孕龄呈负相关,早期感染是最严重的[12]。因为缺乏预防性指南和妊娠筛查的局限性,以及只有30%的原发性弓形虫感染的女性有临床症状,并且这些症状是非特异性的,导致CT的早期确诊复杂和极易被忽视[17]。确定母体感染的时间是评估胎儿感染风险和治疗需求的基础。妊娠前期可用血清学筛查诊断母体感染,妊娠第16周后即可通过PCR进行羊膜穿刺术检测胎儿弓形虫DNA的存在,并每4周对母体进行一次详细的超声检查,以寻找提示胎儿感染的超声征象,即胎儿异常,包括脑室肥大、颅内钙化、白内障、肝脾肿大、腹水和严重宫内发育迟缓[18](图1)。
最近有研究表明,妊娠期间弓形虫病的筛查和治疗可减少母婴传播和临床后遗症。产前治疗可以将CT引起的严重神经系统后遗症的风险降低75%[19]。孕妇在怀孕期间感染弓形虫后,若胎儿未受感染,则选择SPI治疗以防止弓形虫从母体通过胎盘传播到胎儿。一旦胎儿确诊或者高度怀疑,一般选择磺胺嘧啶-乙胺嘧啶-亚叶酸(SPFA)的治疗方案[20](表2)。研究发现,在怀孕初期使用SPI治疗受感染的母亲,可将胎儿的传播率从56%降低至24%。但是,如果母亲在怀孕期间发生了血清转化,该治疗方法并不能降低传播风险,但可以将疾病的严重程度降至最低[21]。乙胺嘧啶和磺胺嘧啶(PS)因为其致畸性,应在妊娠14周前避免使用[22]。对磺胺嘧啶有过敏反应的患者,可将乙胺嘧啶与克林霉素联用(PC)作为替代疗法[23]。
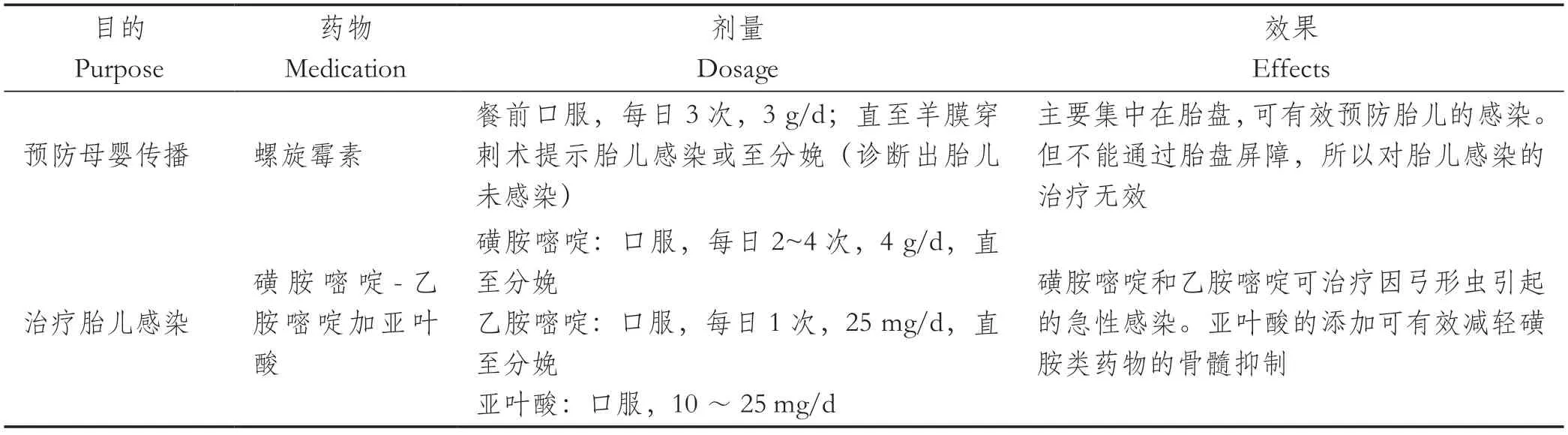
表2 先天性弓形虫病的产前治疗[6, 22]Table 2 Prenatal treatment of congenital toxoplasmosis
2.1.2 产后治疗 胎儿在子宫内感染弓形虫后,虫体可在脑和眼中形成终生的包囊,包囊通常在胎儿出生后被激活,从而导致一系列疾病[21]。先天性感染的婴儿可发生多种临床疾病,轻度可引起视力下降,重度则可引发眼部病变及神经系统病变[24]。其中,CT最常见的后遗症是眼部疾病,脑积水为最严重但最罕见的病变[25]。在妊娠早期感染的母亲所生的新生儿极有可能受到严重感染,而在妊娠晚期感染的新生儿中有80%出生时无症状。但是不管是无症状还是对症治疗的新生儿都存在晚期眼科和神经发育并发症的风险[24]。并有研究表明患有CT的儿童也有听力损失的风险,还可能出现晚期听觉丧失,患病率可高达26%[26]。
在没有产前筛查计划的国家,CT的治疗依赖于产后的诊断。诊断时需要与巨细胞病毒、淋巴细胞脉络丛脑膜炎病毒和单纯性疱疹病毒等其他原因引起的先天性感染相鉴别[27]。《先天性弓形虫病产后治疗指南》建议应尽早治疗,采用以下三种方案之一(表3)连续治疗12个月。该建议基于专家意见和观察性研究,显示长期并发症的发生率比历史对照中的短期治疗要低[28]。磺胺多辛-乙胺嘧啶的不良反应可能比PS更严重,并常发于治疗的前2个月。但是,磺胺多辛-乙胺嘧啶的给药频率(每周1次)更适用于长期治疗。如果婴儿被诊断为CT,在治疗结束时也应该继续定期进行临床和眼科监测。此外,长期治疗应关注药物的不良反应,如严重的骨髓抑制导致中性粒细胞减少、肾功能减退和过敏等。婴儿应定期进行血细胞计数监测及肝肾功能检查[27]。

表3 先天性弓形虫病的产后治疗[13, 29]Table 3 Postpartum treatment of congenital toxoplasmosis
2.2 获得性弓形虫病的治疗
2.2.1 免疫功能低下患者的治疗 在健康的人群中,弓形虫的感染通常无症状,但对免疫功能低下的个体可能致命,例如人类免疫缺陷病毒/艾滋病(human immunodeficiency virus,HIV/ acquired immunodeficiency syndrome,AIDS)患者,癌症患者和器官移植接受者[30]。免疫力低下的患者通常是潜伏感染被重新激活,也可能发生急性获得性感染,造成多器官损伤和其他传播性全身疾病。在免疫功能低下的患者中,治疗需要结合抗弓形虫药物,并将其继续作为抑制疗法,直到发生免疫重建[31]。
对于HIV/AIDS同时又感染了弓形虫的患者的治疗包括针对弓形虫的治疗和帮助免疫恢复的高效抗逆转录病毒疗法(highly active antiretroviral therapy,HAART)。最常用的初步治疗方案还是SPFA,治疗时间通常为6周。因为HIV/AIDS弓形虫病的易复发性,建议维持治疗,直到对HAART产生明显的免疫学改善。对磺胺类药物过敏的患者,可用以下治疗方案替代:克林霉素;乙胺嘧啶-阿托伐醌-亚叶酸;乙胺嘧啶-阿奇霉素-亚叶酸;单独使用阿托伐醌(如果磺胺类药物或乙胺嘧啶都不能耐受)[32]。
由于长期接受高强度免疫抑制治疗,造血干细胞移植和实体器官移植的接受者感染弓形虫后死亡率很高。并且他们的临床症状都是非特异性的,具体的症状取决于所涉及的器官和弓形虫的扩散,但发热是该病最常见的临床症状,当移植的接受者出现无法解释的发热时,医生应考虑弓形虫病[33]。目前推荐的治疗是乙胺嘧啶(50~100 mg/d,口服,每天最多200 mg)与磺胺嘧啶(4~6 g/d,口服或静脉注射)。给药期间需严格监测血细胞数量,还需增加亚叶酸或亚叶酸钙(5~25 mg)以减轻乙胺嘧啶的血液毒性。若对磺胺类药物过敏,可选择阿托伐醌、克林霉素或克拉霉素替代[34]。预期的治疗时间为4~6周,但只有在仔细评估患者的状况后才能终止治疗。
2.2.2 免疫功能正常患者的治疗 弓形虫感染免疫功能正常的机体时,一般经过1~2个月的急性感染后进入潜伏期,形成慢性感染,一旦感染,宿主一生都会携带弓形虫的感染性组织包囊[35]。在21世纪之前,这种弓形虫最常见的感染形式,即终生潜伏的弓形虫病,一直被认为是没有症状的。但是,近些年有不断的研究证实这种潜在性的弓形虫病与多种神经与精神疾病以及行为变化具有一定的联系,如精神分裂症、阿尔兹海默症、双向情感障碍等[36-37],甚至对人类的出生性别比也有影响[35]。
人类的免疫系统可抵抗弓形虫感染,并能够抑制速殖子复制,因此通常是无症状疾病或轻度症状的疾病,例如淋巴结病或发热。只要未观察到免疫力受损并随后重新激活感染,受感染的免疫能力强的个体一般不需要治疗[7]。若患者有持续的不适或表现出严重的症状,应该考虑治疗。目前的做法是用SPFA治疗此类患者2~4周,具体取决于临床疗程和症状出现时对治疗的反应[38]。
3 眼弓形虫病和脑弓形虫病的临床治疗
眼弓形虫病(OT)主要表现为脉络膜视网膜炎,这是CT的主要眼部表现。OT通常是胎儿晚期的获得性感染后遗症,也会由于免疫能力强的人受到急性感染和免疫功能低下的人的急性获得性感染或潜伏感染重新激活而发生[39]。OT治疗的目的是降低永久性视力损害的风险(旨在减少视网膜脉络膜瘢痕的大小)、复发的风险以及急性症状的严重程度和持续时间。
目前,尚无针对OT的明确治疗方法[40]。但是传统上,抗生素和皮质类固醇是治疗OT的主要药物,抗生素通常使用6~8周[41]。其中经典的是乙胺嘧啶、磺胺嘧啶和皮质类固醇的“三联疗法”。然而,由于每天口服药物的大量使用,这种经典疗法可能会伴随着明显的不良反应。有一项研究表明,与PS相比,PC的口服合剂对OT显示出更好的效果和较低的不良反应[42]。与经典疗法相比,已建议将TMP-SMX与口服泼尼松龙的组合作为OT的替代治疗选择,其在缩小视网膜病变的大小和改善视力方面具有相似的疗效[43]。并且,TMP-SMX对复发性OT有预防作用,但因其不良反应,2个月以下的婴儿患者禁止使用[11]。文献中建议的另一种治疗选择是在玻璃体内注射克林霉素和地塞米松,这种给药方式可将高浓度的治疗药物输送到玻璃体腔和视网膜中,同时减少全身性不良反应。并已有研究表明,每周一次的克林霉素玻璃体腔内治疗被证明是严重OT或经典治疗禁忌患者的一种合适的治疗选择[44]。因克林霉素能够在眼组织中浓缩并穿透组织囊肿壁,它常被添加到经典的“三联疗法”中组成“四联疗法”[45]。
脑弓形虫病一般是由于潜在弓形虫病的再激活发生的,表现为神经症状,其中最常见的表现为弥漫性脑病、脑膜脑炎、头痛、意识混乱、协调性差和癫痫;晚期可表现为呼吸系统疾病、高热和视觉障碍[46]。脑弓形虫病是免疫功能低下的弓形虫病患者最常见的临床表现,如果不治疗会危及生命。及时使用适当的抗生素治疗脑弓形虫病是至关重要的,当临床高度怀疑时就应立即开始。在美国卫生与公众服务部(Department of Health & Human Services,DHHS)、欧洲艾滋病临床学会(European AIDS clinical society,EACS)和英国艾滋病协会(The British Association for Sexual Health and HIV,BHIVA)指南中,脑弓形虫病的首选初始治疗方案是PS,PC是首选的替代方案。TMP-SMX也通常作为额外的替代方案出现[47]。与PS和PC相比,TMP-SMX可使用静脉给药,并且具有较低的给药剂量和频率。所以目前的指南建议选择静脉注射TMP-SMX作为重症患者的初始治疗[48]。但是,这些标准治疗方案经常会引起严重的不良事件,比如肝、肾和血液毒性以及超敏反应。Shiojiri等[49]报告了一例脑弓形虫病患者,在所有标准方案治疗后出现了严重的不良反应,但成功地用克林霉素和阿奇霉素联合治疗,说明这种药物组合可以替代这种情况。当患者病情恶化到一定程度时,可能需要其他干预措施,如减压手术,以减少病变效应。
免疫力低下的胎儿可能会因为在母亲体内感染弓形虫而在胎儿时期或出生后表现为脑弓形虫病,其中脑积水会影响约4%的CT婴儿,并且是CT发病率和死亡率的重要原因[50]。除了进行抗弓形虫病的常规治疗外,也可同时接受脑室-腹腔分流术(VP分流术)的治疗。McLone等[51]研究表明即使在神经影像学上有严重脑积水的情况下,CT引起的脑积水患者接受VP分流术,也有助于取得良好的临床效果。
4 动物弓形虫病的临床治疗
弓形虫病是一种高度流行的寄生虫病,不仅可以感染人类,还能感染绝大多数家畜。如:猪、羊、马、鸡等动物,几乎包括了人类的所有肉食来源。同时,弓形虫病能引起母畜的流产、死胎和胎儿畸形,目前弓形虫病已是全世界绵羊和山羊流产的常见原因[52]。动物弓形虫病给人类健康和畜牧生产都造成了严重的影响。因此,控制动物弓形虫病对公共卫生和畜牧业经济发展极为重要。
对于各种畜禽的弓形虫病的治疗多采用“预防为主,治疗为辅”的原则,治疗上也多使用磺胺类药物。各种畜禽的弓形虫病中,猪弓形虫病较为严重,猪弓形虫病一旦在猪群中暴发,整个猪群都可能发病,且死亡率较高[53]。当前国内对猪弓形虫病的治疗,中西药的联合使用是一种趋势。米玉龙的试验研究表明,与单独的西药(复方长效磺胺间甲氧嘧啶钠注射液)或中药(青蒿、黄连等)治疗相比,中药和西药的联合治疗对猪弓形虫病的治疗效果最佳[54]。最近有研究人员发现硫酸葡聚糖10(DS10)对猪弓形虫病也有治疗作用,静脉注射DS10可减轻弓形虫感染引起的寄生虫负担和炎症反应,其中中剂量DS10(50 μg/头)可有效治疗猪弓形虫病,且无副作用[55]。
猫是弓形虫的唯一终末宿主,犬是其重要的中间宿主。随着社会经济的发展,把猫和犬作为宠物饲养的人越来越多,人与猫和犬的关系越来越密切致使弓形虫的传播途径被进一步加强,因此需注重猫和犬弓形虫病的防治工作。猫弓形虫病有多种治疗选择,包括克林霉素、阿奇霉素、乙胺嘧啶和甲氧苄氨嘧啶磺胺类药物,其中克林霉素是文献中最常用的治疗方法,当前对猫的建议是每天剂量25 mg/kg,分次服用[56]。Butts和Langley-Hobbs[57]用克林霉素成功的治疗了一只疑似由弓形虫引起的泛发性肌病的猫。克林霉素也被成功用于治疗犬弓形虫引起的肌病,Migliore等[58]报告了一例罕见而严重的弓形虫I型感染流浪狗的病例,确诊后立即给予了盐酸克林霉素(25 mg/kg,每日2次治疗)弓形虫病。同时,还进行了经典水上理疗以帮助解决肌肉萎缩问题,治疗4周后恢复了正常。
5 新型抗弓形虫药物的研究方向
寻找新的抗弓形虫药物是一项艰巨的任务,因为它需要对弓形虫的速殖子和缓殖子两个阶段有效。当前,虽然还没有非常理想的可用药物,但是开发有应用前景的候选药物的工作仍在持续进行。许多临床前体内、体外研究表明,很多化合物对急性和慢性弓形虫病都表现有治疗作用,其中有些化合物表现出的抗弓形虫活性明显高于目前临床在用的抗弓形虫药物。抗弓形虫药物研究开发的主要方向主要有以下四个方面。首先,是目前热门的天然产物筛选。如metacytofilin(MCF)、肉豆蔻木脂素、熊果酸和白藜芦醇(RSV)。其中MCF可阻止弓形虫的垂直传播,RSV能恢复被弓形虫感染的神经祖细胞的活力[59-62]。其次是新化合物合成。如PPQ-8、噻唑烷丁-4-酮衍生物和氨基硫脲衍生物。其中有14种噻唑烷丁-4-酮衍生物在体外表现出比甲氧苄啶更好的抗弓形虫活性和更低的毒性[63-65]。同时已有药物的再利用也备受关注。如瑞舒伐他汀、硝唑尼特(NTZ)、氯硝柳胺和胍那苄。NTZ是治疗急性和慢性弓形虫病的潜在药物,胍那苄可通过减少神经炎症逆转小鼠因潜在弓形虫病引起的行为变化[66-69]。最后是药物的新剂型研发。如金属纳米粒子、螺旋霉素壳聚糖纳米粒、阿托伐醌纳米乳剂和姜黄素纳米乳剂[70-72]等。纳米制剂可增加原来药物的溶解度,降低毒性和提高生物利用度,还可通过血脑屏障发挥治疗作用。这些特性极大的增强了药物抗弓形虫的作用效果,其中金属纳米粒子可到达组织包囊中,生物银纳米粒子甚至能消除大脑中潜在的缓殖子[73-74]。
6 结语
弓形虫病是一种重要的人兽共患寄生虫病,不仅严重影响着人类的健康,还造成了巨大的经济损失。当前对于弓形虫病的治疗主要依赖基于药物的化学疗法,虽然这些药物可以有效的控制弓形虫的急性感染,但普遍存在毒副作用大、治疗周期长、易复发和对弓形虫组织包囊缺乏疗效等缺点。新的抗弓形虫药物需要降低毒性、到达特定治疗部位和屏障以及满足药物的治疗浓度、缩短治疗时间和保证妊娠安全。越来越多的临床前药物研发工作表明,针对弓形虫病的有效药物防治技术的突破指日可待。

