扣眼穿刺患者动静脉内瘘感染的影响因素分析
赵秀明 刘金凤 牛洪艳 祝喜鹰
理想的血管通路是实施维持性血液透析治疗的基础,由于自体动静脉内瘘(AVF)较高的通畅率和较低的感染率,AVF 是首选血管通路类型[1]。年老体弱患者的增加,加上心脏病、糖尿病、外周血管疾病和血管资源耗竭等合并症,对建立和维护动静脉内瘘提出了一项艰巨的挑战。内瘘功能障碍,尤其是感染,仍然是终末期肾病(ESKD)患者合并症和住院的主要原因之一[2]。正确和适当的内瘘穿刺方法是维护和预防血管通路相关功能障碍的关键[3]。扣眼穿刺法是血管通路指南[4-5]推荐的内瘘穿刺方法之一。这种技术消除了关于最佳穿刺位置、穿刺角度以及从皮肤到血管腔距离的不确定性。这些理论优势,使扣眼穿刺技术在最初几年被广泛推广。其优点在于更容易穿刺、减轻患者疼痛、拔针后快速止血以及减少动脉瘤和血肿的发生,更适用于穿刺点有限或穿刺困难的患者[6-7]。然而,该技术存在很大的争议[8],因为它可能与感染的发生有关[9-13]。通路部位感染需要特别注意,因为它们会导致播散性菌血症或血管通路的功能丧失[14]。AVF感染可引起局部红肿、发热、疼痛、脓性渗出、血管溃烂,甚至通路相关血流感染,从而增加患者的经济负担和死亡风险。本研究通过对实施扣眼穿刺技术患者的调查,探讨感染并发症的影响因素,为医护人员采取针对性的干预措施提供参考依据。
1 对象与方法
1.1 调查对象
选取2018 年10 月—2021 年10 月常州市某三级甲等综合医院血液净化中心进行血液透析患者58例为调查对象,根据随访是否发生内瘘感染分为感染组20 例(病例组)和未感染组38 例(对照组)。纳入条件:血管通路为AVF;年龄>18 岁;连续使用自体动静脉内瘘进行血液透析;接受扣眼式穿刺技术进行动静脉内瘘穿刺,穿刺前均接受评估、确定穿刺点,穿刺时遵循“四同”原则,即同一穿刺点、同一进针角度、同一方向、同一进针深度,待皮下隧道形成后改为钝针穿刺。排除条件:既往或目前患有精神障碍、认知障碍,不能配合检查者;病情不稳定者。脱落条件:扣眼穿刺停止使用者;肾移植、转院、死亡患者。患者自愿参加本研究并签署知情同意书。本研究经过本院伦理委员会审批,编号为:(2022)科第128 号。
1.2 调查内容
通过提取患者病历收集患者的性别、年龄、透析年限、是否有糖尿病、内瘘使用时间、是否高位瘘、实验室检查指标(白细胞计数、白蛋白、hsCRP 等)、扣穿刺情况(有无扣眼感染、感染时间、是否有假隧道、穿刺点周围有无过敏、扣眼使用时间等数据)。扣眼使用时间是指从随访开始到感染、失访或随访结束的时间,即生存时间。局部感染表现主要为穿刺部位发红、肿胀、皮温增高、疼痛、脓性分泌物形成;通路相关血流感染主要表现为发热、血白细胞计数及中性粒细胞百分比升高、血培养阳性。
1.3 数据分析方法
采用SPSS 25.0 统计学软件进行数据分析,正态分布的计量资料以“均数±标准差”表示,非正态分布的计量资料以“M(P25,P75)”表示。中位数比较采用非参数检验。计数资料计算百分比,组间构成比较采用χ2检验。采用 Cox 风险比例回归模型进行多因素分析。以P<0.05 为差异有统计学意义。
2 结果
2.1 入选患者一般情况
本研究中58 例患者随访期3~36 个月,平均15.98±9.77 个月,其中男33 例,女25 例;年龄 26~85 岁,平均53.78±12.45 岁;透析龄7~232 个月,平均95.55±64.01 个月;内瘘使用时间 5~215 个月,平均66.17±54.14 个月;内瘘部位前臂46 例,上臂12 例。
2.2 内瘘发生感染的单因素分析
感染组与未感染组比较,扣眼使用时间、是否有假隧道、有无穿刺点周围皮肤过敏,差异有统计学意义(P<0.05);两组在性别、年龄、透析龄、内瘘使用时间、有无糖尿病、是否高位瘘、白细胞、白蛋白、C 反应蛋白方面比较,差异无统计学意义(P>0.05),见表1。
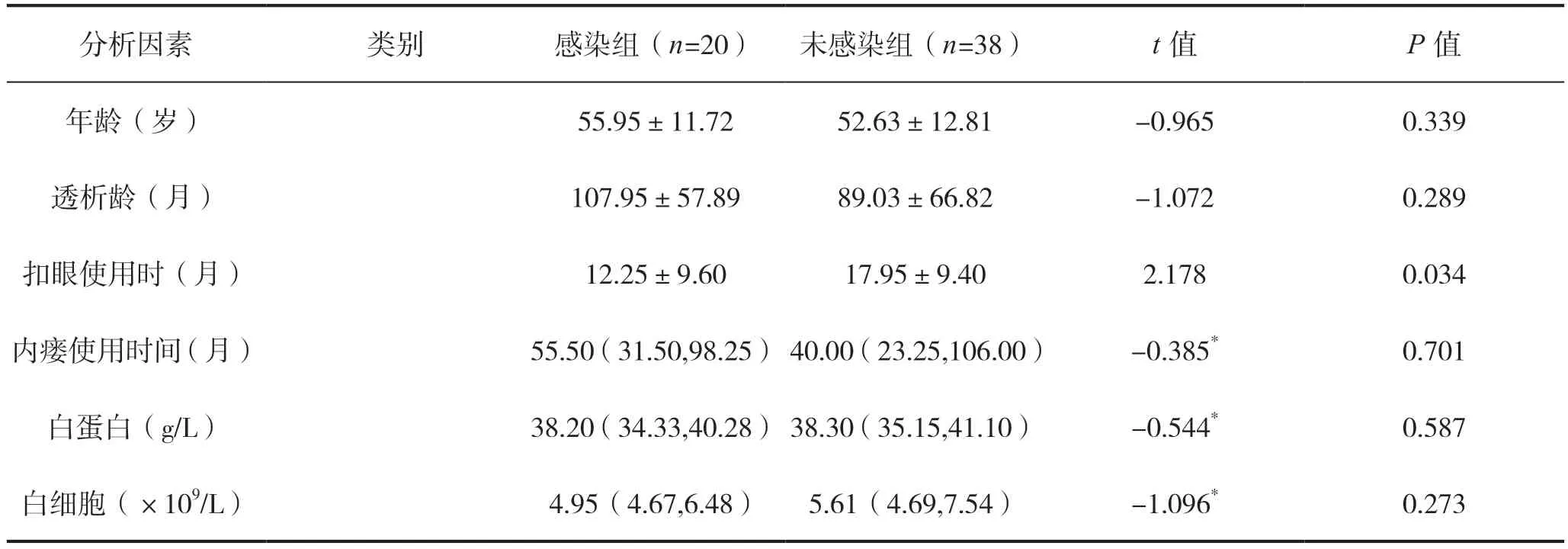
表1 内瘘发生感染的单因素分析
2.3 内瘘感染影响因素的Cox 回归分析
将单因素分析中有统计学意义的因素假隧道、过敏为自变量(扣眼使用时间为随访时间),内瘘是否发生感染因变量(是=1,否=0),进行多因素Cox 回归分析。结果发现,假隧道、穿刺点周围皮肤过敏与扣眼感染有关系(P<0.05),具有假隧道和穿刺点周围皮肤过敏的患者,发生扣眼感染的风险大,见表2。
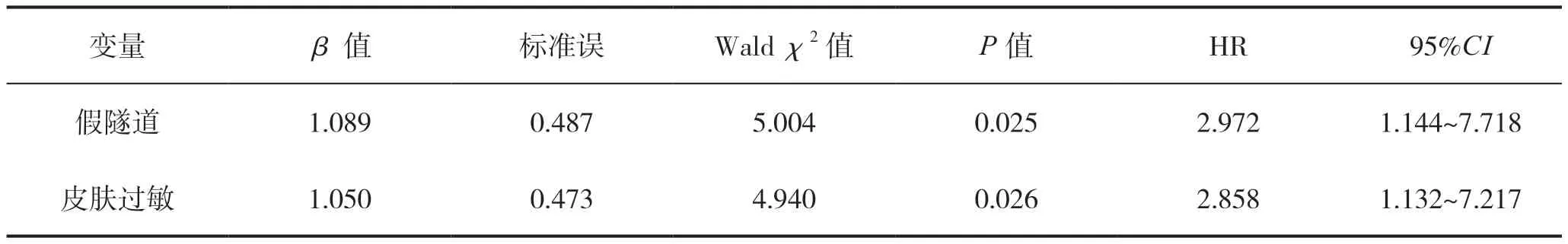
表2 扣眼穿刺发生感染的Cox 回归分析
3 讨论
自体动静脉内瘘是维持性血液透析患者的“生命线”,一旦出现感染,不仅影响血液透析的正常进行,严重者可致血管通路失功甚至危及生命。研究[15-20]发现扣眼穿刺导致菌血症和局部感染的风险增加,尤其是金黄色葡萄球菌,可导致严重的循环系统感染,如心内膜炎。因为皮肤完整性被破坏,结痂需要额外的感染控制措施,感染风险是扣眼穿刺需要关注的主要问题。Christensen 等[21]研究发现在扣眼隧道和/或隧道入口分别存在18%、20%和 17% 的细菌生长。葡萄球菌是最常见的病原体(金黄色葡萄球菌占25%;表皮葡萄球菌占41%)。细菌定植阳性的扣眼穿刺点有更多的局部发红和压痛,在扣眼培养阳性的患者中诊断出更多与通路相关的感染。Lyman 等[22]研究指出扣眼穿刺相关的血流感染住院率较高。与绳梯穿刺相比,扣眼穿刺与通路相关血流感染和局部通路部位感染有关。关于在透析中心使用扣眼穿刺技术的决定应考虑到较高的感染风险。需要研究来评估可能减少与扣眼穿刺相关感染的控制措施。但目前对扣眼穿刺感染影响因素的研究较少,为有效识别高危因素,积极干预,降低扣眼穿刺感染的发生率有必要进一步探索。
3.1 扣眼穿刺患者发生感染的影响因素
本研究分析结果显示,有假隧道、穿刺点周围皮肤过敏是扣眼穿刺患者发生感染的危险因素。扣眼穿刺患者血管通路相关感染发生率较高的原因尚不明确,既往研究表明血管通路相关感染的频率和扣眼使用时间是密切相关的。研究发现[23]扣眼穿刺患者感染发生率较高不仅是由于扣眼技术的方法所致(比如扣眼隧道的存在和同一部位的重复针刺),也可能是由于一段时间内进行扣眼穿刺的继发因素(比如扣眼穿刺处的畸形[24-25])导致的。那么从扣眼穿刺开始经过一段“平静期”后,感染的频率就会增加。Labriola 等[26]报道了扣眼穿刺的患者,感染高发前要经历一段感染“平静期”,1 年后感染概率显著增高,这与本次研究的结果也是相似的。不同研究“平静期”出现的时间差异较大,这可能与各透析中心所用消毒剂种类、护理措施及穿刺人员的培训有关。因此,扣眼穿刺点定期更换穿刺部位,至少1 年甚至更短周期,在一定程度上能减少感染的发生。
3.2 假隧道的形成与内瘘感染有关
有假隧道的患者发生感染相对风险是无假隧道的患者的2.97 倍。假隧道的产生可能与患者手臂摆放位置的变化、是否使用止血带、绷紧皮肤的方向、进针角度、体重的改变所导致血管隧道移位,以及未进入隧道强行刺入有关。良好的隧道可能是减少感染的主要措施,隧道形变、穿刺困难、反复试穿是导致感染的主要原因。在建立隧道初期,应保证穿刺针能顺利滑入血管方可更换钝针。尖锐的针头会导致在原隧道附近产生假隧道,使随后的穿刺复杂化,从而促进感染。扣眼穿刺时应将穿刺点部位的结痂彻底清除,以便于穿刺针经扣眼能直接送出,防止假隧道的产生[27]。穿刺必须遵循精确的进针角度、方向和手臂摆放位置,应在内瘘穿刺图上有所标识,并记录穿刺细节要点。对出现假隧道的患者,应果断更换穿刺点,避免因反复试穿导致细菌随针尖进入血管内,诱发感染。
3.3 穿刺部位过敏易造成内瘘感染
穿刺部位过敏患者发生感染相对风险是无穿刺部位过敏患者的2.86 倍。患者对钝针材质过敏,导致穿刺点周围皮肤出现瘙痒、湿疹、皲裂等临床表现,增加扣眼穿刺患者的感染风险。这一结论与Christensen 等[21]的研究结果一致。患者在透析时穿刺部位出现的皮肤损害符合下列特点即发病急,明确的接触致敏物质史,皮疹炎性反应,皮损界清,仅位于接触部位,皮损多为红斑、丘疹、水疱。导致过敏反应的原因可能是由于环氧乙烷消毒剂过敏或者对穿刺针材质过敏。环氧乙烷具有光谱高效杀菌作用,属最有效的化学冷灭菌剂之一,穿刺针多采用环氧乙烷消毒灭菌,它具有很好的吸附性。如果穿刺针有残留气体,就可能会导致患者发生过敏反应。穿刺前使用生理盐水脉冲式冲洗穿刺针,可以去除残留气体,避免过敏反应的发生。另一方面,穿刺针材质过敏导致患者出现了接触性皮炎。接触性皮炎属于Ⅳ型迟发性变态反应,含有过敏物质的材料与表皮细胞内角质蛋白和胶原蛋白结合,而使机体致敏,因此当再次接触相应变应原后,可发生炎症反应[28]。可使用无菌纱布片垫于针柄下方,避免针柄直接接触皮肤,或引入材质更好的不易致敏的钝针。为了减少细菌进入扣眼隧道,对于有过敏症状的患者,同时在每次穿刺前应保证对扣眼隧道进行充分消毒,可将一块10 mm×10 mm 的碘伏纱布放置在消毒的扣眼入口部位,覆盖1 min,然后再用钝针对通路血管进行穿刺。研究结果表明[29],扣眼隧道的消毒虽不能根除细菌,但能抑制细菌生长,从而减少感染的发生。
综上所述,本研究以扣眼穿刺患者为研究对象,以感染为终点评价指标,证实了除扣眼使用时间外,假隧道、穿刺点周围皮肤过敏是扣眼穿刺患者感染的独立危险因素。在临床工作中应严采取限制性策略,遵循绳梯第一,扣眼第二的原则[30],排除高风险患者,实施严格的操作准入制度[31],加强透析患者再教育,针对高危因素采取预防性护理措施,降低扣眼穿刺感染的发生风险,延长患者血管通路的使用寿命。本研究存在纳入样本量较少等缺点,今后需加入观察样本,深入研究。

