个性化康复联合GnRH拮抗剂方案在OHSS高风险患者中的应用
夏彦?谢素嫣?郭素素
【摘要】目的 探討个性化康复联合促性腺激素释放激素拮抗剂(GnRH-A)方案在卵巢过度刺激综合征(OHSS)高风险助孕患者中的应用效果。方法 选择86例OHSS高风险助孕患者,随机分为个性化康复组和对照组,每组各43例。2组患者均接受GnRH-A方案促排卵,在此基础上对照组接受常规康复方案,个性化康复组接受个性化康复方案。比较2组患者干预后OHSS总发生率,OHSS患者的住院时间、不适症状消退时间,患者焦虑和抑郁状态以及康复满意度。结果 干预后与对照组相比,个性化康复组的OHSS总发生率、OHSS患者住院时间和不适症状消退时间,汉密尔顿抑郁评分和焦虑自评量表评分均低于对照组(P均< 0.05)。干预后,个性化康复组的康复满意度高于对照组(P< 0.05)。 结论 个性化康复联合GnRH-A方案可有效预防OHSS,缩短OHSS患者住院时间及不适症状持续时长,改善患者精神心理状态,提高康复满意度。
【关键词】卵巢过度刺激综合征;促性腺激素释放激素拮抗剂方案;预防;个性化;加速康复
Application of individualized rehabilitation combined with GnRH antagonist protocol in patients with high-risk ovarian hyperstimulation syndrome Xia Yan, Xie Suyan, Guo Susu. Obstetrics and Gynecology Center for Reproductive Medicine, General Hospital of Southern Theater Command, Guangzhou 510010, China
Corresponding author, Xia Yan, E-mail: xiayannanzong@163.com
【Abstract】Objective To evaluate the efficacy of individualized rehabilitation combined with gonadotropin-releasing hormone antagonist (GnRH-A) protocol in women with high-risk ovarian hyperstimulation syndrome (OHSS). Methods Eighty-six patients with high-risk OHSS were selected and randomly divided into the rehabilitation (n=43) and control groups (n=43). All patients in both groups were treated with GnRH-A regimen to promote ovulation. On this basis, patients in the control group received routine rehabilitation therapy, and their counterparts in the rehabilitation group were given with individualized rehabilitation regimen. The overall incidence of OHSS, length of hospital stay, time of symptom remission, anxiety and depression status and patients degree of satisfaction with rehabilitation were compared between two groups. Results After corresponding interventions, the overall incidence of OHSS, length of hospital stay, time of symptom remission, the scores of Hamilton Rating Scale for Depression (HAMD) and Self-rating Anxiety Scale (SAS) in the rehabilitation group were significantly lower than those in the control group (all P< 0.05).The degree of satisfaction in the rehabilitation group was higher compared with that in the control group after corresponding interventions (P <
0.05). Conclusion Individualized rehabilitation combined with GnRH-A protocol can effectively prevent the incidence of OHSS, shorten the length of hospital stay and the duration of discomfort symptoms, improve the psychological status and enhance the patients degree of satisfaction with rehabilitation.
【Key words】Ovarian hyperstimulation syndrome; GnRH antagonist protocol; Prevention; Individualized;
Accelerated rehabilitation
卵巢过度刺激综合征(OHSS)是机体对过量激素的过度反应,常见发生于通过注射激素药物来刺激卵巢内卵子发育和接受辅助生殖技术促进排卵的女性[1]。研究显示,年龄、激素水平异常、卵泡数目过多、既往多囊卵巢综合征(PCOS)病史等是OHSS的高危因素,对于这类群体,促排卵过程中重度OHSS的发生率甚至高达20%,明显高于无风险群体的0.5%~2%[2-3]。2016年,国外指南推荐促性腺激素释放激素拮抗剂(GnRH-A)方案能在不影响婴儿出生率的前提下有效降低患者罹患OHSS 的风险[4]。中国优生科学协会随即提出将快速康复理念应用于围产期的管理,并建议从孕期开始宣教等康复工作[5]。但临床中由于患者个体化差异,GnRH-A方案的实施与起效差异明显[6]。因此,在GnRH-A方案的基础上从生理、心理和家庭社会关系等层面查找OHSS高风险患者问题清单制定并个性化康复方案,或可有效预防OHSS,提高孕产质量,促进快速康复。本研究探讨个性化康复治疗联合GnRH-A方案在OHSS的应用,现报道如下。
对象与方法
一、研究对象
选取2020年6月至2022年10月在我院就诊的伴OHSS高风险因素患者为研究对象。纳入标准:①年龄≤35岁;②PCOS病史;③血清抗米勒管激素(AMH)>3.4 μg/L;④窦卵泡计数(AFC)≥15个,人绒毛膜促性腺激素(HCG)注射日雌二醇(E2)>3 500 ng/L或获卵数≥24个;⑤扳机日血清E2 >15 000 nmol/L,扳机日> 12 mm卵泡数量超过20个[4, 7]。排除标准:①合并有心、脑、肝、肾、肺等重要系统病变者,或合并有精神、认知、心理障碍者;②半年内接受药物等其他干预治疗者;③子宫合并影响胚胎着床的其他疾病者;④存在未经治疗的内分泌疾病者;⑤不配合者。基于样本量计算公式N=;N为每组样本量,α=0.05,双尾;1-β为检验效能,为90%,σ为标准差,为治疗组与对照组平均值的差值。Ζα/2=1.96,Ζβ=1.28,参考既往文献,σ=1.78,=1.3,计算可得N=78,考虑到10%的脱落率,研究最终纳入86例,并用随机数字表法分为个性化康复组和对照组,每组各43例。本研究已获得医院伦理委员会批准(批件号:NZLLKZ2022025),所有入组患者均已签署知情同意书。
二、方 法
1. GnRH-A
所有患者于月经周期第3日予以促性腺激素(Gn)促排卵启动,第5日通过B超监测卵泡的发育情况,根据卵泡数量、大小、同步性、形态、张力及性激素[E2、睾酮(P)、黄体生成素(LH)]水平调节Gn的剂量和扳机时机,同时关注子宫内膜的厚度和形态变化,Gn 使用至扳机前日。根据 LH 水平和卵泡的大小添加 GnRH-A,当主导卵泡达14 mm 或 LH≥10 mIU/mL时添加 GnRH-A至扳机日。本研究使用曲普瑞林0.2 mg 皮下注射,在扳机后36 h B超下取卵。取卵手术前做好注意事项的讲解,术中监测生命体征及阴道出血,术后记录排尿及尿量情况。
2. 康复方案
对照组在GnRH-A治疗基础上接受常规康复方案,包括在患者入组时开展病情评估、促排卵期间用药及相关知识宣教、营养管理、心理咨询等。具体为:①病情评估,建立患者病情档案,记录患者一般资料、日常习惯、激素水平及促排卵期间卵泡数量等关键信息;②康复宣教,在患者注射HCG夜针日,针对夜针作用及用法进行介绍;③营养管理,指导患者每日所需营养进行搭配,高蛋白饮食,尤其对于并发重度OHSS患者进行扩容,补充白蛋白及其他胶体,纠正血液浓缩症状,维持水、电解质平衡;④心理咨询,做好患者情绪和自我管理;⑤取卵术后康复管理,包括观察患者饮食、消化、精神心理症状及院外居家康复,患者如出现腹胀不适和尿少、气促等不适症状时,动态监测血常规、肝肾功能,B超监测腹水及胸腔积液等情况。
个性化康复组在对照组的基础上开展个性化康复方案,包括行为与应对方式干预、精神与心理干预、理解患者期待与渴望、提高自我管理能力等方面。具体为:①组建包括生殖中心、康复科、营养科在内的多学科团队,提供用药、营养及心理等支持;②一对一健康教育,针对患者受教育水平、理解和接受能力,借助微信群、手册与公众号等载体以医学科普及解答形式解释OHSS病因、发病机制、症状特点、危害以及妊娠相关的宣教;③健康行为培养,强化行为与应对方式干预,鼓励患者半卧位卧床休息, 避免长期静坐,同时指导患者进行踝泵动作训练,20次为1组,每日30组,此外日间穿弹力袜配合夜间抬高下肢睡觉以促进下肢静脉回流,预防静脉血栓,并禁止大幅度翻身、起蹲等剧烈运动,避免腹部受压及碰撞发生卵巢破裂或扭转行为;④营养支持,于患者入组时使用《营养风险筛查评分简表 2002》(NRS2002)进行营养筛查,对于存在营养风险的患者,进一步评估营养状况,询问患者饮食喜好、进食量、有无腹泻等,在对照组基础上加强饮食管理,鼓励患者进食,少吃多餐,注意高蛋白、高热量、富含维生素、易消化、低脂肪的均衡饮食;⑤心理咨询,充分理解患者期待与渴望,了解患者对疾病所处阶段的治疗预期以及出院后未来生活的期待,做好患者家屬的沟通工作, 尽可能取得家属最大的支持和配合,使患者感受到来自家庭的支持与鼓励;⑥社会参与,帮助患者正确看待自我,提高自我管理能力。
三、观察指标
1. 轻度、中度、重度OHSS和总OHSS发生率
治疗后比较2组患者OHSS发生情况。OHSS分度标准参照中华医学会生殖医学分会制定的《辅助生殖技术并发症诊断及处理共识》,基于腹胀、腹水、呼吸困难、卵巢等临床表现结合血细胞比容、白细胞数等实验室指标将OHSS分为轻度、中度或重度[8]。
2. 不适症状消退时间
比较2组OHSS患者住院时间和不适症状消退时间。不适症状包括腹水、腹胀、腹泻、腹部不适、轻度恶心呕吐、严重呼吸困难、晕厥等[7]。
3. 抑郁、焦虑状态评价
分别在取卵前和治疗后采用汉密尔顿抑郁量表(HAMD)和Zung焦虑自评量表(SAS)评分评估2组患者的抑郁、焦虑状态[9-10]。HAMD评估项目共涉及24项,总分能较好地反映抑郁症状的严重程度,病情愈重,总分愈高。分别为正常(<8分)、可能有抑郁症(8~20分)、可确诊为抑郁症(21~35分)、严重抑郁症(> 35分)。SAS广泛应用于个人的心理保健和心理健康状况监测,按症状频度分为4级评分,评定结束后,将各项目中的各项分数相加后乘以1.25,得到标准分。SAS标准分的分界值为50分,其中50~59分为轻度焦虑、60~69分为中度焦虑、≥70分为重度焦虑。
4. 康复满意度
采用我院自行设计的康复满意度调查问卷评价康复满意度,内容包括服务态度、专业技能、科室环境、宣传教育、心理指导等5方面,该问卷Cronbachs α系数为0.85,重测效度为0.86。最后统计问卷总分,其中< 70分为不满意、70~90分为基本满意、≥90分为非常满意。
四、统计学处理
采用SPSS 25.0 软件进行统计学分析,计量资料采用 Shapiro-Wilk 进行正态性检验,对满足正态分布的计量资料以表示,组内干预前后比較采用配对t检验,组间比较用两独立样本t检验;不满足正态分布用M(P25,P75)描述,采用基于秩次的非参数检验;计数资料以例(%)表示,采用 2检验。P < 0.05为差异有统计学意义。
结果
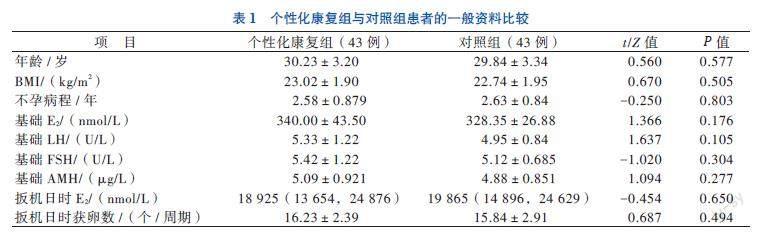
一、个性化康复组与对照组患者的一般资料比较
2组患者的年龄、BMI、不孕病程、基础E2、基础LH、基础卵泡刺激素(FSH)、基础AMH等比较差异均无统计学意义(均> 0.05)。见表1。
二、个性化康复组与对照组患者的OHSS发生情况比较
个性化康复组43例中,发生轻度、中度、重度OHSS分别有2例(5%)、1例(2%)、2例(5%),OHSS总发生率为12%。对照组43例中,发生轻度、中度、重度OHSS分别有6例(14%)、4例(9%)、3例(7%),OHSS总发生率为30%。2组OHSS总发生率比较差异有统计学意义( 2=
4.497,P = 0.034)。
三、个性化康复组与对照组OHSS患者的住院时间及不适症状消退时间比较
个性化康复组5例OHSS患者的住院时间和不适症状消退时间分别为8(6.5,8.5)d和(6.80±
0.87)d,对照组13例患者的住院时间和不适症状消退时间分别为10.0(9.5,13.0)d和(9.92±
1.44)d。对照组的住院时间(Z=-3.094,P=0.002)和不适症状消退时间(t=-4.509,P < 0.001)均长于个性化康复组。
四、个性化康复组与对照组患者干预前后抑郁和焦虑评分比较
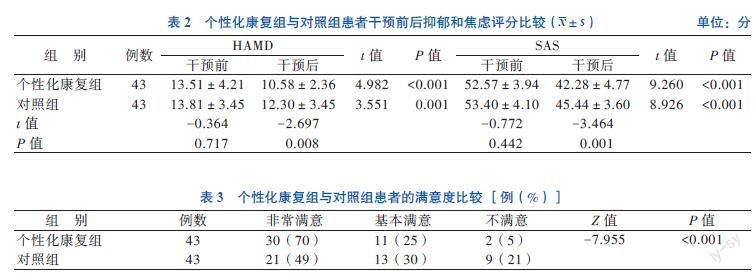
干预前,2组患者的HAMD和SAS评分比较差异无统计学意义(P均>0.05)。干预后,2组患者HAMD和SAS评分均较干预前降低(P < 0.05),且个性化康复组改善情况优于对照组(P均< 0.05)。
见表2。
五、个性化康复组与对照组患者的满意度
比较
2组的满意度比较差异有统计学意义(P < 0.001),其中个性化康复组非常满意者的比例高于对照组。见表3。
讨论
OHSS是辅助生殖技术促排卵过程中最常见的并发症,可增加周期取消率、降低周期妊娠率、延长患者治疗时间,严重者可致胸腔积液、急性肾衰竭和静脉血栓栓塞,甚至危及患者生命[4]。随着接受辅助生殖技术的人数增多,OHSS早期预防和干预越来越受到关注[5]。
2016年,美国生殖医学协会实践委员会在指南中推荐使用 GnRH-A方案降低 OHSS 发生(A 级证据)[4]。Mills等[11]也报道了使用GnRH-A可降低中度和重度OHSS的发生风险,并认为其机制或与降低VEGF的产生和受体反应,从而降低血管通透性有关。虽然目前GnRH-A起效的确切机制尚不清楚,但多数研究公认与GnRH-A降低血清VEGF水平有关[12]。本研究的OHSS发生率与Mills等[11]和Kadoura等[13]的报道一致,或可为GnRH-A的临床应用提供依据。
快速康复外科是强调以患者为中心,为加快手术患者术后恢复、减少术后并发症的发生、降低病死率以及缩短住院时间而采取的一系列围术期多学科措施,主要目的是尽可能降低手术对患者引起的应激反应,促进快速康复[14]。本研究基于前期文献报道的OHSS预防和治疗措施,在就诊时筛查和评估患者OHSS风险,干预过程中通过GnRH-A方案联合个性化一对一心理康复治疗及饮食营养干预等多学科协作,达到减少OHSS、缩短住院时间及促进康复的目的。辅助生殖这一特殊群体在术前、术后及家庭生活中普遍经历不同程度的负面情绪,极易受周围环境的影响,影响妊娠结局。此外,本研究以患者为中心,注重患者自尊和社会满足感,针对患者不同文化水平及疾病认知情况,进行针对性的康复管理与宣教,指导患者认识体外生殖辅助技术与OHSS,掌握自我体位、作息行为、活动运动的适宜方法,培养健康的长期生活习惯;同时基于患者平素饮食与作息习惯,对患者进行营养筛查与评估,由营养师制订适宜的饮食计划[15]。Hubka等[16]认为,缺乏白蛋白是造成OHSS的原因之一,对于部分重度OHSS患者,可通过静脉输注白蛋白来补充集体所需, 但白蛋白可能带来过敏反应且价格较贵, 造成患者的生理及经济负担。因此其推荐低钠饮食、高蛋白饮食作为OHSS的常规疗法。
OHSS高危患者普遍存在心理障碍,常表现出自卑、沮丧、愧疚等不良心态,心理状况差,降低治疗依从性[17]。本研究中,个性化康复组加强对患者精神与心理管理,掌握患者心理变化过程并提供心理疏导,帮助患者消除紧张、恐惧及悲观心理,树立治疗自信心;同时,增加了家属沟通与监督,鼓励家属对患者的情绪理解与关心,让患者最大程度感受家庭的温暖,增强内心安全感,有利于病情的改善。干预后,个性化康复组患者的焦虑、抑郁症状比对照组均有明显改善。
本研究也存在局限性:首先,样本量较少,仅纳入在本生殖中心就诊并筛查为OHSS高风险的患者,未来或需要联合多中心进一步扩大样本量验证疗效。其次,本研究仅观察OHSS发生率,而对于远期妊娠成功率的关注不足。最后,研究仅从拮抗剂方案联合康复角度进行观察,在未来的研究中将考虑激动剂长方案进行个性化康复治疗。
综上所述,OHSS 是促排卵过程中难以完全避免的并发症,应提高警惕性,关注高危人群的识别、采取各种措施及早预防尤为重要。GnRH-A联合个性化康复方案能有效预防OHSS的发生率,缩短OHSS患者住院时间和不适症状消退时间,减轻患者焦虑及抑郁情绪,提高患者满意度。
参 考 文 献
[1] Ovarian Stimulation T E G G O, Bosch E, Broer S, et al. ESHRE guideline: ovarian stimulation for IVF/ICSI. Hum Reprod Open, 2020, 2020(2): hoaa009.
[2] Schirmer D A, Kulkarni A D, Zhang Y, et al. Ovarian hyperstimulation syndrome after assisted reproductive technologies: trends, predictors, and pregnancy outcomes. Fertil Steril, 2020, 114(3): 567-578.
[3] Huang K, Shi Y, Chen G, et al. Predictive factors for recovery time in conceived women suffering from moderate to severe ovarian hyperstimulation syndrome. Front Endocrinol (Lausanne), 2022, 13: 870008.
[4] Practice Committee of the American Society for Reproductive Medicine Electronic address: ASRM@asrm org, Practice Committee of the American Society for Reproductive Medicine. Prevention and treatment of moderate and severe ovarian hyperstimulation syndrome: a guideline. Fertil Steril, 2016, 106(7): 1634-1647.
[5] 劉国成, 蔺莉. 产科快速康复临床路径专家共识. 现代妇产科进展, 2020, 29(8): 561-567.
[6] Nelson S M. Prevention and management of ovarian hyperstimulation syndrome. Thromb Res, 2017, 151(Suppl 1): S61-S64.
[7] Namavar Jahromi B, Parsanezhad M E, Shomali Z, et al. Ovarian hyperstimulation syndrome: a narrative review of its pathophysiology, risk factors, prevention, classification, and management. Iran J Med Sci, 2018, 43(3): 248-260.
[8] 刘风华, 杨业洲, 张松英, 等. 辅助生殖技术并发症诊断及处理共识. 生殖与避孕, 2015, 35(7): 431-439.
[9] 丽扎·满苏尔, 罗晓, 巴哈古丽·阿尔斯朗, 等. 汉密尔顿抑郁量表维吾尔语版本的一致性检验. 中国现代医生, 2017, 55(13): 79-81, 84.
[10] Dunstan D A, Scott N. Norms for Zungs self-rating anxiety scale. BMC Psychiatry, 2020, 20(1): 90.
[11] Mills G, Dahan M H. Gonadotropin releasing hormone (GnRH) antagonist administration to decrease the risk of ovarian hyperstimulation syndrome in GnRH agonist cycles triggered with human chorionic gonadotropin. Arch Gynecol Obstet, 2022, 306(5): 1731-1737.
[12] Luo J, Qi Q, Chen Y, et al. Effect of GnRH-antagonist, mifepristone and letrozole on preventing ovarian hyperstimulation syndrome in rat model. Reprod BioMedicine Online, 2021, 42(2): 291-300.
[13] Kadoura S, Alhalabi M, Nattouf A H. Conventional GnRH antagonist protocols versus long GnRH agonist protocol in IVF/ICSI cycles of polycystic ovary syndrome women: a systematic review and meta-analysis. Sci Rep, 2022, 12: 4456.
[14] Scheib S A, Thomassee M, Kenner J L. Enhanced recovery after surgery in gynecology: a review of the literature. J Minim Invasive Gynecol, 2019, 26(2): 327-343.
[15] 中华医学会妇产科学分会内分泌学组及指南专家组. 多囊卵巢综合征中国诊疗指南. 中华妇产科杂志, 2018, 53(1): 2-6.
[16] Hubka P, Vi?ňová H, Sehnal B, et al. Current possibilities in the prevention and therapy of ovarian hyperstimulation syndrome. Ceska Gynekol, 2021, 86(2): 124-127.
[17] Petrenko A P, Castelo-Branco C, Marshalov D V, et al. Ovarian hyperstimulation syndrome: a new look at an old problem. Gynecol Endocrinol, 2019, 35(8): 651-656.
(收稿日期:2023-06-06)
(本文编辑:林燕薇)

