替雷利珠单抗联合DP 化疗方案治疗晚期肺癌的临床效果及对免疫功能的影响
程家松
(鄱阳湖医院肿瘤科,江西 鄱阳 333100)
肺癌(lung cancer)是临床常见的恶性肿瘤,临床通常需要采用化疗、放疗等方式控制肿瘤病灶进展[1]。DP 化疗方案是晚期(Ⅲ~Ⅳ)肺癌的一线方法,可通过化疗杀灭癌细胞,但是也会对正常机体组织细胞产生一定损伤,从而导致患者出现白细胞减少、耐药等现象,影响临床化疗疗效[2,3]。随着临床对肺癌发病机制的不断深入研究,认为PD-1 信号通路与肿瘤细胞生长具有密切的关系[4]。替雷利珠单抗是一种新型PD-1 抑制剂,但是其与化疗联合应用方面的研究较少,与单独化疗治疗效果方面的对比研究更是存在差异[5]。本研究结合2020 年1 月-2021 年9 月我院接诊的60 例晚期肺癌患者临床资料,观察替雷利珠单抗联合DP 化疗方案治疗晚期肺癌的疗效及对免疫功能的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2020 年1 月-2021 年9 月鄱阳湖医院接诊的60 例晚期肺癌患者为研究对象,采用随机数字表法分为对照组和观察组,各30 例。对照组男17 例,女13 例;年龄45~69 岁,平均年龄(54.18±2.09)岁。观察组男20 例,女10 例;年龄44~70 岁,平均年龄(54.34±1.87)岁。两组性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。本研究患者自愿参加本研究,并签署知情同意书。
1.2 纳入和排除标准 纳入标准:①均符合肺癌临床诊断标准[6];②肿瘤分期均为晚期患者[7];③均经病理诊断确诊[8]。排除标准:①研究药物过敏者[9];②合并其他恶性肿瘤者;③合并严重肝肾功能不全者。
1.3 方法
1.3.1 对照组 应用DP 化疗方案治疗:第1 天将顺铂(云南植物药业有限公司,国药准字H53021741,规格:6 ml∶30 mg)75 mg/m2加入250 ml 的0.9%的氯化钠注射液中静滴;同时将多西他赛(齐鲁制药有限公司,国药准字H20031244,规格:0.5 ml∶20 mg)75 mg/m2加入250 ml 的0.9%的氯化钠注射中静滴,每3 周1 次,连续治疗3 个周期。
1.3.2 观察组 在对照组基础上联合替雷利珠单抗注射液(勃林格殷格翰生物药业<中国>有限公司,国药准字S20190045,规格:10 ml∶100 mg)治疗,每次将200 mg 替雷利珠单抗注射液加入200 ml 的0.9%氯化钠注射中静滴,每3 周1 次,疗程同对照组一致。
1.4 观察指标 比较两组近期疗效、免疫功能指标(CD3+、CD4+、CD4+/CD8+)、血清肿瘤标志物[癌胚抗原(CEA)、糖抗原125(CA125)]、毒副反应(白细胞减少、恶心呕吐、脱发、骨髓抑制)、生存期(治疗后1年,电话随访)。近期疗效[10,11]:①完全缓解:影像学检查病灶完全消失,且持续时间大于1 个月;②部分缓解:病灶体积减小50%及以上,且持续时间大于1 个月;③稳定:瘤体体积减小小于50%,增长小于25%,且持续保持1 个月以上;④进展:病灶体积增长大于25%。客观缓解率=(完全缓解+部分缓解)/总例数×100%;疾病控制率=(完全缓解+部分缓解+稳定)/总例数×100%。
1.5 统计学方法 采用统计软件包SPSS 21.0 版本对本研究数据进行处理,计量资料以(±s)表示,行t检验;计数资料以[n(%)]表示,行χ2检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组客观缓解率、疾病控制率均高于对照组(P<0.05),见表1。
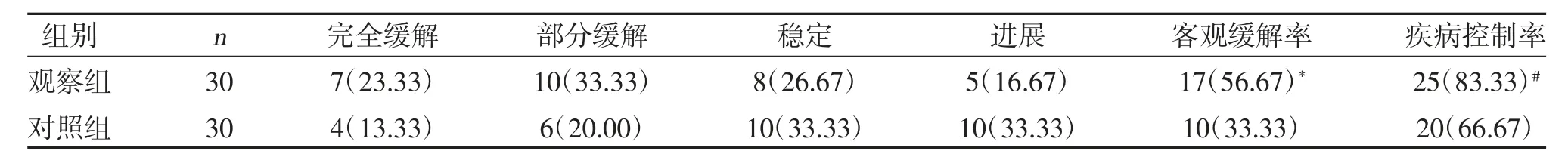
表1 两组临床疗效比较[n(%)]
2.2 两组免疫功能指标比较 两组治疗后CD3+、CD4+、CD4+/CD8+均高于治疗前,且观察组高于对照组(P<0.05),见表2。
表2 两组免疫功能指标比较(±s)
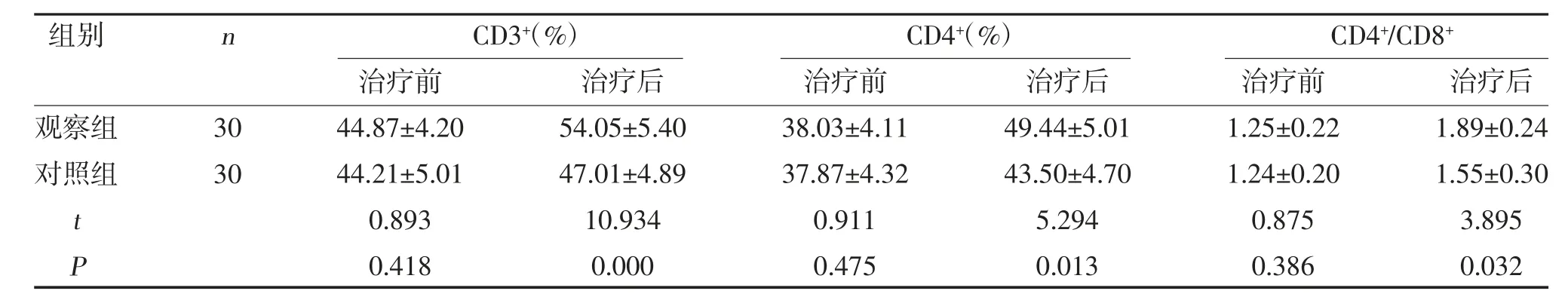
表2 两组免疫功能指标比较(±s)
2.3 两组血清肿瘤标志物水平比较 两组治疗后CEA、CA125 水平低于治疗前,且观察组低于对照组(P<0.05),见表3。
表3 两组血清肿瘤标志物水平比较(±s)

表3 两组血清肿瘤标志物水平比较(±s)
2.4 两组毒副反应发生情况比较 观察组白细胞减少、恶心呕吐、脱发、骨髓抑制发生率与对照组比较,差异无统计学意义(P>0.05),见表4。
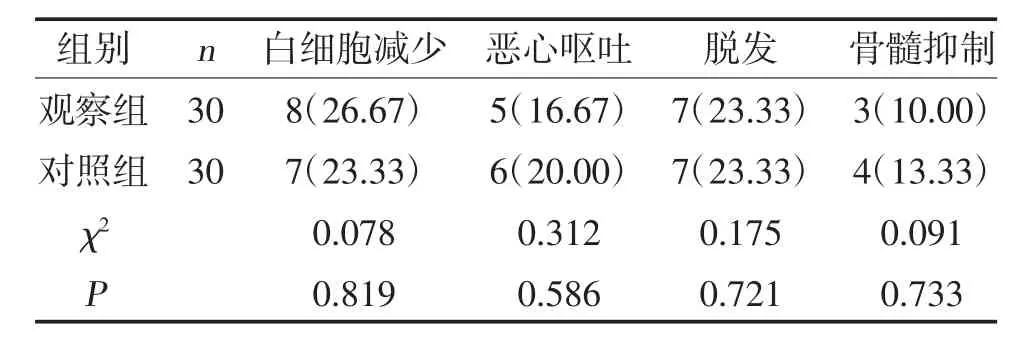
表4 两组毒副反应发生情况比较[n(%)]
2.5 两组生存期比较 随访1 年,观察组平均生存期为(11.29±2.01)个月,大于对照组的(6.02±1.87)个月,差异有统计学意义(t=4.895,P=0.025)。
3 讨论
肺癌早期缺乏特异性症状,多数患者确诊时已处于中晚期,失去手术治疗时机[12]。临床无特效治疗药物,而化疗是目前晚期肺癌治疗的主要方式,其中DP 化疗(顺铂+多西他赛)是临床常用化疗方法,可抑制肿瘤DNA 复制,控制肿瘤进展,但是对患者生存期无显著改善[13,14]。因此,临床寻找更有效的治疗方案,延长晚期肺癌患者生存期仍然是临床研究的热点问题之一。替雷利珠单抗通过阻断PD-1 与其配体结合,从而抑制了PD-1 信号通路的激活[15]。但替雷利珠单抗联合DP 化疗方案治疗晚期肺癌的有效性、对免疫功能和生存期方面的影响研究无明确定论,尤其是较单纯DP 化疗对晚期肺癌患者的应用有效性、安全性缺乏临床样本研究证实[16]。
本研究结果显示,观察组客观缓解率、疾病控制率均高于对照组(P<0.05),提示与单纯DP 化疗治疗方案比较,替雷利珠单抗联合DP 化疗可有效提高客观缓解率和疾病控制率,一定程度改善近期临床疗效,相对具有更优的应用优势,该结论与叶炳南等[17]的研究基本相似。分析认为,替雷利珠单抗属于人源化重组抗PD-1 单克隆抗体,通过改变机体PD-1 信号通路,从而干扰肿瘤微环境,T 细胞表达的PD-1 受体可与配体结合,抑制T 细胞增殖,激活T 细胞的免疫监视,进而上调内源性抗肿瘤免疫效应,有效抑制肿瘤生长,最终可有效提升临床疗效[18,19]。CD3+、CD4+、CD4+/CD8+均可反映免疫细胞的状态,其水平上升,提示联合治疗方案可增强机体免疫功能,建立机体自身的防御,从而有效抑制肿瘤的生长。本研究结果显示,两组治疗后CD3+、CD4+、CD4+/CD8+均高于治疗前,且观察组高于对照组(P<0.05),表明替雷利珠单抗联合DP 化疗可有效提升患者免疫功能,从而改善机体对肿瘤的抵抗作用。两组治疗后CEA、CA125 水平低于治疗前,且观察组低于对照组(P<0.05),提示在DP 化疗基础上联合应用替雷利珠单抗可降低肿瘤指标水平。究其原因可能是因为替雷利珠单抗的应用可干扰肿瘤细胞增殖,抑制肿瘤细胞的复制,从而有效降低血清肿瘤标志物水平[20]。观察组白细胞减少、恶心呕吐、脱发、骨髓抑制发生率与对照组比较,差异无统计学意义(P>0.05),表明联合替雷利珠单抗治疗不会增加毒副反应,具有良好的应用安全性。因替雷利珠单抗属于非细胞毒性抗肿瘤药物,不会对机体正常细胞组织造成损伤,从而不会增加临床毒副反应[21]。此外,随访1 年,观察组平均生存期大于对照组(P<0.05),提示随访1 年后,DP 化疗基础上联合应用替雷利珠单抗治疗患者生存期相对较长,可见应用替雷利珠单抗联合化疗可一定程度改善晚期肺癌患者生存期,具有良好的临床应用价值。
综上所述,替雷利珠单抗联合DP 化疗方案治疗晚期肺癌具有相对良好的近期疗效,可改善患者免疫功能,降低肿瘤标志物水平,在不增加毒副反应的前提下,可延长患者生存期。

