中国118例颅内静脉窦血栓患者的临床特点及危险因素分析
李 蕾,吴 希,戴 菁,武文漫,丁秋兰,王学锋,3
(1.上海交通大学医学院附属瑞金医院检验科,上海 200025;2.上海交通大学医学院附属瑞金医院医学基因组国家重点实验室上海血液学研究所,上海 200025;3.上海交通大学医学院检验系,上海 200025)
颅内静脉窦血栓形成(cerebral venous sinus thrombosis,CVST)是一种相对少见的缺血性疾病,其是由多种因素引起血液异常凝固在颅内静脉窦内,导致管腔部分或完全阻塞,占所有脑卒中的0.5%~1.0%[1]。该疾病在欧美国家的发病率为(0.5~2.0)/10万,在中东和拉丁美洲等发展中国家的发病率可达7/10 万[2-4],而在某些高危人群中,如孕产妇和使用口服避孕药的育龄期女性,CVST 的发病率可能达到(10~40)/10万[2]。我国针对CVST的大样本研究较少,未获得相关的流行病学数据,但随着临床医师对本病的认识和诊断技术的提高,发现CVST 在中国人群中并不少见,尤其在口服避孕药和围产期女性中更值得重视[5]。
CVST 患者的临床表现多样,其中较常见的表现是头痛,患者还可能出现局灶性神经系统症状,包括偏瘫、失语、感觉丧失、眩晕、癫痫发作和意识丧失等[6],缺乏特异性,极易被漏诊和误诊。早期诊断和治疗可以有效减少CVST 导致的严重神经系统并发症的发生。CVST的诊断主要依赖影像学检查,包括计算机断层扫描(computed tomography,CT)、磁共振静脉成像及数字减影血管造影等。
CVST 的危险因素复杂多样,各种因素导致的遗传性和获得性血液高凝均可能导致CVST 的发生。遗传性高凝状态包括抗凝蛋白[抗凝血酶(antithrombin,AT)、蛋白C(protein C,PC)或蛋白S(protein S,PS)]缺陷症、凝血因子ⅤLeiden突变、凝血酶原G20210A突变等;获得性高凝状态主要包括产科因素、口服避孕药、手术、肿瘤、感染、高同型半胱酸血症和抗磷脂综合征等[2]。国外2 项大样本多中心CVST 队列研究显示,约87%的CVST 患者至少有一种血栓危险因素,约22%的CVST 患者存在遗传性血栓危险因素[6-7]。然而,迄今为止,中国人群的CVST 临床特征和危险因素尚未完全明确。既往认为,遗传性血栓危险因素不是我国CVST 的主要病因,但近年来随着对这类疾病的重视和检测水平的提高,其检出率也逐年增高[5]。因此,本研究拟对中国CVST 患者的临床特征、遗传性和获得性血栓危险因素进行综合分析,旨在为CVST 的病因诊断、预防及治疗提供参考。
1 资料与方法
1.1 临床资料
收集2015年1月至2022年12月期间就诊于上海交通大学医学院附属瑞金医院血栓与止血门诊的患者资料。符合以下所有标准的患者被纳入研究:①符合CVST 诊断标准[5];②经CT、磁共振静脉成像或数字减影血管造影等血管影像学检查确认CVST;③临床资料完整。排除标准为符合以下任意一项者:①既往有脑卒中或脑出血病史;②既往或同时合并其他颅内原发病变,如颅内肿瘤。
本研究最终共纳入118 例CVST 患者(CVST组),包括男性66 例,女性52 例;平均入组年龄为(34.42±11.75)岁,平均CVST 初发年龄为(32.59±12.06)岁;其多来自华东和华南地区,绝大多数为汉族。收集这些患者的临床资料,包括一般资料(姓名、年龄、性别、身高、体重)、现病史(发病时间、临床症状)、既往病史(静脉血栓史、脑卒中病史、肿瘤病史、血液系统疾病、自身免疫病、甲状腺疾病、高血压、糖尿病、心脏病、高脂血症、高同型半胱氨酸血症病史、3 个月内感染史等和个人史(吸烟史、饮酒史、口服避孕药、家族史、月经史、妊娠期和产褥期等)。根据患者年龄、性别和地理区域匹配149 名健康人作为正常对照(对照组),包括男性82 名,女性67 名,平均入组年龄为(32.89±7.42)岁(见表1)。
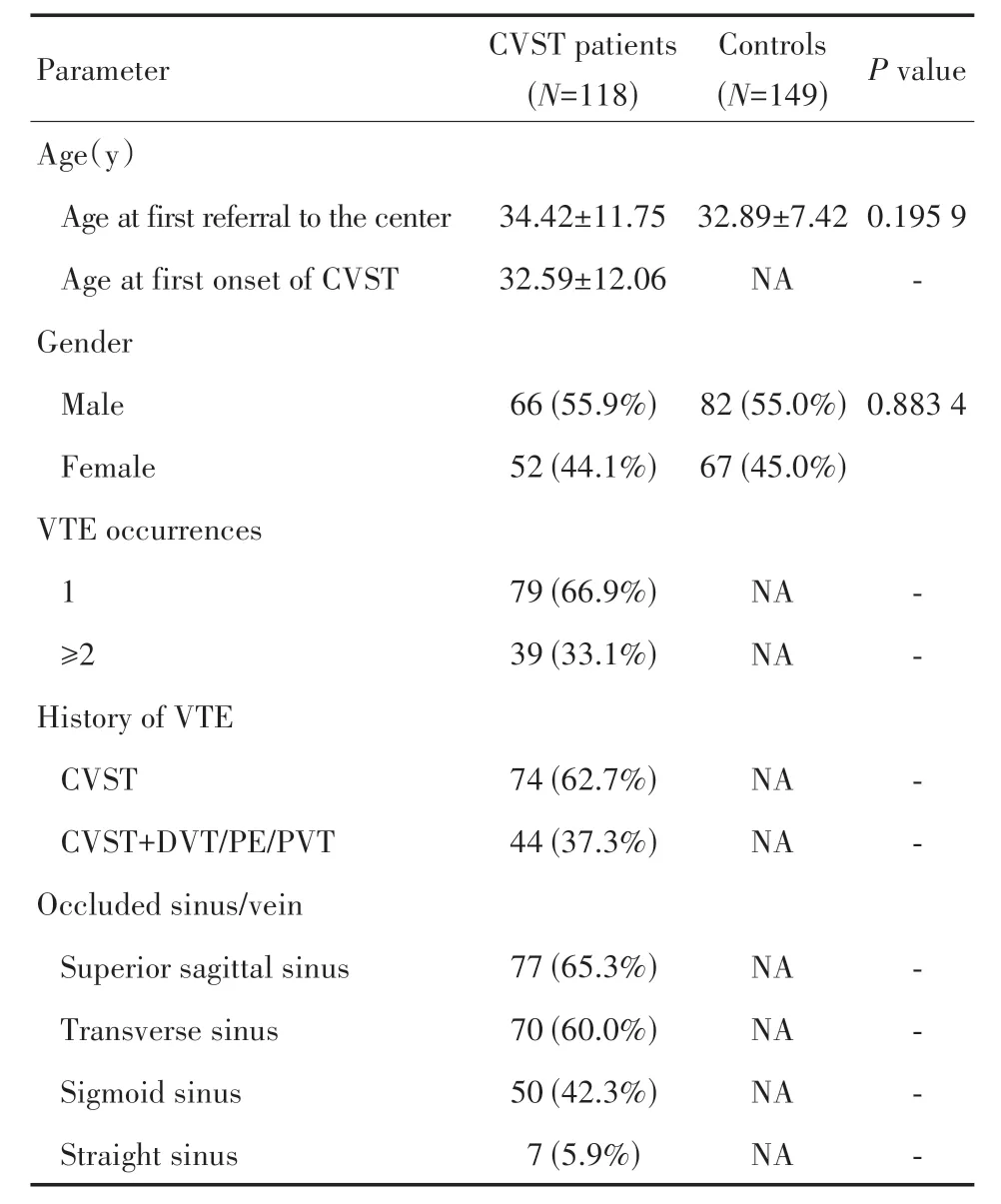
表1 CVST患者及健康对照者的临床特征Table 1 Clinical characteristics of CVST patients and healthy controls
1.2 方法
采用本诊断中心建立的易栓症诊断流程对CVST 组和对照组进行危险因素筛查[8],具体如下。对于非急性期静脉血栓,且未服用口服抗凝药物(>2 周)的患者,进行易栓症表型检测和基因检测;对处于血栓急性期或口服抗凝药物期间,无法进行表型检测的患者,直接进行易栓症基因检测。本研究对所有CVST 患者和健康对照者均进行了易栓症基因检测,其中42 例患者接受了辅助表型筛查。
1.2.1 易栓症的表型检测
采集受试者静脉血,采用ACL-TOP 全自动血凝仪(IL 公司,美国)对血浆中的凝血因子、抗凝蛋白、纤溶蛋白及狼疮抗凝物进行检测[9]。采用贝克曼库尔特AU5800 系列全自动生化分析仪(贝克曼公司,美国),用循环酶法对血清中同型半胱氨酸含量进行检测。采用酶联免疫吸附法对血清中抗心磷脂抗体和抗β2糖蛋白Ⅰ进行测定。
1.2.2 易栓症基因检测
2015 年1 月至2018 年5 月入组的37 例患者,接受了易栓症18 基因的Panel 检测[9];2018 年6 月至2022 年12 月入组的81 例患者,接受了易栓症35 基因Panel 检测[该体系是在原18 基因Panel 的基础上,新增了凝血因子(F13A1、F13B、FGA、FGB、FGG 和vWF)、纤溶相关蛋白(SERPINE1、SERPINF2、PLAT、PLAU 和CPB2)和其他静脉血栓栓塞症(venous thromboembolism, VTE)相关蛋白(JAK2、MPL、CALR、GP6、HABP2 和SERPINA10)检测]。所有健康对照者均接受了易栓症35 基因Panel 检测。突变筛查、验证及生物学分析分析等均参考文献[9]进行操作。
1.3 数据处理
所有数据利用SPSS.26.0 软件进行统计处理。计量资料用均数±标准差描述,2 组间比较采用两独立样本t检验;计数资料用频数(百分比)描述,组间差异用卡方检验或Fisher 精确检验,P<0.05 认为有统计学意义。针对独立危险因素的分析采用单因素和多因素Logistic 回归进行,以α=0.05 为检验水准,将单因素分析中具有统计学意义的变量(P<0.05)以及临床上认为可能会影响结果的变量纳入多因素分析中,同时进行比值比(危险度,odds ratio,OR 值)计算,包含95%置信区间(confidence interval, CI)。针对CVST 发生的危险因素分析在包括对照组和CVST 组的总体数据集中进行,纳入年龄、性别、遗传性危险因素和获得性危险因素为自变量;针对CVST 患者反复血栓及多部位血栓发生的危险因素分析是在CVST 组内进行,纳入CVST初发年龄、性别、遗传性危险因素、获得性危险因素和VTE家族史为自变量。
2 结果
2.1 基本资料(见表1)
118 例CVST 患者中,66.9%(79/118)的患者仅发生过一次VTE,其余33.1%(39/118)的患者发生过至少2 次VTE。62.7%(74/118)的患者血栓部位仅限于CVST,37.3%(44/118)的CVST 患者还曾发生下肢深静脉血栓(deep venous thrombosis,DVT)、肺栓塞(pulmonary embolism,PE)或门静脉系统血栓(portal venous thrombosis,PVT,包含门静脉主干、肠系膜上静脉、肠系膜下静脉或脾静脉的血栓)。研究者对CVST 患者累及的静脉窦位置进行分析后发现,65.3%(77/118)的患者累及上矢状窦,其次为横窦(60.0%,70/118)和乙状窦(42.3%,50/118),另有5.9%(7/118)的患者累及横窦。54.2%(64/118)的患者存在多部位静脉窦同时受累,其中男性患者34例,女性30例。
2.2 CVST患者的血栓危险因素分析
118 例CVST 患者中,70.3%(83/118,包括男性41例、女性42例)的患者存在一个或多个较明确的CVST危险因素(见表2)。

表2 CVST组与健康对照者的血栓危险因素比较a)[n(%)]Table 2 Comparison of risk factors between CVST patients and healthy controls a)[n(%)]
有53.4%(63/118)的CVST 患者携带明确的遗传性血栓危险因素,包括55 例抗凝蛋白缺陷症(22 例PC 缺陷症,16 例PS 缺陷症,12 例AT 缺陷症,2 例AT合并PC缺陷症,3例PS合并PC缺陷症),8 例携带其他血栓相关致病基因突变(如F2基因p.R596Q 突变,JAK2基因p.V617F 突变,MPL基因p.W515K 突变,THBD基因p.R403K 突变等)。健康对照者检出的遗传性危险因素以PC 缺陷症为主,遗传性危险因素检出率显著低于CVST组(5.4%比53.4%,P<0.000 1)。
此外,有32.2%(38/118)的CVST患者携带获得性血栓危险因素,主要包括妊娠及产褥期(11/45,年龄<50 岁的女性)、口服避孕药(5/45,年龄<50 岁的女性)、抗磷脂综合征(6/118)、原发性血小板增多症(5/118)和大型手术(4/118)等,另有存在系统性红斑狼疮、淋巴瘤、甲状腺功能亢进、重度贫血、高同型半胱氨酸、长途飞行和制动因素的患者各1 例。健康对照者检出的获得性危险因素以服用避孕药为主,获得性危险因素检出率显著低于CVST组(4.7%比32.2%,P<0.000 1)。
分析CVST 血栓危险因素的性别分布情况,结果显示,男性患者携带遗传性危险因素的比例与女性患者一致[37/66(56.1%)比26/52(50.0%),P=0.512 3],但男性携带获得性危险因素的比例显著低于女性[10/66(15.2%)比28/52(53.8%),P<0.000 1],这可能与女性特有的产科因素(妊娠期、产褥期和口服避孕药)有关。男性患者主要的危险因素为抗凝蛋白缺陷症(35/66)和抗磷脂综合征(5/66)等,而女性患者的危险因素主要包括抗凝蛋白缺陷症(20/52)、妊娠/产褥期(11/47)及服用避孕药(5/47)等和原发性血小板增多症(5/52)。
2.3 携带血栓危险因素对CVST 患者血栓发生的影响
根据携带血栓危险因素的不同,将CVST 患者分成4 组,38.1%(45/118)的患者携带至少一个遗传性血栓危险因素(组1),16.9%(20/118)的患者携带至少一个获得性血栓危险因素(组2),15.3%(18/118)的患者同时携带遗传性和获得性血栓危险因素(组3),其余29.7%(35/118)的患者未发现明确的血栓危险因素(组4)(见表3)。
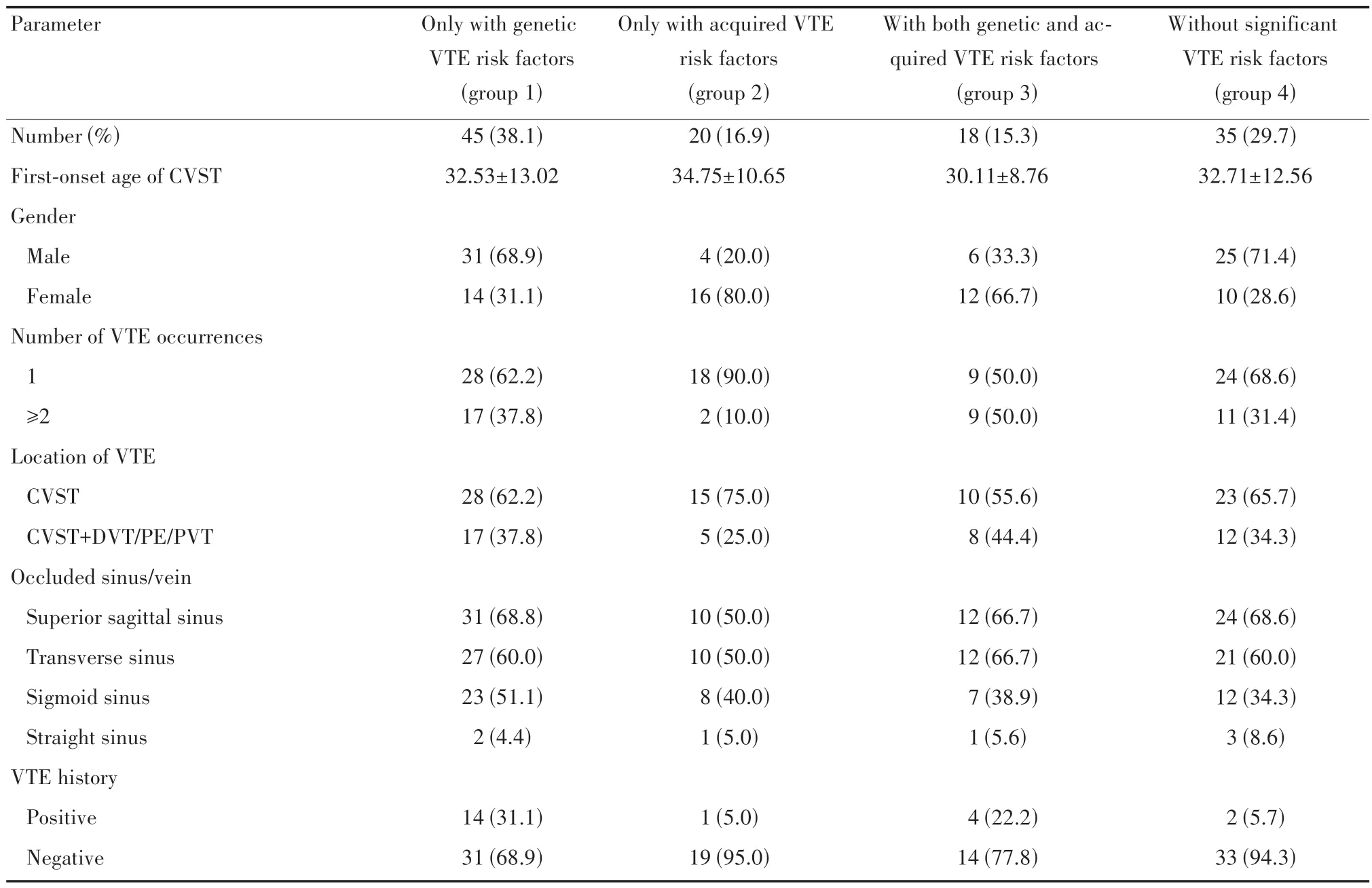
表3 携带血栓危险因素对CVST患者血栓发生的影响比较[n(%)]Table 3 Comparison of the effects of carrying thrombotic risk factors on the occurrence of thrombosis among CVST patients[n(%)]
4 组患者的性别构成有明显差异。携带至少一个遗传性血栓危险因素的患者(组1)中男性与女性的比例为2.2∶1;未发现明确血栓危险因素的患者(组4)中的男女比例为2.5∶1。而携带至少一个获得性血栓危险因素(组2)和同时携带遗传性和获得性血栓危险因素(组3)患者中的男女比例分别为1∶4.0 和1∶2.0,呈现完全相反的趋势,这可能与女性患者特有的产科因素及易发贫血、血小板增多症有关,导致女性携带获得性血栓危险因素的比例较高。
4 组患者间的血栓初发年龄无统计学差异,但同时携带遗传性和获得性血栓危险因素的患者初发CVST 的年龄最早([30.11±8.76)岁],其次为携带遗传性危险因素的患者([32.53±13.02)岁]。与未携带遗传性血栓危险因素的患者(组2 和组4)相比,携带遗传性血栓危险因素的患者(组1 和组3)经历反复VTE 发生的比例明显升高(23.6%比41.3%,P=0.042 2),合并下肢DVT、PE 及PVT 的比例更高(30.9%比39.7%,P=0.320 7),且家族史阳性比例显著升高(5.5%比28.6%,P=0.001 0)。未发现单纯携带获得性血栓危险因素会影响VTE 复发比例和VTE 部位。对4组患者CVST累及的静脉窦位置进行分析后发现,4 组间的静脉窦受累部位不存在统计学差异,受累部位均以上矢状窦和横窦为主,其次是乙状窦和横窦,提示累及静脉窦数量的多少与危险因素无关。
2.4 CVST患者血栓发生的独立危险因素分析
为探究CVST 发生的独立危险因素,首先纳入年龄、性别、遗传性危险因素和获得性危险因素为自变量,采用单因素Logistic 回归分别分析以上自变量与CVST发生间的关系。结果显示,年龄(OR=0.997,95% CI 为0.972~1.022,P=0.807 0)、性别(OR=1.037,95% CI为0.638~1.686,P=0.883 0)与CVST发生不相关,遗传性危险因素(OR=20.189,95% CI 为9.081~44.881,P<0.000 1)、获得性危险因素(OR=9.636,95% CI 为4.113~22.577,P<0.000 1)与CVST发生间具有强相关性(见表4)。进一步行多因素Logistic回归分析,结果显示,遗传性危险因素(OR=21.643,95% CI为9.455~49.544,P<0.000 1)和获得性危险因素(OR=10.836,95% CI 为4.306~27.270,P<0.000 1)是CVST发生的独立危险因素。
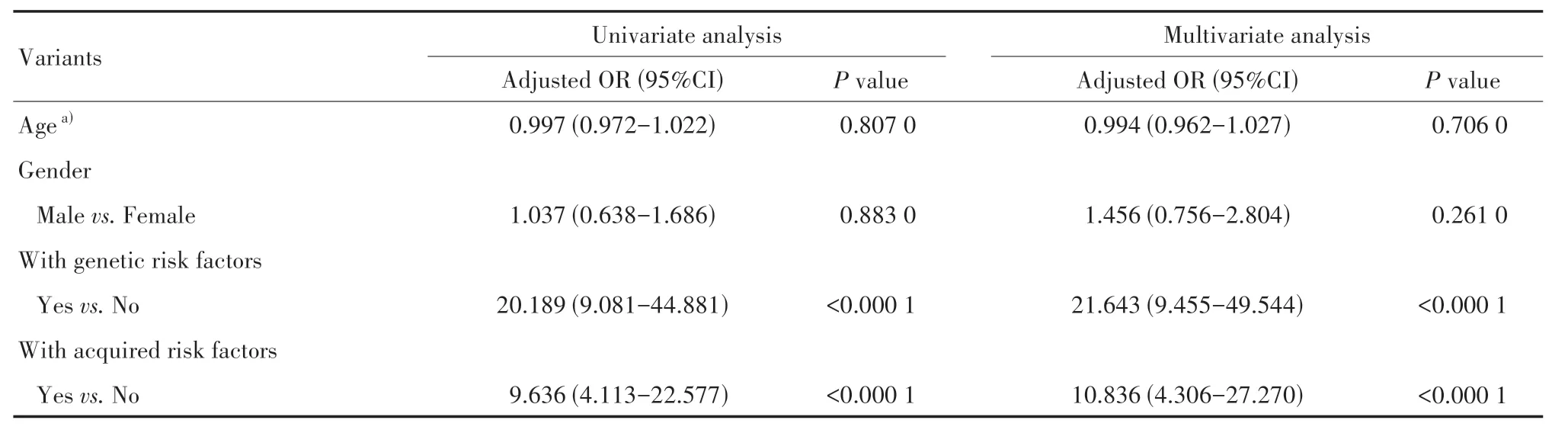
表4 CVST发生的独立危险因素分析Table 4 Analysis of independent risk factors for CVST
为探究CVST 患者反复血栓及多部位血栓发生的独立危险因素(见表5),纳入CVST 发病年龄、性别、遗传性危险因素、获得性危险因素和家族史为自变量,采用单因素Logistic 回归分别分析以上自变量与CVST 患者反复血栓发生间的相关性。结果显示,年龄(OR=0.986,95% CI 为0.954~1.019,P=0.388)、性别(OR=2.158,95% CI 为0.971~4.797,P=0.059)、获得性危险因素(OR=0.757,95% CI 为0.327~1.749,P=0.514)及VTE家族史(OR=1.016,95% CI 为0.373~2.764,P=0.976)与CVST 患者反复血栓发生不相关,遗传性危险因素(OR=2.270,95% CI 为1.021~5.048,P=0.044)与CVST 患者反复血栓发生明显相关。进一步行多因素Logistic 回归分析显示,遗传性危险因素(OR=2.278,95% CI 为1.012~5.129,P=0.047)是CVST 患者反复血栓的独立危险因素。此外,未发现CVST 患者合并其他部位静脉血栓的独立危险因素。
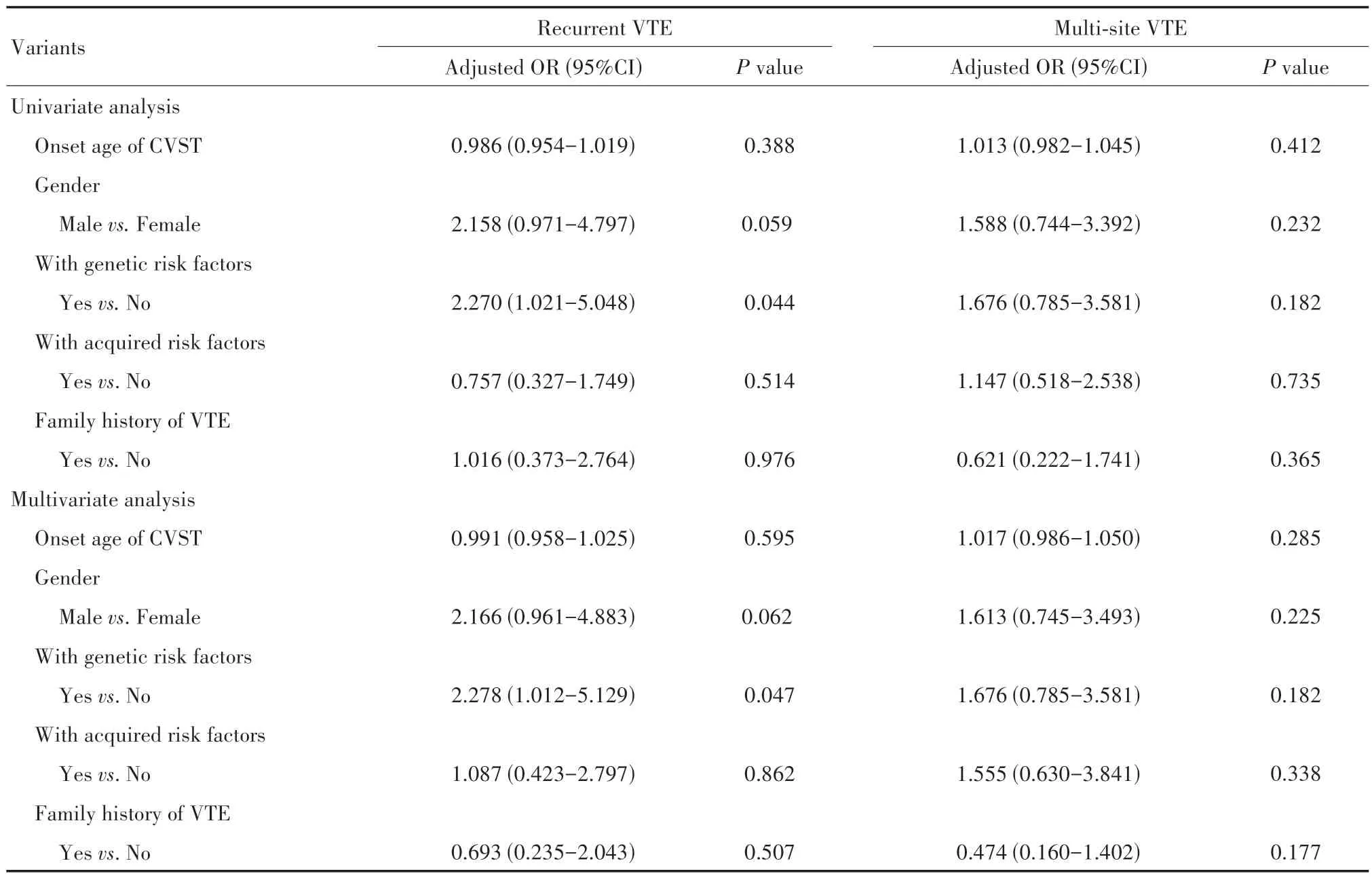
表5 CVST患者血栓复发及多部位血栓形成的独立危险因素分析Table 5 Analysis of independent risk factors for recurrent VTE or multi-site VTE in CVST patients
3 讨论
3.1 中国CVST患者的临床特征
据报道,CVST 好发于中青年期,由于妊娠、围生期和口服避孕药等性别特异性危险因素导致女性比男性高发CVST[10]。本研究中118 例CVST 患者平均初发CVST 年龄为32.59 岁,男、女比例为1.27∶1,该比例与既往国内的研究结果(男∶女=1.4∶1)较为接近[11-13],但与国外报道的性别比例[男∶女=1∶(2.7~2.9)]存在倒置[6-7]。其原因之一,可能与中国女性更少使用口服避孕药及妊娠保健意识的进步有关;原因之二,可能是单中心回顾性研究带来选择性偏倚。本研究入组的CVST 患者大多数是经基层医院的临床医师评估后,认为其高度可能存在易栓倾向[14],为明确病因推荐其前来我院血栓与止血门诊就诊,因男性易栓症患者发生静脉血栓的风险是女性1.4 倍,且血栓复发的风险也比女性高2.7 倍,所以可能导致男性血栓患者的入组比例高于真实世界。
与既往仅纳入初发型CVST 患者的研究相比[11-13],本研究首次探讨了CVST 患者发生反复血栓或其他部位血栓的临床特征,结果显示,62.7%的患者仅发生过CVST,33.1%的患者曾经历至少2 次静脉血栓事件(2 次血栓事件间至少间隔3 个月),37.3%的患者除CVST 外还发生过其他部位的静脉血栓。本研究发现,携带遗传性危险因素的CVST 患者复发VTE 风险增加2.278 倍(95% CI 为1.012~5.129),因此在治疗血栓过程中,要将血栓诱因一同筛查并按照检测结果制定个体化的治疗方案,避免发生血栓复发或其他部位同时再发血栓。
3.2 中国CVST患者的危险因素特征
本研究中,70.3%的患者存在一个或多个明确的CVST 危险因素,其中,遗传性危险因素是我国CVST 患者的主要病因,在53.3%的CVST 患者中检出了遗传性危险因素,明显高于国外报道的22%的遗传性危险因素检出率[6-7]。本研究发现,遗传性危险因素和获得性危险因素均为CVST发生的独立危险因素,可导致CVST风险增加21.643倍(95% CI 为9.455~49.544)和10.836 倍(95% CI 为4.306~27.270)。男性患者中更常见的血栓危险因素是抗凝蛋白缺陷症和抗磷脂综合征,女性患者中更常见的是抗凝蛋白缺陷症、妊娠期/产褥期、口服避孕药和原发性血小板增多症。2019 年,北京宣武医院对243 例CVST 患者进行回顾性研究,发现女性患者中最常见的获得性危险因素是产科因素(19.8%),而男性患者中最常见的危险因素是高同型半胱氨酸血症(22.3%)[15],但该研究并未对遗传性因素进行分析。本研究中24.4%(11/45)的女性携带产科因素,接近既往研究结果,但本研究中男性高同型半胱氨酸血症的检出率约为1.5%(1/66),这可能与北京上海两地高同型半胱氨酸血症发病率有显著差异有关[16]。女性妊娠/产褥期高发CVST的原因可能与妊娠期凝血系统改变、血液动力学改变及大脑静脉结构和功能的改变有关[17-18];而产后出血或补液不当导致的脱水使血液浓缩,加上产后卧床休息和坐位母乳喂养引起的静脉血流缓慢,更容易发生CVST,因此临床医师对于女性易栓症患者应提高妊娠/产褥期CVST预防和管理的意识。
3.3 遗传性易栓症是中国CVST 患者的主要危险因素
国外的大型CVST 病例研究结果显示,约22%的CVST 患者携带至少一个遗传性危险因素,主要包括凝血因子Ⅴ基因Leiden 突变,凝血酶原基因G20210A 突变和抗凝蛋白缺陷症[6-7]。既往国内的各项CVST 病例研究由于缺乏完整的遗传性血栓形成评估,未明确中国人群遗传性易栓症与CVST发病间的关系[15,19]。本研究率先对CVST 患者进行易栓症基因Panel筛查,在53.4%的CVST 患者中检出遗传性血栓危险因素。抗凝蛋白缺陷是中国人群最主要的遗传性血栓危险因素[20-22],共有46.6%(55/118)的CVST 患者经基因检测结合表型检测被诊断为抗凝蛋白缺陷症。检出率最高的抗凝蛋白基因突变为PROC基因p.192del 突变(15/118),另有3例患者分别检出PROC基因p.F181V和p.R189W突变,以上突变均为亚洲人群的蛋白C 热点突变[23-24]。另有6.8%(8/118)的CVST 患者携带其他血栓相关基因突变,其中JAK2基因p.V617F 突变的检出率最高,有5.1%(6/118)的CVST患者携带该突变,而JAK2突变在我国普通人群中的检出率约为1%[25]。已有研究表明,JAK2基因p.V617F 突变可能促进白细胞和血小板活化,常见于真性红细胞增多症和原发性血小板增多症患者,与动脉及静脉血栓栓塞发生有关[26]。
本研究中CVST 患者遗传性危险因素的检出率明显高于此前国外的2 项CVST 大样本研究[6-7],这可能与遗传性易栓症的筛查手段不同有关,国外研究仅对凝血因子Ⅴ和凝血酶原进行基因检测,对抗凝蛋白仅通过表型检测筛查是否存在缺陷。但抗凝蛋白表型诊断有诸多局限性,当患者处于血栓急性期、妊娠/产褥期或口服抗凝药物期间,会影响检测结果的准确性,且表型检测由于方法学上的局限性,很难反映被检蛋白的真实水平[9],仅依赖实验室表型检测进行诊断容易造成漏诊。本研究采用的易栓症基因Panel不受患者生理病理状态及药物的影响,可较为全面、准确地筛查易栓症的分子病因,结合实验室表型检测,可以有效提高遗传性易栓症的检出率[9]。
综上所述,我国的CVST 患者发病多为中青年时期,70.3%的患者至少携带一个较明确的血栓危险因素,遗传性危险因素是主要病因,检出率达53.3%,明显高于国外报道的22%的遗传性危险因素检出率。携带遗传性危险因素的患者发生CVST或反复静脉血栓的风险显著升高,而通过基因检测及实验室检测加强血栓危险因素的早期识别,针对CVST 高风险人群做到早预防、早诊断、早治疗,可最大限度地降低CVST的致残率和病死率。
利益冲突说明/Conflict of Interests
所有作者声明不存在利益冲突。
伦理批准及知情同意/Ethics Approval and Patient Consent
本研究通过上海交通大学医学院附属瑞金医院伦理委员会批准(伦理号2019-54)。本研究纳入的所有患者,其本人或家属均签署了知情同意书。
作者贡献/Authors’Contributions
李蕾收集资料,撰写论文;吴希、戴菁审核并统计数据,丁秋兰进行研究概念设计,武文漫对文章的知识性内容进行修订;王学锋指导写作并行最后审阅和定稿。

