超临界二氧化碳物性参数综述
庄正杰,李 明,张立清,肖 民
(酒泉卫星发射中心,甘肃 酒泉 732750)
1 前 言
超临界流体(Supercritical fluids)是指温度和压力同时高于其临界值的流体,其物理性质相对于气体和液体而言较为独特,密度接近于液体,同时黏度和扩散系数接近气体,因此不仅具有与液体溶剂相当的溶解和萃取能力,而且在化学反应与分离过程中传质速率也远大于处在液态下的速率。超临界流体中最常使用的流体是超临界水和超临界二氧化碳(Supercritical carbon dioxide,以下简称SC-CO2),其中SC-CO2是目前选用最多、用途最广的超临界流体,在物质萃取、材料清洗、汽车空调、材料染色、钻井采油等领域有较多应用,受到国内外学者的广泛关注[1-4]。
CO2的临界温度为31.05℃,临界压力为7.38 MPa,临界条件相对温和,相对于其他物质而言,其超临界条件比较容易达到。在临界区附近CO2对温度和压力的变化异常敏感,随着温度和压力的微小波动,物性参数会发生较大幅度的非线性变化,给SC-CO2物性参数预测带来较大难度,在一定程度上制约了工程上的应用及应用场景的拓展。
本文数据来源于美国国家标准与技术研究院开发的物性参数查询数据库软件REFPROP,据此进行性质分析。
2 SC-CO2物性参数
2.1 密度
SC-CO2的许多独特性质都源于密度对压力的高敏感性。密度是SC-CO2最重要的物性参数之一,根据数据库中CO2密度数据,绘制CO2密度随温度及压力在一定范围内的变化曲线,分析其变化规律。
2.1.1CO2密度随温度变化规律
如图1(a)不同压力下CO2密度随温度变化曲线所示,在CO2压力<临界压力时(如5 MPa),随着温度的升高,密度曲线在温度为10~20℃的范围内陡然降低,CO2密度从830.41 kg/m3降到154.12 kg/m3,这是因为此时CO2的相态发生了突变,由液态转化为气态。与液态相比,进入气态后,密度随着温度的升高而降低的幅度减小。

a. 不同压力下,CO2密度随温度变化曲线;b. 临界点附近CO2密度随温度变化曲线
在临界点附近,随着温度升高到临界温度,CO2密度会急剧减小。然而,如图1(b)临界点附近CO2密度随温度变化曲线所示,不同于CO2压力<临界压力(如7 MPa)的情形,当压力处于近临界区(如8 MPa)时,CO2密度的降低呈连续的变化。
在超临界区,当压力远高于临界压力(>30 MPa)时,CO2密度随着温度的增加而连续、缓慢的减小,没有发生急剧变化;从图1(a)中可以看出,压力越大,CO2密度随温度变化越缓慢,直至接近于线性变化。
2.1.2CO2密度随压力变化规律
如图2(a)不同温度下CO2密度随压力变化曲线所示,在CO2温度低于临界温度时(如10℃),压力较低的CO2处于气体状态,密度较小。随着压力的增加,当压力>CO2饱和蒸气压时,气态CO2变为液态CO2,导致其密度突然变大。当温度高于临界温度时,CO2的密度快速增加。
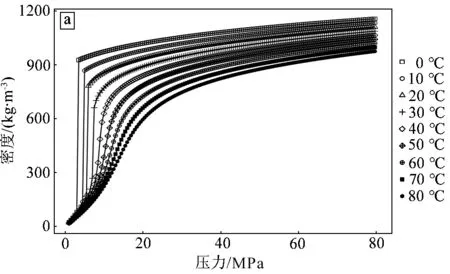
a. 不同温度下,CO2密度随压力变化曲线;b. 临界点附近CO2密度随压力变化曲线
在临界点附近,随着压力增加到临界压力,CO2密度急剧增加,如图2(b)临界点附近CO2密度随压力变化曲线所示。当温度<临界温度时,由相变引起的CO2密度的急剧增加是不连续的;当温度>临界温度时,温度越高,密度随压力变化的增加曲线越平缓,增速降低,增加到同一密度(例如800 kg/m3)所需要的压力区间逐渐变大。
总之,在临界点附近,SC-CO2的密度对温度和压力的变化灵敏度高,这也是SC-CO2应用中经常使用的操作条件。尤其在近临界区,压力或温度的微小变化都会导致SC-CO2密度显著的变化,从而使溶质在流体中的溶解度也产生显著的变化,这也为SC-CO2萃取溶解和解析提供了便利条件。
2.2 比热容
比热容是描述物质热力学性质的一个重要参数,根据测定的条件分为定压比热容Cp和定容比热容Cv。根据数据库中CO2比热容数据,分别绘制CO2定压比热容和定容比热容随温度及压力在一定范围内的变化曲线,分析其变化规律。
2.2.1定压比热容
如图3(a)压力一定时CO2定压比热容随温度变化曲线所示,在CO2压力<临界压力时(如5 MPa),随着温度的升高,密度曲线在温度为10~20℃的范围内陡然降低,CO2密度从830.41 kg/m3降到154.12 kg/m3,这是因为此时CO2的相态发生了突变。如图3(a)所示,在一定压力下,CO2的定压比热容随着温度的上升先升高后下降,在某一温度下出现最大值,称该温度为准临界温度,该物性参数点称为准临界点。当温度比准临界温度低时,流体具有“类液体”[5]性质;当温度比准临界温度高时,流体具有“类气体”性质[6-7]。
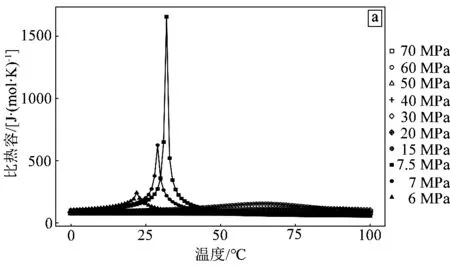
a. 压力一定时,CO2定压比热容随温度变化曲线;b. 临界点附近,CO2定压比热容随温度变化曲线;c. 温度一定时,CO2定压比热容随压力变化曲线;d. 临界点附近,CO2定压比热容随压力变化曲线
压力越高,对应的准临界温度越高。如图3(b)临界点附近CO2定压比热容随温度变化曲线所示,在临界点附近,CO2比热容会急剧升高,且越靠近临界点,CO2的比热容变化越剧烈。例如,压力为7.5 MPa时,CO2比热容峰值明显大于其他压力下比热容峰值,且在临界温度处形成峰值。
考虑不同温度条件对CO2定压比热容的影响,如图3(c)温度一定时CO2定压比热容随压力变化曲线所示,各个温度条件下的CO2比热容在临界压力处会形成最高的峰值。
而在临界点附近,如图3(d)临界点附近CO2定压比热容随压力变化曲线所示,温度为32℃时,CO2比热容在临界压力处形成最高峰,而后随着温度的增加峰值也逐渐变小,且峰值处的压力值也同步在增加。这种现象是由于在临界点附近,体系中分子聚集程度大,而拆散这种“聚集体”的过程为吸热过程[8]。因此,在临界点附近CO2的比热容达到最大值。
2.2.2定容比热容
如图4(a)压力一定时CO2定容比热容随温度变化曲线和4(b)临界点附近CO2定容比热容随温度变化曲线所示,压力一定时,CO2的定容比热容随着温度的增加先增加后减小,并在临界点附近出现峰值。例如,在压力为7.5 MPa时,CO2的定容比热容在临界温度处出现最大峰值,而随着压力的增大,出现峰值的温度值逐渐变大,且峰值逐渐降低;而随着压力的减小则出现峰值向左偏移的类似情形。

a. 压力一定时,CO2定容比热容随温度变化曲线;b. 临界点附近,CO2定容比热容随温度变化曲线;c. 温度一定时,CO2定容比热容随压力变化曲线;d. 临济点附近,CO2定容比热容随压力变化曲线
与之类似,在温度一定时,如图4(c)温度一定时CO2定容比热容随压力变化曲线和4(d)临界点附近CO2定容比热容随压力变化曲线所示,CO2的定容比热容随着压力增加先增加后减小,并在临界点附近出现峰值。且在超临界区,温度越靠近临界温度,比热容峰值越大。
2.2.3定压比热容和定容比热容的比较
保持压力不变,当温度升高时,气体会对外膨胀做功,除温度提升需吸收热量外,还需要热量来补偿气体对外所做的功。因此,对于气体而言定压比热容略大于定容比热容。固体和液体在没有物态变化的情况下其本身体积变化较小,外界提供的热量仅用来改变温度,所以固体和液体的定压比热容和定容比热容的差别较小。
在临界点附近,定压比热容是定容比热容的几百倍,这主要是由于临界点附近CO2的可压缩性很强,当发生相变时,会导致气体体积变化很大,对外做膨胀功较多。液态CO2的定压比热容和定容比热容差别不大,远离近临界的CO2气体,更接近理想气体,其定压比热容和定容比热差别也不大。总之,临界点附近CO2比热容变化剧烈,当远离临界点后,比热容随温度和压力的变化趋势较为缓和。不同压力下比热容变化较大的区间处于不同的温度区域。超临界状态下CO2的热容值与气态CO2的热容值较接近,传热性能较强。
2.3 黏度
当气体受到剪切应力作用而产生相对运动时,气体中任一点的分子都会在自己原有的无规则运动向量上增加一个主体速度向量;由于分子的相互碰撞,使得在整个流体中发生了动量交换,因而主体速度(动量)就产生一定的分布;靠近应力源时,主体速度向量比较大,但随着分子运动而远离应力源时,主体速度在主体流动方向上放慢而引起另一层流体在同一方向上运动,这种无规则分子动量交换就是产生气体黏度的主要原因[9]。
2.3.1黏度随温度变化规律
由图5(a)不同压力下CO2黏度随温度变化曲线可以看出,当压力确定的情况下,增加温度会导致CO2的黏度出现先快速降低后缓慢减小的走向。在温度为0℃和10℃时,各压力状态下的CO2相态均为液态,黏度较高。而p=5 MPa或7 MPa时,在温度为20~30℃范围区间内,黏度会随着温度的升高而快速降低,这是由于CO2由液态转化为气态,相态变化导致了黏度值的急剧降低。随着压力升高,CO2黏度随温度变化越来越平缓,当压力>30 MPa时,CO2黏度随着温度的变化而缓慢降低,接近线性变化。
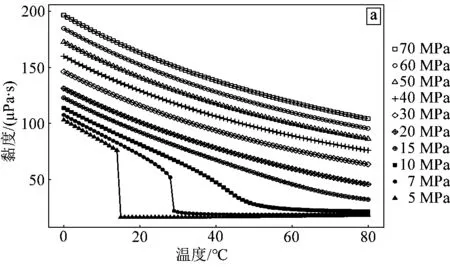
a. 不同压力下,CO2黏度随温度变化曲线;b. 近临界区域CO2黏度随温度变化曲线
在临界点附近,如图5(b)近临界区域CO2黏度随温度变化曲线所示,与密度曲线类似,黏度随温度的升高降低速度变慢。在压力为7.5 MPa、温度为32℃时,CO2黏度仅为26.42 μPa·s;在压力为8 MPa、温度为35℃时,CO2黏度仅为29.84 μPa·s。进入超临界区后,CO2黏度更接近于气体黏度(一般为10~30 μPa·s),而远低于液体的黏度(一般为200~300 μPa·s)[10]。
2.3.2黏度随压力变化规律
在一定的温度条件下,CO2的黏度随压力的增加而增加,如图6(a)不同温度下CO2黏度随压力变化曲线所示。温度较低且压力>CO2饱和蒸气压时,CO2变为液态,使得CO2黏度急剧增大。随着温度升高,CO2黏度随压力增加而变大的速度变慢。

a. 不同温度下,CO2黏度随压力变化曲线;b. 近临界区域CO2黏度随压力变化曲线
近临界点附近CO2黏度随压力变化曲线如图6(b)所示,进入临界区后CO2黏度随压力的变化是连续性变化的,是由连续性相变引起的。在近临界区,CO2黏度都低于80 μPa·s,这也说明了SC-CO2具有良好的传质性能。当CO2温度>临界温度时,压力即使增加到80 MPa,黏度也都在160 μPa·s以下,这是因为CO2处于超临界区时,无论怎样增加压力都不会液化。
2.4 压缩因子
理想气体遵守状态方程(1),但在实际状况下气体的pV虽然不等于nRT,但是如果令z=pV/nRT,则状态方程(2)必然成立,其中z称为压缩因子[11]。
pV=nRT
(1)
pV=znRT
(2)
式中,p为压强,Pa;V为气体体积,m3;n为气体的物质的量,mol;R为摩尔气体常数,J/(mol·K);T为气体温度,K;z为压缩因子。
式(2)中若z>1,则相同的温度和压力条件下实际气体的体积大于等量的理想气体的体积,表明该气体不容易被压缩;若z<1,则相同的温度和压力下实际气体的体积小于等量的理想气体的体积,表明该气体容易被压缩[12]。压缩因子z的大小受气体状态(温度、压力)和气体种类影响,文献[13-14]在研究CO2干气密封时通过实际气体状态方程描述密度与压力、温度之间的关系,其中压缩因子通过维里方程获得,维里方程利用统计力学分析分子间的相互作用力从而获得气体压缩因子如式(3)。
(3)
式中,B为第二维里系数,通过Pitzer方程和Orbey方程[15]可得,如式(4)。
(4)
式中,ε为偏心因子,取值0.225。
图7是CO2压缩因子随压力变化图,可以看到,同等压力下,在温度为-10~70℃的范围内,CO2压缩因子随着温度升高而变大,说明温度更高的CO2更不容易压缩;同等温度下,CO2压缩因子随着压力增加先变小后增加,随着温度升高,压缩因子的最小值出现的压力也变大,在临界条件附近CO2压缩因子只有0.2左右,说明此时的CO2具有很强的可压缩性;压力很小与很大时,CO2压缩因子均接近1,说明在此种条件下CO2更接近理想气体。

图7 CO2压缩因子随压力变化曲线
2.5 导热系数
导热系数是衡量流体分子热能传递能力的物理参数,它与能量的分子传递有关,与黏度、热容也有关系。根据数据库中CO2导热数据,绘制CO2导热系数随温度及压力在一定范围内的变化曲线,分析其变化规律。
2.5.1导热系数随温度变化规律
如图8(a)CO2导热系数随温度变化曲线所示,随着温度的升高,CO2导热系数整体趋于变小,压力越大,变化速度越慢。临界点附近,如图8(b)临界点附近CO2导热系数随温度变化曲线所示,不同于低于或高于临界压力较多时的情形,在压力为7.5 MPa和8 MPa时,导热系数先变大,后变小,有一个明显的拐点,这是近临界CO2特殊的导热性质引起的,说明导热系数在临界点附近随温度和压力变化具有高敏感性。当温度越远离CO2的临界温度时,曲线走势则越平稳。

a. CO2导热系数随温度变化曲线;b. 临界点附近CO2导热系数随温度变化曲线
2.5.2导热系数随压力变化规律
如图9(a)CO2导热系数随压力变化曲线所示,温度不变时,随着压力的增加,CO2导热系数增加,在相态转化区,CO2导热率会急剧升高;在临界压力附近,导热系数会有个明显的拐点,CO2导热系数会达到一个最大值,此时CO2传热能力比较强。

a. CO2导热系数随压力变化曲线;b. 临界点附近CO2导热系数随压力变化曲线
在临界点附近,如图9(b)临界点附近CO2导热系数随压力变化曲线所示,随着温度的升高,CO2导热系数随压力变化趋势变缓慢,结合图9(a)可知,当温度>50℃时,CO2导热系数随着压力增加而缓慢增加,导热系数也不会出现拐点。
总的来说,压力增加、温度降低,CO2的导热系数都将增大。在SC-CO2钻井采油作业中,保证井底的温度和压力对SC-CO2压裂意义重大[16],维持超临界状态可以有较高的导热,有助于SC-CO2与地层热交换。
2.6 表面张力
表面张力存在于液体表面,与液体的类别、液面外物质的类别、温度和纯度有关,影响着相界面的稳定性[17]。由于SC-CO2不存在相界面,因此没有表面张力。图10给出了CO2的表面张力随温度的变化关系曲线[18]。可以看出,随着温度的升高,表面张力逐渐下降,当温度接近CO2临界温度时,表面张力降为零。这使得SC-CO2很容易渗透扩散到溶质微孔内,利于传质速率的提高。
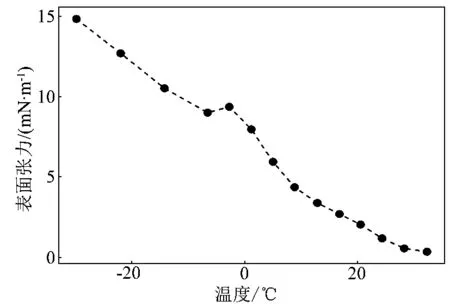
图10 CO2的表面张力随温度的变化曲线
CO2在温度T下的表面张力σ可由公式(5)计算[19]。
σ=0.084 497(1-T/Tc)1.28
(5)
式中,σ为表面张力,N/m;Tc为临界温度,K。
2.7 饱和蒸气压
在密闭条件中,在一定温度下,与液体CO2处于相平衡的蒸气所具有的压力称为液体CO2的饱和蒸气压[20]。如图11所示,CO2在不同温度下有不同的饱和蒸气压,并随着温度的升高而增大。在三相点处,饱和蒸气压为0.52 MPa,在临界温度31.1℃时,饱和蒸气压(即临界压力)为7.38 MPa,温度超过临界点后,CO2变为超临界态,此时,无论怎样施加压力,都不会液化,SC-CO2也就不存在饱和蒸气压的概念。

图11 CO2液态饱和蒸气压图
常用来计算饱和蒸气压的方程为Clapeyron蒸气压方程[21],该方程可由公式(6)表示。
(6)
式中,p为饱和蒸气压,Pa;A、B为与物质有关的常数;T为温度,K。
通过将液体CO2的饱和蒸气压数据带入拟合软件可求得:
A=22.34,B=1987.28
(7)
则液态CO2的Clapeyron饱和蒸气压方程可以表示为:
(8)
若用三次曲线拟合,在-56.6~31.06℃,拟合公式如公式(9)。三次曲线拟合在一定范围内较为准确,但扩展性不如Clapeyron蒸气压方程。
p=-31 318 913.66+450 618.78T
-2239.69T2+3.867T3
(10)
2.8 自扩散系数
自扩散系数是描述传递现象、反映流体传质速率的一个重要参数[22]。如图12(a)所示,CO2的自扩散系数随着温度的升高而增大,且气态CO2的自扩散系数远高于液态CO2。这是由于温度的升高加剧了分子的热运动,使得分子间的距离增大,有利于分子的扩散。另一方面,如图12(b)所示,CO2的自扩散系数随着压力的增大而减小,这是因为压强的增大导致了CO2分子变得更紧密,使得分子之间的碰撞几率增大,阻碍了分子的扩散。图12(a)和图12(b)表明,在临界条件附近,自扩散系数随温度或压力的变化剧烈,表明SC-CO2在临界点附近具有优良的参数敏感性,与SC-CO2的自扩散能力较强的观点[3, 23]相呼应。
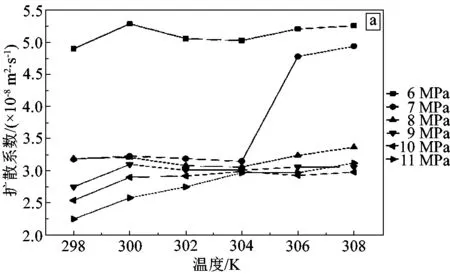
图12 临界点附近CO2自扩散散系数随温度(a)、压力(b)变化曲线
3 结 语
近年来,对SC-CO2的研究越来越多,对其在萃取、印染、传热、钻井采油等诸多领域中的应用进行了探索。作为一种新兴技术,对其基本性质、基础理论仍需加强研究,尤其是对临界点附近的物理性质随温度、压力的变化情况,超临界区的相平衡、传热性质的研究方面仍需进一步探索,同时对于SC-CO2在工业领域的应用而言,其操作条件较难控制,需要进一步提高设备的自动化程度,以便能够更加精准的控制条件参数。随着对SC-CO2性质的深入研究、工业技术的不断发展,SC-CO2的优异性质一定会在工业领域得到充分应用。

