度拉糖肽治疗2型糖尿病的快速卫生技术评估
刘 琛,王 可,董宪喆,张 兰(首都医科大学宣武医院药学部,北京 100053)
近年来,我国2 型糖尿病的患病率不断上升,2015-2017年达到11.2%[1]。2型糖尿病治疗药物种类较多,胰高血糖素样肽-1(glucagon-like peptide,GLP-1)受体激动剂是近年来上市的降糖药物,可促进胰岛素分泌,抑制胰高血糖素分泌,延缓胃排空,并具有中枢性食欲抑制作用[2]。长效GLP-1受体激动剂利拉鲁肽已在临床广泛应用。度拉糖肽作为新近上市的超长效制剂,具有注射次数少、患者依从性高的优势,然而其价格相对较高,需全面评价药物的有效性、安全性和经济性。卫生技术评估(health technology assessment,HTA)利用循证医学和卫生经济学的方法,从有效性、安全性、经济性等方面进行系统评价[3],能够快速整理和评价证据,在决策制定过程中发挥重要作用。本研究针对度拉糖肽治疗2 型糖尿病进行评价,以期帮助医疗机构高效完成药品遴选。
1 资料与方法
1.1 文献检索策略
检索PubMed、Cochrane Library、Web of Science等英文数据库和中国知网、万方、中国生物医学文献服务系统、维普等中文数据库,补充检索英国国家卫生保健服务系统卫生经济评价数据库(National Health Service Economic Evaluation Database,NHSEED)和加拿大药品与卫生技术局(Canadian Agency for Drugs and Technologies in Health,CADTH)等卫生技术评估数据库。检索词:(1)英文数据库:“(dulaglutide)AND (systematic review OR meta analysis OR cost OR economic)”;(2)中文数据库:“度拉糖肽and(系统评价or荟萃分析or meta分析or 成本or经济or费用)”;(3)卫生技术评估数据库:“dulaglutide”。语种:中文和英文。检索时间为建库至2022年12月。
1.2 纳入与排除标准
1.2.1 纳入标准(1)研究人群:年龄≥18岁的2型糖尿病患者。(2)干预措施:度拉糖肽。度拉糖肽药品说明书推荐起始使用0.75 mg,qw。如控制不佳,可将剂量调整为1.5 mg,qw。故将研究中度拉糖肽0.75 mg,qw 定义为低剂量组,1.5 mg,qw 定义为高剂量组。(3)对照措施:目前上市的GLP-1受体激动剂中,利拉鲁肽使用最为广泛,故将利拉鲁肽作为对照措施。利拉鲁肽药品说明书推荐起始使用0.6 mg,qd,一周后加量至1.2 mg,qd作为维持剂量。如控制不佳,可将剂量调整为1.8 mg,qd。故将研究中利拉鲁肽1.2 mg,qd定义为低剂量组,1.8 mg,qd定义为高剂量组。(4)结局指标:①有效性:降低空腹血糖、糖化血红蛋白(HbA1c%)、体质量、血压和血脂;②安全性:全因死亡率、严重不良反应发生率、低血糖事件发生率;呼吸、神经、消化、泌尿、心血管系统不良反应发生率;③经济性:增量成本、增量成本效果比。(5)研究类型:既往发表的HTA报告、系统评价/Meta分析、药物经济学研究。
1.2.2 排除标准(1)非英文/中文的文献;(2)无法获得全文的文献。
1.3 文献筛选
由2 位研究者独立筛选文献,如遇分歧,通过讨论或咨询高级研究者解决。
1.4 数据提取
由2 名研究者独立提取数据,完成数据提取表。数据提取表内容包括研究的作者和发表年限、研究人群的基本特征、样本量大小、干预组和对照组的治疗方案、结局指标和结论等。
1.5 质量评价
采用国际卫生技术评估组织协会制定的HTA checklist 对HTA 报告进行质量评价。采用系统评价评估测量工具(a measurement tool to assess systematic reviews,AMSTAR)量表[4]对系统评价/Meta 分析进行质量评价。采用综合卫生经济评价报告标准(consolidated health economic evaluation reporting standard,CHEERS)量表对经济学研究进行质量评价。
1.6 数据分析
根据纳入研究的类型以及结局指标,采用定性分析方式对纳入研究的结果进行分类汇总。
2 结果
2.1 文献检索结果
通过数据库检索,共获得354篇文献,其中PubMed有70篇、Cochrane Library有0篇、Web of Science有96篇;中国知网有46篇、万方48篇、中国生物医学文献服务系统有40篇、维普有54篇。剔重后有209篇,阅读标题和摘要初筛后有21篇,进一步获取全文,根据纳入排除标准进行复筛,最终纳入15篇研究,其中网状Meta 分析13 篇,经济学研究2 篇。纳入文献基本特征详见表1、表2。

表1 纳入网状Meta分析的基本特征Tab 1 Basic characteristics of network included meta-analysis

表2 纳入药物经济学研究的基本特征Tab 2 Basic characteristics of included pharmacoeconomic analysis
2.2 纳入文献质量评价
共纳入13篇网状Meta分析,发表时间2012-2021年。应用AMSTAR 量表对纳入研究进行方法学质量评价,共计11个条目。每个条目回答“是”记1分,回答“否”、“不清楚”或“不适用”均记0 分,总分在9~11分为高质量,5~8分为中等质量,5分以下为低质量。本研究纳入的文献评分在6~10分,均为中等质量和高质量研究,无低质量研究。详见表3。共纳入2篇经济学研究,发表时间为2016-2021年,涉及的国家有美国和英国,文献总体质量良好。
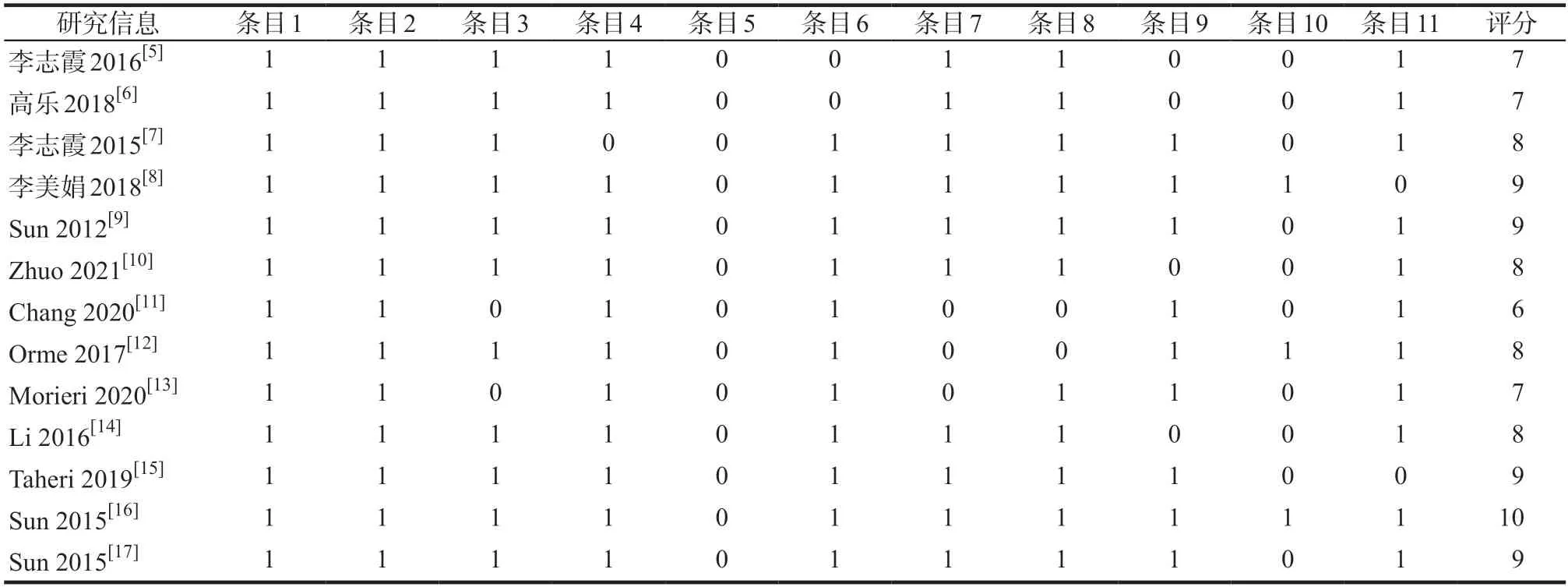
表3 纳入文献的质量评价Tab 3 Quality assessment of included references
2.3 有效性
总体来看,在不考虑剂量分组的情况下,度拉糖肽和利拉鲁肽在降低空腹血糖[8,15]、降低血压[8,15,17]、降低血脂[8]方面作用相似;在降低HbA1c%、HbA1c%达标率、降低体质量方面结果不一致。
降低HbA1c%:3 项研究[11,13,15]提示度拉糖肽降低HbA1c%效果显著优于利拉鲁肽(MD =-0.22,95%CI:-0.11~-0.32;MD =-0.19,95%CI:-0.3~-0.08;MD =-0.1,95%CI:-0.2~-0.01),但研究中未明确度拉糖肽和利拉鲁肽的剂量。1 项剂量分组研究提示,度拉糖肽高剂量组降低HbA1c%的作用显著优于利拉鲁肽高剂量组(MD =-0.21,95%CI:-0.39~-0.02)和利拉鲁肽低剂量组(MD =-0.32,95%CI:-0.57~-0.06),度拉糖肽低剂量组与利拉鲁肽相似[8]。
HbA1c%达标率:2 项研究[12,14]提示度拉糖肽与利拉鲁肽作用相似,但研究中未明确度拉糖肽和利拉鲁肽的剂量。1 项剂量分组研究[8]提示,度拉糖肽高剂量组HbA1c%达标率显著优于利拉鲁肽低剂量组(OR = 2,95%CI:1.18~3.4),度拉糖肽高剂量组与利拉鲁肽高剂量组相似。
降低体质量:1 项研究[13]提示度拉糖肽和利拉鲁肽相似,但研究中未明确度拉糖肽和利拉鲁肽的剂量。1 项剂量分组研究[8]提示,度拉糖肽高剂量组降低体质量作用显著优于利拉鲁肽高剂量组(MD =0.94,95%CI:0.26~1.62),与低剂量组相似。
2.4 安全性
本研究结果显示,度拉糖肽和利拉鲁肽在全因死亡率[10]、严重不良反应发生率[8,15]、低血糖事件发生率[8,10,14-15]、呼吸系统不良反应发生率[5,8,15]、泌尿系统不良反应发生率[10]、甲状腺癌发生率[10]和视网膜病变发生率[10]无显著性差异。不同系统的不良反应发生情况稍有不同,详细情况如下。
神经系统不良反应发生率:度拉糖肽和利拉鲁肽头疼的发生率相似,但度拉糖肽眩晕的发生率显著高于利拉鲁肽(OR = 1.76,95%CI:1.14~2.73)[6]。
消化系统不良反应发生率:度拉糖肽和利拉鲁肽致恶心[15-16]、呕吐[16]、腹泻[15-16]、消化不良[7]、厌食[7]、便秘[15]、胃肠功能紊乱[15]、胰腺炎[10]的发生率均相似。从剂量分组来看,度拉糖肽高剂量组恶心、呕吐、腹泻的发生率显著高于利拉鲁肽低剂量组(OR = 1.8,95%CI:1.13~29;OR = 2.53,95%CI:1.16~5.75;OR = 2.15,95%CI:1.02~4.54),与利拉鲁肽高剂量组相似[8]。
心血管系统不良反应发生率:度拉糖肽和利拉鲁肽在主要心血管事件(major adverse cardiovascular events,MACE)发生率[10]、心血管不良反应发生率[9-10]、非致命性心梗[10]、非致死性卒中[10]、因心衰再住院[10]、高血压[17]发生风险均相似。在心率方面,2篇文献报告的结果不一致,一篇文献报告度拉糖肽组患者心率显著低于利拉鲁肽组(MD =-1.14,95%CI:-1.90~-0.38)[15],另一文献报告度拉糖肽组患者心率与利拉鲁肽组相似[17]。
2.5 经济性
2篇药物经济学研究报告了度拉糖肽和利拉鲁肽的间接比较。1篇英国的成本效益分析[18]从英国国家医疗服务体系的角度比较了多种GLP-1 受体激动剂的成本效益,结果发现,度拉糖肽高剂量组和利拉鲁肽低剂量组相比,增量成本效果比(incremental cost effective ratio,ICER)为1 357英镑,远低于支付阈值(20 000~30 000英镑);利拉鲁肽高剂量组和度拉糖肽高剂量组相比,ICER为704 333英镑,远超过支付阈值。因此,度拉糖肽高剂量组和利拉鲁肽高、低剂量组相比均具有成本效益优势。
1 篇美国的成本效益分析[19]从美国支付方的角度比较了多种GLP-1受体激动剂的成本效益,结果发现,利拉鲁肽和度拉糖肽相比,ICER为529 571美元,远超过支付阈值(150 000 美元),因此,度拉糖肽和利拉鲁肽相比具有成本效益优势。
3 讨论
通过快速卫生技术评估的方法,本研究发现对于2型糖尿病患者,度拉糖肽疗效略优于利拉鲁肽,安全性与利拉鲁肽相当,度拉糖肽降低HbA1c%和体质量的作用优于利拉鲁肽,但眩晕的不良反应较多。从药物经济学的角度来看,度拉糖肽增量成本效果比在意愿支付阈值范围内,是一种具有经济性的治疗选择。
目前,我国缺少GLP-1受体激动剂的上市后药物警戒研究。一项基于美国食品药品监督管理局公共数据开放项目数据库的研究报告,利拉鲁肽致急性胰腺炎、头痛、头晕、急性肾损伤、低血糖的发生风险均高于度拉糖肽[20]。一项基于美国FDA 不良事件报告系统(FDA adverse event reporting system,FAERS)数据库的研究报告,度拉糖肽药品不良反应主要集中于胃肠系统疾病、全身性疾病及给药部位反应;利拉鲁肽主要集中于胃肠系统疾病和检验指标异常[21]。另一项基于美国FAERS 数据库的研究报告,度拉糖肽的不良反应表现主要为恶心、注射部位疼痛、腹泻、呕吐、注射部位出血等,而利拉鲁肽的不良反应表现主要有恶心、呕吐、腹泻、胰腺炎、食欲减退等[22]。由此看来,注射部位反应在使用度拉糖肽时需要特殊关注,注射部位反应主要与针头的使用有关,建议针头使用一次后丢弃,重复使用针头会使针头变得粗糙,引起注射部位不适。同时,消化系统不良反应在使用度拉糖肽时应特别关注。消化系统不良反应可能在用药初期出现,随着治疗时间的延长,机体耐受性会逐渐增加,因此治疗时应从小剂量开始逐渐加量[23]。有严重胃肠道疾病的患者不推荐使用度拉糖肽,特别是1.5 mg每周一次的剂量。
少数研究报告了度拉糖肽的严重不良反应。一项文献研究共检索到12 例度拉糖肽引起的不良反应文献,患者不良反应表现为严重恶心、呕吐、急性肾损伤、血管性水肿、坏疽性脓皮病、坏疽性胆囊炎、肝损伤等[24]。度拉糖肽说明书中的黑框警告提示其在大鼠中使用引起甲状腺肿瘤的风险。由于该药上市时间较短,对于严重不良反应的报告较少,长期应用发生药品不良反应的风险研究不多,在应用时应重点监测。
基于现有的研究结果,度拉糖肽注射次数少,疗效优于利拉鲁肽,安全性和利拉鲁肽相当,适用于2型糖尿病患者,使用时应重点关注其注射部位反应和消化系统的不良反应,从小剂量开始逐渐加量,并关注上市后长期使用发生药品不良反应,特别是严重不良反应的情况。度拉糖肽在英国和美国的研究中具有成本效益优势,但在我国的经济性仍需进一步研究。

