NiAl-LDHs 电极材料的水热合成及其超级电容器电化学性能
刘宽鑫, 黎 阳, 王利军, 乔永民
(1. 上海第二工业大学能源与材料学院,上海 201209; 2. 上海杉杉科技有限公司,上海 201209)
0 引言
近年来,环境问题已经引起了人类社会的高度关注,特别是大气中二氧化碳的大量排放引起的全球变暖。目前,化石燃料仍然是主要的能源来源,造成了巨大的能源和环境危机[1]。为应对全球能源危机、环境污染、气候变化等问题,达到“碳达峰、碳中和” 战略目标, 发展可持续的可再生能源系统已成为世界范围内非常重要的任务之一[2]。迫切需要开发清洁、可再生的新能源, 利用先进的能源储存及转换装置以维持全球经济的平衡发展。近年来,超级电容器逐渐成为一种重要的电化学储能器件,具有充放电倍率高、循环稳定性好、功率密度高[3]、使用寿命长等优点。然而, 其较低的能量密度限制了实际应用[4]。因此, 通过优化合成工艺研究出具有高比能量的电极材料显得尤为重要。
层状双金属氢氧化物(layered double hydroxides, LDHs) 是一类重要的二维阴离子型层状化合物, 由层间阴离子与带正电荷的层板有序组装而成, 是一种类水滑石的片层结构[5]。作为一种低廉、清洁、高效的储能材料, LDHs 具有高的理论比容量、可调谐的组分、高的氧化还原活性[6]和环保性[7], 是一种理想的超级电容器电极材料, 在新能源材料、催化、储能等领域有着良好的应用前景。LDHs 常用的制备方法有共沉淀法、水热合成法、离子交换法、焙烧复原法、微波法、溶胶-凝胶法和电沉积法[8]。Memon 等[9]以SiO2/AlOOH 微球为模板, 通过水热法制备了石墨烯/NiAl-LDH 纳米线球, 其比表面积达到了230 m2/g, 在3 A/g 电流密度下循环1 000 圈后容量未有明显变化。Li等[10]以γ-Al2O3为前体, 通过溶液法制备NiAl-LDHs/CNTs 复合材料,它可以在1 A/g 下产生1 500 F/g 的高比电容, 在10 A/g 电流密度下具有70.3%的容量保持率, 有良好的倍率性能。Elgendy 等[11]使用连续离子层吸附和反应方法制备了无黏合剂的镍-锌-铁LDHs(NiZnFe-LDH),具有高的比表面积(119.79 m2/g),以AC 为负极构建的非对称超级电容器装置, 在能量密度为14.9 Wh/kg, 表现出1 077.6 W/kg 的高功率密度。Lee 等[12]报告了一种可用于高能量密度混合超级电容器电极的钴-钒层状双氢氧化物,CoV-LDH 在1 A/g 电流密度下表现出1 579 F/g 的高比电容。
本文通过水热合成法制备NiAl-LDHs, 探究不同镍铝物质的量比对NiAl-LDHs 特征形貌、物相组成和电化学性能的影响。使用扫描电子显微镜(SEM)、X 射线衍射仪(XRD)、拉曼光谱仪(Raman)及红外光谱仪(FT-IR)对NiAl-LDHs 的形貌结构进行表征,并通过电化学工作站研究其电化学性质。
1 实验部分
1.1 NixAly-LDHs 样品制备
实验中使用的试剂均为分析纯,使用前不做其他处理。合成示意图如图1 所示, 依次称取六水硫酸镍、十八水硫酸铝, 加入到25 mL 去离子水中, 磁力搅拌10 min, 然后加入1.2 g 尿素, 继续磁力搅拌10 min, 完全溶解后将溶液移入反应釜中,在180 ℃下保温6 h。反应结束后倒掉上层清液,用去离子水、无水乙醇离心洗涤沉淀物3 次, 然后在60 ℃下干燥12 h 得到NixAly-LDHs 纳米粉末。实验制备了不同Ni 和Al 物质的量比的样品(1:2、1:1、3:2、2:1 和5:2), 依次命名为Ni1Al2-LDHs、Ni1Al1-LDHs、Ni3Al2-LDHs、Ni2Al1-LDHs和Ni5Al2-LDHs。

图1 NixAly-LDHs 的合成示意图Fig.1 Synthesis schematic of NixAly-LDHs
1.2 电极制备
集流体的预处理: 选用2 cm×1 cm 尺寸金属泡沫镍作为集流体,将裁剪好的泡沫镍先置于丙酮中超声清洗,后用0.5 mol/LHCl 溶液除去表面氧化物,最后用去离子水清洗并置于80 ℃真空干燥箱中干燥。
电极片的制备: 将NixAly-LDHs 电极材料、乙炔黑和聚偏氟乙烯按质量比8:1:1 混合,加入N-甲基吡咯烷酮溶剂调至膏状后均匀涂覆在处理好的泡沫镍上,涂覆面积大小为1 cm2,然后放入60 ℃干燥箱干燥12 h。
1.3 材料表征
使用德国 BRUKER-AXS 公司的 D8-ADVANCE 型XRD、德国BRUKER-AXS 公司的SENTERRA 型Raman、美国Perkin Elmer 公司的Spectrum Two 型FTIR 对样品的组成、结构进行分析, 使用日本HITACHI 公司的S-4800 型冷场发射SEM 观察样品的表面形貌并进行能谱分析。
1.4 电化学测试
三电极体系:以3 mol/LKOH 溶液为电解液,Pt箔为对电极, 饱和甘汞电极(saturated calomel electrode,SCE)为参比电极。在电位区间为0~0.4 V、扫描速率为0.02~1 V/s 范围内测量循环伏安(cyclic voltammetry, CV)曲线;在电位区间为0~0.4 V、电流密度为1~20 A/g 的条件下进行恒流充放电(galvanostatic charge/discharge, GCD)试验; 电化学阻抗谱(electrochemical impedance spectroscopy, EIS) 的测量频率为10 mHz~100 kHz,振幅为5 mV。
Ni1Al1-LDHs//AC 非对称超级电容器: 以Ni1Al1-LDHs 电极为正极, 活性炭(activated carbon,AC) 电极为负极组装成非对称超级电容器进行电化学测试。在电位区间为0~1.4 V、扫描速率为0.02~0.1 V/s 范围内测量CV 曲线; 在电位区间为0~1.4 V、电流密度为1~10 A/g 的条件下进行GCD测试。
伴随着经济的快速发展,市民需求层次不断提高,不仅仅局限于对物质的需求,更体现出对生活环境质量提升的内在需求渴望,在不断追求美化居家环境的同时,也在着力提升厨房的整洁、卫生和科学化。然而,人们在厨房精工细作时,时常会忽略一个严重的问题,即厨房食物垃圾或下角料的处理,从而造成生活垃圾的排放量急剧增长。
所有电化学测试均在法国Biological 公司的VMP3 型电化学工作站上进行。
2 结果与讨论
2.1 表征分析
2.1.1 电极材料的SEM 表征
利用冷场发射SEM 对NixAly-LDHs 样品的微观形貌进行表征。样品的表征结果如图2(a)~(c)所示, Ni1Al1-LDHs 样品显示出三维纳米花状微球形貌,直径在2~5 μm,由众多垂直生长的纳米片构成,纳米片交互生长形成紧密的花球形状,纳米片的平均厚度大概为10~30 nm。纳米片之间相互连接且片之间的间距较小, 排布较为致密。这种构象不仅为电子/离子扩散提供了快速路径,而且为氧化还原反应提供了丰富的电化学活性位点,从而潜在地增加了材料的电容特性[13]。对于不同镍铝比的样品,纳米片的表面形貌并未出现明显变化,形貌结构具有较好的一致性,本文不再一一列出。此外,还利用能谱仪(energy dispersive spectroscopy,EDS)对样品中各元素的分布进行了表征。图2(d)~(e)中所示为Ni1Al1-LDHs 样品对应的元素分布图像和EDS 谱线,测试的元素为C、O、Ni、Al4 种元素,从图中可以看到4 种元素在纳米片中均匀分布。

图2 Ni1Al1-LDHs 在(a)5 000 万倍(b)20 000 倍(c)100 000 倍下的SEM 图;(d)Ni1Al1-LDHs 的EDS 图;(e)Ni1Al1-LDHs 能谱图Fig.2 SEM diagram of Ni1Al1-LDHs at (a) 5 000 X (b) 20 000 X (c) 100 000 X; (d) EDS mapping of Ni1Al1-LDHs; (e) Energy dispersive spectrum of Ni1Al1-LDHs
2.1.2 电极材料的XRD 表征
图3 为NixAly-LDHs 样品的XRD 图谱, 与标准图谱(PDF: 15-0087) 比对, 各个样品的衍射峰与标准卡片的衍射峰的出峰位置基本一致, 在2θ值为11.64°、23.63°、35.21°、39.85°、47.27°、61.29°和 62.61°出 现 的 衍 射 峰 分 别 对 应(003)、(006)、(012)、(015)、(018)、(110)和(113)晶面的特征衍射峰[14],同属六方晶系(空间群R-3m),为典型的类水滑石结构特征。图中Ni1Al1-LDHs 的(003)晶面特征衍射峰的衍射峰强度最高,表明其具有良好的结晶度和晶体的完整性。
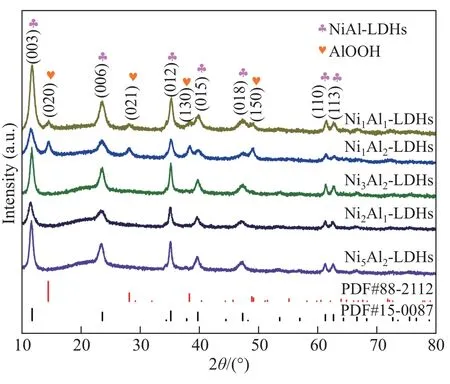
图3 NixAly-LDHs 的XRD 谱图Fig.3 XRD spectrum of NixAly-LDHs
此外,图3 中除Ni1Al2-LDHs、Ni1Al1-LDHs 有杂峰出现外, Ni3Al2-LDHs、Ni2Al1-LDHs、Ni5Al2-LDHs 都没有其他杂峰, 表明其所合成的样品为纯相的NiAl-LDH。经过与标准图谱(PDF:88-2112) 对比, Ni1Al2-LDHs、Ni1Al1-LDHs 样品在2θ值为14.57°、28.02°、38.39°、48.99°出现(020)、(021)、(130)、(150) 晶面的衍射峰, 属于AlOOH 的特征衍射峰。生成AlOOH 的原因是由于在反应体系中Al 元素的含量较高,导致在反应过程中生成AlOOH,从而在XRD 图谱中出现了少量AlOOH 相。
2.1.3 电极材料的光谱表征
图4 (a)是NixAly-LDHs 的FT-IR 谱图, 从样品的FT-IR 谱图可以清楚地看到NiAl-LDH 的吸收峰,对于不同比例的NixAly-LDHs,其谱图基本一致,在3 500cm-1左右有一个较宽的吸收带,且峰形相似,该峰是由试样表面和层间空隙中H2O 分子的伸缩振动引起的,与自由-OH(约3 600 cm-1)相比,由于层间水分子与层间阴离子及层板羟基发生氢键作用使此峰向低波数偏移。在1 638 cm-1处为层间水分子的弯曲振动谱带。在1 355 cm-1和795 cm-1吸收峰属于产物NiAl-LDHs 层间存在的伸缩振动和弯曲振动。低于800 cm-1的吸收峰,是金属氧键(M—O)或(M—OH)[15](其中M 为Ni、Al 元素)骨架振动引起的吸收峰。FT-IR 的数据结果与XRD谱图的结果相互对应, 进一步证明了NixAly-LDHs的层状结构。
图4 (b) 是NixAly-LDHs 的Raman 谱图, 不同镍铝比的拉曼光谱峰形大致相同, 位于496 cm-1处的拉曼峰认为是由于金属-氧键造成的[16], 位于1 064 cm-1的尖强峰和695 cm-1的弱峰是LDH 层间阴离子的V1和V4振动峰[17],在547 cm-1位置附近的拉曼峰是LDH 材料层间H2O 分子的特征峰[18]。通过Raman 光谱分析, 进一步确定了NiAl-LDHs 材料的成功制备。
2.2 电化学性能
2.2.1 不同镍铝含量NixAly-LDHs 电极的电化学性能对比
对不同镍铝含量的样品NixAly-LDHs 进行电化学性能测试,其结果如图5 所示。由下式计算表1中电极材料的放电比容量
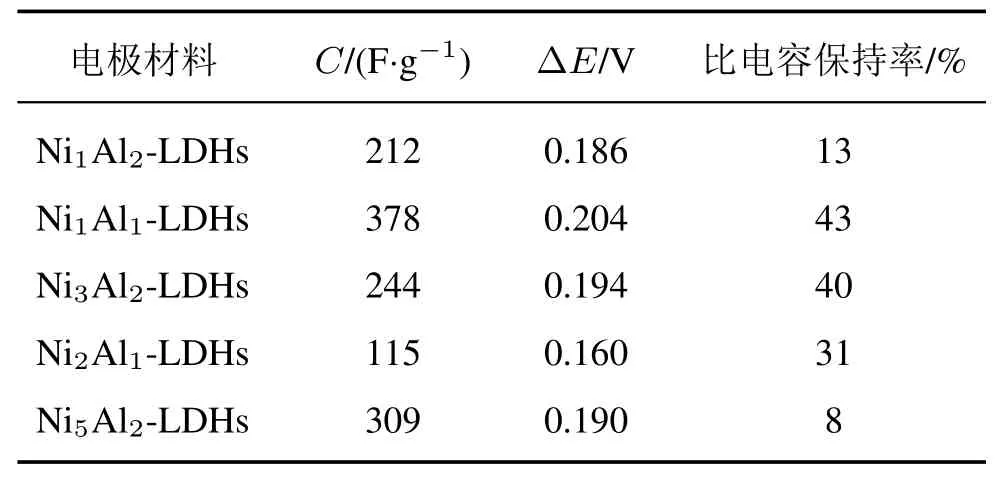
表1 NixAly-LDHs 电极材料电化学性能对比情况Tab.1 Comparison of electrochemical properties of NixAly-LDHs electrode materials
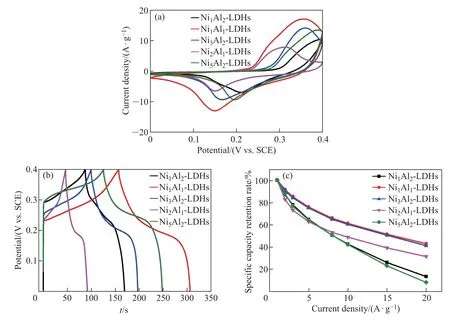
图5 (a)NixAly-LDHs 电极材料的CV 曲线(扫描速率20 mV/s);(b)NixAly-LDHs 电极材料的GCD 曲线(电流密度1 A/g);(c)NixAly-LDHs 电极材料不同电流密度下的容量保持率Fig.5 (a)CV curves of NixAly-LDHs electrode material(scanning rate 20 mV/s);(b)GCD curves of NixAly-LDHs electrode material(current density 1 A/g);(c)capacity retention of NixAly-LDHs electrode material at different current
式中:C为电容(F/g);I为电流(A); Δt为放电时间(s);m为活性物质质量(g);ΔU为工作电压窗口(V)。
图5 (a)是扫描速率为20 mV/s 时NixAly-LDHs的CV 曲线图, 可以看出各CV 曲线具有明显的氧化还原峰,表明其主要的电荷存储是通过材料表面的快速法拉第反应完成的。由表1 中可知,NixAly-LDHs 材料都具有较小的氧化还原峰电位差值ΔE,表明所制备的NixAly-LDHs 电极材料氧化还原反应可逆性较好,易于发生氧化还原反应。图5(b)是NixAly-LDHs 电极材料在1 A/g 电流密度下的恒电流充放电曲线, 能够清楚地看到GCD 曲线存在明显的充放电平台,说明其比容量主要来自于赝电容的氧化还原反应,其中Ni1Al1-LDHs 具有最大比容量(378 F/g)。图5(c) 是在不同电流密度下NixAly-LDHs 电极材料的比容量保持率,其中Ni1Al1-LDHs随着电流密度的增大,表现出了良好的倍率性能,而且在电流密度为20 A/g 时,比容量保持率为43%。因此,由表1 及图5 可知,相较于纯的NiAl-LDH,具有AlOOH 杂相的Ni1Al1-LDHs 具有更好的电化学性能,这可能是由于Ni1Al1-LDHs 电极材料中适量的AlOOH 杂相为氧化还原反应提供了更多的反应活性位点,体现出了一种协同效应,从而获得了较大比容量。下面将进一步探究Ni1Al1-LDHs 电极材料的电化学性能。
2.2.2 Ni1Al1-LDHs 材料电化学性能分析
在三电极体系下测试了Ni1Al1-LDHs 电极的电化学性能。由图6(a)可见,在20 mV/s 扫速时,从Ni1Al1-LDHs 电极的CV 曲线中可观察到明显的氧化还原峰,扫速>20 mV/s 时,CV 曲线中的氧化峰变得不太明显,当扫速大于200 mV/s 时,CV 曲线出现了非常明显的极化, 这是由于在高扫速下, 电子运动速率较快,致使扩散阻力加大,材料表面发生极化,活性物质不能充分利用,使得阳极峰与阴极峰分别移动到更正与更负的电位。由图6(b)可见,GCD曲线中有较为明显的充放电平台,但随着电流密度的增大,GCD 曲线充放电平台明显减小, 这是因为较大的充放电电流会降低活性材料的利用率,导致活性材料来不及发生法拉第反应储存和释放电荷。
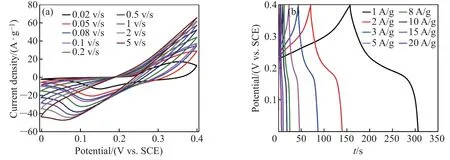
图6 Ni1Al1-LDHs 材料在(a)不同扫描速率下的CV 曲线;(b)不同电流密度下的GCD 曲线Fig.6 Ni1Al1-LDHs materials at(a)CV curves at different scanning rates,(b)GCD curves at different current densities
为探究Ni1Al1-LDHs 的氧化还原动力学特征,测量了低扫描速率下的CV 曲线如图7(a)所示,其具有明显的氧化还原峰,且对称性较好,具有良好的反应可逆性,这是因为在低的扫描速率下,电化学反应的离子/电子转移速率较慢,电极活性材料能充分发生氧化还原反应,有利于电极材料动力学特征的研究。NixAly-LDHs 材料在电化学充放电过程中的反应方程式如下[19]:

图7 (a)Ni1Al1-LDHs 的CV 曲线;(b)Ni1Al1-LDHs 的Ip 与V 1/2 的关系;(c)Ni1Al1-LDHs 的lg Ip 与lg V 的关系;(d)Ni1Al1-LDHs的电化学活性面积Fig.7 (a)Cyclic voltammetric curves of Ni1Al1-LDHs;(b)the relationship between Ip and V 1/2 of Ni1Al1-LDHs;(c)Relationship between lg Ip and lg V of Ni1Al1-LDHs(d)electrochemical active area of Ni1Al1-LDHs
运用Randles-Sevick 公式来计算Ni1Al1-LDHs电极在电荷转移过程中离子的扩散系数, 如下式所示:
式中:Ip为峰值电流(A);n为法拉第电化学反应过程中发生转移的电子数;A为电解液与活性物质的接触面积(cm2);D为扩散系数(cm2/s);C为K+的浓度(mol/cm3);V为扫描速率(V/s)。据文献[20] 中所述, 以扫速平方根(V1/2) 为x轴、峰电流(Ip) 为y轴, 并对其进行线性拟合, 结果如图7(b) 所示。根据拟合结果得到的斜率再根据式(2) 得到Ni1Al1-LDHs 的氧化过程离子扩散系数D=11.08×10-7cm2/s,还原过程离子扩散系数D=4.13×10-7cm2/s,表明所得的Ni1Al1-LDHs 具有较大的扩散系数,有着较好的动力学性能。
此外,根据
中峰值电流(Ip)与扫描速率(V)之间的关系进一步来判别Ni1Al1-LDHs 的材料类型和电荷在氧化还原过程中的存储机理。式中:Ip为峰值电流(A);b为常数;V为扫描速率(V/s);k为常数。lgIp与lgV函数关系如图7(c) 所示。经过线性拟合得到氧化峰、还原峰的k值分别为0.730 67、0.673 21(介于0.50~1.00),说明Ni1Al1-LDHs 属于典型的电池型电极材料, 充放电过程中电荷储存机制均主要为扩散控制。
Ni1Al1-LDHs 电极材料的电化学活性表面积(electrochemcial active surface area,ECSA)通常正比于其在非法拉第电位区间内的双电层电容值(Cdl),存在如下关系: ECSA =Cdl/Cs(其中Cs是理想光滑氧化物表面双电层电容)。因此,可在非法拉第电位区间通过CV 测试得到不同扫描速率下的CV 曲线以确定材料在单位面积下的Cdl, 进而计算得到相应的ECSA。本研究中对Ni1Al1-LDHs 材料进行非法拉第区的多扫速CV 测试,根据文献[21]对材料的双电层电容进行量化处理,结果如图7(d)所示,Ni1Al1-LDHs 的Cdl值(8.35 mF/cm2), 具有较大的电化学活性表面积。
2.2.3 Ni1Al1-LDHs 材料EIS 分析
Ni1Al1-LDHs 电极材料的交流阻抗曲线如图8所示,图中的EIS 曲线是由高频区的半圆和低频区的斜线组成, 其中曲线与实轴截距表示电极材料、电解液、电极-电解质界面的固有阻抗(Rs);高频区的半圆直径反应了材料电荷的转移电阻(Rct), 直径越小, 电荷转移电阻越小; 低频区的直线反映了离子在溶液中的扩散电阻,也称为Warburg 电阻(W),直线的斜率越大,表示离子扩散电阻越低[22]。由交流阻抗谱可知, Ni1Al1-LDHs 电极材料的固有阻抗(Rs= 0.441), 高频区的半圆直径较小, 其电极材料内部和电极/电解液界面之间的电荷转移能力强,具有良好的电荷转移能力;低频区斜线有较大的斜率,其电解质离子扩散到电极表面的阻力较小,有良好的离子传输能力。
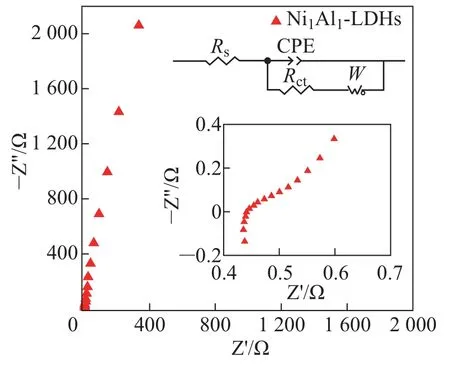
图8 Ni1Al1-LDHs 的Nyquist 图(插图为局部放大图及模拟平衡电路图)Fig.8 Nyquist plot of Ni1Al1-LDHs(Illustrated are partial enlarged view and analog balanced circuit diagrams)
2.2.4 Ni1Al1-LDHs//AC 非对称超级电容器性能分析
为了评估Ni1Al1-LDHs 电极材料的实际应用, 以Ni1Al1-LDHs 电极为正极, AC 电极为负极,3 mol/L KOH 为电解液组装了非对称型超级电容器(Ni1Al1-LDHs//AC),可以提供1.4 V 的工作电压。通过图9(a) 不同扫描速度下在0~1.4 V 电位区间的CV 曲线,可以看到在20 mV/s 的扫描速度下曲线在0~0.8 V 之间没有明显的氧化还原峰,在0.8~1.4 V之间曲线有明显的氧化还原峰, 属于赝电容放电。随着扫描速率增大, 曲线未发生明显极化, 即使在100 mV/s 高扫描速率下仍可以保持CV 曲线的形状,说明该非对称超级电容器具有较好的循环可逆性和快速充放电能力。图9(b)为Ni1Al1-LDHs//AC在不同电流密度下的GCD 曲线,在1 A/g 电流密度下可以具有112 F/g 的高比电容, 即使在电流密度为10 A/g 时, 其比电容仍然可以达到64 F/g, 表现出了良好的倍率性能。Ni1Al1-LDHs//AC 在10 A/g电流密度下, 经过10 000 次充放电循环后, 比电容保持率在53%, 充放电循环的库伦效率>99%, 如图9(c)所示。图9(d)为Ni1Al1-LDHs//AC 的Ragone图, 在能量密度为27.5 Wh/Kg 时, 功率密度可以达到1.4 kW/kg, 即使在高功率密度7 kW/kg 下放电,仍可达到17.5 Wh/kg 的能量密度,与相关文献[23-27]报道的非对称超级电容器相比, Ni1Al1-LDHs//AC非对称超级电容器具有明显的优势。

图9 (a)Ni1Al1-LDHs//AC 不同扫速下的CV 曲线;(b)Ni1Al1-LDHs//AC 不同电流密度下的GCD 曲线;(c)Ni1Al1-LDHs//AC的循环稳定性(10 A/g);(d)Ni1Al1-LDHs//AC 的Ragone 图Fig.9 (a) CV curves of Ni1Al1-LDHs//AC at different scanning rates; (b) GCD curves of Ni1Al1-LDHs//AC at different current densities;(c)Cyclic stability of Ni1Al1-LDHs//AC(10 A/g);(d)Ragone diagram of Ni1Al1-LDHs//AC
3 结 论
本研究采用简易的水热合成法制备了具有层状结构的、呈现纳米花球状的NixAly-LDHs 材料, 探究了不同镍铝比LDH 材料的微观形貌、物相组成、结构特征及电化学性能。结果表明,当镍铝比为1:1时所制备的Ni1Al1-LDHs 作为超级电容器电极材料表现出极好的电化学性能, 在1 A/g 电流密度下能达到378 F/g 的高比容量, 在20 A/g 的高倍率下具有较高的比容量保持率(43%)。以AC 为负极,组装的Ni1Al1-LDHs//AC 非对称超级电容器在能量密度为27.5 Wh/kg 时,功率密度可以达到1.4 kW/kg,显示出了良好的电化学性能及广阔的应用前景。

