子宫颈恶性肿瘤的影像诊断思维
钱吉芳 翟晓静 徐生芳 梁宗辉
1 病例资料
患者,女,31 岁,超声发现下腹部肿物5 个月余。患者平素月经规律,量中,色暗红,有痛经,白带量多,色白,无异味。专科检查:宫颈光滑,无举痛,触血阴性;双侧附件区触及直径约11~15 cm 的肿物,边界清,质软,表面光滑,活动度可,无明显压痛。实验室检查:肿瘤标志物CA-125(51.85 U/mL)、CA-199(105.10 U/mL)升高;余未见异常。
影像表现:盆腔MRI 平扫和增强示宫颈囊性为主囊实性肿物,范围约2.4 cm×2.1 cm×2.5 cm,T1WI 呈等及中低信号,T2WI 及脂肪抑制序列中高及高信号,DWI 呈等信号,ACD 值为1.178×10-3mm2/s;双侧附件区见不规则囊实性肿物,其内多发分隔,左侧约7.4 cm×7.8 cm×10.0 cm,右侧约12.4 cm×8.9 cm×14.1 cm,T1WI 呈等及中低信号,T2WI 呈高信号并多发分隔状低信号,DWI 序列部分病灶为中高信号;增强扫描囊性成分未见强化,囊壁及分隔呈中高强化,病灶向双侧宫旁延伸,与盆壁、直肠分界不清(图1)。
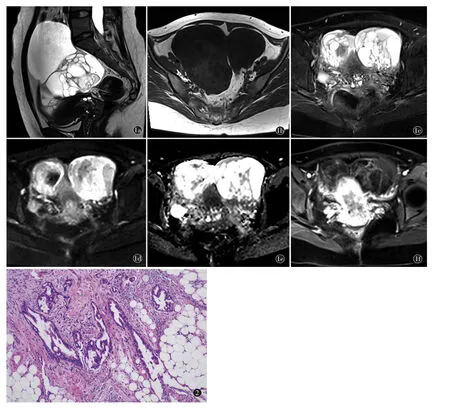
图1a)~e)盆腔MRI 平扫示宫颈囊性为主肿物,双侧附件区不规则囊实性肿物。a)矢状位T2WI 呈中高及高信号;b)横断位T1WI 呈等及中低信号;c)横断位脂肪抑制T2WI 呈中高及高信号;d)DWI 及e)ADC图部分病灶呈等及中高信号;f)横断位增强扫描示病灶囊性成分未见强化,囊壁及分隔呈中高强化,病灶向双侧宫旁延伸,与盆壁、直肠分界不清。图2 镜下见癌细胞不规则腺管状排列(HE×100)。
手术记录:患者行次广泛性子宫切除术和双侧附件切除术,术中所见子宫增大如孕2 个月,宫颈粗大,质硬,直径约3.0 cm;双侧附件区囊性肿物,表面光滑,呈多房性,右侧病灶表面见菜花样结节,与右侧盆壁腹膜致密粘连,界限不清;病灶累及直肠、阑尾、大网膜、腹膜及膈肌。
病理结果:镜下增生的纤维脂肪组织内见癌细胞不规则腺管状排列,癌细胞低柱状,胞浆淡染,核圆形、卵圆形,染色加深,核浆比轻度升高,核分裂像罕见(图2,HE×100),病理提示宫颈浸润性腺癌(胃型腺癌),双侧附件区转移性黏液性腺癌,直肠、阑尾、大网膜、腹膜、膈肌受侵。免疫组化:左侧卵巢肿物:P16(-)、CK7(+)、CK20(-)、P53(无义突变型)、PAX8(-)、Vimentin(-);宫颈病变:MUC2(-)、MUC6(+)、CK7(+)、CK20(-)、P53(无义突变型)、P16(-)。
2 讨论
子宫颈胃型腺癌(gastric-type endocervical adenocarcino ma,G-EAC)包括高分化型G-EAC 和典型G-EAC[1]。2003年WHO 宫颈腺癌分类中没有胃型腺癌,2007 年由日本学者Kojima 等[2]首次提出,因日本人胃型腺癌的发病率高于西方人,占宫颈腺癌的25%,但分化好的胃型腺癌仅占宫颈腺癌的1%。典型的胃型腺癌由黏液上皮组成,以表达胃型黏蛋白为特点,形态学上类似于胃底腺上皮。2021 年国际宫颈内膜腺癌标准和分类(International Endocervical Adenocarcinoma Criteria and Classification,IECC)[3]及2020 版WHO 女性生殖系统肿瘤分类[4]中,宫颈癌被分为人类乳头瘤病毒(human papillomavirus,HPV)相关型(HPV-associated,HPVA)和非HPV 相关型(non-HPVA,NHPVA),而NHPVA 最常见的亚型为宫颈胃型腺癌,其与HPV 相关型腺癌存在明显不同的分子基础。G-EAC 发病率仅次于普通型宫颈腺癌(usual-type endocervical adenocarcinoma,UEA),占宫颈腺癌10%~15%[5]。但由于其临床表现不典型,病理易漏诊,早期诊断困难,误诊率可达34%[6]。
G-EAC 发病年龄为25~76 岁(中位年龄42 岁),多数患者早期常无明显临床症状,宫颈表现为外观肥大,外口光滑或伴有糜烂,也有部分患者仅表现为阴道大量排液。由于该肿瘤与HPV 感染无关,仅HPV 筛查难以发现,分化好的胃型腺癌在细胞学筛查中也易漏诊,确诊时大多数患者处于进展期(Ⅱ~Ⅳ期),易发生远处转移,如淋巴结、卵巢、腹膜等。因此,针对反复或持续阴道排液的患者,应警惕G-EAC 的风险,必要时需反复、多点活检及颈管搔刮、诊断性锥切、分段诊刮等来明确诊断。
组织学上表现为大量胃型黏液腺体沿着宫颈间质浸润性生长,形成桶状宫颈,通常无肉眼可见的菜花状病灶[1],只是显示管壁增厚、质地硬韧,黏膜表面光滑,容易被忽视。仅少数晚期患者宫颈可见菜花状或质硬结节状外观。约有50%的G-EAC 患者肿瘤标志物CA-199 升高,另有30%的患者表现为CA-125 升高,但两者在其疗效评估和病情预后方面的价值目前研究较少[7]。而肿瘤异常蛋白(tumor abnormal protein,TAP)与宫颈癌患者治疗效果及预后则密切相关。高分化型G-EAC 的腺癌细胞具有分化程度较高,形态温和,含大量透明或苍白、嗜酸性胞质,细胞边界清楚,细胞核轻度增大、深染,核分裂像罕见等,易被误认为良性的宫颈内膜腺体[8],所以在宫颈活检时,因取材较少而易漏诊。病理学是诊断G-EAC 的金标准,表现为宫颈扩张呈桶状,质硬,切面呈灰白色,其内可见囊腔;腺体大小和形状相差悬殊是其特征。特异性免疫组化CEA、CDX2、CK7、P53、MUC6 阳性,P16 阴性或局灶性阳性,ER 和PR 阴性[9]。
G-EAC 的影像学表现与病理有一定的相关性[10]。以实性成分为主的G-EAC 主要为中低分化腺癌,肿瘤细胞异型性明显,细胞排列密集,呈不规整腺体或实性表现,腺体周围促纤维反应明显,因此病灶在T1WI 序列呈等信号,T2WI 为中高信号,DWI 呈明显高信号,增强扫描明显强化;此类病例恶性征象明显。以囊性成分为主的G-EAC,肿瘤细胞分化程度高,病灶通常位于宫颈管中上段,中央为较小的囊性或实性病灶,周围包绕着较大的囊肿,T1WI 为低信号,T2WI 为高信号,即“宇宙征”,增强扫描实性部分呈轻度强化;此类病例容易与宫颈纳氏囊肿混淆,但宫颈纳囊极少导致阴道持续排液。
本例患者31 岁,超声提示双侧附件区肿物,实验室检查CA-125、CA-199 升高,病史及实验室检查均符合卵巢来源肿瘤的可能性。盆腔MRI 示宫颈增大并宫颈囊性为主囊实性肿物,宫颈肌层外T2WI 低信号环连续性中断,病灶沿宫颈向双侧宫旁延伸至盆壁,邻近盆壁肌层及筋膜T2WI 信号增高。病灶向后延伸与直肠界限不清,病灶向上延伸,双侧卵巢正常形态不可见,双侧附件区囊性为主囊实性肿物,以多房囊信号为主、其内多发分隔,囊与囊信号不同,T1WI 为低信号及中高信号,T2WI 为高信号及中高信号,DWI 序列附件区病灶ADC 值与宫颈病灶ADC 值相近;动态增强扫描囊性成分未见强化,囊壁及分隔呈中高强化。以上综合考虑,得出宫颈胃型腺癌侵犯双侧盆壁、双侧卵巢的诊断不难。遗憾的是该患者未行全腹CT 平扫加增强进一步评估病灶范围。因胃型腺癌组织类型的特殊性,临床表现不典型、早期诊断困难,一经发现已是晚期。
因无明显临床症状、HPV 筛查难以发现,G-EAC 早期诊断困难,漏诊率高,发现即具有更深的宫颈间质浸润,常深至1/2 宫颈管壁,甚至累及宫颈管壁全层。浸润范围广,向上可累及子宫体,向下侵及阴道,双侧可侵及宫旁脂肪间隙乃至卵巢。治疗要采用手术与放化疗相结合[11],但术前要进行充分的影像学评估,以更好地了解病灶累及范围及术前分期。对于晚期G-EAC 患者可先行新辅助化疗,再补充根治性手术可能获益更大。与非胃型宫颈腺癌相比,G-EAC具有更差的预后,因此精准的早期诊断对患者意义重大。
3 影像诊断思维
子宫颈肿瘤定位容易,关键在于定性,更重要的是要确定肿瘤与周围组织的关系,如与双侧宫旁脂肪间隙、阴道的关系,恶性病灶向宫体延伸则不在肿瘤分期范围内。宫颈肿瘤的定性及定期的重点在于对影像学表现进行综合分析。CT 具有方便快捷、空间分辨率高、三维重组直观的优点,但原发病灶密度与正常宫颈组织相近时,对病灶的显示有限。MRI 软组织分辨率高弥补了CT 的缺点,可清楚显示肿瘤信号、大小、边缘及与周围组织的关系。
子宫颈管黏膜是一个复杂的黏膜内褶系统,由外向内分为纤维膜、肌层和黏膜,所以发生的肿瘤分类较多,包括上皮性肿瘤、间叶性肿瘤和瘤样病变、混合性上皮和间叶肿瘤等。子宫颈良性肿瘤种类较多。囊性肿瘤包括宫颈纳氏囊肿、囊性腺肌症/瘤、肌瘤囊性变性、浆液性囊肿等;实性良性肿瘤常见宫颈肌瘤和宫颈息肉。宫颈肌瘤起源于宫颈肌层,由于宫颈肌瘤位置较低,病灶大可以压迫周围血管、输尿管及其他盆腔脏器,MRI 表现为形态规则肿物,边缘清,T1WI 等信号、T2WI 低信号、DWI 扩散不受限;肌瘤发生变性时MRI 表现多样,T1WI 及T2WI 呈高低混杂信号,增强后病灶强化方式多数与肌层一致,信号强度与肌层相似或低于子宫肌层。宫颈息肉是慢性宫颈炎的一种临床表现,是子宫颈部位最常见的良性病变,MRI 表现为条状或结节状,T1WI 呈低信号,T2WI 呈中高信号,有时与增厚的宫颈黏膜信号相似,极易漏诊。增强后与邻近肌层强化相似,略低于内膜强化程度。
子宫颈癌主要包括宫颈鳞状细胞癌、腺癌、腺鳞癌及其他少见类型,其中鳞状细胞癌最常见,约占80%,分为HPV 相关型和HPV 不相关型,单独根据形态学不能区分时则必须进行P16 免疫染色或HPV 检测。腺癌占15%~20%,亦分为HPV 相关性腺癌和HPV 非相关性腺癌。各种病理类型中鳞癌的预后最好,宫颈腺癌和腺鳞癌的预后相对较差,这种差别在晚期患者中更为明显。宫颈神经内分泌肿瘤分为类癌及神经内分泌癌(大细胞神经内分泌癌及小细胞神经内分泌癌)。宫颈类癌罕见,神经内分泌癌具有高度侵袭性,就诊时远处转移常见。
宫颈癌MRI 表现为宫颈管扩大,外缘不规则或不对称,肿块表现为不规则形,T1WI 呈中低信号,T2WI 呈中高信号,DWI 上扩散受限、局部高信号,ADC 值低于宫颈基质黏膜。动态增强显示早期明显强化,静脉期及延迟期逐渐廓清,至延迟期信号强度低于周围基质,增强曲线多为平台型及流出型。有研究发现肿瘤的ADC 值[12]有助于定性鉴别,良性肿瘤的ADC 值高于恶性肿瘤,宫颈鳞癌ADC平均值为(0.95±0.12)×10-3mm2/s,宫颈腺癌ADC 平均值为(1.02±0.23)×10-3mm2/s,其中也有特例,宫颈小细胞神经内分泌癌ADC 平均值为(0.54±0.11)×10-3mm2/s。此外,MRI 可准确反映对宫旁侵犯、阴道壁受侵、盆壁及膀胱直肠受侵、淋巴结转移的情况,可准确术前分期、评价术前化疗、放疗疗效,可作为首选的影像学检查。
宫颈癌临床取活检相对容易,影像学检查的目的是对肿瘤进行分期。子宫颈癌分期系统包括国际抗癌联盟(Union for International Cancer Control,UICC)和美国癌症联合委员会(American Joint Committee on cancer,AJCC)的肿瘤-淋巴结-转移(tumor node metastasis,TNM)系统(2021年第九版)[13]和国际妇产科学联盟(International Federation of Gynecology and Obstetrics,FIGO)系统(2018 年更新版)[14]。本版分期标准相对于上一版有比较大的改动,首先是在ⅠA 期诊断中,不再考虑水平间质浸润宽度,新版标准仅根据间质浸润深度来区分ⅠA1 期和ⅠA2 期,主要是考虑宽度可能会受人为因素的影响。其次是细化了ⅠB 期的亚分期,由原来的2 个亚分期增加到3 个亚分期,更有利于患者术后辅助治疗选择和预后判断。最后一个重要的变化就是将淋巴结转移纳入分期系统,将淋巴结转移定义为ⅢC 期。
宫颈癌ⅠA 期的MRI 可表现为阴性,重点需对ⅡA1及ⅡA2 期、ⅡA 及ⅡB 期以及盆腔转移性增大淋巴结准确诊断,因这几个期别与临床治疗原则密切相关,影响患者预后。ⅡA1 肿瘤最大径线小于等于4 cm、ⅡA2 肿瘤最大径线大于4 cm,MRI 轴位及矢状位测量肿瘤上下径、前后径及横径。病灶超出宫颈、最大径小于4 cm 则为ⅡA1期,大于4 cm 则为ⅡA2 期。宫颈癌诊疗指南(2023 版)[15]中,ⅡA1、ⅡA2 期在非保留生育要求治疗的Ⅰ级推荐及Ⅲ级推荐,两者在淋巴结清扫范围等方面有很大不同,故MRI 准确测量肿瘤大小同样至关重要。ⅡA 及ⅡB 期诊断的关键点为宫旁是否受侵。病灶破坏宫颈筋膜环是宫旁受侵的标志、T2WI 表现为宫颈肌层外低信号环的不完整,ⅡA 期可手术,但ⅡB 期属中晚期宫颈癌,Ⅰ级推荐放化疗、Ⅱ级放疗。有研究表明,影像学评估病灶侵犯范围较实际局限,故ⅡA 期临床医师手术时应充分淋巴结清扫。FIGO系统(2018 年版)指出盆腔或腹主动脉旁只要发现转移性增大淋巴结、无论原发病灶大小及范围,即为宫颈癌ⅢC期,故准确评判盆腔内腹主动脉周围淋巴结性质至关重要。常规MRI 判定标准表现为短径/长径大于0.7 并短径大于10 mm,边缘毛糙,增强为均匀强化或环形强化,DWI为高信号,ADC 值明显减低。文献报道MRI 以淋巴结短径大于10 mm 视为淋巴结转移,忽略了更小的短径淋巴结转移,故MRI 在准确评判转移性淋巴结中准确率相对较低,指南中增加了淋巴结转移的证据。
宫颈癌治疗手段包括手术、放疗、系统性治疗(包括化疗、免疫治疗和靶向治疗)[16]。早期宫颈癌的手术与根治性放疗两者的疗效相当,5 年生存率、病死率、并发症发生率相似。由于放疗可能导致的相关并发症,对于未绝经患者,特别是年龄小于45 岁并无禁忌证的患者可选择手术。对于符合条件,有保留生育要求的患者尽量采用保留生育的术式。对于局部晚期宫颈癌(ⅠB3 期和ⅡA2 期)首选同步放化疗,在放疗资源匮乏地区也可选择手术。对于ⅡB 期至ⅣA 期宫颈癌,治疗方式首选同步放化疗。对于ⅣB 期宫颈癌一般以系统性治疗为主,部分患者可联合个体化放疗。
总之,宫颈恶性肿瘤的影像学诊断首选MRI。对于特殊类型的宫颈胃型腺癌,因临床症状隐匿,早期诊断困难,确诊时大多数患者处于进展期,病灶可表现为实性或囊实性肿物,MRI 上具有一定的特征性。需要强调的是无论是鳞癌还是腺癌,分期仍然是最重要的临床预后因素。