Pt-Ni/SiC 催化肉桂醛选择性加氢性能
焦志锋,姚梦梦,赵吉晓,郭向云
(常州大学 石油化工学院,江苏 常州 213164)
氢化肉桂醛是一种重要的化工中间体,广泛用于食用香精、化妆品及药物等的生产过程中[1-2]。通常采用肉桂醛选择性加氢制备氢化肉桂醛,但肉桂醛分子中同时含有C=C 和C=O 两种不饱和键,在加氢过程中存在三种主要的加氢产物,即肉桂醇、氢化肉桂醛和氢化肉桂醇[3]。因此,如何高选择性地制备氢化肉桂醛仍是一个具有挑战的难题。
目前人们研究较多的是贵金属催化剂[4-5]。贵金属活性高,但价格昂贵,对加氢产物的选择性较差。相比之下,非贵金属因储量丰富、价格低廉受到了研究者的青睐。研究结果表明,金属Ni 因d带宽度较窄有利于氢化肉桂醛的生成。如 Ni/La2O3催化肉桂醛加氢反应,产物主要为氢化肉桂醛[6]。在Pd/SBA-15 中添加Ni 能明显提高C=C 加氢的活性,氢化肉桂醛的选择性可达87.8%[7]。但单组分Ni 催化剂加氢活性较低,如果在其中掺入少量贵金属构建双金属催化剂,则有望显著提高催化剂的加氢活性[8]。
高比表面积SiC 不仅具有良好的导电、导热性能,且和金属组分之间可发生电子转移,作为催化剂载体在许多反应中表现出了独特的性能[9-10]。研究结果表明,SiC 不仅可作为活性组分的载体,也可为反应底物提供活性表面[11]。
本工作以高比表面积的SiC 为载体,制备了Ni/SiC 和Pt-Ni/SiC 催化剂,研究Pt 的加入对催化剂结构、电子状态以及肉桂醛加氢性能的影响,并对双金属催化剂性能提高的原因进行了探究。
1 实验部分
1.1 试剂及仪器
SiC:比表面积30 m2/g,常州永蓁材料科技有限公司;肉桂醛:纯度大于99.5%(w),上海阿拉丁生化科技股份有限公司;H2PtCl6·6H2O(Pt 含量不小于37.0%(w))、聚乙烯吡咯烷酮K3(PVP,优级纯)、Ni(NO3)2·6H2O(分析纯)、甲醇(分析纯)、异丙醇(分析纯)、乙醇(分析纯):国药集团化学试剂有限公司。
JEOL JEM-2100 型透射电子显微镜:日本电子株式会社;D/Max 2500 型X 射线粉末衍射仪:日本理学公司;Thermo ESCALAB 250XI 型X 射线光电子能谱仪:美国赛默飞世尔科技公司;Agilent 725 型电感耦合等离子体质谱分析仪(ICPOES):美国安捷伦科技公司;TENSOR27 型傅里叶变换红外光谱仪:德国布鲁克仪器公司;TP-5080-D 型程序升温化学吸附仪:天津先权工贸发展有限公司。
1.2 Ni/SiC 和Pt-Ni/SiC 催化剂的制备
采用硝酸氧化法对SiC 进行预处理。称取500 mg 的SiC,将其分散在7.5 mL 的去离子水中,加入1.12 mL 的70%(w)HNO3溶液,得到悬浮液;在60 ℃下,搅拌悬浮液400 min,冷却至室温后,滤出固体,用去离子水洗涤固体至中性,干燥,储存备用。
采用液相还原法制备Ni/SiC 和Pt-Ni/SiC 催化剂。首先称取600 mg 的PVP 溶解于15.8 mL 去离子水中,然后加入475 mg 上述处理过的SiC,在搅拌下逐滴加入4.2 mL 的Ni(NO3)2·6H2O(30 mg/mL)水溶液。搅拌均匀后移入高压反应釜内,用H2置换3 次后充入2 MPa 的H2,升温至150 ℃后保持2 h。反应结束后冷却降温,对混合液进行抽滤、洗涤、干燥,最后得到理论负载量为5%(w)的Ni/SiC 催 化 剂。将4.2 mL 的Ni(NO3)2·6H2O(30 mg/mL)替换为0.33 mL 的H2PtCl6·6H2O(4 mg/mL) 和4.12 mL 的Ni(NO3)2·6H2O(30 mg/mL)水溶液,重复上述步骤即可制得Pt-Ni/SiC 催化剂。
所有催化剂在性能测试前均先进行还原:称取100 mg 制备的催化剂装入氧化铝瓷舟中,并放置于管式炉内。向炉内充入10%(φ)H2-N2混合气,维持气体流量为40 mL/min,以10 ℃/min 的速率升温至450 ℃,保温1 h。然后在N2气氛下降至室温,催化剂取出后迅速置于反应釜中进行加氢反应。
1.3 肉桂醛选择性加氢性能测试
加氢反应在100 mL 不锈钢高压反应釜中进行。将上述还原后的Ni/SiC 或Pt-Ni/SiC 催化剂(100 mg)、20 mL 溶剂和1 mmol 肉桂醛加入反应釜中,用H2置换3 次后充入1 MPa H2,在磁力搅拌下升温至反应温度(50 ~90 ℃)后反应一定时间(2 ~6 h)。待反应结束冷却至室温后,取出部分反应液,高速离心分离得到的上清液进行检测分析。下层催化剂用异丙醇清洗3 次后干燥,在10%(φ)H2-N2混合气中还原进行稳定性实验。
1.4 In-situ FTIR 测试
将催化剂与KBr 按质量比为1∶20 混合并研磨均匀,装入原位池中。首先升温至200 ℃,在Ar 气氛下吹扫2 h 以除去催化剂表面的水分和杂质。冷却至室温后,采集背景,滴加5 μL 肉桂醛,继续采用Ar 进行吹扫,在500 ~4 000 cm-1范围内进行分析,分辨率为4 cm-1。每间隔5 min 记录一次,直至不再变化为止。
1.5 H2 吸附量测试
称取100 mg 催化剂放入石英管中,将石英管置于程序升温吸附仪中。首先将催化剂升温至200℃(升温速率为10 ℃/min),并利用10%(φ)H2-N2混合气预处理2 h;然后在N2氛围下升温至300 ℃吹扫30 min,再降温至40 ℃进行H2脉冲吸附,记录吸附曲线,计算得出不同催化剂对H2的吸附量。
2 结果与讨论
2.1 催化剂表征结果
图1 为Ni/SiC 和Pt-Ni/SiC 催化剂的XRD 谱图。从图1 可看出,无论是单金属Ni 还是双金属Pt-Ni 催化剂,都只在2θ=35.7°,41.3°,59.8°,71.6°,75.5°处出现了与SiC 对应的衍射峰,没有出现与金属对应的衍射峰,这可能是因为金属负载量低、尺寸小且高度分散在SiC 载体表面。
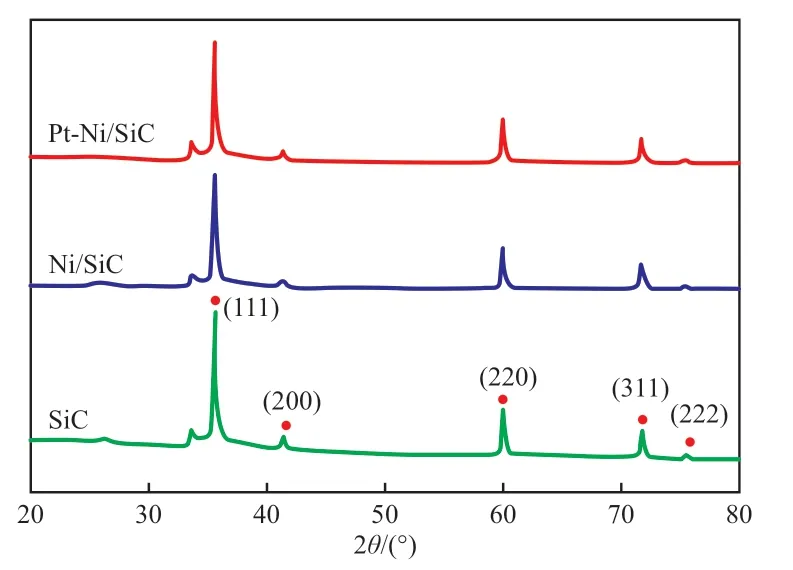
图1 不同催化剂的XRD 谱图Fig.1 XRD patterns of different catalysts.
ICP-OES 表征结果表明,Pt-Ni/SiC 催化剂中Pt 的负载量为0.08%(w),Ni 的负载量为4.36%(w)。
图2 为Ni/SiC 和Pt-Ni/SiC 催 化 剂 的TEM 照片。由图2 可知,Ni 颗粒和Pt-Ni 颗粒都均匀分布在SiC 表面,平均粒径分别为5.2 nm 和4.3 nm,与XRD 表征结果一致。
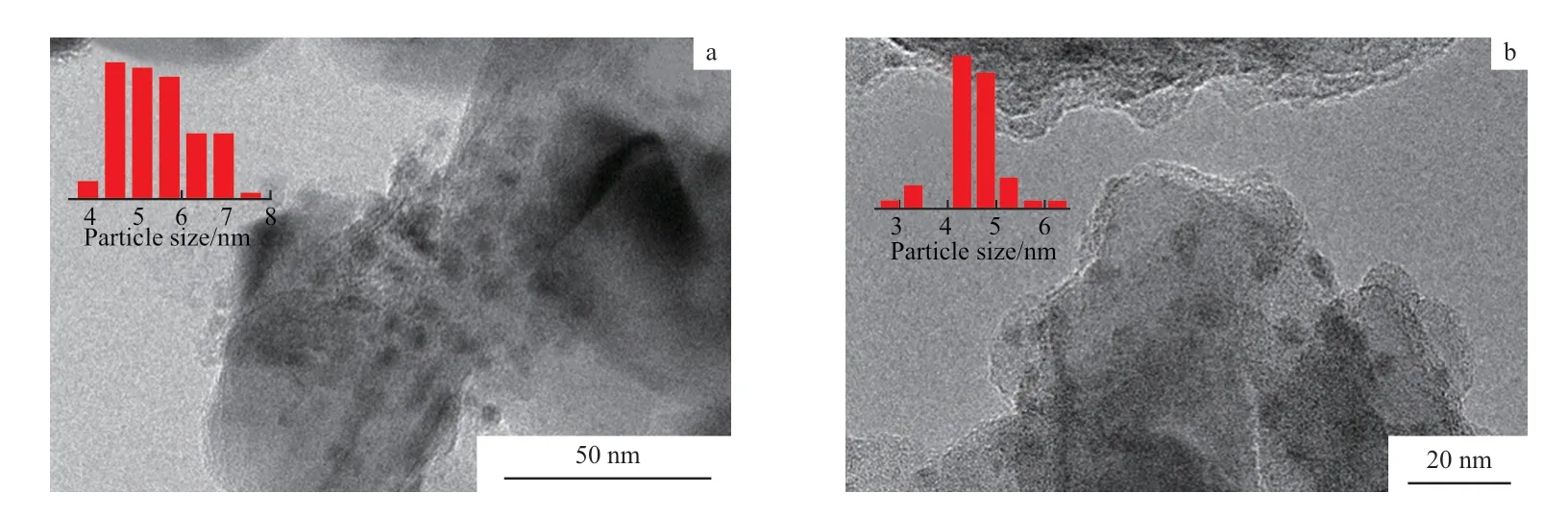
图2 Ni/SiC(a)和Pt-Ni/SiC(b)催化剂的TEM 照片Fig.2 TEM images of Ni/SiC(a) and Pt-Ni/SiC(b) catalysts.
图3a 为添加Pt 前后催化剂中Ni 2p轨道的XPS 表征结果。从图3a 可看出,Ni/SiC 催化剂中Ni 2p3/2的结合能为856.0 eV,可归属为NiO 的特征峰[12]。当在催化剂中添加少量Pt 后,Ni 2p3/2的峰位置向高结合能方向移动,说明双金属催化剂中Ni 的电子云密度降低。图3b 是Pt/SiC 和Pt-Ni/SiC 的Pt 4f轨道的XPS 表征结果。与Pt/SiC 相比,Pt-Ni/SiC 中Pt 4f7/2轨道的电子结合能向低结合能方向移动(由70.9 eV 下降至70.8 eV),即电子云密度提高了。综上可知,在Pt-Ni/SiC 中Ni 的电子向Pt 发生迁移。一般来说,富电子的Pt 更有利于H2的吸附和解离。图3b 中,与Pt-Ni/SiC中Pt 4f电子结合能对应的峰的强度非常低,这可能是因为双金属催化剂中Pt 的含量较低。
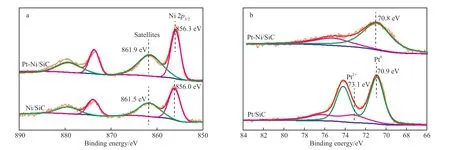
图3 Ni/SiC 和Pt-Ni/SiC 的Ni 2p(a)及Pt 4f(b)XPS 谱图Fig.3 Ni 2p(a) and Pt 4f(b) XPS patterns of Ni/SiC and Pt-Ni/SiC.
2.2 肉桂醛选择性加氢性能
考察了Ni/SiC 和Pt-Ni/SiC 对肉桂醛选择性加氢的催化性能。实验结果表明,单金属Ni/SiC 对肉桂醛加氢的活性非常低,几乎可以忽略不计。在Ni/SiC 中加入0.1%(w)Pt 后,催化剂对肉桂醛的加氢活性显著提升,可高效催化肉桂醛加氢生成氢化肉桂醛。
以Pt-Ni/SiC 为催化剂,研究了反应温度、反应时间、溶剂等因素对肉桂醛加氢性能的影响,结果见图4 ~5 及表1。从图4 可看出,反应温度对催化剂的加氢性能影响较大。随反应温度的升高,肉桂醛的转化率逐渐提高。当反应温度升至70 ℃时,反应物几乎全部转化(肉桂醛转化率为99.3%)。氢化肉桂醇选择性随温度的变化正好相反,当温度为60 ℃时,氢化肉桂醛的选择性最高(89.4%),反应温度大于70 ℃时选择性下降,主要产物变成了3-苯丙醇。因此,在后续的实验中选择60 ℃ 为反应温度。
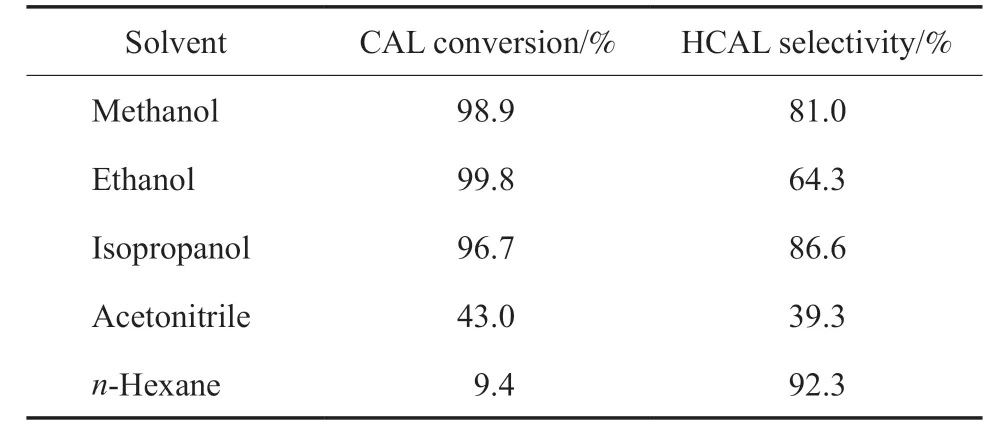
表1 溶剂对肉桂醛选择性加氢性能的影响Table 1 Effect of solvents on selective hydrogenation performance of cinnamaldehyde
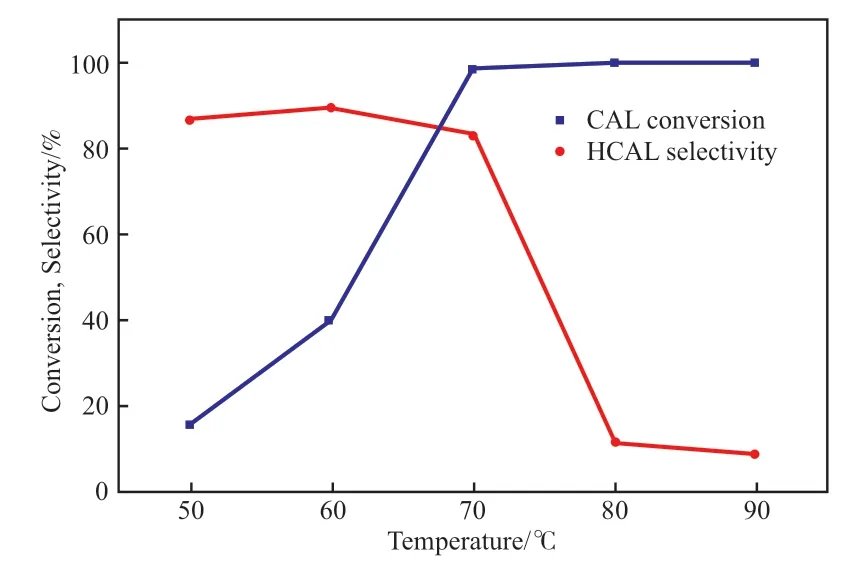
图4 反应温度对Pt-Ni/SiC 肉桂醛加氢性能的影响Fig.4 Effect of reaction temperature on hydrogenation performance of cinnamaldehyde over Pt-Ni/SiC.
从图5 可看出,随反应时间的延长,肉桂醛的转化率不断提高,但氢化肉桂醛的选择性变化不大。当反应时间为5 h 时,目标产物的收率最高,肉桂醛转化率96.7%,氢化肉桂醛选择性86.6%。当反应时间延长至6 h 时,虽然肉桂醛的转化率达到100%,但氢化肉桂醛的选择性有所下降(79.8%)。
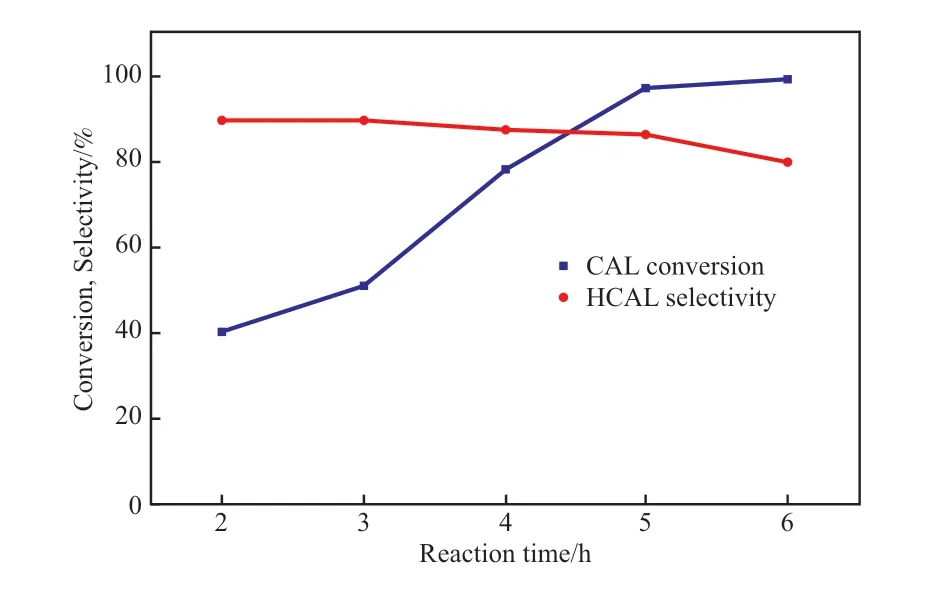
图5 反应时间对肉桂醛选择性加氢性能的影响Fig.5 Effect of reaction time on selective hydrogenation performance of cinnamaldehyde.
由表1 可知,与中等极性的乙腈和非极性的正己烷相比,在甲醇、乙醇和异丙醇这类强极性溶剂中,催化剂的加氢活性更高,这可能是因为催化剂在乙腈和正己烷中分散性较差。
综上所述,当反应温度为60 ℃、反应时间为5 h、异丙醇为溶剂时肉桂醛加氢制备氢化肉桂醛的性能最优。在最优反应条件下,研究了Pt-Ni/SiC 催化剂的循环稳定性,结果见图6。
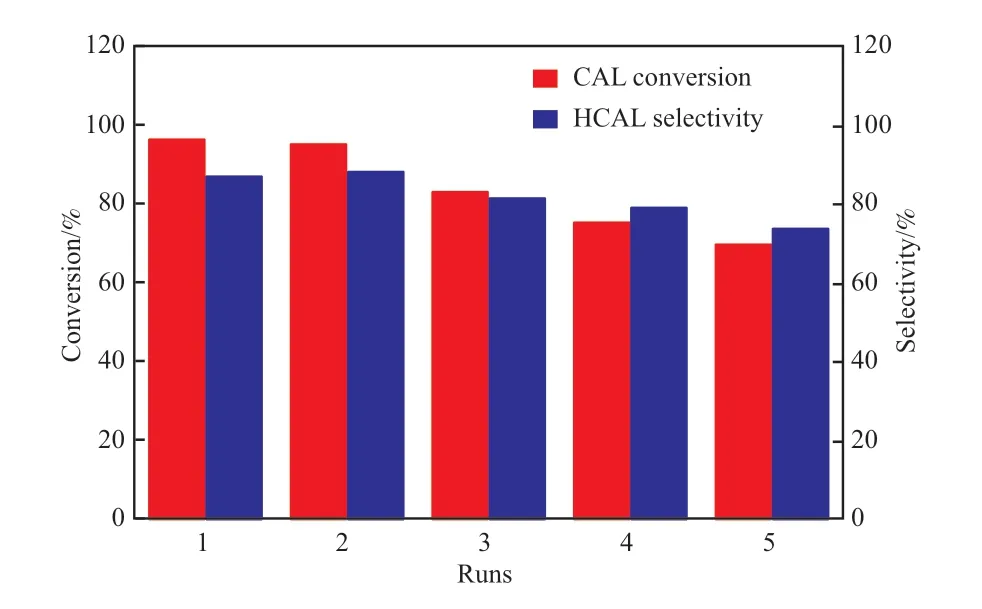
图6 Pt-Ni/SiC 对肉桂醛选择性加氢的循环稳定性Fig.6 Cyclic stability of Pt-Ni/SiC for selective hydrogenation of cinnamaldehyde.
从图6 可看出,催化剂循环使用2 次后,催化剂的活性和选择性变化较小。但催化剂循环使用5次后,肉桂醛转化率和氢化肉桂醛选择性均有明显下降,这可能是因为多次高温还原过程使催化剂中金属的粒径有所变化以及回收过程中少量催化剂的流失。
2.3 催化机理研究
利用in-situ FTIR 研究了肉桂醛分子在不同催化剂表面的吸附行为,结果见图7。从图7 可看出,肉桂醛分子中C=O 键在SiC,Ni/SiC,Pt-Ni/SiC表面的吸收峰位置基本相同(约1 692 cm-1),说明C=O 键主要吸附在SiC 载体表面。但肉桂醛分子中C=C 键在不同催化剂表面吸附的峰位置却有所差异。相较于SiC(约1 632 cm-1),C=C 键在Ni/SiC 表面的吸收峰位置明显发生偏移(约1 629 cm-1),说明负载Ni 后C=C 键更容易在金属Ni表面吸附活化,这一结论与文献报道结果相符[13]。从Pt-Ni/SiC 对应的红外光谱可以看出,C=C 键吸收峰位置明显向更低波数偏移(约1 627 cm-1),说明少量Pt 的加入有利于C=C 键的吸附和活化。这可能是Pt-Ni/SiC 能够高效催化肉桂醛选择性加氢制氢化肉桂醛的主要原因。
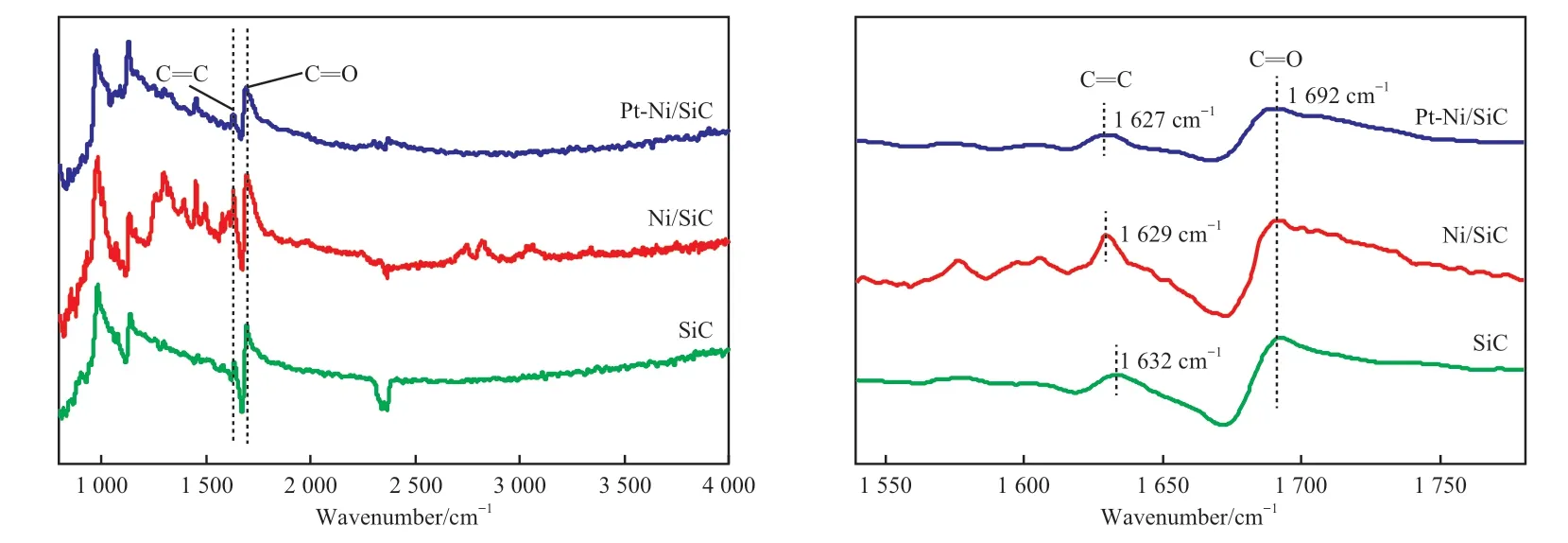
图7 肉桂醛在不同催化剂上吸附时的in-situ FTIR 谱图Fig.7 In-situ FTIR spectra of cinnamaldehyde adsorbed on different catalysts.
结合H2脉冲吸附和氢溢流实验研究了不同催化剂对H2的吸附解离能力。H2脉冲吸附实验结果表明,双金属Pt-Ni/SiC 的H2吸附量明显高于Ni/SiC,从7.6 μmol/g 增加至11.4 μmol/g。进一步考察了催化剂的氢溢流效应,结果见图8。从图8 可看出,Ni/SiC 催化剂的氢溢流现象不明显,通入氢气120 min 后混合物的颜色变化很小。而Pt-Ni/SiC 催化剂则出现了明显的氢溢流现象,60 min 后混合物由浅黄色变为蓝色。说明Pt 的加入增强了催化剂对H2的吸附和解离作用。

图8 Ni/SiC 和Pt-Ni/SiC 的氢溢流结果Fig.8 Results of hydrogen spillover on Ni/SiC and Pt-Ni/SiC catalysts.
由以上结果推测,Pt-Ni/SiC 催化肉桂醛加氢的反应过程可能为:肉桂醛分子中的C=C 键在Ni表面吸附并活化,H2在Pt 表面解离后产生活性氢,活性氢进一步溢流到Ni 表面与吸附态肉桂醛发生反应生成氢化肉桂醛。
3 结论
1)当反应温度为60 ℃、反应时间为5 h、以异丙醇为溶剂时,Pt-Ni/SiC 催化肉桂醛加氢制备氢化肉桂醛的性能最优,肉桂醛转化率为96.7%,氢化肉桂醛选择性为86.6%。
2)Pt-Ni/SiC 催化剂中Ni 的电子会向Pt 发生迁移,使Pt 处于富电子状态,增强了Pt 对H2的吸附和活化。
3)H2在Pt 表面解离后产生活性氢,氢物种进一步溢流到Ni 表面与吸附在Ni 表面的C=C 双键发生反应生成氢化肉桂醛。

