基于H 省药品不良反应真实世界数据对信号检测方法的比较研究
夏旭东
河南省药品评价中心
药品监测科
柳鹏程
中国药科大学国际医药商学院
周明
中国药科大学国际医药商学院
敬赟鑫
中国药科大学国际医药商学院
莫鸿仪
中国药科大学理学院
国林楠
中国药科大学理学院
朱依曦*
中国药科大学国际医药商学院
目前,药品不良反应(adverse drug reaction,ADR)监测系统是获取ADR数据的重要途径,也是药物警戒系统的重要组成部分。在我国,国家药品不良反应监测中心主要通过药品上市许可持有人(marketing authorization holder,MAH)和医疗机构报告2 种途径收集ADR 报告,并形成ADR 数据库。基于ADR 数据库中的ADR 数据,利用报告比值比(reporting odds ratio,ROR)法、英国药品和保健产品管理局(Medicines and Healthcare Products Regulatory Agency,MHRA)综合标准法、贝叶斯置信传播神经网络(Bayesian confidence propagation neural network,BCPNN)法、比例报告比值比(proportional reporting ratio,PRR)法等几种常用的信号检测方法对数据库中的药品进行信号检测[1-3],能够识别潜在的ADR 信号,为药品上市后安全性研究提供相关证据支持。
信号检测方法目前尚无金标准[4]。在选择信号检测方法时,必须深入研究相应的数据结构。从另一个角度来说,只有实践才能知道哪种方法更适用于哪种数据库。有研究者基于美国食品药品监督管理局不良事件报告系统(FDA adverse event reporting system,FAERS)中的数据,分别对巴瑞替尼、利伐沙班、阿法替尼进行信号检测,研究分析潜在的ADR[5-7]。还有研究者运用FAERS 数 据,对ROR 法、BCPNN 法等多种信号检测方法的灵敏度进行比较研究[8],结果显示BCPNN 法的灵敏度可能更高。然而,上述研究的数据来源均为美国FAERS。对于来源于我国ADR 监测系统的ADR 数据,进行信号检测方法学比较分析的研究仍较少。
因此,本研究作为一篇方法学研究文献,以H 省药品不良反应监测中心上报的ADR 数据作为数据来源,分别使用ROR 法、MHRA 法、BCPNN 法对国家药监局提示出现安全风险信号的药品进行检测,比较3 种信号检测方法间的灵敏度差异,探索适合H 省ADR 数据库的信号检测方法,以期吸引更多研究者参与我国药物警戒信号检测方法学研究。
1 方法
1.1 数据来源
本研究的数据来源于H 省药品不良反应监测中心的ADR 数据库,报告主要来源为医疗机构与患者个人,内容包含ADR 上报时间、患者信息(性别、年龄、原患疾病等)、用药情况(用药名称、用药时间、用药剂量等)与ADR 发生情况(ADR 发生时间、严重性、转归情况)等信息。本研究选取数据库中2016 年1 月至2020 年12 月期间收集的所有不良反应和(或)事件报告。
1.2 数据处理
从数据库获取数据后,对数据进行初步处理:首先,删除不同上报来源的重复报告,取上报时间最新的数据;其次,删除上报时间缺失、患者ADR 缺失及ADR 不明确或无法辨认的报告;最后,以监管活动医学词典(medical dictionary for regulatory activities,MedDRA)24.1 版不良反应术语集为规范化处理标准,用Python3.10 软件实现编码自动化处理,将数据库中的所有ADR数据编码为MedDRA 首选术语(preferred term,PT),同时自动匹配系统器官分类(system organ class,SOC)[9],从 而完成数据的初步处理。
之后,进行数据库二次处理:对5 年的数据按季度分组,并进行依次累加。每组数据含有从2016 年第1 季度开始至当前季度的所有累积数据。最终,形成20 个小型季度组合数据库,分别编号为2016Q1、2016Q2、2016Q3……2020Q4。
1.3 药品-事件选择
从2021~2022年国家药监局发布的药品公告通告(https://www.nmpa.gov.cn/yaopin/ypggtg/index.html)中,选取需要修订药品说明书安全性内容的10 种药品,具体包括:西咪替丁注射制剂、阿米卡星注射剂、奥沙利铂制剂、盐酸甲氧氯普胺注射液、甲氧氯普胺片、注射用生长抑素、银杏达莫注射液、阿米卡星注射剂、全身用氟喹诺酮类药品、康复新液与奥拉西坦注射制剂。
对于以上药品相关的具体ADR,选取国家药监局公示的安全性内容以及药品说明书中原有记录的合集。
1.4 数据分析
分别采用ROR 法、MHRA法、BCPNN 法这3 种信号检测方法对上述10 种药品进行信号检测。计算基于构建的目标药品及其他所有药品,列为目标疑似ADR 及其他所有疑似ADR 的2×2 矩阵表。获取首要怀疑药品的目标ADR 报告数及ADR 发生的背景数等数据后,根据公式分别计算ROR、PRR 及信息成分(information component,IC)值(指所关注药品和所关注事件同时出现的关联强度)[10]。将ROR 法中95%置信区间(CI)下限大于1 且报告数不少于3 例的事件、MHRA 法中PRR ≥2、χ2≥4 且报告数不少于3 例的事件、BCPNN 法中IC-2SD>0且报告数不少于3 例的事件定义为ADR 信号,统计分析采用Microsoft Excel 2019 版软件。
将上述3 种信号检测方法的检测结果与上述10 种药品的修订后说明书进行对比,通过比较采用每种方法发现的信号总数、信号在药品说明书中的体现情况及每个信号最早被检测出来的时间,进而比较方法间的灵敏度差异。
2 结果
2.1 数据处理结果
2016 年1 月 至2020 年12月,H 省药品不良反应监测中心的ADR 数据库中共有570 876 例ADR 报告,删除上报时间缺失、患者ADR 缺失及ADR 不明确或无法辨认的报告后剩余569 843 份。
2.2 信号数量比较
2.2.1 检测出的所有药品不良反应信号
采用上述3 种信号检测方法对20 个季度组合检测出的10 种药品的所有ADR 信号如表1 所示。对于西咪替丁注射液,采用ROR 法、MHRA 法、BCPNN 法分别检测出13、9、10 个信号;对于注射用奥沙利铂,分别检测出28、24、23个信号;对于盐酸甲氧氯普胺注射液,分别检测出23、22、21个信号;对于甲氧氯普胺片,3种方法均检测出13 个信号;对于注射用生长抑素,分别检测出3、2、3 个信号;对于银杏达莫注射液,分别检测出21、10、11 个信号;对于硫酸阿米卡星注射液,分别检测出22、19、20 个信号;对于盐酸左氧氟沙星注射液(属于氟喹诺酮类药品),分别检测出30、23、26个信号;对于康复新液,分别检测出2、2、1 个信号;对于注射用奥拉西坦,分别检测出4、3、1 个信号。针对上述每种药品使用ROR 法检测出的ADR 信号数量最多(对于甲氧氯普胺片用3 种信号检测方法检测出的信号数量相同)。

表1 采用3 种信号检测方法检测出的10 种药品的不良反应信号
2.2.2 药品不良反应信号在药品说明书中的体现
采用3 种方法检测出的ADR信号在药品说明书中的占比情况如图1 所示。西咪替丁注射液、注射用奥沙利铂、盐酸甲氧氯普胺注射液、甲氧氯普胺片、注射用生长抑素、银杏达莫注射液、硫酸阿米卡星注射液、盐酸左氧氟沙星注射液、康复新液、注射用奥拉西坦说明书中15.24%、23.58%、55.00%、32.50%、7.02%、27.45%、45.19%、40.51%、9.26%、5.13% 的ADR 被检测出来。

图1 采用3 种方法检测出的药品不良反应信号在药品说明书中的占比情况
除对于甲氧氯普胺片用3 种信号检测方法检测出的ADR 信号数量相同外,对于其余9 种药品用ROR 法检测出的信号数量最多,其检测出的信号数量在说明书中平均占比29.79%,而MHRA法与BCPNN法检测出的信号数量在说明书中平均占比均为24.24%。
2.2.3 新的药品不良反应信号及其占比
使 用ROR 法、MHRA 法、BCPNN 法,分别检测出西咪替丁注射液4、2、2 个新的ADR信号,在采用上述3 种方法检测出的所有信号数量中的占比分别为30.77%、22.22%、20.00%;注射用奥沙利铂分别检测出8、7、6 个新信号,在所有信号中分别占比28.57%、29.17%、26.09%;盐酸甲氧氯普胺注射液分别检测出6、5、5 个新信号,在所有信号中分别占比26.09%、22.73%、23.81%;对于甲氧氯普胺片均检测出3 个新信号,在所有信号中均占比23.08%;银杏达莫注射液分别检测出9、6、4 个新信号,在所有信号中分别占比42.86%、60.00%、36.36%;硫酸阿米卡星注射液分别检测出12、10、10个新信号,在所有信号中分别占比54.55%、52.63%、50.00%;盐酸左氧氟沙星注射液分别检测出4、2、2 个新信号,在所有信号中分别占比13.33%、8.70%、7.69%;对于注射用生长抑素、康复新液、注射用奥拉西坦均未检测出新信号(图2)。

图2 采用3 种方法检测出的新的药品不良反应信号占比情况
对于上述10种药品,用ROR 法、MHRA 法、BCPNN法检测出的新信号的平均占比分别为21.92%、21.85%、18.70%。其中,采用ROR 法发现的新信号数量最多,MHRA 法次之,BCPNN 法最少。
2.3 药品不良反应信号出现时间比较
2.3.1 方法间产生时间差异的信号占比
采用3 种信号检测方法检测结果产生时间差异的ADR 信号数量占比情况如图3 所示。对于注射用奥沙利铂、盐酸甲氧氯普胺注射液、甲氧氯普胺片与硫酸阿米卡星注射液这4 种药品,3 种方法没有时间差异的ADR 信号数量占比较高;西咪替丁注射液、注射用生长抑素、银杏达莫注射液等6 种药品的ADR 信号中,3 种方法产生时间差异的ADR 信号数量占比较高,其中康复新液与注射用奥拉西坦检测出的所有信号在方法上均产生了时间差异。在这10种药品中,采用3 种方法检测产生时间差异的信号数量平均占比59.15%,不具有时间差异的信号数量平均占比40.85%,一半以上的药品的ADR 信号具有方法学上的时间差异。
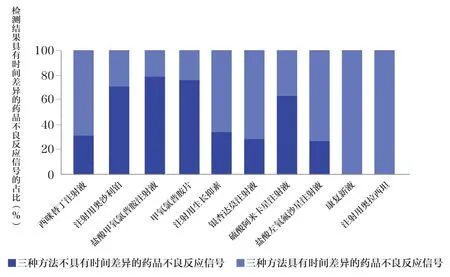
图3 采用3 种信号检测方法检测结果产生时间差异的药品不良反应信号数量占比情况
2.3.2 方法间产生时间差异的药品不良反应信号
本文仅选取前3 种药品产生时间差异的ADR 信号进行详细描述,其他药品最早被检测出的ADR 信号情况在此不再赘述。3 种信号检测方法下,西咪替丁注射液、注射用奥沙利铂、盐酸甲氧氯普胺注射液的最早被检测出的ADR 信号的时间及统计学比较情况如表2 所示(其他药品情况见表3)。其中,西咪替丁注射液的“潮红”信号被ROR 法最早在2019年第2 季度检测出来,被BCPNN法最早在2019 年第4 季度检测出来,上述两方法分别比MHRA 法提早5 个和3 个季度;注射用奥沙利铂的“低血压”信号最早由ROR 法与MHRA 法在2017 年第4 季度被检测出来,比BCPNN 法提早2 个季度;盐酸甲氧氯普胺注射液的“心悸”信号最早由ROR 法在2017 年第2 季度被检测出来,比MHRA 法与BCPNN 法均提早4 个季度。
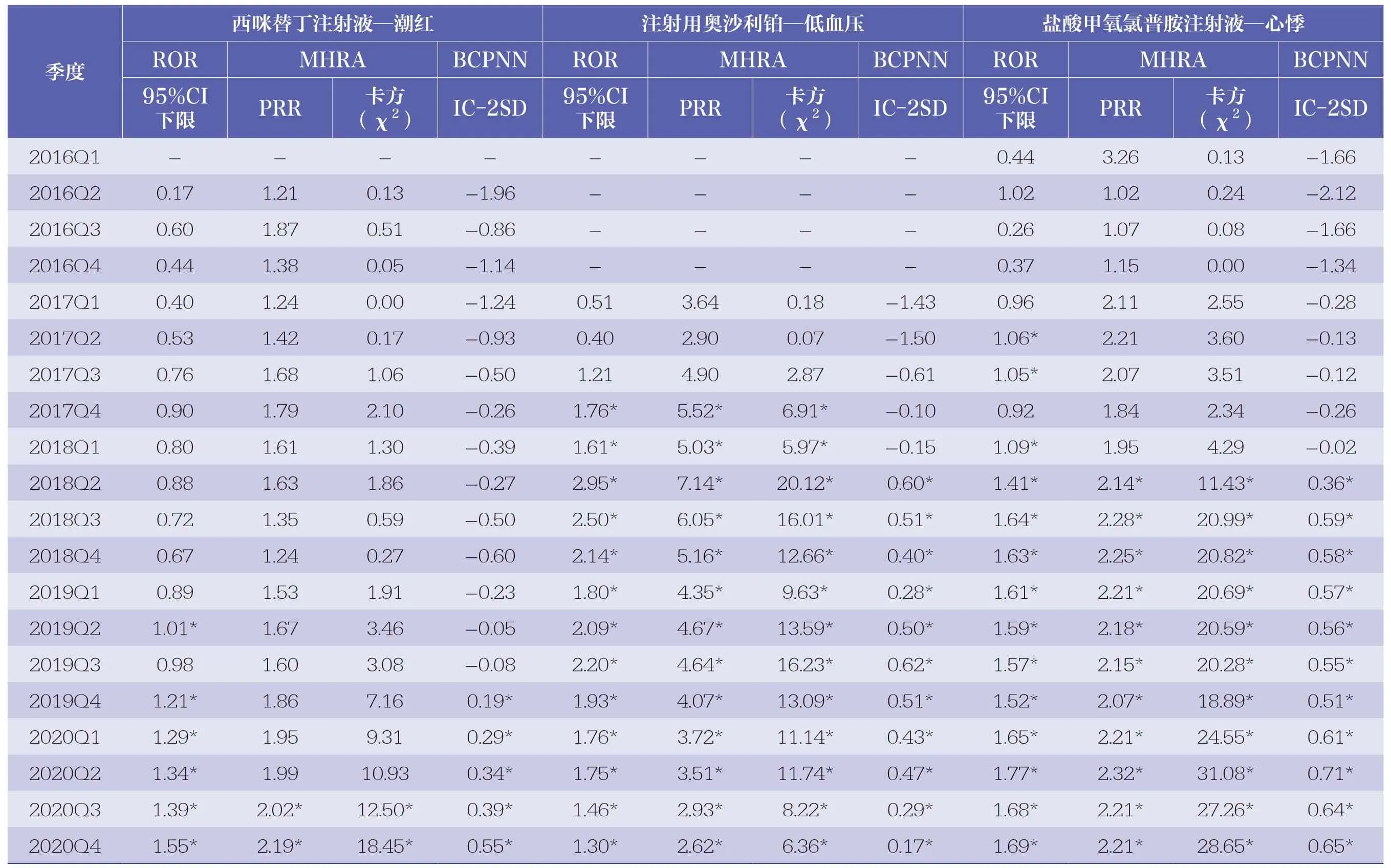
表2 3 种信号检测方法下3 种药品最早被检测出的药品不良反应信号的时间及统计学比较情况
因此,在上述3 种方法中,ROR 法是最早检测出ADR 信号的方法,灵敏度最高;MHRA 法检测出同一信号的时间次之,灵敏度次之;BCPNN 法检测出同一信号的时间最晚,灵敏度最差。
3 讨论
3.1 数据处理结果讨论
本研究数据来自于2016~2020 年H 省药品不良反应监测系统,按季度进行处理后发现,2020 年第2 季度之前,ADR 报告数量的增长趋势较为平稳;从2020 年第3 季度开始,ADR 报告数量增长较快,增长率远大于前18 个季度组合。笔者分析认为,这可能与2019 年12 月1 日MAH 制度的正式实施有关,该制度强化了MAH 上市后研究管理、ADR 监测及报告与处理等责任,因此2020 年H 省上报的ADR 报告数量较前几年大幅增加。
3.2 药品不良反应信号数量比较结果讨论
3.2.1 检测出的所有药品不良反应信号
本文基于H 省药品不良反应监测系统的数据,对西咪替丁注射液、注射用奥沙利铂、盐酸甲氧氯普胺注射液等10 种药品进行ADR 信号检测,结果显示对每种药品使用ROR 法检测出的信号数量最多,使用MHRA 法与BCPNN 法检测出的信号数量平均值相同。
3.2.2 药品不良反应信号在说明书中的体现
在上述10种药品中,采用3 种信号检测方法对盐酸甲氧氯普胺注射液检测出说明书中55.00%的ADR 信号,硫酸阿米卡星注射液检测出45.19%的信号,而注射用奥拉西坦仅检测出5.13%的信号,这可能与每种药品的上市时间及使用量有关。数据库中上报的注射用奥拉西坦上市日期为2020 年1 月,由于上市时间较短,上报的ADR 报告较其他药品少,检测出来的ADR 信号也较其他药品少。
3.2.3 新的药品不良反应信号及其占比
在对10 种药品检测出的所有新ADR 信号中,使用ROR 法、MHRA 法、BCPNN 法检测出的新信号平均占比分别为21.92%、21.85%、18.70%,其中ROR法发现的新信号最多,MHRA 法次之,BCPNN 法最少。由此可见,虽然使用MHRA 法与BCPNN法检测出的信号数量平均值相同,但是MHRA 法比BCPNN 法检测出的新信号数量多。
虽然BCPNN 法检测出的新信号数量较少,但与说明书中的ADR 具有较高的一致性,说明其结果可信度可能较高。同时,虽然ROR 法检测出的信号总数及新信号的数量最多,但是可能存在一定的假阳性。
3.3 药品不良反应信号出现时间比较结果讨论
ROR 法源于荷兰药物警戒中心Lareb 实验室,具有偏倚较少、灵敏度较高等特点,因此应用广泛[11]。MHRA 法是对PRR 法的拓展,其在保证最低组合例数的基础上将PRR 值、绝对报告值和卡方值结合在一起,灵敏度高、结果稳定性高,目前在英国药品和保健产品管理局(MHRA)中广泛使用。但也有研究表明,该方法的灵敏度会随着报告数的增加而下降[12]。目前,BCPNN 法是一种国内外应用比较成熟的信号检测方法,其在数据量较少或者数据缺失的情况下也可以较早检测出信号,且随着报告数的不断增加,其检测结果更加稳定[13],但该方法计算较为复杂,透明度低。
有研究表明,BCPNN 法是上述3 种方法中灵敏度最高的方法,ROR 法次之,MHRA法(该研究者实际使用的PRR法,其信号产生阈值及计算公式目前被称为MHRA 法)灵敏度最差[14]。还有研究显示,PRR 法、BCPNN 法和多项伽马-泊松缩量评估法(multi-item gamma passion shrinker,MGPS)的灵敏度分别为49%、45%和26%,使用修正后的BCPNN方法灵敏度达到51%,灵敏度最高[15]。
本研究在对H 省ADR 数据库进行信号检测时,采用ROR法检测出来的ADR 信号数量是3种方法中最多的,也是最早检测出信号的方法。因此本研究表明,ROR 法灵敏度最高,MHRA 法次之,BCPNN 法灵敏度最差。
此外,在对西咪替丁注射液进行信号挖掘时,“潮红”信号在2019 年第2 季度开始出现后,在2019 年第3 季度信号消失,随后在2019 年第4 季度后一直出现,盐酸甲氧氯普胺注射液的“心悸”信号也出现类似情况,这可能与该ADR 上报例数及数据库中当季其他ADR 报告数量增加有关。
当前,信号检测方法虽然没有金标准,但每种方法都有自己的特点,在不同的数据库中的适用性和实施可能性方面各有优点和缺点[4,16]。例如,美国的FAERS 数据库与我国的国家药品不良反应监测系统的数据库在结构与内容上有所不同,故使用相同的信号检测方法检测出的结果也会有所不同。
3.4 局限性分析
3.4.1 样本量不足
本文基于2016年1月至2020年12月H省药品不良反应监测系统的ADR 数据对10 种药品进行分析研究,样本量相对较小,检测出的ADR 信号仅反映该期间H 省的ADR 发生情况,因此不能将药品说明书上的信号全部检测出来。同时,H 省药品不良反应监测系统上报的ADR数据质量对信号检测结果的准确性也会产生一定的影响。
虽然本研究使用了3 种信号检测方法进行信号检测,但仍无法完全排除假阳性信号,部分信号还可能被漏查。运用信号检测方法检测出的信号只能说明药品与信号存在关联,但不能代表ADR 的群体发生率,其疗效及安全性仍需临床研究论证。
3.4.2 方法适用性有待进一步探索
虽然本研究旨在研究3 种信号检测方法应用于我国ADR 数据库进行信号检测的差异,探索适合我国ADR 数据库的方法,但事实上每种方法的信号产生阈值是基于国外数据库定义的,本文未探索3 种方法用于我国ADR数据库时信号产生的阈值,这可能对信号检测结果的准确性产生一定的影响。
此外,本文得出的ROR 法更适合现阶段H 省ADR 信号检测的结论,是基于H 省ADR数据得到的,不能代表其适用于我国ADR 监测系统中的所有数据,方法间的比较有待进一步研究论证。
4 结论
本研究通过3 种信号检测方法,对H 省药品不良反应监测系统ADR 数据库中西咪替丁注射制剂、阿米卡星注射剂等国家药监局2021~2022 年公示的10 种修订说明书的药品,按照组合季度分别进行ADR 信号检测,每种药品均得到20 个组合季度的信号检测结果。
在信号数量方面,采用ROR法检测出的信号数量与新信号的数量最多;MHRA 法与BCPNN法检测出的信号数量相同,MHRA 法检测出的新信号的数量多于BCPNN 法。在信号出现时间方面,ROR 法是最早检测出信号的方法,灵敏度最高;MHRA法次之,灵敏度次之;BCPNN法检测出信号的时间最晚,在3种方法中灵敏度最差。
综上,在上述3 种信号检测方法中,ROR 法检测出的信号数量与新信号的数量最多,检测出信号的时间最早,灵敏度最高,其可能更适合现阶段H 省的ADR 信号检测工作。但是,在当前信号检测过程中,为了保证信号的全面性及可信度,建议仍采用多种联合的信号检测方法。

