1例替雷利珠单抗致免疫相关性肝炎病例的治疗分析
邓慧
安化县人民医院,益阳 413500
1 病例资料
患者,男性,56岁,身高165cm,体重54kg,体表面积1.59m2,美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)体能状态评分1分。因确诊左肺腺癌并全身多处转移(肝转移、骨转移),2021年5月16日于某院行贝伐珠单抗注射液[Roche Pharma(Schweiz)AG,国药准字SJ20170035,规格100mg(4ml)/瓶]700mg,D1+注射用顺铂[冻干型,齐鲁制药有限公司,国药准字H20023460,注射剂(冻干粉针剂)]700mg,D1+注射用培美曲塞二钠[齐鲁制药有限公司,国药准字H20103287,规格0.1g(按C20H21N5O6计)]0.8g,D1,3周给药1次,联合化疗治疗,患者耐受可。2021年9月8日加用免疫治疗,静脉滴注替雷利珠单抗注射液[广州百济神州生物制药有限公司,国药准字S20190045,规 格100mg(10ml)/瓶]200mg,3周给药1次。治疗期间未使用其他药物及保健品。患者除少许恶心、呕吐感外,未诉特殊不良反应。9月5日患者肝功能基本正常:谷丙转氨酶(alanine aminotransferase,ALT)12.00U/L(9~50U/L),谷草转氨酶(aspartate aminotransferase,AST)15.00U/L(15~40U/L),总胆红素(total bilirubin,TBIL)5.2μmol/L(3~22μmol/L),直接胆红素(direct bilirubin,DBIL)1.6μmol/L(0~8μmol/L)。9月28日患者入院拟行第6次化疗,并诉近日食欲减退,全身乏力。患者无肝炎、结核等传染病史,无高血压、糖尿病等病史,无药物、食物过敏史,无手术外伤史,无饮酒史,无输血史,无献血史,预防接种史有按规定接种。
入院查体:体温36.2℃,脉搏110次/min,呼吸20次/min,血压112/70mmHg;神志清醒;皮肤黏膜无黄染,无肝掌,无蜘蛛痣,无贫血貌;全身浅表淋巴结无肿大;口唇红润;颈软,颈静脉无怒张,肝颈静脉回流征阴性,双侧甲状腺无肿大;双肺呼吸音清、未闻及干湿啰音;心率110次/min,心律齐,无病理性杂音;腹壁柔软,无压痛,无反跳痛,无肝区叩击痛,移动性浊音(-)。完善相关检查:肝病相关自身抗体测定、肝炎全套检测均为阴性。9月29日血常规示:血小板计数65.0×109/L,其余正常。但肝功能示:ALT 407.00U/L,AST 853.00U/L,TBIL 27.7μmol/L,DBIL 20μmol/L,ALB 26.0g/L。血糖及血脂等无异常。考虑患者血小板减少及肝功能受损与化疗及免疫治疗相关,立即予注射用重组人白介素-11[齐鲁制药有限公司,国药准字S20030016,规格1.5mg(1200万U)/瓶]、注射用复方甘草酸苷[瑞阳制药股份有限公司,国药准字H20090231,规格:每瓶含甘草酸苷40mg、甘氨酸400mg和盐酸半胱氨酸20mg]、葡醛内酯片[安徽环球药业股份有限公司,国药准字H34023107,规格50mg]护肝。10月3日患者鼻腔中可见少许凝血,大便可见少许鲜红色血液。完善凝血功能检查示各项指标正常,肝功能:ALT 781.0U/L,AST 1212.0U/L,ALB 27.7g/L,TBIL 95.2μmol/L,DBIL 72.8μmol/L。肝功能进一步受损,考虑患者无肝炎病史、伴肝转移但患者既往4次化疗均未出现肝功能损伤,且第一次行免疫治疗,此次肝功能受损可能与替雷利珠单抗引起的免疫相关性肝炎有关,立即静脉滴注给予注射用甲泼尼龙琥珀酸钠[天津金耀药业有限公司,国药准字H20103047,规格40mg(按C22H30O5计)]80mg,qd冲击治疗。10月4日患者鼻腔未见血痂,大便转黄。10月6日患者肝功能较前明显好转:ALT 349.0U/L,AST 220.0U/L,TBIL 33.8μmol/L,DBIL 23.9μmol/L,调整静脉滴注给予甲泼尼龙琥珀酸至60mg,qd。随后患者肝功能指标逐渐下降,分别于10月9日、10月18日、10月24日将静脉滴注甲泼尼龙琥珀酸调整至40、30mg和20mg,qd。10月25日肝功能ALT 199.0U/L,AST 155.0U/L,TBIL 23.8μmol/L,DBIL 12.8μmol/L。患者病情稳定,当日出院。出院诊断:①肺恶性肿瘤:左下肺腺癌并全身多处转移。②免疫性肝炎。③低蛋白血症。出院后口服给予序贯醋酸泼尼松片[浙江仙琚制药股份有限公司,国药准字H33021207,规格5mg]20mg,qd(一周后更改为10mg)。后续随访患者肝功能稳定,11月8日肝功能:ALT 56.0U/L,AST 55.0U/L,TBIL 17.9μmol/L,DBIL 13.7μmol/L。患者肝功能指标变化情况见图1。
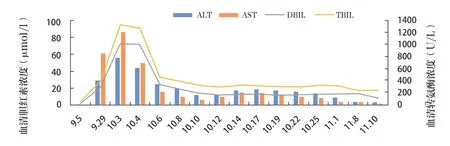
图1 患者肝功能指标变化情况
2 问题
2.1 患者抗肿瘤治疗方案是否合理
患者为56岁男性,左肺腺癌并全身多处转移(肝转移、骨转移),ECOG评分1分,体力状况一般。根据《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南》(2020年版)[1]:Ⅳ期无驱动基因、非鳞状非小细胞肺癌(non-small cell lung cancer,NSCLC)一线治疗可选用贝伐珠单抗与含铂药物联合化疗,同时指南推荐可联合帕博利珠单抗行免疫治疗[1]。
替雷利珠单抗是我国自主研发的程序性死亡受体-1(programmed death receptor-1,PD-1)人源化单克隆抗体,对PD-1具有高度的亲和力及特异性。其具有独特的作用机制与PD-1结合的Fab段特有结合位点[2],在PD-1的结合面与其配体PD-L1大范围重叠,能够彻底阻断PD-1与PD-L1的结合。此外,替雷利珠单抗是唯一将抗体Fc段经基因工程改造、去除FcγR结合能力的PD-1单抗,可避免单抗与巨噬细胞的FcγR结合,从而消除抗体依赖细胞介导的吞噬作用,避免了T细胞数量减少而影响抗肿瘤疗效。相关研究显示[3],在中位随访时间9.8个月时,替雷利珠单抗联合化疗可以将患者mPFS提升至9.7个月,使疾病进展风险下降36%,客观缓解率(objective response rate,ORR)达57.4%,较化疗组(36.9%)显著提升。无论PD-L1的表达如何,替雷利珠单抗联合化疗均可为患者带来获益,且总体安全性和耐受性良好[3]。基于该研究[3],《CSCO免疫检查点抑制剂临床应用指南》(2021年版,以下简称《指南》)[4]推荐:替雷利珠单抗联合化疗一线治疗驱动基因阴性的晚期非鳞状NSCLC。本研究中,患者无基因突变,再行贝伐珠单抗+顺铂+培美曲塞化疗3周后耐受可,为加强治疗效果,加用替雷利珠单抗治疗合理。
2.2 如何判断替雷利珠单抗与患者肝损伤的相关性
本研究患者接受替雷利珠单抗治疗前未出现肝功能损伤,使用替雷利珠单抗3周后出现氨基转移酶异常升高(ALT>10倍正常值上限和AST升高>20倍正常值上限, DBIL及TBIl>3倍正常值上限,属于肝毒性4级),替雷利珠单抗与肝功能损伤有合理的时间关联。该患者既往无饮酒史、无肝炎、结核病史。此外患者无其他药品及保健品使用史,行4次化疗肝功能均未出现异常,在联合替雷利珠单抗治疗后出现肝功能指标异常升高,患者出现肝功能损伤与使用替雷利珠单抗存在明确的时间相关性,且使用糖皮质激素冲击治疗后患者肝功能持续好转,根据药物性肝损伤RUCAM量表[5]评分为10分(极可能),考虑为替雷利珠单抗导致的急性药物性肝损伤(4级)。
3 知识点
3.1 免疫相关性肝炎的临床表现
免疫相关不良事件(immune-related adverse events, irAEs)是由于免疫检查点抑制剂导致过度的免疫激活,对正常组织细胞产生破坏而带来相应的症状、体征、实验室检查结果异常。正常组织中免疫细胞活化,失去对自身抗原的免疫耐受,可出现类似自身免疫性疾病的症状。常见的irAEs包括甲状腺功能低下、免疫性肺炎、免疫性肝损伤、免疫性心肌损伤等[6]。
免疫相关肝毒性(immune-mediated hepatotoxicity,IMH)主要表现为ALT和(或)AST升高,伴或不伴有胆红素升高。一般无特征性的临床表现,有时伴有发热、疲乏、食欲下降、早饱等非特异性症状,胆红素升高时可出现皮肤巩膜黄染、茶色尿等。症状也可来自同时发生的其他脏器毒性,如结肠炎、甲状腺炎或肺炎等。
3.2 免疫相关肝脏毒性发生率
IMH可发生于首次用药后的任意时间,最常出现在首次用药后的8~12周。且在接受不同的免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)或者对于不同癌种的发生率都会有所差异。其中,使用细胞毒性T淋巴细胞相关蛋白4(cytotoxic T lymphocyte associate protein-4,CTLA-4)抑制剂患者出现肝毒性的时间相对更早。《指南》[4]中IMH的发生率差异很大,根据ICIs的种类、剂量以及是否使用联合治疗,其发生率约0.7%~16.0%。
3.3 IMH的发生机制
目前,ICIs诱导的免疫性肝损伤机制尚不清楚。相关研究认为[7],由于ICIs非特性导致T细胞活化,活化的T细胞不能准确识别正常细胞与肿瘤细胞,从而增加了肝细胞损伤。也有可能与免疫效应细胞过度激活、调节性T细胞减少等相关[8-9]。也有研究证实[10],肝巨噬细胞是介导免疫治疗肝毒性的关键原因。
3.4 IMH发生的危险因素
一项研究ICIs诱导肝毒性潜在危险因素分析的回顾性研究显示[11],由于生物学因素(性染色体、遗传多态性和性激素)和社会学因素(医疗保健、社会身份和食物摄入)的差异,免疫性相关反应可能会因性别而显著不同,相比女性患者,男性患者有更高的肝毒性风险。另外,年龄小于65岁、潜在的肝脏疾病(包括非酒精性和酒精性肝病)、病毒感染、同时使用对乙酰氨基酚和羟甲基戊二酸辅酶A(HMG-CoA)还原酶抑制剂等肝毒性药物会增加免疫相关性肝炎的风险。
Peeraphatdit等[7]认为伴有肝转移灶、自身免疫性疾病、既往出现过免疫性相关性疾病及使用ICIs药物剂量较大或联合使用ICIs类药物会增加IMH的风险。本研究中,患者男性、年龄<65岁并伴肝转移是其发生IMH的危险因素。
3.5 IMH的治疗措施
对于IMH的处理,CSCO、美国临床肿瘤学会(ASCO)联合美国国立综合癌症网络(NCCN)以及欧洲临床肿瘤学会(ESMO)都发布了免疫检查点抑制剂相关的毒性管理指南[12-14]。虽然各国指南在不良反应的分级管理中略有不同,但总体思路大体一致:根据IMH的严重程度不同,对是否停用ICIs及针对性的治疗措施提出了分级管理。糖皮质激素是治疗IMH的基础药物,对于1级IMH,可在密切观察下继续肿瘤免疫治疗;对于2级IMH,应暂停使用ICIs治疗,并口服泼尼松(0.5~1mg/kg),如肝功能好转,缓慢减量;对3级或4级IMH应立即静脉滴注大剂量泼尼松龙(1~2mg/kg)冲击治疗,并永久性停用ICIs,如果3天后无好转可加用麦考酚酯,如效果仍不佳,可换用低剂量他克莫司。英夫利西单抗因其自身潜在的肝脏毒性,不建议在IMH患者中使用。
4 讨论
替雷利珠单抗耐受性良好,其说明书提到[15]:在替雷利珠单抗与化疗联用的NSCLC患者中,5例(1.9%)患者发生免疫相关性肝炎,其中1级1例(0.4%),3级2例(0.8%),4级和5级各1例(0.4%)。致免疫相关性肝炎发生的中位时间为1.3个月(范围0.5~4.3个月),中位持续时间为3.4个月。替雷利珠单抗与其他ICIs所致肝损伤临床表现大体类似,多以ALT或AST及胆红素的升高作为判断依据,个别情况下会出现发热、食欲下降等非特异性症状[16]。也有研究证实[17],低蛋白血症是免疫治疗相关肝功能障碍的表现之一。本患者为左下肺腺癌并全身多处转移,使用替雷利珠单抗约3周后出现免疫相关性肝炎,与既往研究数据相符,该患者临床症状为食欲减退、乏力、出血,实验室检查表现为肝氨基转移酶、胆红素的升高及白蛋白水平下降。根据患者临床表现及相关的实验室检查结果,可判断该患者为急性药物性肝损伤(4级,重度)。根据《指南》[4],经激素治疗后肝功能逐渐好转,但考虑到该患者合并多发转移灶,且营养状况不好,重启ICIs存在再次发生严重肝损伤可能,因此永久性停用ICIs。
5 小结
本研究通过1例替雷利珠单抗导致IMH的案例分析,总结了替雷利珠单抗IMH的发生特点、可能的发生机制、危险因素及相应的处理措施,以期提高医生和临床药师对该药品不良反应的充分认识,在诊疗过程中做到密切监测、尽早识别并规范处理。

