液相氢还原沉钒制备V2O3及其动力学研究
胡艺博, 张一敏, 薛楠楠, 胡鹏程, 张刘洪
(1.武汉科技大学资源与环境工程学院, 湖北 武汉 430081;2.国家环境保护矿冶资源利用与污染控制重点实验室, 湖北 武汉 430081;3.战略钒资源利用省部共建协同创新中心, 湖北 武汉 430081;4.湖北省页岩钒资源高效清洁利用工程技术研究中心, 湖北 武汉 430081)
V2O3是一种重要的钒氧化物,主要应用于制备钒铁和氮化钒[1],其中以V2O3为原料利用电铝热还原法制备出的高钒铁占国内钒铁市场的60%~70%[2]。同时,V2O3在碳化钒、氮化钒铁等钒合金产品的制备上也具有较强的应用前景[3-4]。此外,由于V2O3还是一种优良的相变材料[5-6],其在特殊材料开关、全息存储材料、涂层材料以及各类传感器等方面也具有较为广泛的应用[7]。目前,还原焙烧是V2O3制备的主要方法[8],原料一般为V2O5[9]、NH4VO3[10]等前驱体,该工艺需要经过富钒液沉钒的过程,不仅会产生大量的氨氮废水和废气,同时还延长了V2O3制备流程[9]。为此,引入了液相氢还原技术沉钒制备V2O3,既可从源头上消除氨氮污染和降低焙烧能耗,又能从页岩富钒液直接制备V2O3,缩短了工艺流程。
在液相氢还原反应中,氢气扮演了还原剂的角色,但其本身稳定性极强,反应惰性较大,故提高氢气的反应活性就成为了氢还原制备金属的关键[11]。一般而言,工业上提高氢气的反应活性主要是添加催化剂[12]。张国斌等[12]发现加入PdCl2作催化剂后,液相氢还原可以获得沉钒率达99.25%的V2O3产品,但钯作为贵金属,在工业应用中并不经济,同时PdCl2中的钯元素以钯单质的形式与钒一并沉淀,导致难以回收,因此有必要寻找一种与其催化效果和产品指标相近的催化剂。尹春雷等[13]在120~130 ℃、搅拌转速900 r/min、氢分压为4.0 MPa、催化剂蒽醌浓度0.05~0.20 g/L的条件下,获得了包覆效果较佳的镍包金刚石,同时发现,多次包覆可改善镍在金刚石上的沉积均匀性,减少釜壁“结疤”现象的产生。舒代萱等[14]以镍粉做晶种及催化剂,对镍氨溶液的液相氢还原过程进行了研究,结果发现,该反应属于非均相反应,反应速度与加入的晶种量和氢分压平方根成正比,与镍离子浓度无关。张育潜等[15]对石墨粉用SnCl2敏化处理,再用PdCl2进行活化处理,在190 ℃、镍浓度110~130 g/L、硫酸铵浓度425~475 g/L、氢分压4.0~4.5 MPa、搅拌速度900 r/min的条件下,可以获得包覆率90%以上的镍包石墨。
综上,本研究选择价格低廉的镍粉和蒽醌作为催化剂,以期替代PdCl2用于液相氢还原沉钒并制备出合格的V2O3产品;同时,确定液相氢还原制备V2O3的最佳条件,并对所得沉钒产品进行物相表征。另外,对镍粉、PdCl2、蒽醌和自催化作用的液相氢还原试验进行了沉钒动力学分析,对镍和钯在氢还原过程中的催化作用进行模拟和吸附动力学分析。
1 试验原料及方法
1.1 试验原料
在工业上,钒页岩经过焙烧、浸出后得到的浸出液杂质含量高、钒浓度低,需进一步的净化与富集工艺以获得页岩富钒液,其中P204萃取-H2SO4反萃是应用最为普遍的净化与富集工艺。氧化预处理后的页岩富钒液的主要化学成分见表1。

表1 页岩富钒液的主要化学成分
1.2 试验方法
本研究所采用主要试验方法如下:利用NaOH溶液调节页岩富钒液pH值;调节pH值后的页岩富钒液以填充率40%的体积置于高压反应釜内,加入一定量的催化剂(或不加),关闭釜盖、锁紧密封圈后,通入氮气并利用真空泵排出釜内空气;升至预设温度后,打开进气阀通入一定分压的高纯氢气进行搅拌反应;搅拌反应一段时间后,打开冷却水阀,将高压反应釜内的温度降至50 ℃以下,排出釜内残余气体,倒出其中的沉钒浆体;沉钒浆体经过固液分离后,固体样品真空干燥即得液相氢还原产品。液相氢还原过程的主要化学反应见式(1)。
(1)
沉钒母液经测定钒浓度后按式(2)计算沉钒率(λ)。
(2)
式中:c1为页岩富钒液中的钒浓度,g/L;c2为洗水或沉钒母液中的钒浓度,g/L;V1为页岩富钒液的体积,L;V2为洗水或沉钒母液的体积,L。
2 结果与讨论
2.1 催化剂的选型
2.1.1 使用不同催化剂时反应温度、氢分压、初始钒浓度和溶液pH值对沉钒率的影响
为了确定液相氢还原制备V2O3的最佳条件,以氧化预处理后的页岩富钒液为原料,以PdCl2、Ni粉、蒽醌为催化剂,对反应温度、氢分压、初始钒浓度和溶液pH值进行单因素试验,结果如图1(a)~(d)所示。由于V2O3本身也具有一定的催化作用,因此不添加催化剂,以“自催化作用”的液相氢还原沉钒为对照试验。
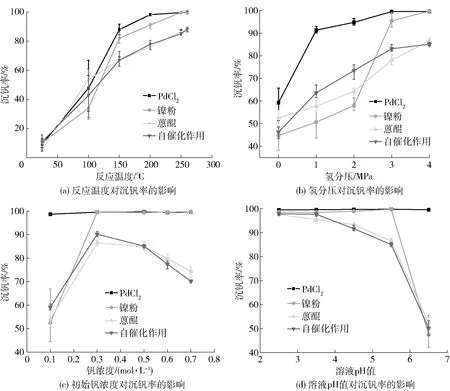
图1 不同催化剂的液相氢还原在不同条件下的沉钒率的变化
反应温度不仅影响液相氢还原的沉钒率,而且影响产物的结晶度。在氢分压4 MPa、初始钒浓度0.5 mol/L、溶液pH值5.5的条件下,考察不同反应温度对沉钒率的影响,结果如图1(a)所示。随着反应温度的升高,沉钒率先急剧增加,然后基本保持稳定。反应温度越高,氢气的反应活性越高,沉淀结晶的概率越大。蒽醌和自催化作用的沉钒率变化曲线基本一致,在250 ℃时的沉淀率分别为84.74%和85.04%。镍粉和PdCl2催化剂的液相氢还原沉钒率变化曲线也一致,在250 ℃处的沉淀率分别为99.38%和99.66%。
氢气作为还原气体,可为液相氢还原反应提供足够的还原电势。在反应温度250 ℃、初始钒浓度0.5 mol/L、溶液pH值5.5的条件,考察不同氢分压对沉钒率的影响,结果如图1(b)所示。由于还原气氛的加强,液相氢还原的沉钒率随着氢分压的升高而增加。PdCl2催化的液相氢还原沉钒率高于其他催化剂,在氢分压为3 MPa时,沉淀率可达99.66%。当氢气分压从0 MPa增加到4 MPa时,镍粉催化的液相氢还原沉钒率从44.76%增加到99.38%,这表明镍粉对氢气的催化作用略低于PdCl2。在氢分压为4 MPa条件下,自催化作用和蒽醌的液相氢还原沉钒率基本相等,分别为84.74%和85.04%。
V(V)在高浓度时更容易生成多聚钒酸盐,同时对液相反应的传质能力有影响。在反应温度250 ℃、氢分压4 MPa、溶液pH值5.5的条件下,考察不同钒浓度对沉钒率的影响,结果如图1(c)所示。初始钒浓度对PdCl2催化的液相氢还原沉钒率没有明显的影响,沉钒率均在98%以上,表明在钒浓度低于0.7 mol/L的条件下,PdCl2对氢气的催化能力满足液相氢还原沉钒的要求。镍粉试验表明,浓度从0.1 mol/L增加到0.3 mol/L时,沉淀率从52.39%增加到99.55%,继续增加钒浓度对沉钒率没有太大的影响。在工业生产中,页岩富钒液应保持在较高的钒浓度以降低工作负荷和入料体积。因此,对于镍粉和PdCl2的液相氢还原试验而言,应选择初始钒浓度为0.7 mol/L。随着钒浓度的增大,自催化作用和蒽醌的沉钒率表现出先升后降的趋势,并在0.3 mol/L时达到最大值,分别为86.56%和90.19%。
2.1.2 使用不同催化剂时沉钒产品的XRD图谱分析
根据图1可知,自催化试验和蒽醌催化试验的最佳条件即反应温度250 ℃、氢分压4 MPa、初始钒浓度0.3 mol/L、溶液pH值2.5,在此条件下,对获得的自催化作用和蒽醌催化的液相氢还原沉钒产品进行了XRD图谱分析,结果如图2(a)和(b)所示。从图2(a)可以看出,自催化作用的液相氢还原沉钒产物XRD图谱中的主要物相成分是NaV2O5,同时伴有少量的四价VO2(H2O)0.5和五价NaVO3·1.9H2O 衍射峰,这表明无任何催化剂加入的情况下,高压反应釜内的还原氛围不足。图2(b)显示,蒽醌的加入会促使液相氢还原形成稳定的VO2(H2O)0.5,这是由于蒽醌在沉淀的晶体周围形成了活性位点[13],促进了四价钒的沉淀和晶体的生长。
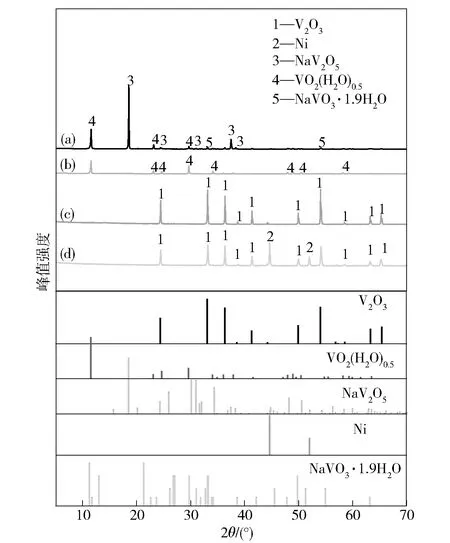
(a) 自催化作用;(b) 蒽醌;(c) PdCl2;(d) 镍粉
根据图1可知,在镍粉和PdCl2催化试验的最佳条件即反应温度250 ℃、氢分压4 MPa、初始钒浓度0.7 mol/L、溶液pH值5.5,在此条件下,对获得的镍粉和PdCl2催化的液相氢还原沉钒产品进行了XRD图谱分析,结果如图2(c)和(d)所示。镍粉和PdCl2催化的液相氢还原沉钒产物的主要成分均为V2O3,但由于镍粉用量过大,在镍粉催化液相氢还原产品的XRD图谱中出现了较强的Ni衍射峰,表明V2O3纯度较低。但同时发现并没有其他镍类化合物或其他含钒化合物的产生,这表明镍粉在液相氢还原过程中并不参与反应,不会与溶液中的钒形成复杂的钒酸镍沉淀,这表明后续钒、镍的进一步分离可采用较为简单的磁选进行分离。镍粉催化液相氢还原沉钒产品与PdCl2的XRD图谱对比显示,镍粉催化的沉钒产品衍射峰宽度更窄、峰值更低,这表明晶粒更细、晶体形态发育比PdCl2的沉钒产品要差,在工业上利用V2O3生产钒铁等钒制品时,粒度较细的V2O3反应更完全、钒的利用率更高[1]。
综上,镍粉催化的液相氢还原反应能获得与PdCl2相同的V2O3沉钒产物,最佳试验条件为m(NaClO3)∶m(V2O5)=0.4、反应温度250 ℃、氢分压4 MPa、初始钒浓度0.7 mol/L、溶液pH值5.5,在此条件下,可获得99.87%的沉钒率,但沉钒产物含有较多的Ni,为此,可采用成本较为低廉的磁选进行钒镍分离。在磁场电流强度2.0 A、磁介质丝直径1.5 mm、磁选时间15 s、固液比为15 g/L、冲洗次数3次、磁选尾矿扫选3次的条件下,可获得纯度达99.21%的V2O3产品。
2.2 动力学研究
2.2.1 沉钒动力学
针对PdCl2、镍粉、蒽醌和自催化作用的沉钒反应,研究了不同沉钒温度下溶液中残留的钒浓度和时间的变化关系,同时以钒浓度对时间进行微分求导,得到在该时间段的反应速率,进而可获得反应速率与钒浓度的线性关系,不同催化液相氢还原沉钒Arrhenius方程拟合结果与拟合参数见图3和表2。

图3 不同催化液相氢还原沉钒Arrhenius方程拟合结果

表2 不同催化剂液相氢还原沉钒动力学拟合参数

2.2.2 吸附动力学

图4 氢气的裂解模型和态密度的变化

程序升温脱附谱(TPD)可以表征气体分子与催化剂之间的相互作用,还能反映出气体从催化剂表面解吸和脱附的程度,进而间接表明液相氢还原过程中的传质扩散是催化的有效手段。为了验证图4(a)的氢气吸附、裂解和活化过程,本研究采用程序升温脱附进行表征分析,结果如图5所示。

图5 镍和钯对氢气的程序升温脱附谱及拟合结果
图5(a)和(b)显示,镍和钯的程序升温脱附谱上只出现了单个脱附峰,温度范围均在250 ℃~300 ℃,这表面只有反应温度高于250 ℃时,液相氢还原沉钒产物中才会出现V2O3的衍射峰。单个脱附峰的出现只表明氢气分子在镍和钯颗粒表面的化学吸附,即H—H键的裂解,这与模拟结果一致。镍和钯的TPD曲线的峰值均随升温速率的增加而增大,但钯的峰值更高,且脱附曲线拐点更加明显,在215~260 ℃的温度范围内“急升急降”,而镍对氢气的脱附曲线在200~400 ℃的温度范围内“缓升缓降”。镍和钯对氢气的吸附量分别为0.257 90~0.283 08 mmol/g、2.175 40~2.250 61 mmol/g,后者对氢气的吸附量约为前者吸附量的9倍,这表明了如要达到相同的液相氢还原催化效果,镍粉的用量需远大于钯的用量。根据程序升温测试升温速率和峰值温度的不同以及图5(c)~(d)脱附动力学Arrhenius方程拟合直线的斜率,可以计算出和钯的脱附活化能分别为EPd··H=21.744 7 kJ/mol和ENi··H=9.699 4 kJ/mol。很明显,氢在镍颗粒表面的脱附活化能更低、脱附更容易,这证明了图4模拟吸附的结果。
3 结论
1) 自催化作用和蒽醌的液相氢还原产品分别为NaV2O5和VO2(H2O)0.5,但无法制备出V2O3。镍粉催化的液相氢还原反应能获得与PdCl2相同的V2O3沉钒产物,在m(NaClO3)∶m(V2O5)=0.4、反应温度250 ℃、氢分压4 MPa、初始钒浓度0.7 mol/L、溶液pH值5.5的最佳条件下,可以获得99.87%的沉钒率。利用镍粉获得的沉钒产品经磁选钒镍分离后,可获得纯度达99.21%的V2O3产品,该结果表明可采用镍粉替代PdCl2进行液相氢还原沉钒制备V2O3。
2)自催化作用、蒽醌、镍粉与PdCl2催化液相氢还原反应活化能分别为195.573 6 kJ/mol、188.83 kJ/mol、140.09 kJ/mol和38.07 kJ/mol,反应控制步骤分别为化学反应控制、化学反应控制、化学反应控制和混合控制。
3)吸附动力学研究表明,H2分子在Ni或Pd表面发生裂解,同时H原子的s轨道与Pd、Ni的p轨道和d轨道发生了杂化,形成还原性较强的Pd—H或Ni—H键,Pd和Ni对氢气的化学吸附能分别为1.34 eV和2.04 eV;Ni—H键的能带更宽、离域性更强、更容易被脱附。镍和钯的氢气吸附量分别为0.257 90~0.283 08 mmol/g和2.175 40~2.250 61 mmol/g,脱附活化能分别为EPd··H=21.744 7 kJ/mol和ENi··H=9.699 4 kJ/mol。

