加热方式对紫色马铃薯营养成分及抗氧化活性的影响
赖灯妮,朱向荣,李 涛,张 群,彭清辉
(1.湖南省农产品加工研究所,湖南 长沙 410125;2.农业农村部农产品质量安全风险评估实验室(长沙),湖南 长沙 410002;3.湖南省生产力促进中心,湖南 长沙 410013)
马铃薯是全球重要的粮食作物,其中,紫色马铃薯除具备普通马铃薯的所有营养价值外,还富含重要的功能活性成分——多酚及花色苷[1]。多酚、花色苷等活性成分具有抗氧化、抗肿瘤、抗病毒、预防心血管疾病和调节血糖等功能[2-7]。马铃薯通常采用煮、蒸、微波、烘焙等热处理方式烹饪、加工。热加工会影响紫色马铃薯的营养素及活性成分[8]。研究认为,热加工过程中,马铃薯组织结构发生变化,原本结合在组织上的生物活性物质得到释放[9];同时,还会发生化学反应(如美拉德反应等)产生新的物质。热加工引起的活性物质变化必然对紫色马铃薯的活性功能如抗氧化造成影响[10-11];但目前,热加工方式对紫色马铃薯活性功能影响方面的相关研究报道还较少。
根据自由基理论,抗氧化活性是大多数食物健康成分发挥生物活性的基础,所以,有关评价健康食品抗氧化活性的研究非常多。目前,评估食物活性成分抗氧化能力的方法有化学法和生物法两大类;其中化学法包括1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2’-联氮双(3-乙基苯并噻唑啉-6-磺酸)(2,2’-azinobis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)、Fe3+还原法等;生物法主要是检测相关的抗氧化蛋白及其通路。核转录因子红系2相关因子2(nuclear factor-erythroid 2-related factor 2,Nrf2)是调控细胞抵抗氧化损伤、维持细胞内氧化还原平衡的关键转录因子。Nrf2的缺失或激活障碍均可增强氧化应激对细胞的毒性,引起细胞功能障碍、凋亡甚至死亡;从而与许多疾病密切相关[12-13]。
本实验研究微波、热风、水煮3 种热加工方式对紫色马铃薯的营养成分、总酚、花色苷等含量的影响,采用DPPH、ABTS、Fe3+还原法等分析了热处理对紫色马铃薯花色苷提取物抗氧化活性的影响;并以未处理组为对照,研究微波处理组的花色苷提取物对大鼠胰岛β细胞中Nrf2和血红素氧合酶1(heme oxygenase 1,HO-1)蛋白表达水平的影响,以期为紫色马铃薯的热加工提供一定参考依据。
1 材料与方法
1.1 材料与试剂
大鼠胰岛β细胞株(RIN-m5F)购于ATCC细胞库CRL-11605(CB34806782);紫色马铃薯(黑金刚、黑美人)希森薯业有限公司;乙醇、柠檬酸、乙酸乙酯、甲醇、DPPH、过硫酸钾、醋酸钠、氯化铁、丙烯酰胺(均为分析纯)国药集团化学试剂有限公司;核质分离试剂盒 赛默飞世尔科技公司。
1.2 仪器与设备
WP-UP-WF-20超纯水制备机 四川沃特尔水处理设备有限公司;万分之一电子天平 梅特勒精密仪器上海有限公司;DNM-9602酶标仪 北京普朗新技术有限公司;K9840凯氏定氮仪、SH220M消化炉 济南海能仪器股份有限公司;Image Quant LAS 4000 mini凝胶成像仪 美国Cytiva公司。
1.3 方法
1.3.1 紫色马铃薯的热处理方法
将新鲜的马铃薯去皮,清洗干净,切成6 mm×6 mm的扇形小块(厚度4 mm)。采用不同的加热方式处理紫色马铃薯,具体操作如下:①新鲜:切好的紫色马铃薯;②微波:将切好的紫色马铃薯放入宽口培养皿中,用封口膜封口,加工条件为25 W/g、3.5 min;③热风:将切好的紫色马铃薯放入热风干燥箱,60 ℃、2 h;④水煮:将切好的紫色马铃薯放入烧杯中,加水没过材料,封口膜封口,加工条件:100 ℃、15 min。
所有待测样品都制备成冷冻干燥样品,用粉碎机磨成粉末,过80 目筛,分别标记后放置于-80 ℃冷冻保存。
1.3.2 花色苷提取分离纯化
参照方芳等[14]的方法并稍作调整。称取适量的紫色马铃薯粉末,用75%的乙醇溶液(含2%柠檬酸)为提取溶剂,采用料液比1∶20(g/mL)、提取时间10 min、提取温度45 ℃、超声波功率300 W。采用真空抽取,将滤液置于55 ℃条件下旋转蒸发,得到花色苷的粗提浓缩液。向浓缩液中加入乙酸乙酯,进行萃取数次,弃黄色液,下层液再进一步进行浓缩直至黏稠。最后采用D101大孔树脂对所得浓缩液进行纯化,洗去杂质,用乙醇溶液洗脱花色苷。所得花色苷再进一步浓缩,冷冻干燥,放置于-80 ℃冷冻保存备用。
1.3.3 紫色马铃薯中主要营养成分的测定
干物质、水分:根据GB 5009.3—2016《食品中水分的测定》直接干燥法进行测定;灰分:根据GB 5009.4—2016《食品中灰分的测定》进行测定;蛋白质:根据GB 5009.5—2016《食品中蛋白质的测定》凯氏定氮法进行测定;脂肪:根据GB 5009.6—2016《食品中脂肪的测定》索氏抽提法进行测定;淀粉:根据GB 5009.9—2016《食品中淀粉的测定》酶水解法进行测定;VC:根据GB 5009.86—2016《食品中抗坏血酸的测定》高效液相色谱法进行测定;碳水化合物:根据GB/Z 21922—2008《食品中营养成分基本术语》中的减法进行测定。
1.3.4 紫色马铃薯中抗氧化成分含量的测定
总酚:采用福林-酚法,参照Deuβer等[15]的方法略作修改。准确称取绿原酸,溶于蒸馏水中,5、10、15、20、25 mg/L配取绿原酸的标准溶液。取花色苷粗提液1.0 mL,加入至2.0 mL蒸馏水摇匀,再加0.5 mL 1 mol/L福林-酚溶液,均质机均质5min,后加入1.0 m L 15% Na2CO3溶液,均质5 min并用蒸馏水定容至10 mL,避光反应45 min,测定765 nm波长处吸光度,蒸馏水作对照。
花色苷:采用pH值差示法,取0.5 mL花色苷提取液加入到试管中,加入2.5 mL 0.025 mol/L氯化钾(pH 1.0)溶液和0.4 mol/L醋酸钠(pH 4.5)溶液,反应15 min,在520/700 nm波长处测定。花色苷含量计算公式如下:
式中:C为花色苷含量/(g/k g);A为吸光度((A520nm-A700nm)pH1.0-(A520nm-A700nm)pH4.5);mw为矢车菊-3-葡萄糖苷的相对分子质量(449.1085);DF为稀释因子;V为最终体积/mL;ε为摩尔吸光系数(26900 L/(mol·cm));W为样品质量/g。
1.3.5 化学法分析紫色马铃薯花色苷提取物的抗氧化活性
DPPH自由基清除率测定:参照王全逸[16]的方法并稍作调整,将40 μg/mL DPPH自由基溶液、0.05 mmol/L VC依次移取1.0、2.0、3.0、4.0、5.0 mL于容量瓶中,用蒸馏水定容至5.0 mL,再加入5.0 mL DPPH自由基溶液,充分混匀。对照组:5.0 mL蒸馏水加5.0 mL DPPH自由基溶液;空白组:5.0 mL蒸馏水加5.0 mL甲醇。样品组:取5.0 mL 26 μg/mL花色苷-甲醇溶液,再加入5.0 mL DPPH自由基溶液。室温下避光反应30 min,取5.0 mL样品于517 nm波长处测定吸光度。
ABTS阳离子自由基抑制率测定:参照Liang Linghong等[17]的方法并稍作调整配制ABTS阳离子自由基溶液稍作修改。将7 mmol/L ABTS阳离子溶液与2.45 mmol/L过硫酸钾溶液10 mL,室温下避光反应12~16 h配制成ABTS阳离子自由基母液,依次取0.5、1.0、1.5、2.0、2.5 mL浓度为0.1 mmol/L的VC溶液于容量瓶,且用蒸馏水补足至2.5 mL;26 μg/mL花色苷-甲醇溶液后取2.5 mL,然后分别加入5.0 mL ABTS阳离子自由基溶液避光反应10 min后,样品稀释5 倍后取1.0 mL于734 nm波长处测定吸光度。对照组为2.5 mL蒸馏水加5.0 mL ABTS阳离子自由基溶液,空白组为蒸馏水。
Fe3+还原能力测定:参照Fawole等[18]的方法并稍作调整。FRAP工作液由25 mL 300 mmol/L醋酸钠缓冲液(pH 3.6)、2.5 mL 10.0 mmol/L TPTZ溶液与2.5 mL 20.0 mmol/L FeCl3·6H2O溶液组成。依次取0.1 mmol/L的VC 0.2、0.4、0.6、0.8、1.0、1.2 mL于容量瓶,定容至2.0 mL,26 μg/mL花色苷-甲醇溶液后取2.0 mL,分别加入5.0 mL反应试剂,混匀后5 min即可于593 nm波长处测定吸光度。以2.0 mL蒸馏水加5.0 mL反应试剂作对照组,以蒸馏水作空白组,样品取2.0 mL测定。
1.3.6 生物学方法分析紫色马铃薯花色苷提取物抗氧化活性
RIN-m5F细胞株用含10%胎牛血清的RPMI 1640培养基在37 ℃、100%饱和湿度、5% CO2条件下常规传代培养。将1×106cell/mL密度的细胞接种于培养板中,待细胞贴壁单层生长后,加入花色苷提取物于培养液中诱导8 h;氧化应激状态条件为花色苷提取物预处理2 h,随后加入1 μL H2O2诱导30 min。待细胞处理结束后,弃培养液,用预冷的磷酸盐缓冲溶液(phosphate buffer saline,PBS)洗两遍。每孔加入300 μL RIPA裂解液。充分混匀后移至新离心管中,冰上孵育20~30 min。14000×g离心10 min,将上清液移至新离心管中,置100 ℃金属浴10 min,随后加入6×Loading Buffer,充分振荡混匀,再次100 ℃金属浴10 min,获得细胞裂解液,置-80 ℃冰箱保存备用。
核质分离实验:根据Thermo Scientific核质分离试剂盒说明书操作;细胞裂解液加入200 μL CERI,充分混匀,冰浴10 min;再加入200 μL CERII,振荡5 s使之充分混匀,冰浴1 min;4 ℃、18000×g离心5 min,将上清移至新离心管中。上清液即为胞质蛋白,沉淀用于提取胞核蛋白。根据Thermo Scientific核质分离试剂盒说明书操作,上述沉淀中加入400 μL NER,振荡5 s,冰育10 min,继续振荡15 s,以上条件重复4 次;4 ℃、18000×g离心10 min;将上清液移取至新离心管中即为胞核蛋白。
蛋白印迹检测:根据不同蛋白分子质量的大小选择不同浓度的分离胶,其中LC3的检测选择15%的分离胶,而其他核因子Nrf2、HO-1、核因子κB(nuclear factor kappa-light-chain-enhancer of activated B cells,NF-κB)、内参蛋白GAPDH、泛素化蛋白质聚集体SQSTM1/p62、半胱天冬酶-3(Caspase 3)、腺苷酸激活蛋白激酶、磷酸腺苷酸激活蛋白激酶选择10%~12%的分离胶。将配制好的胶装入电泳槽中,根据不同蛋白分子质量选择合适的电压大小和电泳的时间。一般加入5~20 µL待测蛋白至各泳道。电压稳定在50~80 V,电泳1~2.5 h,转膜,封闭后,用1∶1000的比例稀释一抗于4 ℃冰箱孵育过夜,去除一抗,用抗体洗脱液将膜清洗3 次,每次5~10 min。用1∶5000的比例稀释二抗,摇床下孵育1 h,吸去二抗,PBS将膜清洗3 次,每次10 min。加入化学发光显色液后,通过Image Quant LAS 4000 mini凝胶成像仪显影,拍照、保存。
1.4 数据处理与分析
用Image J分析软件对蛋白印迹条带进行定量分析。实验数据采用SPSS 20.0软件对其进行单因素方差分析,再用Duncan法进行多重比较,P<0.05,差异显著,有统计学意义;P<0.01,差异极显著。每次实验结果重复3 次,所得数据用±s表示。
2 结果与分析
2.1 热加工方式对紫色马铃薯主要营养成分的影响
如表1所示,与新鲜(新鲜代表未处理,下同)样品相比,微波、热风、水煮3 种热加工方法处理后的紫色马铃薯中VC、灰分以及淀粉含量下降,其中VC呈显著下降,热风最为明显,黑金刚从120.41 mg/100 g下降到55.05 mg/100 g,黑美人从103.17 mg/100 g下降到30.44 mg/100 g;其次是水煮,黑金刚从120.41 mg/100 g下降到67.80 mg/100 g,黑美人从103.17 mg/100 g下降到62.15 mg/100 g,而微波对其影响最小。热处理后的紫色马铃薯灰分与对照组比较有下降,但差异不显著。微波处理后黑金刚和黑美人的蛋白质含量显著上升,分别增加了3.29%和3.21%;而热风和水煮后的黑金刚蛋白质含量呈显著下降,分别下降了2.20%和1.97%;相较之下,黑美人的蛋白质含量下降趋势较慢,分别下降了1.91%和1.41%。紫色马铃薯中脂肪含量很低,经热加工后,变化不明显。
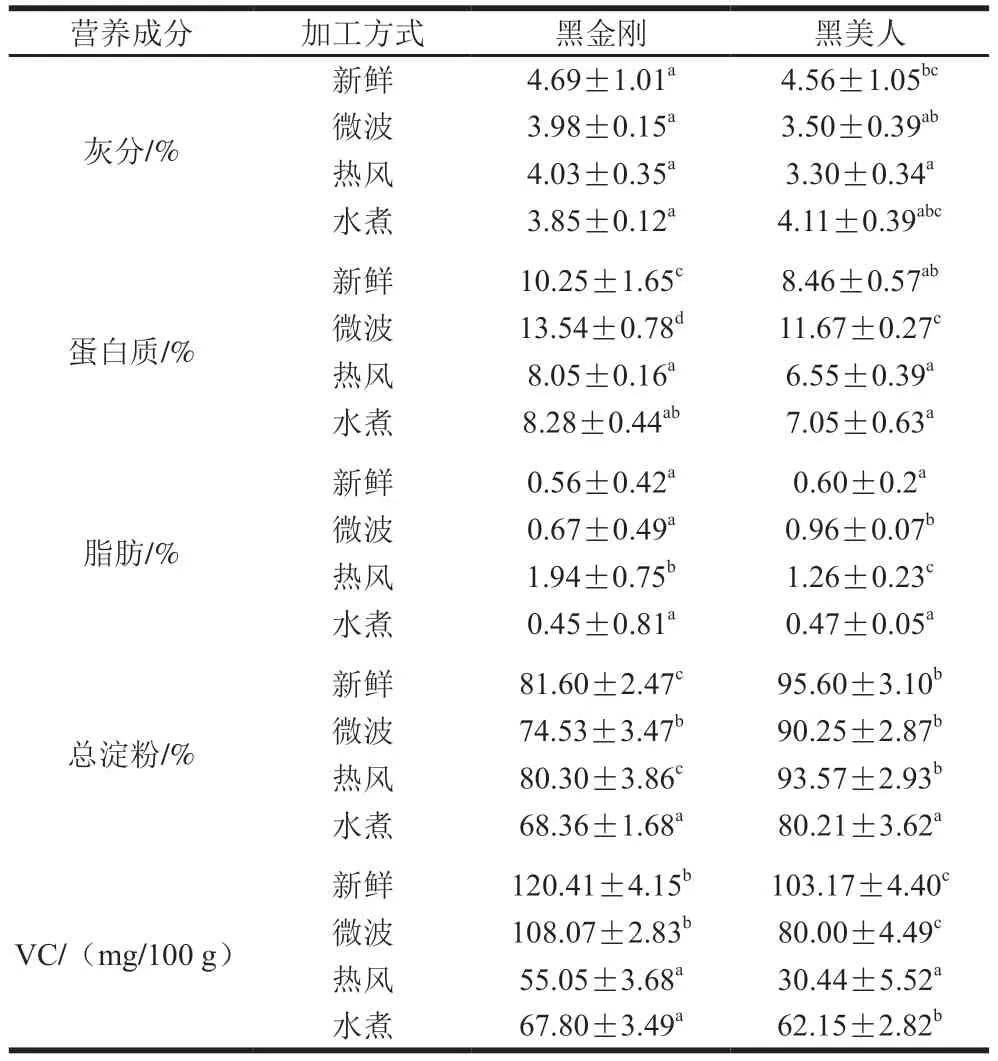
表1 热加工方式对紫色马铃薯营养成分的影响Table 1 Effects of heat treatment methods on nutrient contents of purple-fleshed potato
2.2 热加工方式对紫色马铃薯中总酚的影响
马铃薯中主要酚类物质是绿原酸,其次是咖啡酸、香草酸、没食子酸、香豆酸及黄酮等[16]。如图1所示,新鲜(未热处理)黑美人和黑金刚中总酚(以绿原酸计)含量分别为1025.50 mg/100 g和2209.14 mg/100 g,经热处理后,两种紫色马铃薯中总酚含量下降,其中微波对总酚的影响最小,水煮后的总酚含量下降最为显著。与新鲜比较,微波处理后黑金刚总酚含量仅下降9.36%,而黑美人仅下降4.40%;水煮后黑金刚总酚含量下降25.73%,而黑美人下降31.42%。
2.3 热加工方式对紫色马铃薯中花色苷含量的影响
由图2可见,黑金刚的花色苷含量整体高于黑美人,黑美人的花色苷在烹饪过程中变化不显著,黑金刚经水煮和微波处理后其花色苷含量增加,分别为98.52、93.51 mg/100 g,其中与新鲜的紫色马铃薯花色苷组相比分别上升了22.92%、16.67%。由于黑金刚在多酚以及花色苷的含量都显著高于黑美人品种,所以选定黑金刚作为后续的研究对象。
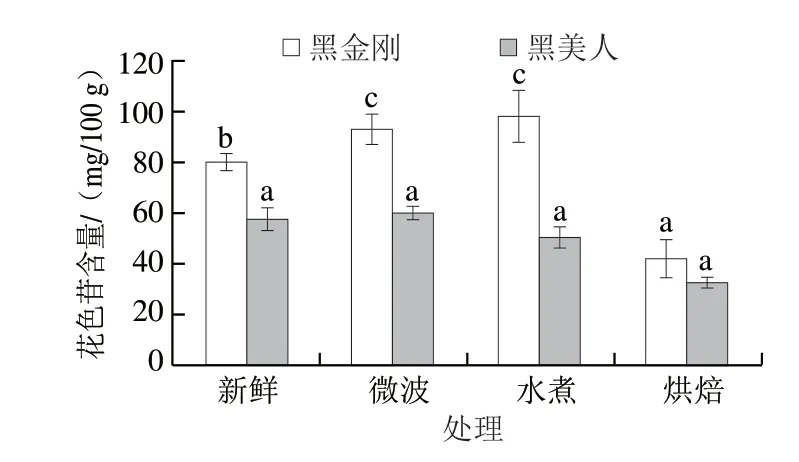
图2 烹饪方式对紫色马铃薯花色苷的影响Fig.2 Effects of cooking methods on anthocyanin content of purplefleshed potato
2.4 热加工方式对紫色马铃薯花色苷提取物抗氧化作用的影响
2.4.1 化学法分析热加工方式对紫色马铃薯花色苷提取物抗氧化活性的影响
由表2可见,热风、水煮明显降低了花色苷提取物对DPPH自由基、ABTS阳离子自由基的清除能力;但微波处理对花色苷提取物DPPH自由基、ABTS阳离子自由基清除能力的影响较小,且明显提高了Fe3+还原能力。因此,选择新鲜紫色马铃薯和微波处理方式作为后续细胞学实验的研究对象。

表2 烹饪方式对紫色马铃薯花色苷抗氧化能力的影响Table 2 Effects of cooking methods on antioxidant capacity of anthocyanins in purple-fleshed potato
2.4.2 紫色马铃薯花色苷提取物对抗氧化蛋白表达的影响
新鲜和微波处理紫色马铃薯的花色苷提取物(0.1、1 mg/mL)诱导大鼠胰岛β细胞(RIN-m5F)的结果(图3)表明,花色苷提取物增强了抗氧化蛋白Nrf2及HO-1的表达,且呈剂量依赖性上升;微波加工马铃薯的花色苷提取物组的抗氧化蛋白Nrf2及HO-1表达水平高于新鲜样品组,说明微波处理紫色马铃薯的花色苷提取物在RIN-m5F细胞抗氧化能力较强。

图3 紫色马铃薯花色苷提取物对抗氧化蛋白表达量的影响Fig.3 Effects of anthocyanins from purple-fleshed potato on the expression levels of antioxidant proteins
2.4.3 紫色马铃薯的花色苷提取物在氧化应激状态下对Nrf2和NF-κB的影响
如图4所示,通过H2O2诱导细胞处于氧化应激状态下,发现RIN-m5F细胞中NF-κB蛋白表达水平增加,而加入1 mg/mL的MA降低了RIN-m5F细胞中NF-κB蛋白表达水平。

图4 紫色马铃薯的花色苷提取物在氧化应激状态下对Nrf2和NF-κB蛋白的影响Fig.4 Effects of anthocyanins from purple-fleshed potato on the expression levels of Nrf2 and NF-κB proteins in cells under oxidative stress
2.4.4 紫色马铃薯的花色苷提取物对Nrf2核转录的影响
紫色马铃薯的花色苷提取物对大鼠胰岛β细胞核中Nrf2转录的影响见图5。通过核质分离技术,使得RIN-m5F细胞质和细胞核的蛋白分离。在氧化应激状态下,MA能显著增强细胞核内Nrf2抗氧化蛋白表达,而对细胞质中的Nrf2蛋白表达基本无差异。说明在氧化应激反应中,MA使得Nrf2的Neh2片段不能与Keap1偶联,因此Nrf2不能泛素化降解,从而导致细胞质中Nrf2大量积累并转移到细胞核中,启动II相脱毒酶和抗氧化蛋白相关基因的表达,提高细胞抗氧化应激能力。

图5 紫色马铃薯的花色苷提取物对Nrf2核转录的影响Fig.5 Effects of anthocyanins from purple-fleshed potato on Nrf2 nuclear translocation
3 讨论
3.1 热加工方式对紫色马铃薯主要营养成分的影响
相对微波和热风处理,水煮处理对紫色马铃薯中VC的影响最大,可能是由于VC为水溶性维生素,并具有热敏感性;因此,热处理和水处理极易造成VC的流失,这与Murniece[19]和Han[20]等研究结果一致。紫色马铃薯总淀粉含量较高,经热处理后,总淀粉有不同程度的损失,其中以水煮损失较多,这可能是水煮使得马铃薯细胞组织受到影响,从而导致其淀粉流失。微波处理后紫色马铃薯的蛋白质含量显著上升,与其他文献报道的结果类似,Murniece等[19]也发现烹饪处理后马铃薯中的蛋白质都有所增加,Finglas等[21]研究发现经发酵和烘烤后马铃薯蛋白质分别增加至2.2%和2.8%。该现象的原因可能是在热加工条件下,水分蒸发后干物质含量都有所增加,从而导致了蛋白质含量的增加。
3.2 热加工方式对紫色马铃薯总酚含量的影响
采用3 种热加工方式均使紫色马铃薯总酚含量明显降低,与Lemos等[22]研究结果相似,因为水溶性酚类物质容易随水流失且遇热分解。此外,热处理过程中,酚类化合物发生了美拉德等反应也导致其含量减少。因此,较低温度、较短时间的热加工方式是保留酚类化合物较好的方法。
3.3 热加工方式对紫色马铃薯花色苷含量的影响
花色苷含量在微波和水煮处理中上升,在热风处理中下降。本研究结果与Lemos等[22]的研究报道基本一致。花色苷极易发生酶促降解,而热处理抑制了酶活性,使得马铃薯中的花色苷得到保留。其次,有些热处理方式改变了马铃薯的微观结构,使花色苷更易于提取。黑金刚热风处理组中花色苷下降了46.87%,其原因可能是花色苷长时间暴露在高温空气中被分解。
3.4 热加工方式对花色苷提取物抗氧化作用的影响
3.4.1 热加工方式对花色苷提取物化学抗氧化作用及其抗氧化蛋白表达的影响
Bontempo等[23]研究认为,紫色马铃薯花色苷提取物的抗氧化活性主要以Fe3+还原能力为主,本实验发现微波处理黑金刚紫色马铃薯的花色苷提取物与新鲜紫色马铃薯的花色苷提取物比较,提高了Fe3+的还原能力,其可能主要存在两个方面的原因:微波的热处理使得紫色马铃薯花色苷种类发生变化,不同花色苷抗氧化能力与它所含羟基的数目和位置相关,因此不同的花色苷抗氧化能力不一样[24];其次,由于花色苷的热不稳定性,可能使得紫色马铃薯花色苷的糖苷配基丢失,形成花青素单体,而花青素单体的抗氧化活性一般强于花色苷。
3.4.2 花色苷提取物在氧化应激状态下对Nrf2和NF-κB的影响
目前研究发现紫色马铃薯中花色苷提取物诱导HepG2细胞,通过激活Nrf2途径从而上调HO-1、谷胱甘肽硫转移酶和NAD(P)H表达,这与本实验研究结果相似[25]。
在正常生理状态下,细胞质中Nrf2的Neh2片段上的ETGE和DLG位点与Keap1结合。Keap1和Cul-Rbx-E3泛素连接酶偶联Neh2赖氨酸残基从而使Nrf2被泛素化标记,最后被引导进入蛋白酶体进行降解。因此,正常情况下,细胞质中Nrf2蛋白含量较低[26]。在氧化应激和亲电反应中,Keap1中半胱氨酸残基的结构改变,从而不能与Neh2偶联,因此不能泛素化降解掉Nrf2。这样会导致细胞质中Nrf2大量积累并转移到细胞核中,然后在分子伴侣Maf的协助下与ARE结合形成二聚体,启动II相脱毒酶和抗氧化蛋白相关基因的表达和蛋白的合成,从而提高细胞抗氧化应激能力[27]。同时在氧化应激状态下,MAPK、NF-κB、AP-1等信号通路被激活,使得下游炎症COX-2、iNOS等蛋白以及部分炎症细胞因子和趋化因子的表达增加[28]。
已有研究报道矢车菊素、飞燕草色素、锦葵色素不仅可以激活Nrf2作用于ARE,诱导II相抗氧化蛋白谷胱甘肽还原酶、醌氧化还原酶等的表达,从而Caspase-3的活性,而且能抑制LPS,IFN-γ诱导的NF-κB的活化[29]。在氧化应激状态下,1 mg/mL微波处理紫色马铃薯的花色苷提取物与对照组相比增强了RIN-m5F细胞中Nrf2蛋白表达水平。这说明在氧化应激状态下紫色马铃薯花色苷提取物通过提高大鼠胰岛β细胞抗氧化能力,从而降低炎症蛋白的表达水平。
4 结论
热处理后紫色马铃薯中VC、灰分以及淀粉含量下降;从VC来看,所有的处理方式均使含量显著下降,热风处理中黑金刚减少了65.36 mg/100 g,黑美人减少了72.73 mg/100 g,变化最为明显,微波对其影响最小;微波处理后蛋白质含量显著上升,黑金刚和黑美人的蛋白质含量分别增加了3.29%和3.21%,而热风(60 ℃、2 h)和水煮(100 ℃、15 min)使黑金刚马铃薯的蛋白质含量显著下降。
热处理后紫色马铃薯的总酚(以绿原酸计)含量显著下降,其中微波处理对紫色马铃薯的总酚含量影响最小,黑金刚和黑美人下降率分别为9.36%和4.40%,水煮方式中总酚含量下降最为显著,分别达到了25.73%和31.42%。
研究结果表明,微波处理能明显提高紫色马铃薯花色苷提取物的还原能力,经微波处理的紫色马铃薯的花色苷提取物可明显提高大鼠胰岛β细胞中对抗氧化蛋白Nrf2和HO-1的表达水平,并降低NF-B炎症蛋白的表达水平。
综上所述,微波(25 W/g、3.5 min)是紫色马铃薯最佳的热处理方法。

