125I腔内照射联合仑伐替尼治疗进展期肝外胆管癌的效果和安全性分析
朱兴书, 陈鹏飞, 张萌帆, 李方正, 陈金威, 张文广, 段旭华, 任建庄, 韩新巍
郑州大学第一附属医院介入科, 郑州 450052
胆管细胞癌为胆道系统中的恶性肿瘤,根据解剖位置的不同分为两种亚型:肝内胆管癌、肝外胆管癌。肝外胆管癌指的是源于肝外胆管包括肝门区至胆总管下端胆管的恶性肿瘤。肝门部胆管癌和远端胆管癌两者合称为肝外胆管癌[1]。手术切除是其首选的治疗方式,但多数患者由于缺乏特定症状,确诊时已经失去根除手术机会[2]。无法行根治性手术切除的患者,顺铂联合吉西他滨作为一线化疗方案,中位生存期(median overall survival,mOS)为11.7个月[3]。但存在部分患者不能耐受副反应或不愿接受化疗,所以继续探索进展期肝外胆管癌的姑息性治疗方法受到极大关注。
近年来,125I腔内照射联合胆道支架植入用于治疗进展期肝外胆管癌[4-6],可快速改善黄疸症状,并延长支架通畅时间及患者生存期。此外有研究使用酪氨酸激酶抑制剂仑伐替尼单药用于治疗胆管癌,并且观察到良好的抗肿瘤效果[7-8],但目前尚未有研究证实125I腔内照射联合仑伐替尼能进一步改善患者的预后。因此本研究对125I腔内照射联合仑伐替尼治疗进展期肝外胆管癌的有效性和安全性进行探索。
1 资料与方法
1.1 研究对象 选取2018年1月—2021年11月就诊于本院介入科并经病理学和影像学检查确诊为肝外胆管癌患者25例,根据不同的治疗方案分为:125I腔内照射联合仑伐替尼组患者13例(联合组)和单纯125I腔内照射组12例(对照组)。纳入标准:(1)行胆道内钳夹活检病理证实为肝外胆管癌;(2)肝功能分级为Child-Pugh A、B级;(3)没有外科手术机会或者身体不能耐受外科手术;(4)无严重凝血功能障碍;(5)不愿或者身体不能耐受一线化疗。排除标准:(1)碘剂过敏;(2)重要脏器严重功能不全,不能耐受治疗;(3)依从性差,未能配合持续治疗。
1.2 设备和材料 血管造影机(SEMENS公司,Artis Q zeego),经皮肝穿刺胆道引流(PTCD)套装、KMP导管(美国COOK公司)。胆道自膨胀支架(selfexpandable metallic biliary stent,SEMS):镍钛合金支架(太雄医疗有限公司),长度6~10 cm,直径8~10 mm;125I粒子(天津赛德生物有限公司),籽源长度(4.5±0.2) mm,直径(0.80±0.03) mm,半衰期59.4 d,平均活度0.79 mCi。
1.3 治疗方法
1.3.1 对照组 (1)患者仰卧于血管造影机检查台上,肝区消毒、铺巾,利多卡因局麻注射后采用22G千叶针成功穿刺肝内胆管,造影证实后引入PTCD穿刺套装,交换引入0.89 mm(0.035 inch)导丝及5F KMP导管,二者配合下打通胆道梗阻段并行胆管造影,造影反复证实梗阻段位置。(2)交换入加硬导丝,经加硬导丝引入8F鞘管,鞘管头端抵紧梗阻段起始部,经鞘管引入胆道活检钳并推出鞘管后,张开活检钳在病变内前推5~10 mm,然后收紧活检钳夹取病变组织,放入10%甲醛溶液标本瓶中固定,反复3~5次,夹取2~3块白色病变组织,行病理学检查[9]。后拔除鞘管,经导丝引入8.5F或10.2F引流管,远端成袢于胆道或者肠道内,外固定。(3)待病理结果证实并取得家属及患者同意后,行胆道支架植入及将125I粒子链置入胆道内。(4)粒子链的制作:根据CT /MRCP显示肿瘤范围计算出所需125I粒子量,体外将PTCD引流套件中4F软管剪至需要的长度,远端加热封闭,所需的粒子自近端逐一装填入软管内,近端管腔以明胶海绵条堵塞,用以固定粒子位置。(5)透视下将8.5F或10.2F引流管送入胆道内,后125I粒子链经胆道引流管引入并覆盖病变区域。(6)术后3天内行单光子发射计算机断层成像检查明确放射剂量分布。2个月后拔出粒子链,根据影像学检查及检验学检查决定是否再次植入粒子链(图1)。
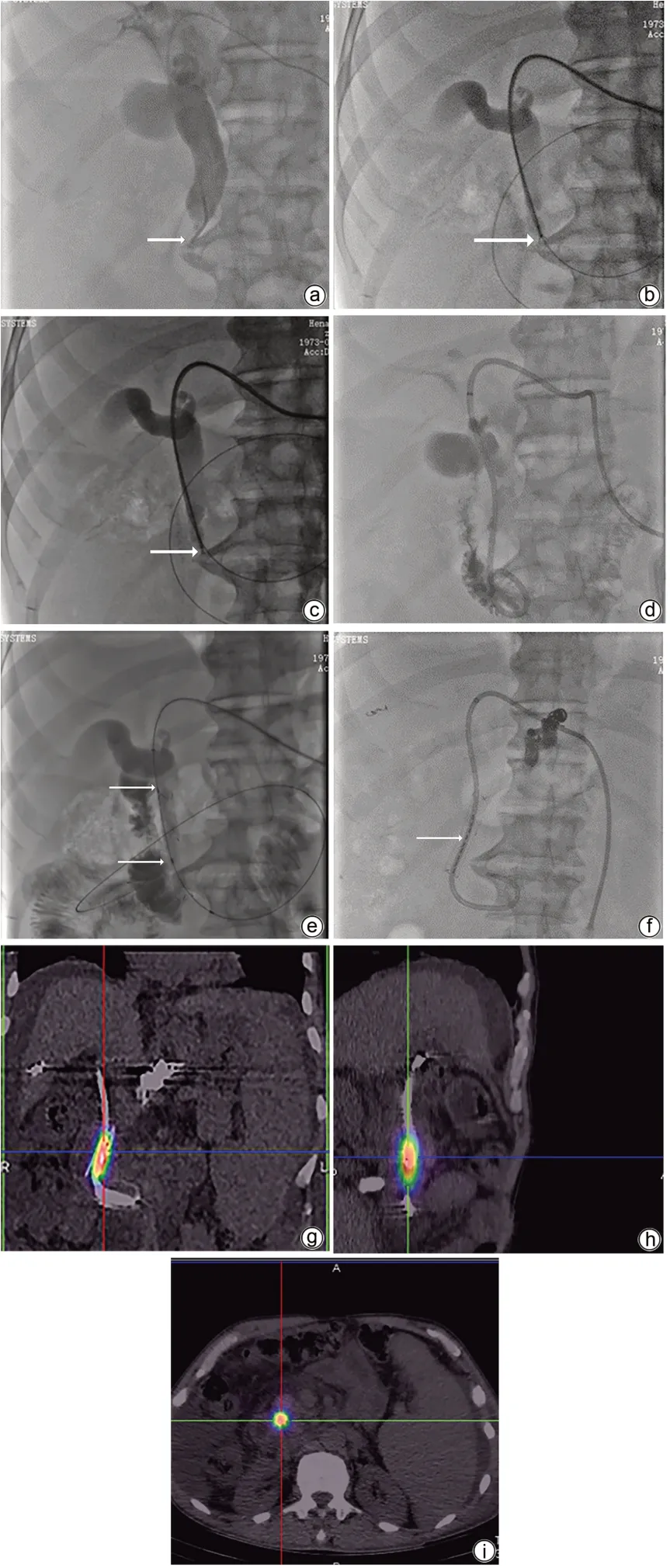
图1 49岁男性胆管恶性肿瘤伴梗阻性黄疸患者活检和介入治疗过程Figure 1 Biopsy and interventional procedure in a 49-year-old male patient with biliary malignancy with obstructive jaundice
1.3.2 联合组 在对照组的治疗方法上,患者术后给予仑伐替尼口服,剂量为12 mg/d(体质量≥60 kg者)或8 mg/d(体质量<60 kg者),1、2级不良事件可以继续使用药物治疗,如果发生3级药物相关不良事件可降低药物剂量至8 mg/d或暂时中断治疗至症状降至1、2级不良事件,发生4级不良事件则立即停止药物治疗,因肿瘤进展或者不可耐受任何级别药物不良事件,患者均可自行选择停止药物治疗。
1.4 随访及疗效评估 采用电话随访、门诊、微信和住院检查相结合的方式进行随访。观察指标主要有以下几点:(1)两组患者的技术成功率,技术成功定义为成功置入胆道支架和125I粒子链,且置入后对比剂流畅通过支架;(2)两组患者术前和术后1个月TBil、DBil、ALT和AST等肝功能指标;(3)两组患者的支架通畅情况和生存情况,支架通畅期定义为治疗开始至再发黄疸并经CT/MRI检查证明支架堵塞的时间间隔,或无黄疸复发患者的死亡时间或最后随访时间,生存期定义为从接受该研究的方案治疗到最后随访的时间或患者死亡时间;(4)参考《不良事件通用术语标准》(CTCAE)5.0版记录联合组患者药物相关不良事件。
1.5 统计学方法 统计分析用SPSS26.0及GraphPad Prism8.0软件进行,正态分布的计量资料用表示,两组间比较采用成组t检验;偏态分布的计量资料用M(P25~P75)表示,两组比较采用Wilcoxon秩和检验;计数资料组间比较采用Fisher确切概率法。采用Kaplan-Meier和Log-rank检验评估生存期和支架通畅情况。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者基线特征 联合组和对照组患者基线资料具有可比性,差异无统计学意义(P值均>0.05)(表1)。
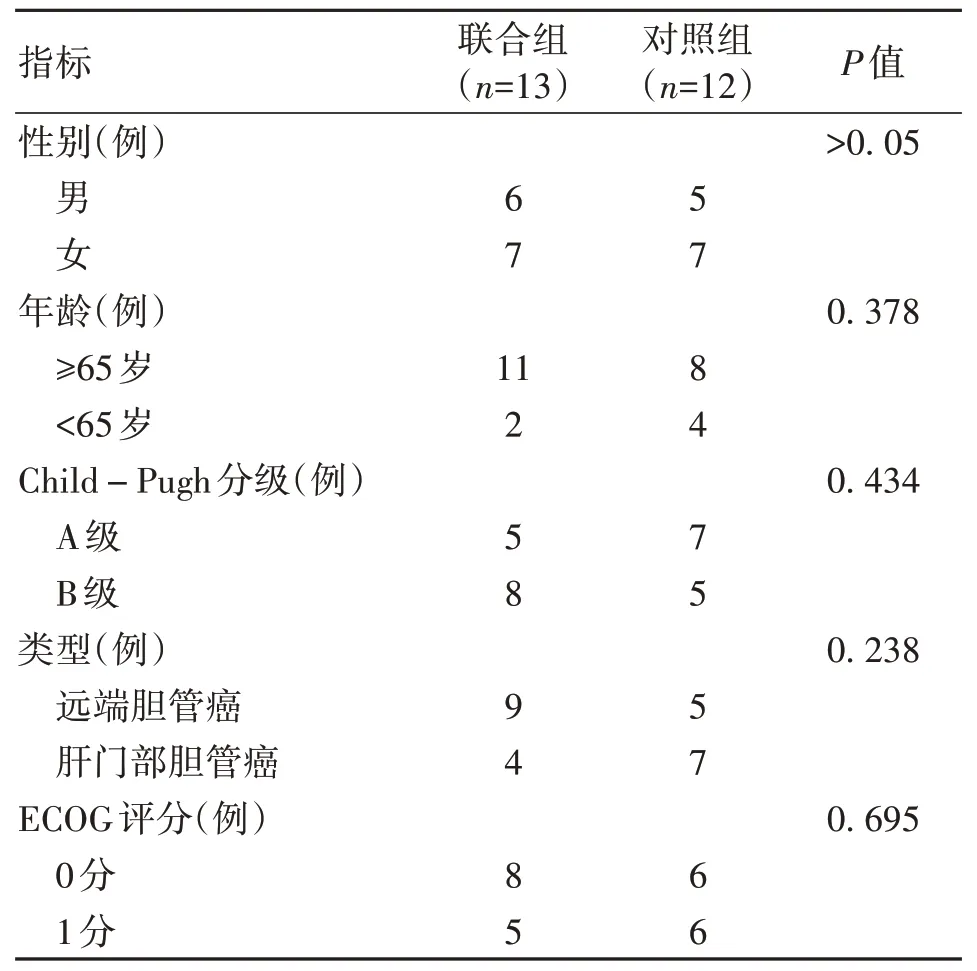
表1 两组患者基线资料对比Table 1 Comparison of information between the two groups
2.2 技术成功率及肝功能变化 随访时间为4~20个月,两组患者均成功植入胆道支架和125I粒子链,技术成功率100%。治疗后1个月两组间TBil、DBil、ALT和AST差异均无统计学意义(P值均>0.05)。两组患者组内术前和术后1个月血清TBil、DBil、ALT和AST比较,差异均有统计学意义(P值均<0.05)(表2、3)。

表2 两组间治疗后1个月肝功能指标对比Table 2 Comparison of liver function indicators between the two groups at 1 month after treatment
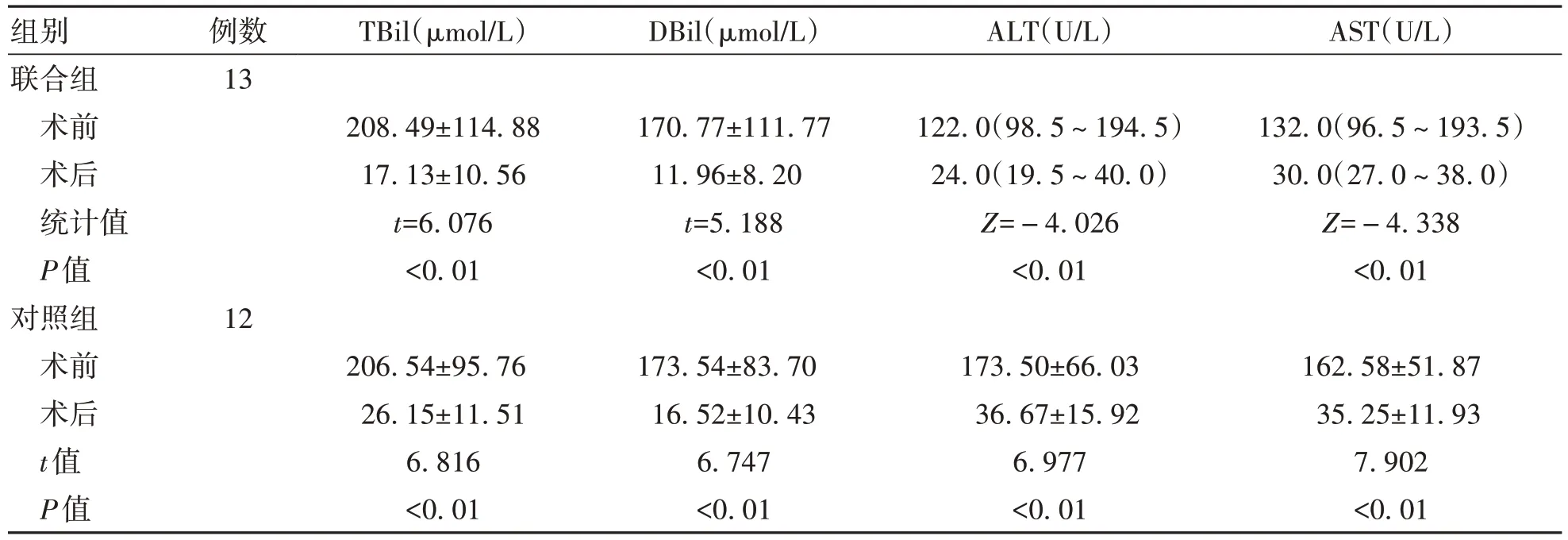
表3 两组患者治疗前、治疗后1个月肝功能指标组内比较Table 3 Comparison of liver function indicators before and after 1month of treatment in two groups
2.3 支架通畅情况和生存情况 对照组和联合组的mOS分别为11.5(8.0~13.6)个月和15.6(14.8~16.7)个月,差异有统计学意义(P=0.008);对照组和联合组的支架通畅期分别为7.0(5.6~8.5)个月和9.5(7.2~13.5)个月,差异有统计学意义(P=0.022)(图2、3)。
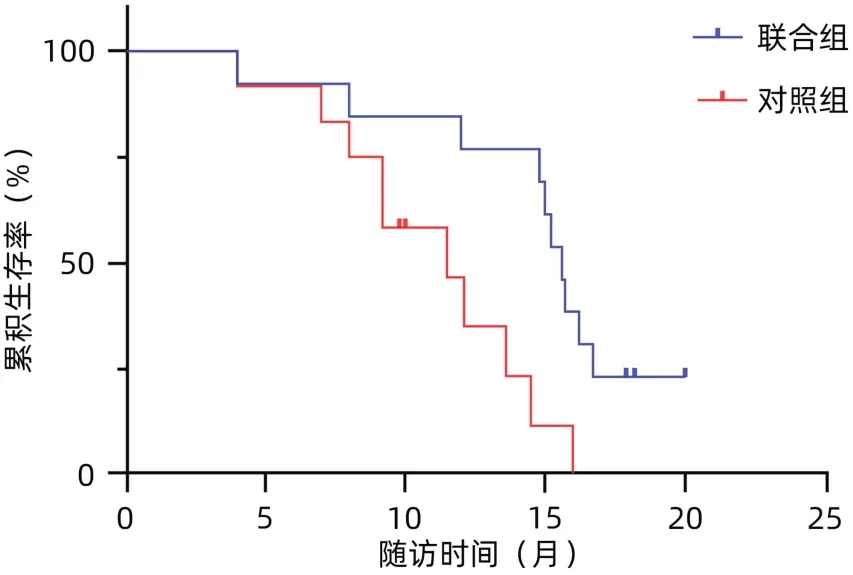
图2 两组患者的生存期比较Figure 2 Comparison of survival between the two groups of patients
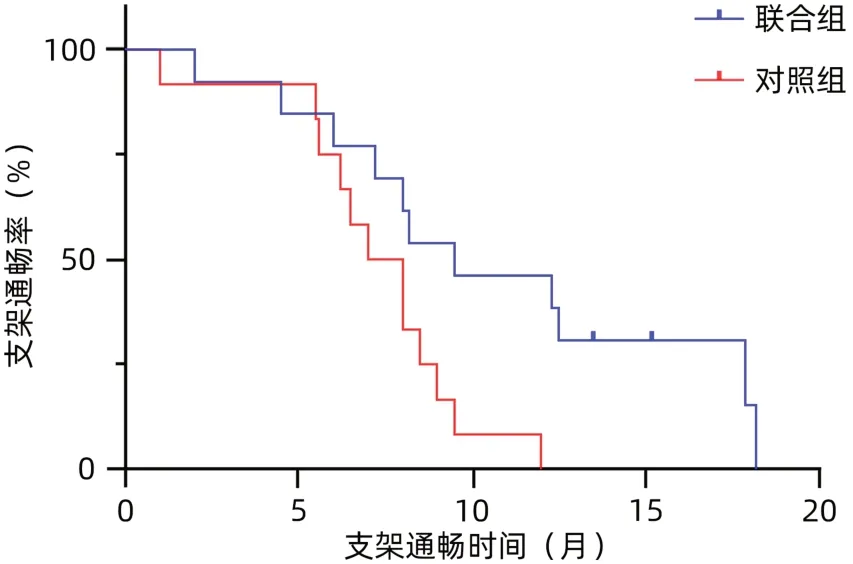
图3 两组患者的支架通畅时间比较Figure 3 Comparison of stent patency times between the two groups
2.4 仑伐替尼相关不良事件 联合组13例患者均出现药物不良事件,但无5级不良事件发生。其中主要不良事件为高血压、乏力、食欲减退、手足综合征等,3~4级药物不良事件的发生情况为高血压1例、腹痛1例、蛋白尿1例,所有不良事件经对症处理、降低服用药物剂量或者停止服用药物后好转(表4)。
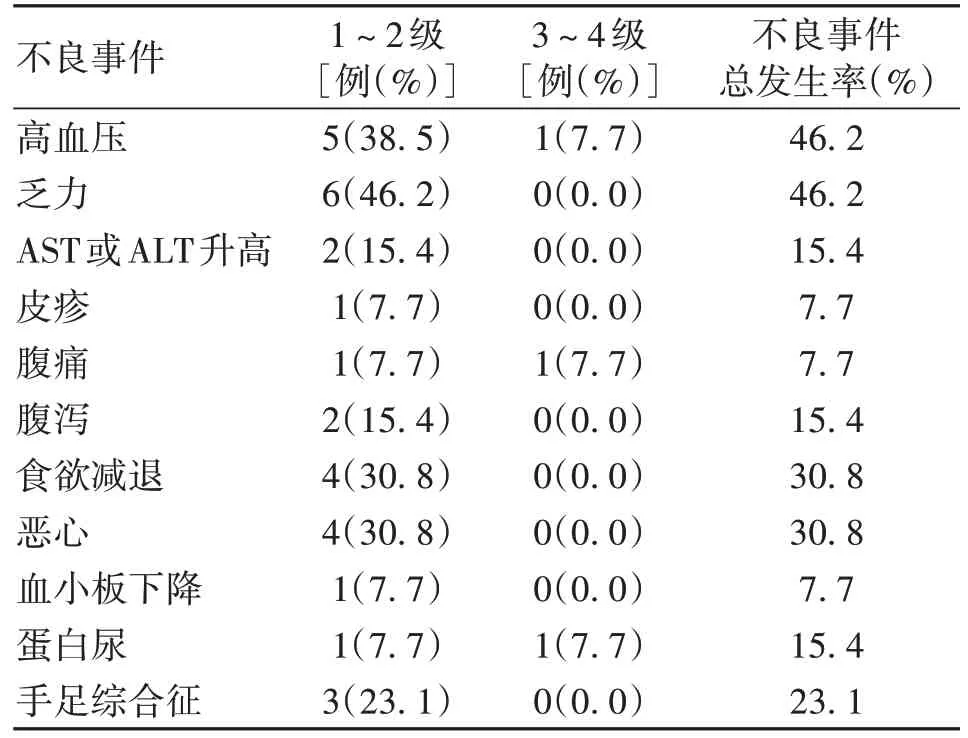
表4 联合组不良事件的发生情况Table 4 Occurrence of adverse events in the combined group
3 讨论
肝外胆管癌引起的恶性胆道梗阻性黄疸,需要迅速引流胆汁,降低胆红素,改善肝功能,目前125I粒子联合支架植入已经成为包括胆管癌、胆囊癌、胰腺癌等在内的肿瘤导致的恶性胆道梗阻的重要治疗方法[5-6,10],中位支架通畅期为231~279天,mOS为310~454天,粒子的持续辐射作用能抑制肿瘤细胞,减少胆道内膜的增生,同时改善细胞免疫功能[11],但随后仍会因为支架上下缘新发肿瘤、肿瘤向支架腔内生长、胆泥堵塞等问题会引发胆道堵塞[12],所以如何有效控制肿瘤的生长进而延长支架通畅时间和进一步改善预后仍然是一个难题。
近年来,靶向治疗已成为进展期胆管癌的一种选择[13]。既往有报道使用索拉非尼单药、瑞戈非尼单药用于治疗胆道恶性肿瘤[14-15],但效果均不理想。既往研究发现血管内皮生长因子(vascular endothelial growth factor,VEGF)、成纤维细胞生长因子受体4(fibroblast growth factor receptor-4,FGFR-4)和血小板衍生生长因子受体(platelet-derived growth factor receptor,PDGFR)在胆管癌患者中高表达,且与患者的不良预后存在关联[16-18]。仑伐替尼是一种多靶点选择性酪氨酸激酶抑制剂,可以抑制VEGFR、FGFR1-4、PDGFRα、RET和KIT[19-22]。有研究[7]使用仑伐替尼单药治疗不可切除胆道恶性肿瘤患者26例,客观缓解率(objective response rate,ORR)为11.5%,中位无进展生存期(median progression-free survival,mFPS)为3.19个月,mOS为7.35个月,显示出良好的抗肿瘤效果。另一项使用仑伐替尼单药治疗不可切除胆道恶性肿瘤的研究[8]也显示出较好的疗效,其ORR为12%,mFPS为3.8个月,mOS为11.4个月。本研究中联合组患者规律口服仑伐替尼,相对于对照组,具有更长的支架通畅期(9.5个月 vs 7.0个月)和mOS(15.6个月 vs 11.5个月),差异均有统计学意义。本研究两组患者治疗1个月后,黄疸和肝功能均有明显改善,每组患者治疗前后TBil、DBil、ALT和AST差异均有统计学意义。本研究对照组患者的中位支架通畅期和mOS与上述3个使用125I粒子联合支架植入治疗恶性胆道梗阻的研究[5-6,10]相似,而联合组患者中位支架通畅期和mOS则较上述研究延长。此外,与上述2个使用仑伐替尼单药治疗晚期胆道恶性肿瘤的研究[7-8]比较,联合组患者的mOS明显延长。分析联合组显示出更强的抗肿瘤效果的原因:(1)125I粒子持续放出γ射线破坏肿瘤细胞,同时改善细胞免疫功能;(2)仑伐替尼抑制VEGFR1-3、FGFR1-4、PDGFRa、KIT、RET等使得肿瘤血管的生成减少,进而抑制肿瘤的生长;(3)仑伐替尼通过减少肿瘤相关巨噬细胞的数量和增加CD8+T淋巴细胞的数量,进而调节肿瘤微环境和控制肿瘤的生长[23]。
在治疗安全性方面,联合组患者均出现药物不良事件,主要为高血压、乏力、食欲减退、手足综合征等,3、4级不良事件的发生率为23.1%,无5级不良事件的发生。3、4级不良事件发生率与Wang等[8]先前采用仑伐替尼单药治疗晚期胆道恶性肿瘤患者的19.5%相类似,但远低于Makoto等[7]采用仑伐替尼治疗晚期胆道恶性肿瘤患者的80.5%,分析原因可能为:联合组患者口服的药物剂量为12 mg/d(体质量≥60 kg)或8 mg/d(体质量<60 kg),与Wang等研究中的药物剂量一致,低于Makoto等研究中的24 mg/d,提示不良事件的发生可能与药物剂量大小相关。虽然联合组相关不良事件较多,但是经过对症处理或者减轻剂量、停药后,症状均有效缓解,可见125I腔内照射联合仑伐替尼治疗进展期肝外胆管癌是一种安全的治疗方法。
虽然本研究提示125I腔内照射联合仑伐替尼治疗进展期肝外胆管癌存在良好的疗效,但本研究存在一些局限性:样本量较小,为单中心回顾性研究,存在一定的选择偏倚及受试者偏倚,所得结论需要前瞻性、大样本、多中心对照研究进一步评估。在今后的研究中,将会继续纳入更多的病例,以验证该结论。
综上所述,对于进展期肝外胆管癌患者,125I腔内照射联合仑伐替尼比单纯125I腔内照射更有优势,是一种安全、有效的治疗方案。
伦理学声明:本研究方案于2023年3月6日经郑州大学第一附属医院伦理委员会审批通过,批号:2023-KY-0064,符合《赫尔辛基宣言》,患者均签署知情同意书。
利益冲突声明:本文不存在任何利益冲突。
作者贡献声明:朱兴书负责收集数据,资料分析,撰写及修改论文;陈鹏飞、张萌帆负责修改论文;李方正、陈金威参与收集数据与资料分析;任建庄、段旭华、张文广拟定课题设计,写作思路,指导撰写文章;韩新巍负责写作思路并最后定稿。

