精神分裂症合并NAFLD 患者血清甲状腺激素水平与精神症状的相关性*
虞 莹,金亚玲,赵 坚,何 泽,孙怡华,王诗芳
(1 江苏省南通市疾病预防控制中心微生物检验科,南通 226007;江苏省南通市第四人民医院2 检验科,3 精神科;江苏省南通市疾病预防控制中心4 信息科,5 办公室)
精神分裂症(schizophrenia,SCH)是一种严重影响人类身心健康和生活质量的疾病,常伴有特殊的思维、知觉、情感和行为等方面的障碍。长期服药、饮食不规律、行为异常等精神症状会影响患者的生理代谢功能。非酒精性脂肪肝性肝病(nonalcoholic fatty liver disease,NAFLD)是多种原因所致的以肝细胞弥漫性脂肪变性的病理学改变为主要特征(肝细胞脂肪堆积>5%)的应激性代谢肝脏损伤,包括单纯性脂肪变性、非酒精性脂肪性肝炎、纤维化、肝硬化及其并发症[1]。最新的研究[2]显示中国精神分裂症患者的NAFLD 患病率(22.44%)高于其他精神疾病,如双相情感障碍(17.89%)、抑郁症(12.62%)和精神障碍(12.99%)。甲状腺激素(thyroid hormone,TH)与NAFLD的发生存在一定的联系,亚临床甲状腺功能减退患者的NAFLD 发病风险较甲状腺功能正常人群增加1.24 倍[3]。本文以合并NAFLD 的SCH 患者为研究对象,探讨其血清TH 水平与精神症状的相关性。
1 资料与方法
1.1 一般资料 随机筛选2019 年1 月—2022 年4月在南通市第四人民医院精神科住院治疗的符合国际疾病分类诊断标准(international classification of diseases 10,ICD-10)的SCH 患者161 例,年龄18~71 岁,平均(43.14±12.74)岁;男78 例,女83 例。入组标准:(1)无过量饮酒史,即男性乙醇量<30 g/d;女性<20 g/d。(2)肝脏影像学检查示弥漫性脂肪肝。(3)患者和(或)家属签署知情同意书。排除标准:(1)酒精性肝病、基因3 型病毒性肝炎、自身免疫性肝炎、肝豆状核变性等可导致脂肪肝的特定性肝病。(2)药物、全胃肠外营养、炎症性肠病、乳糜泻及代谢性疾病等所致的综合征。依据中华医学会肝病学分会脂肪肝和酒精性肝病学组、中国医师协会脂肪性肝病专家委员会《非酒精性脂肪性肝病防治指南(2018 更新版)》[4],以临床超声检查结果有无肝区近场回声弥漫性增强(强于肾脏和脾脏)、远场回声逐渐衰减以及肝内管道结构显示不清楚等特征,将患者分为NAFLD 组(SCH合并NAFLD 组)77 例(42.9%),其中男37 例,女40例,年龄20~71 岁,平均(43.99±12.65)岁;对照组(SCH 无合并NAFLD 组) 84 例(57.1%),其中男41例,女43 例,年龄18~68 岁,平均(42.39±12.88)岁。本研究方案经南通市第四人民医院伦理委员会批准(2018-K023)。
1.2 研究方法
1.2.1 样本的收集与检测 入院次日清晨采集研究对象2 管空腹静脉血5 mL,静置30 min 后,以3 000 r/min 离心10 min 后分离血清。TH 检测仪器为Access Immunoassay System UncelDxI800 电化学发光分析,检测试剂为配套试剂,检测项目包括:三碘甲状腺原氨酸(total triiodothyronine,TT3)、总甲状腺素(total tetraiodothyronine,TT4)、游离三碘甲状腺氨酸(free tetraiodothyronine,FT3)、游离甲状腺素(free thyroxine,FT4)、促甲状腺激素(thyroid stimulating hormone,TSH)。操作步骤严格按照仪器标准规程进行。
1.2.2 精神症状评估 以国际公认的阳性与阴性症状量表精神症状量表(positive and negative syndrome scale,PANSS)评估患者精神症状。PANSS 量表内含30 个条目,包括阳性量表(P 分值)7 项、阴性量表(N分值)7 项、一般精神病理量表(G 分值)16 项,PANSS总分为P 总分、N 总分、G 总分之和。
1.3 统计学方法 采用SPSS 25.0 统计软件进行分析,正态分布、近似正态分布变量以±s 表示,非正态分布变量以中位数及四分位数间距[M(QL,QU)]表示,分类变量以频率和百分比表示。各组间各项指标分析采用t 检验、Mann-Whitney U 检验或χ2检验,采用Pearson 相关性分析血清TH 指标指与精神症状的相关性。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组一般资料比较 两组之间年龄、性别、最近一次入院时间、既往住院次数总和、病情诊断分化类型等比较差异均无统计学意义(均P>0.05),见表1。
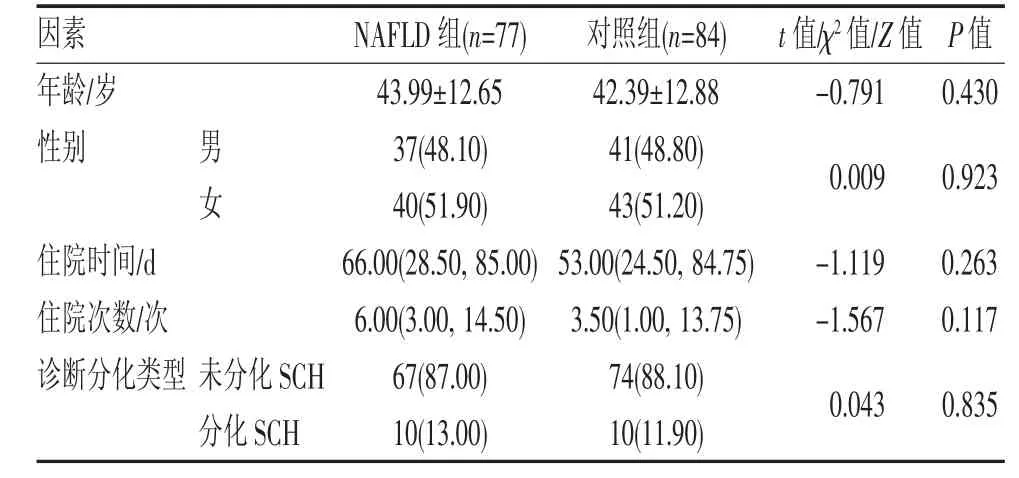
表1 NAFLD 组与对照组一般资料的比较[n,%,M(QL,QU)]
2.2 两组血清TH 水平及精神症状比较 实验室血清TH 结果显示,NAFLD 组TT4、FT4 水平显著低于对照组(P<0.05);PANSS 精神症状量表分值显示,NAFLD 组阴性症状(N 总分)显著高于对照组(P<0.05),见表2。
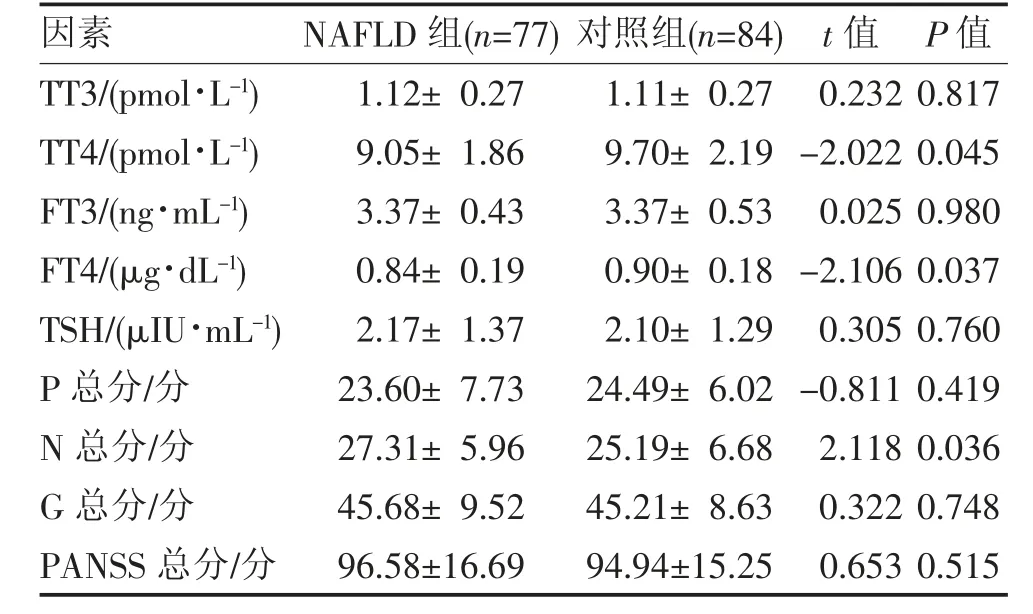
表2 NAFLD 组与对照组TH 水平及精神症状的比较
2.3 TH 水平与精神症状的相关性 Pearson 相关性分析结果显示,总体SCH 患者、NAFLD 组和对照组与TT3、FT3 无相关关系(P>0.05);总体SCH 患者TT4与阳性症状(P 总分)、一般精神症状(G 总分)及PANSS 量表总分呈正相关(P<0.05),FT4 与P 总分呈正相关(P<0.05);NAFLD 组TT4 与G 总分呈正相关(P<0.05);对照组TSH 与阴性症状(N 总分)呈正相关(P<0.05),见表3。

表3 各组患者血清TH 水平与精神症状相关性(r 值)
3 讨论
TH 是维持人体正常成长发育的激素,人体摄入充足的TH 能起到促进骨骼、脑和生殖器官的生长发育、提高神经兴奋性、加速糖、脂肪和蛋白质的代谢等作用,特别是促进许多组织的糖、脂肪及蛋白质的分解氧化过程,它刺激脂肪分解产生游离脂肪酸(free fatty acid,FFA)并促进其吸收以调节肝脏脂质代谢。此外,TH 还可以直接或间接促进由过量葡萄糖刺激的肝脏中的新脂肪生成[5-6]。亚甲状腺功能减退人群其NAFLD 患病率较正常人群有所升高,低TH 水平可能会破坏循环中现有的脂肪因子,如TNF-α、脂联素和瘦素,并且FFA 在TH 的刺激下进入肝脏,酯化为三酰甘油,三酰甘油清除率降低和肝脏三酰甘油沉积引起的肝脂肪酶活性下降可诱发NAFLD。有研究[7-8]表明血清FT4 水平降低或TSH 水平升高与NAFLD 的发生呈显著独立相关。动物实验[9]中注入甲状腺素受体激动剂的NAFLD 大鼠肝损害可有效改善。补充选择性TH-β 受体激动剂可有效降低甲状腺功能减退患者NAFLD 发生率和血脂异常等代谢障碍[5]。研究[10]表明二代抗精神病药物治疗后患者有甲状腺功能减退趋势。本研究结果中也证实,SCH 合并NAFLD 组TT4、FT4 水平显著低于对照组,说明合并NAFLD 的SCH 患者有明显甲状腺功能减退症或亚临床甲状腺功能减退症的特征,但两组药物使用是否有差异,未能进一步证实。而甲状腺功能减退症与NAFLD 发生也可能与肝脏中TH 信号的中断或减少,从而导致其对脂质的利用降低有关[11]。
TH 与精神分裂症、焦虑症和抑郁症等精神疾病有关[12]。SCH 患者精神症状的病情程度、认知功能、情绪和行为可能与住院患者的临床特征及其下丘脑-垂体-甲状腺轴激素水平有关[13-14]。PANSS 量表中阴性症状评分包含情感迟钝、情感退缩、情感交流障碍、被动/淡漠社交退缩等7 项指标。本次研究中合并NAFLD 组的SCH 患者其阴性症状(N 总分)显著高于对照组,说明与无NAFLD 的SCH 患者相比,合并NAFLD 的SCH 患者其情感淡漠、退缩的阴性精神症状更明显。当懒散、少动、活动量减少等为特征的精神症状愈显著,身体能量消耗降低,肝脏三酰甘油沉积增加,则更易诱发SCH 患者合并NAFLD的可能。FT4 活性成分的慢性毒理学变化可能是SCH 慢性精神病理的原因之一[14]。认知能力下降、抑郁状态是甲状腺功能减退症的常见表现,而甲状腺功能亢进症多表现为急性发病、暴躁等症状[15]。本研究结果中总体SCH 患者TT4 与阳性症状(P 总分)、一般精神症状(G 总分)、PANSS 量表总分呈正相关,FT4 与阳性症状(P 总分)均呈正相关,表明SCH 患者体内血清TT4、FT4 水平上调,其妄想、兴奋、猜疑等阳性症状越明显;TT4 水平越高,一般精神症状越严重。这与TH 会影响情绪和行为,高水平的FT4 可维持神经系统的兴奋性,当甲状腺功能障碍时会影响神经递质系统导致精神疾病的研究结论[16-17]一致。本研究结果显示,合并NAFLD 的SCH 患者血清TT4水平与一般精神症状存在相关性。G 总分包括:焦虑、紧张、装相和作态、冲动控制缺乏等16 个项目,当合并NAFLD 的SCH 患者血清TT4 水平降低时,其焦虑、紧张、冲动控制障碍等一般精神症状有所缓解。TSH 与甲状腺素相互作用表现为:TSH 刺激甲状腺合成和释放TH,同时TH 作用于垂体和下丘脑以抑制TSH 的产生。TSH 通过上调肝脏中3-羟基-3-甲基-戊二酰辅酶A 还原酶的表达,以促进胆固醇的合成,影响血脂代谢[18]。SCH 患者中较低的TSH 水平与体内较高水平的血浆过氧化物含量显著相关,后者可能通过调节自由基和氧化应激来促进SCH 患者更好的甲状腺稳态[13]。对照组中TSH 与阴性症状(N 总分)的线性关系中呈正相关,说明在无NAFLD的SCH 患者体内,随着TSH 水平的降低,阴性症状有所缓解,即情感退缩、被动淡漠社交退缩的症状较少,该类人群自主活动量相对有所增加,体内三酰甘油代谢增加以及胆固醇合成减低,罹患NAFLD 的风险也相应降低。
综上所述,SCH 是由一组症状群所组成的临床综合征,其合并NAFLD 患病率明显高于正常人群,二者之间的相互作用可能是多因素的,包括自身代谢、生存环境、药物依从性等。本研究再次证实SCH患者体内血清TH 水平与临床精神症状相关,同时也发现与无NAFLD 的SCH 患者相比合并NAFLD的SCH 患者TT4 水平较低,且该人群体内血清TT4水平与一般精神症状有关,而无NAFLD 合并的SCH 患者TSH 水平与阴性症状有关。在临床诊疗工作中,定期监测SCH 患者的甲状腺功能水平,合理用药可以有助于改善患者的精神症状,降低SCH 患者罹患NAFLD 的风险。

