基于HPLC、GC指纹图谱及化学计量学的金莲花质量评价研究
都青钰 高 欣 李 琳 施 杰 和 敏 于永杰,2,3 张 霞,2,3*
1.宁夏医科大学药学院,宁夏 银川 750004;2.宁夏药物创制与仿制药研究重点实验室,宁夏 银川 750004;3.宁夏少数民族医药现代化教育部重点实验室,宁夏 银川 750004;4.宁夏启元药业有限公司,宁夏 银川 750004
金莲花(flos trollii,FT)为毛茛科金莲花属植物金莲花(TrolliusChinensisBunge)的干燥花,味苦性寒。研究[1]表明,金莲花具有抗炎、抗菌、抗病毒、抗氧化等药理活性,临床主要用于治疗呼吸道感染、感冒发热、口疮、牙龈肿痛、疔疮肿毒等症。2020年版《中国药典》收载了金莲花的6个单方及复方品种[2],其复方制剂2003年被确定为对非典型肺炎的不同病理环节能够明显改善患者症状的8个中成药之一[3],在新冠疫情防控中,金莲花复方制剂入选了5个省市的《新型冠状病毒感染肺炎诊疗方案》。同时,金莲花也被广泛应用于功能食品、化妆品及保健品领域。金莲花中的化学成分类型主要有黄酮类、生物碱类、有机酸、甾醇类及挥发油类等[4]。目前对金莲花黄酮类和酚酸类成分的药理学研究较多,其挥发油虽然含量低,但药理作用丰富,有较大的开发利用空间。研究[5]表明,金莲花挥发油能够降低卷烟烟气的刺激性,提高香气质和香气量,可作为卷烟的新型中草药香原料。
金莲花多分布于河北北部、内蒙古东部、山西等寒冷地区。2010年,宁夏固原市引种成功,现已有近千亩的种植规模。由于不同地区气候条件、土壤等的差异,可能导致不同产地金莲花化学成分及产品质量的差异。目前金莲花质量评价研究多为对一个或几个成分的含量测定,难以全面反映其内在质量属性。中药指纹图谱可在整体层面反映中药内在化学物质信息的数据和变量,已广泛应用于中药真实性鉴定、安全性评价及有效性评价等各个方面[6-9]。高效液相色谱(HPLC)指纹图谱多用于天然产物非挥发性成分的质量控制及评价,而气相色谱(GC)指纹图谱可实现对挥发性成分的质量控制[10-14]。本文将HPLC指纹图谱技术与GC指纹图谱技术相结合,并采用PLS-DA,从多角度综合评价不同产地金莲花的质量,以期为金莲花的全面质量控制和综合利用提供参考。
1 仪器与材料
1.1 仪器 LA-20T型高效液相色谱仪(日本岛津公司);8890型气相色谱仪(美国安捷伦公司);GC Agilen7890B气质联用仪(MS Agilen5977A);XS105DU型分析天平(瑞士Mettler-Toledo公司);KQ5200B 型超声波清洗器(昆山市超声仪器有限公司);FW177型中草药粉机(中国天津泰斯特仪器有限公司);同时蒸馏萃取装置(安徽天长康玻实验设备有限公司)。
1.2 材料 荭草素(批号:PS1326-0020)、荭草素-2″-O-β-L-半乳糖苷(批号:PS1327-0025)、牡荆素(批号:PS0760-0025)对照品均购自成都普思生物科技股份有限公司。藜芦酸(批号:AF8051850)购自成都埃法生物科技有限公司。十五烷(批号:12361)购自上海晶纯试剂有限公司。月桂酸(批号:111774-201602)、肉豆蔻酸(批号:A15S6L2)、棕榈酸(批号:M02D11K133109)、二十三烷(批号:Z16N9H75194)均购自上海源叶生物科技股份有限公司。色谱分析用乙腈、甲醇、二氯甲烷为色谱级,购自美国Fisher公司;其他试剂均为分析纯。
1.3 药材 金莲花样品共27个,于2020年6~8月采自3个产地,其中采自河北省承德市(样品编号:S1-S8)、内蒙古呼伦贝尔市(样品编号:S9-S17)和宁夏固原市(样品编号:S18-S27)的样品数量分别为8个、9个和10个。由宁夏医科大学张霞正高级工程师鉴定为毛茛科金莲花属植物金莲花的干燥花,样品存放于宁夏医科大学药学实验中心。取所有样品适量,等量混合均匀得QC样品。
2 方法与结果
2.1 HPLC指纹图谱
2.1.1 供试样品溶液的制备 精密称取的金莲花药材粉末约0.5 g,置于100 mL具塞锥形瓶中,精密加入25 mL 80%甲醇溶液,称重,40 kHz超声30 min。将锥形瓶放冷至室温,称定重量后用80%的甲醇补重,10000×g离心10 min,上清液作为供试样品溶液,取10 μL进行HPLC分析。
2.1.2 对照品溶液的制备 分别精密称取荭草素-2″-O-β-L-半乳糖苷、荭草苷、牡荆苷、藜芦酸适量,加80%甲醇制成质量浓度分别为125.00 μg/mL、268.50 μg/mL、53.13 μg/mL、11.59 μg/mL的混合对照品溶液。
2.1.3 色谱检测条件 色谱柱:EClipse Plus C18色谱柱(250 mm×4.6 mm,5 μm);流速:1.0 mL/min;柱温:30 ℃;检测波长:272 nm。流动相:乙腈(A)-0.05%H3PO4水溶液(B),梯度洗脱分别为0~10 min,96% ~84%B;10~27 min,84%~84%B;27~28 min,84%~78%B;28~31 min,78%~78%B;31~36 min,78%~76%B;36~43 min,76%~75%B;43~52 min,75%~64%B;52~60 min,64%~0%B;60~70 min,0%B;进样量:10 μL。
2.1.4 方法学考察
2.1.4.1 精密度试验 取金莲花QC样品,根据2.1.1项下方法制备样品溶液,用2.1.3项下色谱分析条件,进样6次。以峰(8)荭草苷作为参比,计算得到各共有峰的相对保留时间RRT(relative retention time,RRT)的RSD(relative standard deviation,RSD)为0.02%~0.14%,各共有峰相对峰面积RPA(relative peak area,RPA)的RSD为0.67%~2.00%,表明仪器的精密度在规定范围之内。
2.1.4.2 稳定性试验 取金莲花QC样品,按2.1.1项下方法制备供试样品溶液,分别于0 h、2 h、4 h、6 h、8 h、12 h按2.1.3项下色谱条件进样,用峰(8)荭草苷作为参比,得到各共有峰RRT的RSD为0.01%~0.08%,各共有峰RPA的RSD值为1.76%~2.95%,说明样品溶液在12 h内稳定。
2.1.4.3 重复性试验 精密称取金莲花QC样品,根据2.1.1项下方法平行制备6份样品溶液,照2.1.3项下色谱分析条件进样,用峰(8)荭草苷作为参比,各共有峰RRT的RSD为1.42%~1.81%,各共有峰RPA的RSD为0.99%~2.93%,说明方法的重复性良好。
2.1.5 金莲花HPLC指纹图谱的构建、相似度评价以及共有峰指认 根据2.1.1项下方法,分别制备S1-S27 金莲花样品溶液,照2.1.3项下色谱分析条件进样。运用《中药色谱指纹图谱相似度评价系统(国家药典委员会研制,2012版)》软件对色谱结果进行共有峰匹配。设时间宽度为0.1 min,参照图谱为各峰信号强度较大,峰形较佳,分离度较好的S1号样品图谱。运用“中位数法”,多点矫正和自动匹配各个指纹图谱的色谱峰,对照指纹图谱(R)和27批金莲花样品生成的指纹图谱共有模式。如图1所示。

图1 对照指纹图谱和27批金莲花样品生成的指纹图谱共有模式图
荭草苷为金莲花的主要有效成分之一,《中国药典》2020年版一部收载的5个金莲花制剂均以荭草苷为含量测定的指标成分,且荭草苷在金莲花HPLC色谱图中峰面积较大,与相邻峰有较好的分离效果,因此选择荭草苷色谱峰为参照峰(S),金莲花HPLC指纹图谱的共有模式生成了15个共有峰。
相似度评价:计算金莲花样品的HPLC指纹图谱和对照图谱的相似度,见表1。各批金莲花指纹图谱的相似度除S4样品外均大于0.900,表明来源于河北、内蒙古、宁夏3个产区的金莲花各批样品的整体化学成分类似,样品之间的一致性良好,本实验建立的HPLC指纹图谱适用于金莲花药材的质量评价。各指纹峰RPA的RSD值为16.79%~77.50%,说明各样品的共有峰差异较大。

表1 金莲花样品HPLC指纹图谱相似度评价表
共有峰的指认:经比对对照品与样品色谱峰的保留时间及光电二极管阵列检测器(PDA)光谱图,指认出4个色谱峰,分别是7号峰荭草素-2″-O-β-L-半乳糖苷,8号峰荭草苷,9号峰牡荆苷,10号峰藜芦酸。如图2所示。

图2 混合对照品(A)和金莲花样品(B)的HPLC图及指认化合物的PDA光谱图(C1-C4)
2.2 GC指纹图谱
2.2.1 供试品溶液的制备 同时蒸馏萃取(simultaneous distillation extraction,SDE)可将挥发性成分的提取与溶剂萃取过程同时进行,是分析中药挥发性成分简便且重复性好的前处理方法。本实验采用同时蒸馏萃取法制备供试品溶液。称取金莲花粗粉20 g,与350 mL纯化水及40 g NaCl加入到1000 mL圆底烧瓶中并混合均匀。在另一个250 mL烧瓶中加入40 mL二氯甲烷。两个烧瓶在电热套中加热至沸腾,提取回流2 h。冷却至室温后,将装有二氯甲烷的烧瓶从仪器中取出,加入2 g无水硫酸钠静置1 h用于除去水分,上清液作为供试品溶液。
2.2.2 对照品溶液的制备 分别精密称取十五烷、二十三烷、月桂酸、肉豆蔻酸、棕榈酸适量,加二氯甲烷制成混合对照品溶液,质量浓度分别为13.18 μg/mL、37.35 μg/mL、58.23 μg/mL、49.78 μg/mL、23.65 μg/mL。
2.2.3 色谱检测条件 程序升温:初始温度为50 ℃,保持3 min,再以2 ℃/min升至250 ℃,保持10 min;进样口温度为280 ℃;检测器温度为300 ℃;载气流速为40.0 mL/min(恒压模式);分流比为2∶1,进样量为1 μL。色谱柱:Agilent HP-5(30 m×0.32 mm×0.25 μm)毛细管柱。
2.2.4 质谱分析条件 离子源:EI离子源;离子源温度:230℃;质量范围:m/z 50~500 Da。四级杆温度为150 ℃,质谱接口温度280 ℃,电子能量70 eV;采用全扫描模式(SCAN)。按2.2.1项下方法制备供试溶液,进样量为1 μL。
2.2.5 方法学考察
2.2.5.1 精密度试验 按2.2.1项下方法制备金莲花QC样品供试溶液,照2.2.3项下GC分析条件,连续进样6次,以峰4(月桂酸)作为参比,得到各共有峰RRT的RSD为0.02%~0.04%,各共有峰RPA的RSD值为0.28%~2.19%,说明仪器有良好的精密度。
2.2.5.2 稳定性试验 根据2.2.1项下方法制备金莲花QC样品溶液,依照2.2.3项下GC分析条件,分别于0 h、2 h、4 h、6 h、8 h、12 h、24 h进样。以峰4作为参比,各共有峰相对保留时间RRT的RSD值为0.02%~0.06%,各共有峰RPA的RSD值为0.23%~2.65%,说明金莲花样品溶液在24 h内有良好的稳定性。
2.2.5.3 重复性试验 依照2.2.1项下方法平行制备金莲花QC样品溶液6份,照2.2.3项下GC分析条件进样,以峰(4)月桂酸作为参比,得到各共有峰RRT的RSD值为0.04%~0.10%,各共有峰RPA的RSD值为1.97%~6.25%,结果表明该方法重复性良好。
2.2.6 GC指纹图谱的建立及相似度评价 按2.2.1项下方法,分别制备S1-S27 批金莲花样品GC供试品溶液,照2.2.2项下色谱分析条件进样。选取的参照图谱为峰形较佳,各峰信号强度较大,分离完全的S1号样品图谱。以与2.1.5项下 HPLC指纹图谱相同的方法生成金莲花GC对照指纹图谱(R)和样品指纹图谱共有模式,如图3A所示,其中R为生成的对照指纹图谱。因为在各批金莲花中均有月桂酸(峰4),且RRT适中且RPA较大,因此选其作为参照峰(S),共有8个共有指纹峰被标定出。
相似度评价:对27批金莲花样品的GC指纹图谱运用《中药色谱指纹图谱相似度评价系统(2012版)》软件与对照图谱进行相似度计算,计算结果见表2。不同产地金莲花指纹图谱相似度均>0.950,表明来源于河北、内蒙古、宁夏3个产地的金莲花样品整体挥发性化学成分有类似性,各批次样品之间一致性较好。
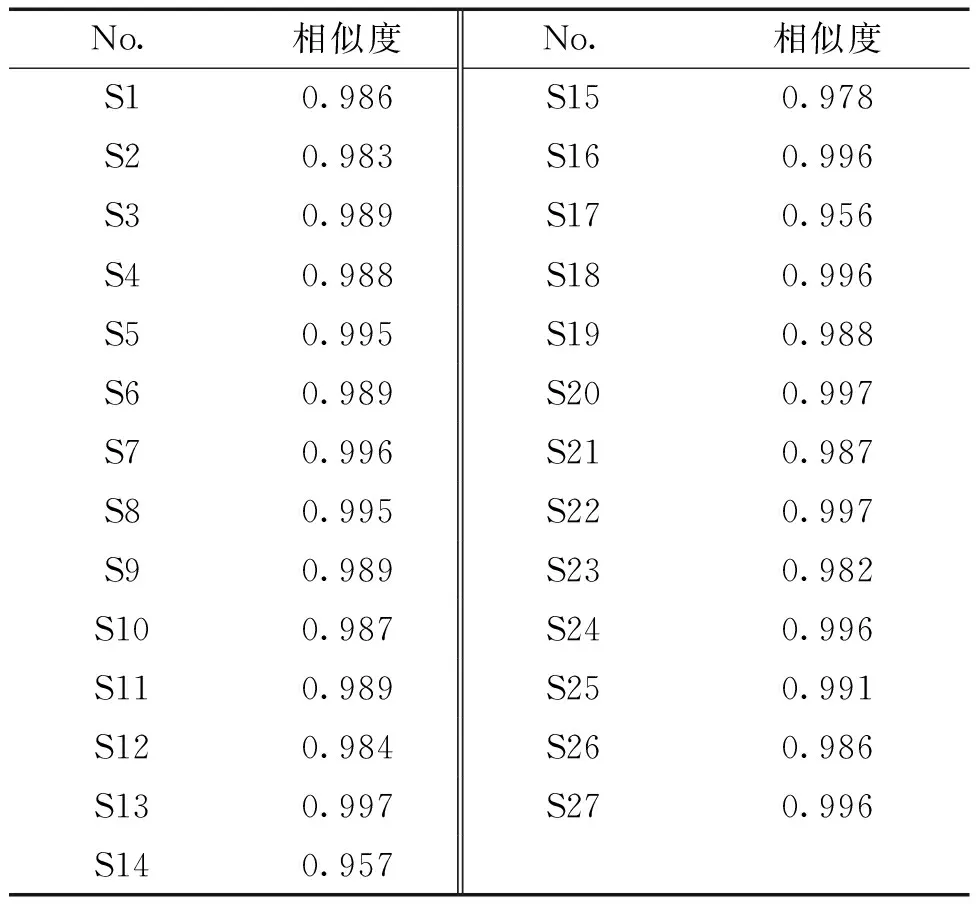
表2 金莲花样品GC指纹图谱相似度评价表
2.2.7 共有峰的指认 通过比对对照品保留时间及高分辨质谱谱库检索并经对照品验证,确认了5个色谱峰,分别是峰3为十五烷,峰4为月桂酸,峰5为肉豆蔻酸,峰6为棕榈酸,峰7为二十三烷。如图3B和3C1至C5所示。
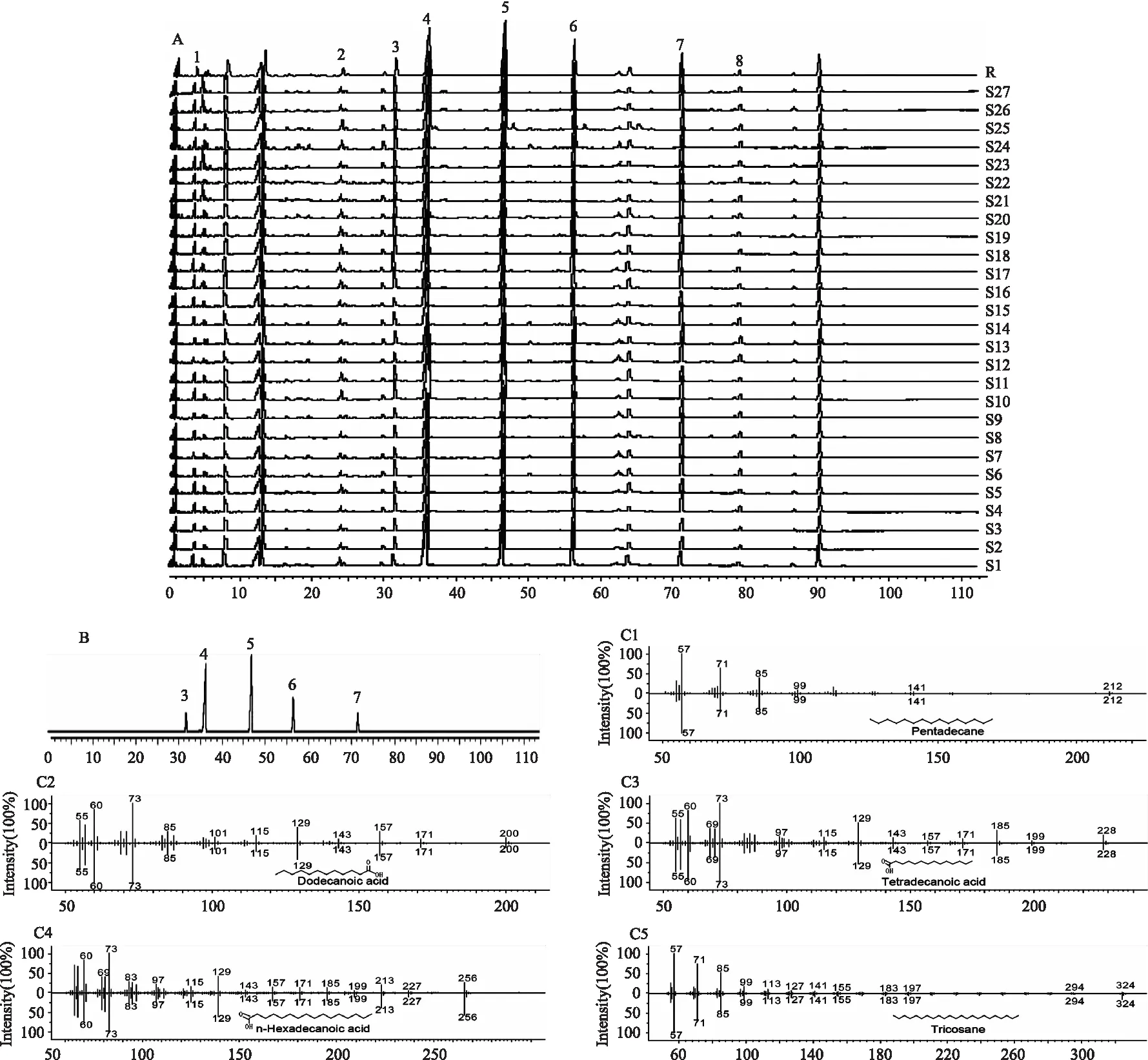
C1:15烷;C2:月桂酸;C3:肉豆蔻酸;C4:棕榈酸;C5:23烷
2.3 化学计量学模式识别 分别将金莲花HPLC和GC指纹图谱共有峰数据导入SIMCA-P 14.1软件,采用PLS-DA进行分析。
2.3.1 基于HPLC共有峰的不同产地金莲花药材差异比较分析 基于HPLC共有峰进行PLS-DA分析,所建模型中R2X和R2Y分别为0.658和0.664,预测能力参数Q2(Cum)为0.608,均大于0.5,表明该模型预测能力较好,可用于不同产地金莲花药材的识别。PLS-DA的Scores图显示,27批金莲花样品可按产地分成3类(如图4A所示)。河北、宁夏和内蒙古所产金莲花分别主要集中在第一象限、第四象限和第二、三象限。通过变量权重重要性排序(VIP)值筛选影响金莲花产地差异的标志性成分,以VIP值>1为筛选标准,标记出9个贡献较大的成分(如图4B所示)。按影响显著性排序,分别为峰11>荭草苷>峰1>峰12>峰6>峰15>峰13>藜芦酸>牡荆苷,不同产地金莲花的荭草苷、藜芦酸、牡荆苷具有显著差异。因此,可将金莲花中VIP值>1的9个峰作为特征图谱,荭草苷、藜芦酸、牡荆苷作为含量测定的指标成分。

图4 金莲花药材HPLC共有峰的PLS-DA分析scores图(A)和VIP图(B)
2.3.2 基于GC共有峰的不同产地金莲花药材差异比较分析 基于GC共有峰的PLS-DA:R2X为0.92,R2Y为0.557,Q2为0.29,表明该模型不能有效识别样品间差异。PLS-DA的 scores 图5显示,27批不同产地金莲花交错分布,说明金莲花中挥发性成分的种类及含量较相近,和产地无显著性关联。
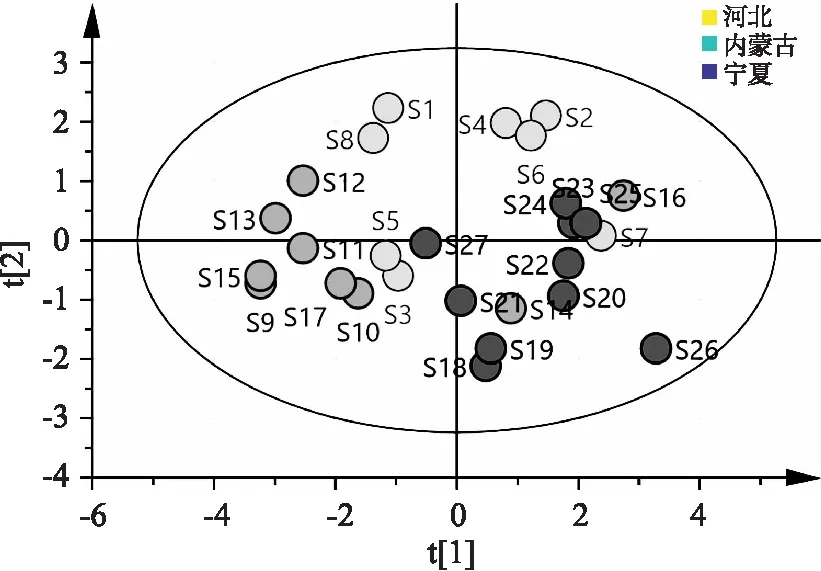
图5 金莲花药材GC共有峰的
3 讨论
3.1 样品制备方法的优化 超声提取法能促使植物组织破壁或变形,更充分提取中药有效成份,因此本研究选取超声提取法制备样品。考察了不同提取溶剂(水、甲醇、乙醇),结果表明以甲醇为溶剂提取效率最高。进而比较了不同甲醇浓度(80%、60%、40%)以及不同提取时间(10 min,30 min,50 min),结果表明80%甲醇超声提取30 min的提取效率最高,能更充分提取中药有效成分。
3.2 色谱条件的优化 样品全波长扫描结果表明检测波长为272 nm时,色谱峰数目较多且具有较强的信号。本研究考察了InertSustain C18(4.6 mm×250 mm,5 μm)、Waters Xbeiage C18(4.6 mm×250 mm,5 μm),Agilent Eclipse Plus C18(4.6 mm×250 mm,5 μm)等不同色谱柱,结果发现采用Agilent Eclipse Plus C18色谱柱进行洗脱时,金莲花中各化学成分的分离效果较佳。本实验在文献中[15]流动相系统的基础上进行了优化,实验发现采用乙腈-0.05%磷酸水为流动相时各成分分离效果理想,色谱峰峰型较好。
3.3 挥发性成分提取方法的选择 提取方法对金莲花挥发性成分的测定具有重要影响,水蒸气蒸馏法、有机溶剂提取和SDE法是从植物样本中提取热稳定挥发物的有效方法,本实验对3种提取方法进行了比较。SDE法仅需约2.5 h,提取时间远少于HD法和有机溶剂提取法,而且,SDE法重复性好,提取得到的成分更丰富,因此,金莲花气相色谱分析中挥发性成分的提取方法选择SDE法。
综上,本研究分别采用HPLC、GC法对27批不同产地的金莲花药材进行分析,利用“中药色谱指纹图谱相似度评价系统”建立相应的色谱指纹图谱。采用PLS-DA对不同产地金莲花药材的成分差异进行比较。结果显示:金莲花药材HPLC指纹图谱有15个共有峰,经与对照品的保留时间及PDA光谱图比对,指认出4个色谱峰,分别是荭草素-2″-O-β-L-半乳糖苷、荭草苷、牡荆苷和藜芦酸。GC色谱指纹图谱有8个共有峰,通过高分辨质谱解析并经对照品比对,确认了5个色谱峰,分别是十五烷、月桂酸、肉豆蔻酸、棕榈酸和二十三烷。共有特征峰基本上可以反映药品的整体质量状况。经PLS-DA分析,基于金莲花HPLC指纹图谱共有峰可将样品按产地明显地聚集为3组,以VIP值>1为筛选标准,标记出9个对差异贡献较大的成分。基于金莲花GC指纹图谱共有峰不能进行产地区分,金莲花中挥发性成分的种类及含量较相近,和产地无显著性关联。研究结果为金莲花的全面质量控制和综合利用提供了参考。
金莲花药材产地分布于我国北方较寒冷地区,本研究主要对来源于河北,内蒙,宁夏3个产地金莲花药材的指纹图谱及成分差异进行了分析,还需要收集更多药材对本研究结果加以佐证。同时,不同产地金莲花植物代谢物差异的影响因素以及不同产地金莲花的药理作用效果是否有差异还需进一步研究。

