多组元掺杂对NiCoCrAlY氩气雾化粉末1200 ℃高温氧化行为的影响
任智强,尹轶川,王晓明,王文宇,朱 胜,韩国峰*
(1 陆军装甲兵学院 装备再制造技术国防科技重点实验室,北京 100072;2 南京理工大学 材料科学与工程学院,南京 210094)
NiCoCrAlY涂层常被用于保护工业零件的热端部分(特别是燃气涡轮机的叶片)免受高温腐蚀和高温氧化,在高温氧化环境下涂层面临的主要问题是氧化后的剥落和开裂[1-2]。此外,由于不断追求更高的推重比和燃烧效率,对燃气轮机的服役温度提出更高的要求。所以,为了满足更高的服役温度(>1150 ℃),材料性能提升是十分必要的[3]。而NiCoCrAlY材料由于具有高强度、高弹性模量、优良的抗氧化性和抗热腐蚀性,具有巨大的应用潜力。起初,研究者的焦点主要集中在通过掺杂Y,Pt和Si等元素提高涂层中Al2O3层的稳定性和附着力[4-6]。之后,科研工作者们通过弥散氧化物的添加来改善NiCrAlY涂层的力学性能以及涂层与高温合金基体之间的相容性[7-9],如难熔金属铼(Re),作为有益的合金元素被引入,以改善涂层的高温抗氧化性和耐热腐蚀性能[10-11]。近年来,在NiCoCrAlY材料中掺杂其他金属元素,如Ta,Nb,Hf,Re等以增强其抗氧化性的研究逐渐增多[12-14]。Gao等[15]报道了氧化温度对NiCoCrAlYTa粉末微观结构演变的影响,Ta在长时间氧化后会扩散到氧化层和金属的界面,提高粉末的抗氧化能力。Nb在β-NiAl体系中能够形成Nb(C, N),起到钉扎晶界的作用,降低材料的氧化速率[16]。Hf掺杂的NiCoCrAlY材料显示出更长的热循环寿命,而Hf的氧化物也具有出色的稳定性,能够改善NiCoCrAlY材料的塑性和强度[17-20]。王晓明等的研究表明,Nb,Hf和Ta复合添加对提高NiCoCrAlY高温性能十分有益[21]。由于粉末颗粒是制备涂层的基本原料,因此NiCoCrAlY粉末抗氧化能力的高低会直接影响最后涂层抗氧化性能的好坏。
本工作选择氩气雾化NiCoCrAlYNbHfTa粉末和商用NiCoCrAlY粉末,对粉末原始形貌、显微结构和相组成进行对比,并对粉末在1200 ℃干燥空气中进行3个不同测试时长(24,48 h和72 h)的等温氧化实验,对比氧化后两种粉末的氧化动力学曲线、显微形貌和相组成,以验证Nb,Hf和Ta复合添加对NiCoCrAlY粉末高温氧化性能的影响,为优质涂层材料的制备提供参考和借鉴。
1 实验材料与方法
1.1 多组元掺杂NiCoCrAlY粉末制备
利用高纯度的Ni,Co,Cr,Al,Y,Nb,Hf和Ta金属(>99.95%,质量分数,下同),采用传统的气体雾化法制备NiCoCrAlYNbHfTa粉末。首先用高频感应炉在氩气保护气氛下熔炼Ni,Co,Cr,Al,Y,Nb,Hf和Ta原料块体,然后将熔化的液体混合物倒入气体雾化喷嘴,利用高压惰性气流将其分裂成小液滴,最后在惰性气体气氛下,冷却固化的NiCoCrAlYNbHfTa粉末被筛分成粒度为15~53 μm的粉末。制备的NiCoCrAlYNbHfTa粉末(表示为P1)以及对照用商售NiCoCrAlY粉末(表示为P2)的理论成分如表1所示。两种粉末均在同一粉末生产厂家(安徽盛赛再制造科技有限公司)以相同工艺条件制备。

表1 粉末的理论成分(质量分数/%)Table 1 Nominal compositions of powders(mass fraction/%)
1.2 多组元掺杂NiCoCrAlY粉末氧化实验
将气雾化获得的P1粉末以及对照用P2粉末分散在刚玉坩埚内,目的是为了避免粉末高温烧结对氧化层生长造成影响。随后将含有粉末的刚玉坩埚放置在马弗炉中,马弗炉提前加热至1200 ℃。最后,在所需的氧化时间(24,48,72 h)后,将坩埚取出,随空气冷却至室温,以备后续测试使用。此外,将测定好体积的粉末随坩埚放入加热至1200 ℃的马弗炉内,每隔8 h将坩埚取出,并记录称重,直至氧化至72 h后,停止加热。
1.3 材料表征
采用D/MAX-2500/PC X射线衍射仪在30 kV CuKα辐射下测定氧化前后粉末的物相组成,扫描范围10°~90 °,扫描速率4 (°)/min;利用FEI XL30扫描电子显微镜对等温氧化前后粉末的微观形貌进行表征;使用ISIS-3000能量色散X射线分析检测器对氧化层和粉末的化学成分进行识别。
2 结果与分析
2.1 粉末原始形貌、显微结构及相组成
图1是两种粉末的表面形貌。可以看出,两种粉末颗粒整体表面较为光滑,只有较少的颗粒具有卫星球,表面无明显缺陷与裂纹,粉末质量较好。选取P1粉末中A区域放大观察,发现颗粒表面紧实致密,深色相“Ⅰ”和浅色相“Ⅱ”分别为富Cr,Ni,Co的γ/γ′相和富Al的β相;同样地,放大观察P2粉末颗粒表面B区域,发现亮色相“Ⅲ”和暗色相“Ⅳ”的元素含量大致相同,均为富Cr,Ni,Co的γ/γ′相。

图1 两种粉末的表面形貌 (a)P1粉末;(b)P2粉末Fig.1 Surface morphologies of two types of powders (a)P1 powder;(b)P2 powder
图2为两种粉末的截面形貌及其元素分布情况。

图2 粉末的截面形貌及其元素分布 (a)P1粉末;(b)P2粉末Fig.2 Cross-section morphologies and element distributions of powders (a)P1 powder;(b)P2 powder
观察发现,基本元素在颗粒内分布都比较均匀,但是两种粉末中Al和Y元素在颗粒表面都有不同程度的富集,此外,Hf元素也在P1粉末颗粒表面微量聚集,其中以Al元素的富集最为显著。原因是:一方面,粉末在大气环境中与空气接触,优先生成Al,Y和Hf的氧化物,且Al等元素的氧化膜在粉体表面阻止了氧化反应的进一步进行,使得粉体表面的Al,Y和Hf含量高于粉末平均的含量;另一方面,由于各种元素在相同温度下的饱和蒸气压不同,Al元素不论在什么情况下都具有较大的饱和蒸气压,而真空熔炼系统的真空度约为10-3Pa,Al有向真空系统中挥发的动力,所以容易在颗粒表层富集。
对气雾化后室温下的两种粉末样品进行XRD分析,如图3所示。可知,P1粉末的XRD图谱中β相具有较强的衍射峰,γ/γ′相具有较低强度的衍射峰出现。而P2粉末的XRD图谱与掺杂改性粉末不同,仅含有γ/γ′相衍射峰。这是由于,掺杂改性的P1粉末中Ni,Co等元素的析出,使β相含量相对增加,γ/γ′相含量减少。
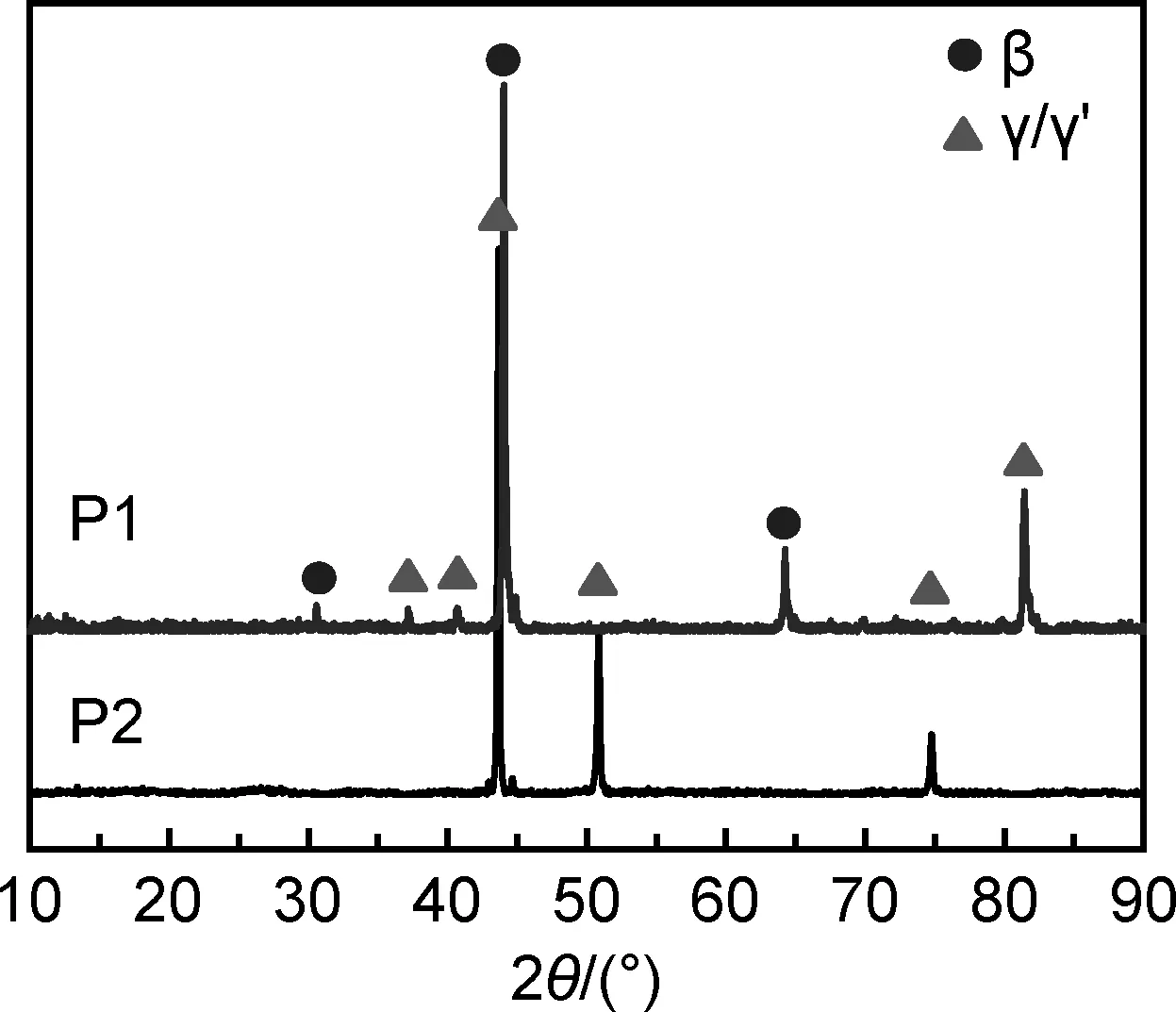
图3 室温下粉末XRD谱图Fig.3 XRD patterns of powders at room temperature
2.2 粉末1200 ℃等温氧化性能
为了阐明在1200 ℃下长时间氧化后粉末上形成的氧化层生长情况,分别研究24,48 h和72 h等温氧化后P1和P2粉末氧化层的微观组织结构,如图4,5所示。可以看出,不同时长的高温氧化后,粉末发生明显的结块和团聚,这是由于1200 ℃已经明显超过粉末的熔点,导致粉末发生结块。此外,可以发现高温氧化后,P1粉末表面形成许多微米颗粒,这些微米颗粒的尺寸和致密性随氧化时间的不同而有所差异。相应的放大图像显示,在氧化24 h后表面形成相对较大的氧化物,并且出现大量间隙和相对松散的结构。说明在氧化初期,P1粉末中的金属元素与空气中的氧气接触,迅速发生氧化反应,但氧化不充分,从而产生相对疏松的氧化层。随着氧化时间增加到48 h,P1粉末颗粒表面的氧化增强,氧化物完全生长,导致在表面生成相对均匀且较为致密的氧化铝膜。当氧化时长为72 h后,颗粒表面形成了更为致密的氧化铝膜,能够有效防止大气中的氧进入颗粒内部,从而抑制粉末的严重氧化。然而,P2粉末在氧化初期(24~48 h)时,粉末表面就已经出现大量不规则、棒状的尖晶石相以及较为致密的氧化铝膜。粉末中过早出现尖晶石相意味着Al的过度消耗,不利于延长涂层的寿命[22]。

图4 P1粉末在1200 ℃氧化不同时间的表面形貌 (a)24 h;(b)48 h;(c)72 hFig.4 Surface morphologies of P1 powders after oxidation at 1200 ℃ for different time (a)24 h;(b)48 h;(c)72 h

图5 P2粉末在1200 ℃氧化不同时间的表面形貌 (a)24 h;(b)48 h;(c)72 hFig.5 Surface morphologies of P2 powders after oxidation at 1200 ℃ for different time(a)24 h;(b)48 h;(c)72 h
对在1200 ℃下氧化24,48 h和72 h后的两种粉末进行XRD分析,如图6所示。首先,在不同氧化时间下氧化层的相组成与图4,5中的表面形貌都非常吻合。其次,P1粉末高温氧化后主要由Al2O3相、尖晶石相、β相和γ/γ′相构成,而P2粉末则由γ/γ′相、Al2O3
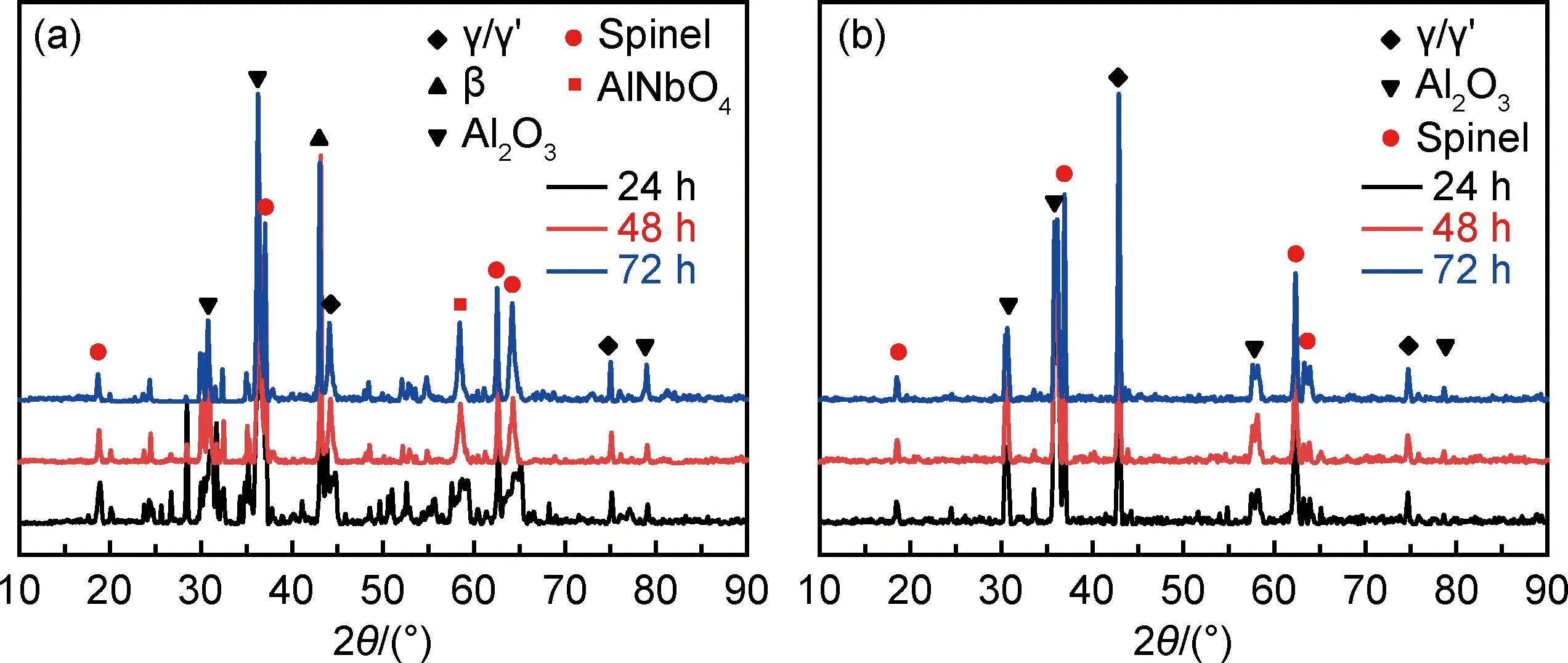
图6 1200 ℃下氧化不同时间的粉末XRD谱图 (a)P1粉末;(b)P2粉末Fig.6 XRD patterns of powders oxidized in different time at 1200 ℃ (a)P1 powder;(b)P2 powder
相和尖晶石相构成。最后,随着氧化时间的增加,P1粉末中Al2O3相的衍射峰强度增大,而P2粉末中对应的衍射峰变化并不显著,说明在1200 ℃下长时间氧化后,P1粉末表层形成了致密的氧化铝膜,并且粉末中的Al元素并未消耗殆尽,仍能为颗粒提供保护,而P2粉末只含有γ/γ′相,这是在P2粉末中常见的由于Al消耗导致的相转变,最终会造成Al消耗殆尽,并且不能支持连续的氧化铝膜继续形成[23],这也与图4中反映出的情况相似,说明掺杂改性后的粉末能够延缓Al的扩散与消耗。
图7为P1粉末在1200 ℃下氧化24,48 h和72 h后的截面形貌和元素分布。可知,氧化层在粉末表面均匀生长,并且随着氧化时间的增加,氧化层在不断变厚。通过放大图像可以发现,在氧化铝层中还存在着少量的尖晶石结构。图8为P2粉末在1200 ℃下氧化24,48 h和72 h后的截面形貌和元素分布。可以发现,P2粉末在高温氧化早期已经发生严重的烧结,颗粒结构基本被破坏,当氧化时长达到72 h之后,整个颗粒已经烧结变形,各元素发生严重的扩散,分布已毫无规律。
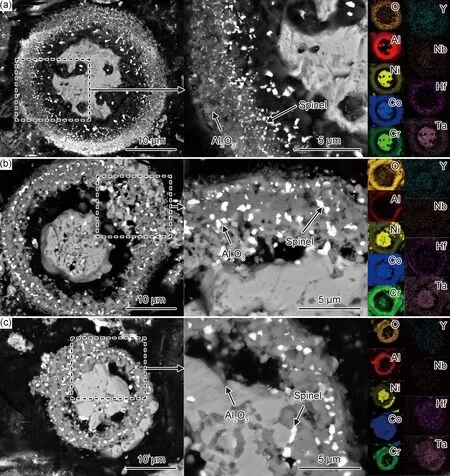
图7 P1粉末在1200 ℃下氧化不同时间的截面形貌及相应元素分布 (a)24 h;(b)48 h;(c)72 hFig.7 Cross-section morphologies of P1 powders with different oxidation time at 1200 ℃ and corresponding element distributions (a)24 h;(b)48 h;(c)72 h
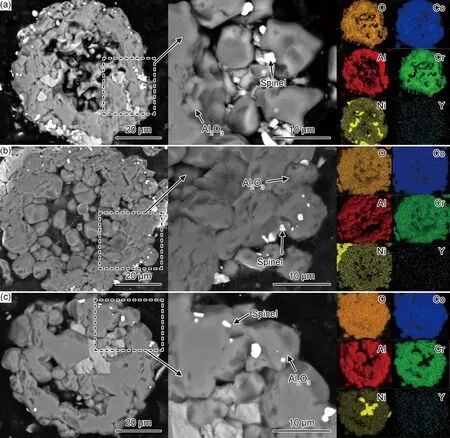
图8 P2粉末在1200 ℃下氧化不同时间的截面形貌及相应的元素分布 (a)24 h;(b)48 h;(c)72 hFig.8 Cross-section morphologies of P2 powders with different oxidation time at 1200 ℃ and corresponding elemental maps (a)24 h;(b)48 h;(c)72 h
随着粉末在1200 ℃下从24 h等温氧化至72 h,其微观结构发生明显的变化(图7,8)。首先,由于氧化层不断地增长,在颗粒外层形成较厚的氧化铝层。其次,由于Al是β相稳定剂,结合图6可以发现,P1粉末在72 h后仍有一部分β相存在,说明掺杂元素能够有效减缓Al在高温氧化中的消耗,而P2粉末在高温氧化72 h后,Al消耗很快,因此在粉末中只能发现γ/γ′相。
根据氧化物生成反应标准吉布斯自由能的相关经验方程,计算粉末中各个元素生成氧化物的反应标准吉布斯自由能(ΔG)[24],结果列于表2。基于金属热力学和动力学,较小的吉布斯自由能表示较为容易与氧发生氧化反应。粉末中的所有元素都可以在上述等温条件下被氧化,同时,涂层中氧化物的形成速度也高度依赖于各种元素的含量,即元素Nb(4%),Hf(4%),Ta(3%)和Y(<1%)的含量远小于Al元素(12%)。此外,由于Al元素较高的含量和扩散系数以及较低的ΔG值,更容易聚集在涂层表面并与空气中的氧气发生反应。与此同时,γ-(Ni,Co)基体晶粒在氧化过程中被细化,形成新的晶界,为Al的转移提供更方便的路径,大量的Al会在热处理时迅速滞留在涂层表面。所以,致密的氧化铝薄膜有助于提高金属基涂层的高温抗氧化性和耐热腐蚀性。
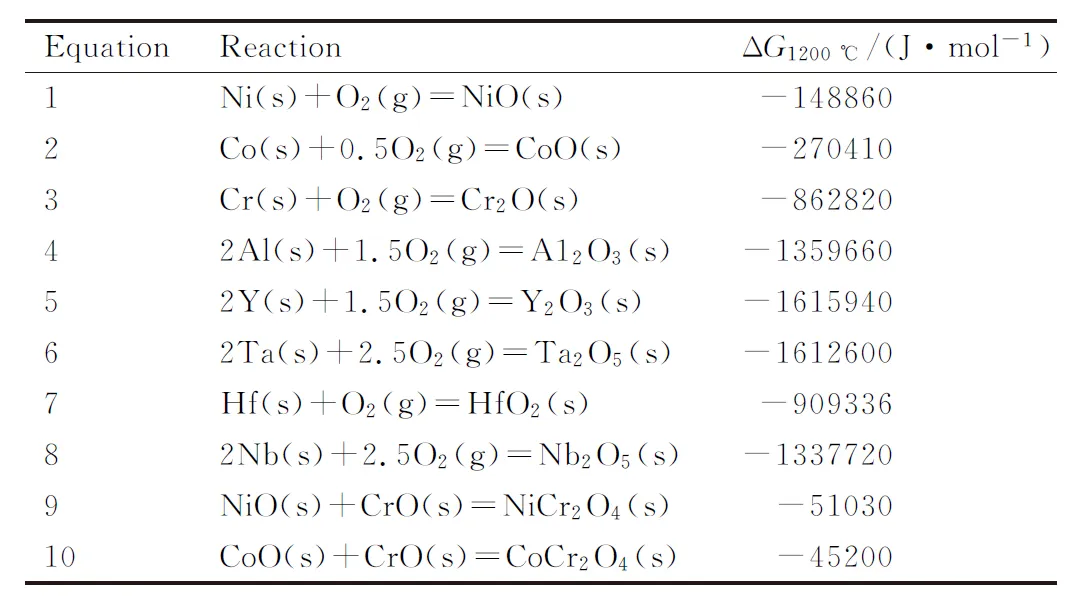
表2 1200 ℃下可能生成氧化物的反应标准吉布斯自由能Table 2 Standard Gibbs free energy of reactions that may generate oxides at 1200 ℃
尽管粉末在长时间氧化后微观结构发生改变,但Al2O3层的持续生长并未受到影响。根据Al2O3选择性氧化的经典理论,一旦在粉末表面形成连续的Al2O3氧化层(图7,8),由于界面处的氧分压显著低于氧化层表面的氧分压,在氧化层/颗粒内部界面形成Al2O3所需的Al浓度将显著降低。同时,由于Nb,Hf和Ta等元素的加入,能够有效减少Al的消耗,确保了在长时间氧化过程中氧化层/颗粒内部界面的界面稳定性。因此,P1粉末在长时间高温氧化后,仍然可以保持独有的Al2O3结构,并且还保留有β相,足以支持后续Al2O3层的形成。
2.3 粉末1200 ℃等温氧化行为对比
图9为1200 ℃时两种粉末的氧化动力学曲线。可见,P1粉末在氧化的前25 h,氧化动力学曲线呈现快速增长的趋势,说明颗粒表面未形成完整致密的氧化膜,在高温下发生了剧烈的氧化反应,质量增长较快。在25 h之后,曲线趋于平缓,这可能是由于颗粒表面形成了较为连续且致密的氧化膜,有效阻止氧进入颗粒中,从而减缓颗粒表面的氧化反应。而P2粉末在氧化的前50 h,氧化动力学曲线呈现快速增长的趋势,并且曲线有一定程度的波动,在50 h之后,曲线趋于平缓。粉末的氧化增重曲线呈现先快速上升后平稳波动的趋势,这可能是因为,随着氧化反应的进行,初期生成的氧化膜并不连续且结构松散,构成氧进入涂层内部的新通道,加剧涂层内其他元素和氧的反应。当其他元素与氧形成稳定氧化产物的时候,粉末的氧化增重又得以趋稳。
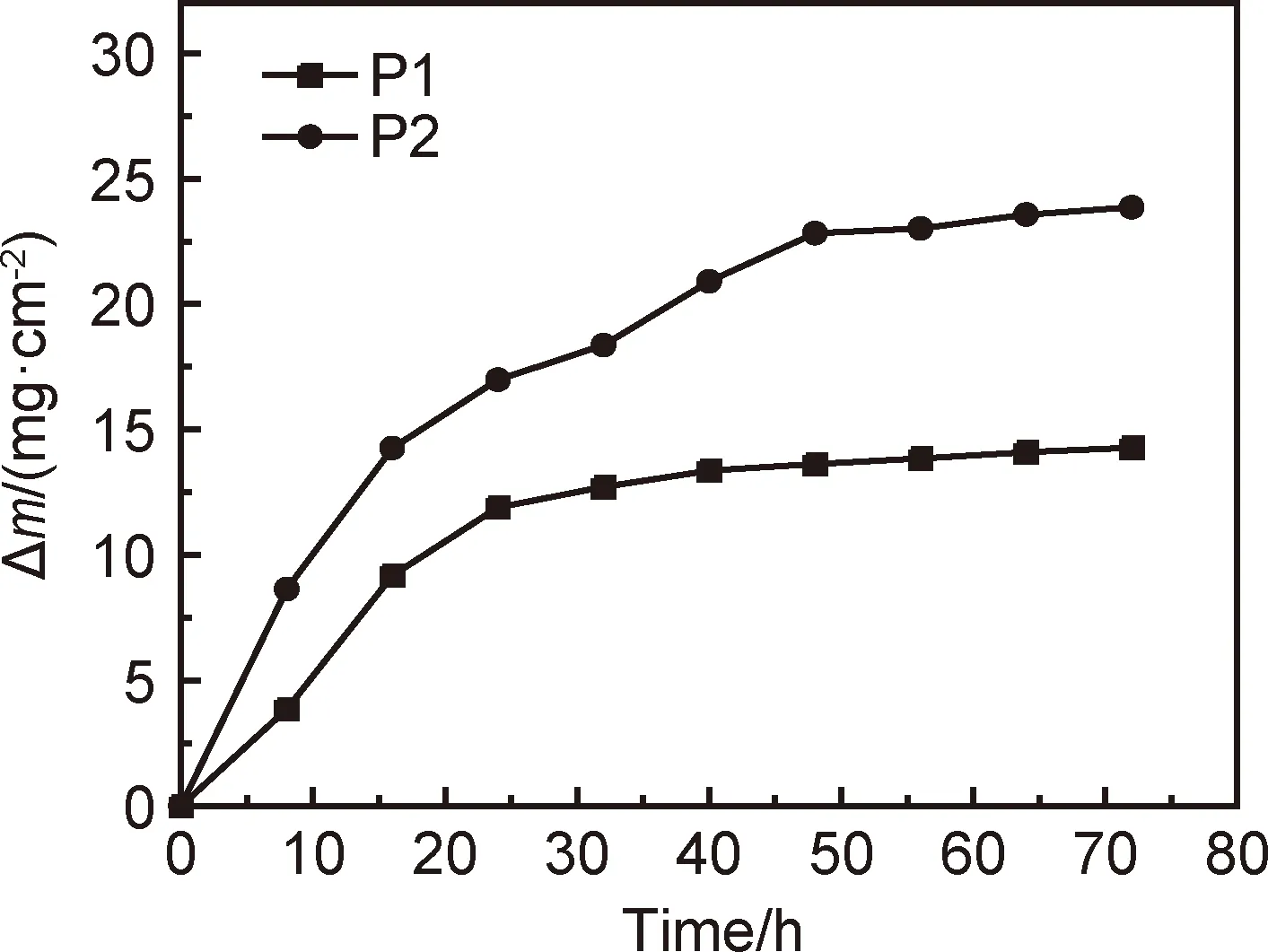
图9 1200 ℃时粉末的氧化动力学曲线Fig.9 Oxidation kinetics curves of powders at 1200 ℃
采用Origin软件依据最小二乘法对图9中粉末的质量变化进行拟合,并求出氧化动力学曲线方程,结果如表3所示。在1200 ℃时,P1和P2粉末的氧化动力学方程中的二项式系数分别为-0.0049和-0.0063,氧化速率降低了22%,说明P1粉末的氧化速率明显低于P2粉末。所以,与P2粉末相比,P1粉末在1200 ℃时表现出优异的抗氧化性能和较低的氧化速率。分析氧化动力学曲线可知,两种不同粉末在1200 ℃下72 h氧化增重曲线总体变化趋势十分接近,氧化初期,氧化膜的形成过程主要以氧在颗粒表面发生氧化反应为主,氧化物优先在颗粒表面的缺陷处形成,此阶段氧化膜生长迅速,但是结构疏松,氧化速率受界面反应控制。随着氧化时长的增加,氧化曲线逐渐平稳,氧化速率降低,氧化膜连续且致密,其保护性增强。不同的是,P2粉末虽然也经历以上阶段,但是发生了较为严重的烧结,颗粒完整性遭到破坏,并且经历的氧化初期时间也较长,不能够有效地对粉末内部结构进行防护,这更加说明P1粉末具有较为优异的高温抗氧化性。

表3 不同粉末拟合的氧化动力学曲线方程Table 3 Oxidation kinetics curve equations fitted by different powders
熵工程是合金领域新提出的策略,已成功应用于铁基、铝基、镍基合金体系中。原则上,给定成分的总混合熵ΔSmix的主要组成部分是构形熵ΔSconf。ΔSconf是描述材料中原子排列的无序程度,是固体材料领域的熵理论应用,如式(1)所示。计算可知,P1粉末的ΔSconf为1.55R,高于目前分类的高熵合金(>1.5R),从而使粉末有类似于高熵合金的一些性能。如在高温下,这种高熵效应会导致Al的缓慢扩散效应,则将在一定程度上延缓Al从颗粒内部向外扩散的速度。因此,P1粉末中Al扩散缓慢,能够进一步降低粉末的氧化速率。
ΔSconf=-RXiln(Xi)
(1)
式中:R为气体常数,约为8.314 J·mol-1·K-1;Xi为元素i的原子分数。
3 结论
(1)P1和P2粉末均显示出较好的球形度,元素分布均匀。P1粉末主要由β相和γ/γ′相组成,而P2粉末由γ/γ′相组成。
(2)两种粉末1200 ℃等温氧化72 h后,P1粉末表层形成致密的氧化铝膜,粉末中的Al元素并未消耗殆尽,仍然保持独有的Al2O3结构;P2粉末由于Al快速消耗,导致γ/γ′相到尖晶石相的相转变,颗粒已经烧结变形。
(3)改性元素的加入,促进P1粉末致密氧化膜的形成,延缓Al的扩散和消耗;P2粉末发生较为严重的烧结,经历的氧化初期时间较长,加速Al的扩散与消耗。P1粉末具有更佳的高温抗氧化性和抗高温烧结性能。

