单颗粒电感耦合等离子体质谱法对地表水中纳米银的检测
曾庆招
(广东省矿产应用研究所(自然资源部放射性与稀有稀散矿产重点实验室)广东韶关512026)
为了充分了解纳米粒子(NPs)的性质和功能,有必要对其进行适当的表征和量化。含有NPs的物体或样品可以从构成NPs的元素或化合物的质量浓度、颗粒数浓度、粒度、粒度分布、表面电荷、表面积、形状、团聚、结构和组成的角度来表征[1]。ICP-MS是一种元素分析方法,自20世纪80年代以来广泛应用于分析实验中。使用基于高时间分辨率信号采集的单粒子分析(SP-ICP-MS),在其用于NPs表征方面取得了革命性进展[2]。如果分析充分稀释的NPs水分散体,NPs单独进入光谱仪,并且(在最佳条件下)每个NP在等离子体中产生一个小离子云,可作为持续约0.5ms~0.7ms的峰值被检测到。为了获得准确的结果,有必要协调分析水分散体中NPs数量浓度和基本测量步骤的持续时间[3]。这种方法的主要缺点是延长的停留时间增加了两个或更多NPs在一个停留时间窗口内同时发生的可能性。可能会得到有偏差的结果。NPs数量浓度被低估,而表观粒径分布偏移到较大的值。分析结果质量与进入质谱仪NPs的数量密切相关。检测到的NPs数量少,导致对其数量浓度和大小分布的统计估计不够有效[4]。同时过多的检测到的NPs可能会由于其单个信号的重叠而扭曲结果。估计NP大小的准确性也受到分析灵敏度影响。由于NPs的直径与峰面积立方根有关,因此高灵敏度是其准确估计的先决条件[5]。
本文重点描述Ag-NPs直径和Ag-NPs数浓度对传输效率和测量灵敏度的影响。其结果可能有助于开发更准确的SP-ICP-MS应用,因为传输效率和灵敏度在可靠的NP表征中起着至关重要的作用。
1 材料与方法
1.1 试剂和样品
实验采用直径10nm、20nm、40nm、60nm和100nm的Ag纳米粒子标准品,Ag纳米粒子总浓度20mg/L。以柠檬酸钠和氢氧化钠为原料制备pH9.15缓冲溶液。用硝酸对样品进行分解以测定总Ag。将Ag和Rh原液稀释1000±2mg/L,制得以添加Rh为内标的Ag校准液。添加明胶用于稳定NPs。所有溶液在milliq超纯水设备中使用水脱盐制备。所有试剂均为分析级。
2020年1月采集广东某地地表水样本(温度14℃~16℃,pH值6)。将样品放入塑料容器中,并立即加入2.5mL%(w/w)明胶溶液。所有样品在随后10小时内进行分析。分析前用Ag-NP标准品加标,得到浓度1.02×105mg/L溶液。
1.2 仪器与设备
所有测量均使用配备高效等离子体炬的NexION 350d ICP-MS光谱仪进行。样品导入系统由内置的蠕动泵、直径0.38mmPVC管、聚四氟乙烯同心喷雾器和玻璃旋风(100 mL)喷雾室组成。数据评价采用Syngistix 1.1软件。样品分解在Speed Wave 4微波分解装置中进行。采用NanoSight NS300对60nm Ag-NP标准品的颗粒数浓度测定进行纳米颗粒跟踪分析。使用EFTEM Jeol 2200 FS电子显微镜获得Ag-NP标准品TEM图像。使用ImageJ 1.50i软件进行图像评估。
1.3 方法
用适当的稀释液(水、缓冲液或明胶溶液)稀释制备所需数量浓度的Ag-NPs水分散体。在使用前,所有的溶液都在超声波浴中进行彻底的人工混合和均质。
采用SP-IICP-MS法测定NPs标准分散体中总Ag浓度,条件见表1。取0.1 mL Ag-NPs标准品,用3mL浓HNO3和1mL去离子水在微波分解装置中分解20min,移入100mL聚丙烯容瓶中,加入铑作为内标,终浓度20ng/mL Rh。通过稀释Ag和Rh原液,制备浓度分别为0和20 ng/mL Ag以及20ng/mL Rh的校准液。

表1 SP-IICP-MS测量条件参数
样品中Ag-NPs分析包括以下步骤:(1)SP-ICP-MS测定已知数量浓度的充分稀释Ag-NPs标准品;(2)计算观测信号脉冲频率f估计的传输效率ηtrans;(3)用SP-ICP-MS对适当稀释的未知样品进行分析和数据采集;(4)评价Ag-NPs浓度,利用仪器响应-质量浓度校准、ηtrans估算值评价Ag-NPs粒径分布。
2 结果与分析
2.1 Ag-NPs标准品的表征
供应商给出的Ag-NPs在所有标准分散体中总浓度均为20mg/L。10nm、20nm、40nm和100nm Ag-NPs标准品测定总浓度略低(18.7mg/L~19.6mg/L),60nm Ag-NPs标准的测量浓度12.3mg/L(表2),与标准品相差很大。另一方面,TEM测定Ag-NPs尺寸(图1)与供应商给出的标准值吻合很好。

图1 Ag-NPs标准品透射电子显微图:(a)20nm,(b)40nm,(c)60nm,(d)100nm。

表2 供应商给出的Ag-NPs标准浓度和实际测量浓度
2.2 Ag-NPs数目浓度影响
从图2看出,只有在NPs浓度较低情况下(低于5×105/mL),对传输效率的估算接近其真实值。在银纳米粒子浓度较高区域,传输效率估算值和测量值明显下降,这可能是因为形成完全或部分重叠的NPs簇的NPs彼此之间没有区别,并且仅被计数为一个粒子。结果表明,在高数字浓度区域,传输效率显著降低。同时,它们与实验测量结果相差较大。由于Ag-NPs标准中Ag离子的存在,可以预期会有一个小的增加,但在这种情况下,趋势应该是线性的,这与测量结果不符(图2)。因此,0.5×105~5×105/mL数量浓度是一个合理的范围,以确保准确的测量结果。

图2 银纳米粒子数量浓度对传输效率的影响
2.3 Ag-NPs尺寸影响
所有测量均使用Ag-NPs的水分散体进行。从图3可以看到,对于较低尺寸(小于40nm)的纳米粒子,传输效率是一致的。然而,10nm Ag和20nm Ag纳米粒子的传输效率很低,这是由于系统对低信号强度的错误评估造成的,与这些Ag-NPs对应的大部分峰几乎消失在周围背景中,计算的运输效率被低估了。在40nm和100nm银纳米粒子中,SP-ICP-MS测量值与估算值相近,结果较准确。
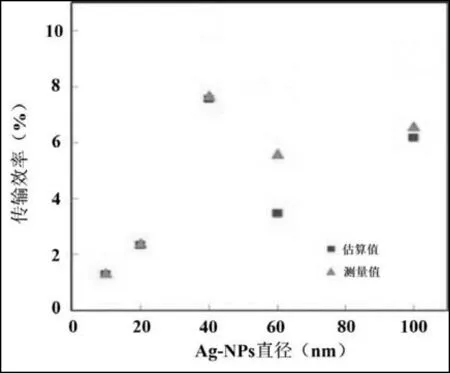
图3 银纳米粒子尺寸对传输效率的影响
2.4 方法验证
NPs数浓度检出限可由NPs统计行为来估算,本文检出限对应的NPs的数量浓度为97/mL。定量限被定义为“可在可接受的重复性、精度和真实性水平上确定的最低测量浓度”。本文测量条件对应的定量限数量浓度1950/mL。尺寸检出限计算基于Ag-NPs切片数浓度影响中提到的5σ算法。该参数计算为平均背景强度加上5倍其标准差,并转换为NPs直径。因此,尺寸检测限是具体情况,取决于样品中溶解银的浓度。例如,0.05%明胶溶液在脱盐水中尺寸检测限为15nm。从两组结果中计算重复性,每组结果包含10个重复分析,间隔两周测量。采用单因素方差分析(ANOVA)计算。测定银NPs数浓度相对重复性为1.3%,测定银纳米粒直径的相对重复性为0.4%。为了量化实际样品可能的基质效应,在河流水样中加入Ag-NPs标准品。便于区分加Ag-NPs和最初存在的Ag-NPs。本研究选用了100nm Ag-NPs标准品。结果表明基质对数目浓度影响不大,回收率达到98%。表3。

表3 SP-ICP-MS检测Ag-NPs的方法验证
2.5 真实样本分析
优化后SP-ICP-MS方法应用于广东省某地不同地点收集的地表水样本。测定各样品中银总浓度和银NPs数目浓度(表4)。结果表明,研究区域地表水中Ag-NPs浓度范围5.0ng/L~21.7ng/L,数量浓度最大值1670±250/mL,最小值340±140/mL,粒径分布平均值42~72nm。

表4 广东某地不同地点地表水中Ag-NPs的分析
3 结论
本文建立了单颗粒电感耦合等离子体质谱法测定Ag纳米粒子的方法。结果表明,在高数字浓度区域,传输效率显著降低,与实验测量结果相差较大,比较合理的数量浓度范围为0.5×105~5×105/mL,以确保准确的测量结果。在40nm和100 nm银纳米粒子中,SP-ICP-MS的测量值与估算值相近,结果较准确。方法验证得到以下参数:检测限数量浓度97/mL,定量限数量浓度1950/mL,尺寸检测限15nm,重复性1.3%,回收率达到98%。经验证后,将该方法应用于广东省某地地表水Ag-NPs测定。发现Ag-NPs粒径为42nm~72nm,数量浓度最大值1670±250/mL,最小值340±140/mL。

