不同剂量汽化过氧化氢和消毒时间对A2生物安全柜消毒效果的研究
吴大伟,何振健,程双来,雷迅
(1. 中山大学公共卫生学院,广东 广州 510080;2. 广州美岸生物科技有限公司,广东 广州 510080)
0 引言
生物安全柜是开展病原微生物实验必不可少的设备,它能有效降低生物实验中病原微生物等产生的有害气溶胶对实验操作人员的危害,同时也能降低实验样品的污染,起到隔离的作用。卫生行业标准WS 233—2017《病原微生物实验室生物安全通用准则》[1]对病原微生物生物安全实验室配置生物安全柜有明确要求,通常生物安全柜虽然本身配置有紫外消毒和高效过滤功能。但经过长时间地开展病原微生物实验,其生物安全风险依然存在。因此,我国的GB 19489—2008《实验室生物安全通用要求》中第6.4.16条和《实验室生物安全认可准则对关键防护设备评价的应用说明》中第5.7.3条均指出在安装和更换HEPA前必须进行彻底消毒,并对其消毒效果进行评价[2-4]。另外生物安全柜每年的性能检测前也必须预先进行消毒,以降低检测人员的生物安全风险。因此定期对生物安全柜进行全面消毒已经成为实验室生物安全管理的常规工作,从而最大程度降低生物安全隐患。由于采用汽化过氧化氢对生物安全柜的消毒具有诸多优势:第一,对生物安全级别较高的密闭场所空气和物体表面联合消毒取得较好的效果,在高级别生物安全实验室同样具有较可靠的消毒效果;第二,汽化过氧化氢的分解产物为水和氧气,基本无残留,使用相对安全[5]。因此目前普遍采用汽化过氧化氢对生物安全柜进行消毒。本文探索在特定过氧化氢汽化设备的工作下,不同剂量和消毒时间对A2二级生物安全柜的消毒效果的研究,为生物安全柜的规范消毒提供参考。
1 材料与方法
1.1 试验仪器材料
(1)汽化过氧化氢发生装置:MiniX过氧化氢消毒机,由广州美岸生物科技有限公司生产。
(2)过氧化氢试剂:食品用过氧化氢消毒液,型号:SX-XD-Ⅱ,浓度:35%,由荆州双雄化工科技有限公司生产。
(3)生物指示剂:进口嗜热脂肪芽孢杆菌(Bt93 Biological indicator, geobacillus stearothermophilus ATCC7953)。
(4)过氧化氢浓度检测仪:MiniX过氧化氢消毒机集成检测仪,由广州美岸生物科技有限公司生产。
(5)嗜热芽孢脂肪杆菌培养基:胰酪大豆胨液体培养基,规格:9 mL/管,由广州市迪景微生物科技有限公司生产。
(6)A2生物安全柜:选用Thermo Scientific公司生产的TELSTAR BIO II Advance 4生物安全柜。主体外部尺寸(长×宽×高):1 354 mm×759 mm×1 260 mm。
(7)封装材料:PVC塑料膜。
(8)湿度计:MiniX过氧化氢消毒机集成湿度计,由广州美岸生物科技有限公司生产。
(9)培养箱:ASH-269型生化培养箱,由上海安弋仪器有限公司生产。
1.2 研究方法
1.2.1 剂量设计
(1)过氧化氢剂量设计
根据预实验结果设计30 g、40 g、50 g三个剂量组和一个空白对照组,选取15个次A2生物安全柜,随机分为三个组,每组5个,分别对应三个剂量组,同时设置空白对照组和阳性对照组。空白对照组采用无菌蒸馏水代替生物指示剂,阳性对照组则是生物指示剂不用消毒剂进行消毒。
(2)时间剂量设计
分别对各个过氧化氢剂量组在0.5 h、1.0 h、1.5 h和2.0 h的消毒时长,检查消毒效果,同时在这些时间点记录环境温度和环境湿度。
1.2.2 消毒前准备
(1)生物安全柜准备
用PVC塑料膜对生物安全柜进行密封,如图1所示,并将其与汽化过氧化氢发生器通过管路连接。

图1 生物安全柜用用PVC塑料膜密封后的状态图
(2)温度测量准备
用动态温度计记录各个时间点消毒空间的环境温度。
(3)相对湿度测量准备
以A2生物安全柜放置湿度传感器作为检测单元,实时记录各个时间点A2生物安全柜内环境湿度。
(4)过氧化氢浓度测量准备
以A2生物安全柜集成安装的过氧化氢气体浓度检测传感器作为检测单元,实时记录A2生物安全柜内各时间点过氧化氢浓度值。
(5)设置生物指示剂
分别在各个A2生物安全柜的操作台面的左边、中间、右边各放置4片生物指示剂,同时在各个A2生物安全柜顶部的左边、中间和右边各放置4片生物指示剂,如图2所示。

图2 生物指示剂(BI)在生物安全柜的各个监测位置
1.2.3 消毒过程
在消毒前准备工作完成后,分别往各组的汽化设备加入30 g、40 g和50 g过氧化氢溶液,并启动汽化过氧化氢消毒装置,按设定条件完成消毒运行程序,并记录消毒时间,在0.5 h、1.0 h、1.5 h和2.0 h取出一片生物指示剂进行培养,并记录消毒空间的温度、湿度和过氧化氢的浓度。
1.2.4 嗜热脂肪芽孢杆菌培养
从放置在消毒空间中取出生物指示剂,并接种于相应培养基中,嗜热脂肪芽孢杆菌置55±1 ℃恒温培养箱内培养7 d±2 h。
1.2.5 消毒效果判定
结果判定为合格的标准为同时具备以下三个条件:(1)试验组培养为无菌生长;(2)阴性对照组培养为无菌生长;(3)阳性对照组培养为有菌生长。
2 结论
实验结果如下:消毒剂剂量为30 g的过氧化氢汽化后的生物指示剂杀灭情况如表1所示,消毒剂剂量为40 g的过氧化氢汽化后的生物指示剂杀灭情况如表2所示,消毒剂剂量为50 g的过氧化氢汽化后的生物指示剂杀灭情况如表3所示。消毒环境温度为:28~31 ℃,消毒环境湿度为:52%~95%,阴性对照和阳性对照均合格。
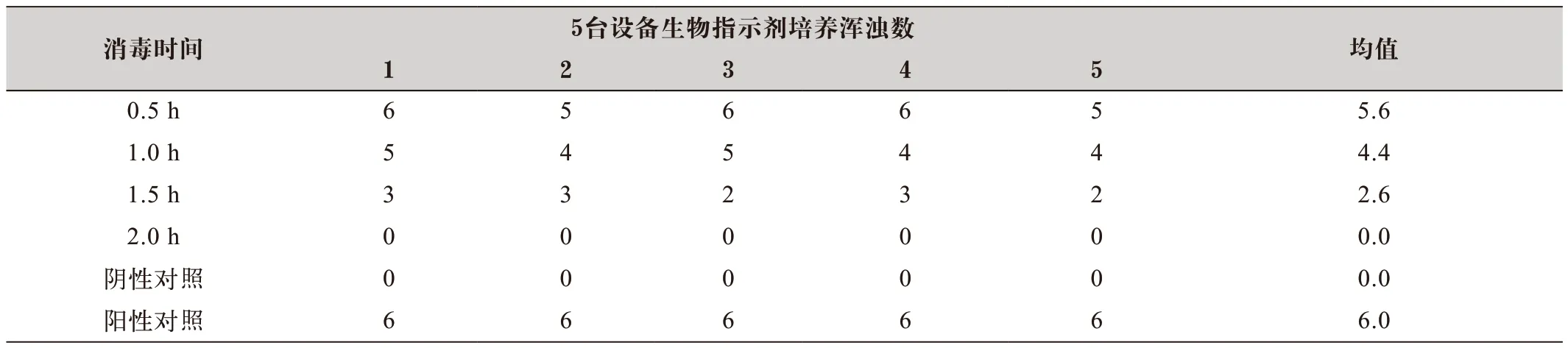
表1 消毒剂剂量为30 g的过氧化氢汽化消毒后生物指示剂培养浑浊数
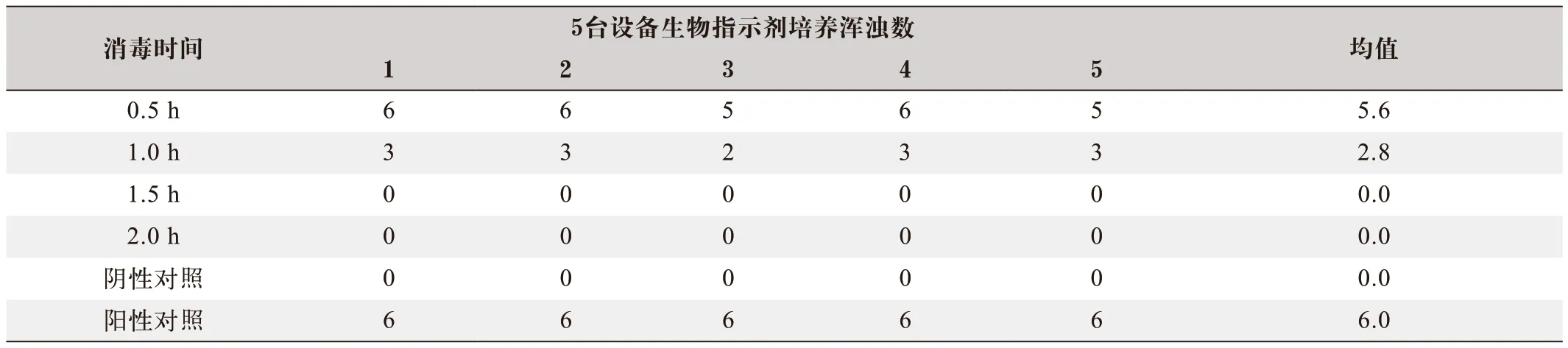
表2 消毒剂剂量为40 g的过氧化氢汽化消毒后生物指示剂培养浑浊数
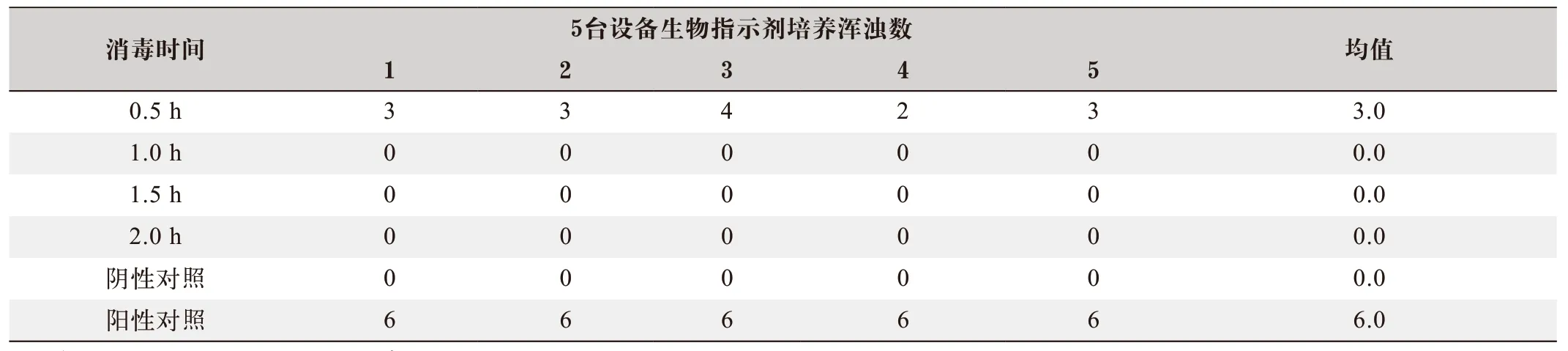
表3 消毒剂剂量为50 g的过氧化氢汽化消毒后生物指示剂培养浑浊数
3 结语
生物安全柜是一种有效的隔离安全屏障设备,对保护实验操作人员生命安全和保证实验质量起到重要作用,随着生物安全柜在各个应用领域的使用日益增加[8],人们对生物安全柜本身的消毒也越来越重视和规范。根据《中国药典》和《美国药典》的定义,气相灭菌法是以气态形式扩散,以冷凝态液体接触微生物进行快速彻底灭菌的方法。目前气相灭菌法所用的消毒剂包括过氧化氢(HP)、环氧乙烷(EO)、臭氧(O3)、二氧化氯(ClO2)等。然而,有些消毒剂在使用中存在一些缺陷:或具有毒性/致癌性、对环境不友好(如甲醛),或对仪器设备、彩钢板及环氧地面具有一定的腐蚀性(如过氧乙酸和高浓度过氧化氢等),或存在易燃、易爆等安全隐患(如环氧乙烷和二氧化氯等)[6]。其中,汽化过氧化氢(VHP)则相对具有较多种优点,包括在功效方面:灭菌有效性更好、扩散性更好、应用范围更广、“穿透性”更好等;在安全方面:几乎无毒,可分解为水和二氧化碳;在残留物方面:自动分解为水和二氧化碳,无明显残留[7]。因此汽化过氧化氢(VHP)已成为生物安全柜消毒的首选消毒剂[8]。
汽化过氧化氢(VHP)消毒法主要用到的设备是汽化过氧化氢发生装置,以前大多为进口设备,目前国产的设备在性能上大大提高,而且价格合理,已经占据越来越大的市场份额。本研究采用国产的MiniX过氧化氢消毒机进行消毒,并使用理想的进口的生物指示剂作为消毒效果监测指标。在消毒实践中,往往需要在消毒剂使用剂量和消毒时间寻找一组理想的数据,如果使用剂量和消毒时间不够,无法杀灭生物指示剂,则必须重复消毒直到过关为止,这将造成包括时间、试剂和人工等的浪费。但如果使用过量的消毒剂剂量和消毒时间,则会损害仪器设备,所以寻找一组合适的剂量和消毒时间非常重要。本研究发现,分别使用浓度为35%的过氧化氢消毒剂溶液进行汽化[9],在消毒剂使用量为30 g这个剂量下,消毒时间为2.0 h,能有效杀灭嗜热脂肪芽孢杆菌;而在使用量为40 g时,则需要耗时1.5 h才能有效杀灭嗜热脂肪芽孢杆菌;如果使用剂量达到50 g时,则消毒时间最小,只需1.0 h即可有效消毒。由于过氧化氢具有强的氧化性,特别是在高浓度的情况,对设备具有一定的腐蚀性,因此,可以使用30 g,消毒耗时2.0 h,作为A2型生物安全柜的常规消毒剂量,但如果要减少消毒时间,则选用40 g,耗时1.5 h进行消毒,至于高达50 g剂量组则不建议采用。
值得进一步思考的几个指标:第一个指标是浓度。目前使用剂量是以35%的过氧化氢消毒剂溶液计算,分别以30 g、40 g和50 g进行实验,如果按照目前的消毒空间换算,消毒空间为生物安全柜主体体积和支架体积之和,主体外部尺寸(长×宽×高):1 354 mm×759 mm×1 260 mm,主体体积约为1.3 m3,支架高度为740 mm,支架部分的尺寸为1 354 mm×759 mm×740 mm,约0.76 m3,即消毒空间的总体积为2.06 m3。因此本实验过氧化氢液体全部汽化后,理论上汽化过氧化氢的使用剂量分别是30 g、40 g和50 g,换算成浓度依次是5.10 g/m3、6.80 g/m3和8.50 g/m3。由于在消毒过程中,部分过氧化氢将会分解成水和氧气[10],以及消毒空间各种其他影响因素,导致实际的浓度将会低于理论浓度。消毒空间的汽化过氧化氢的浓度是如何变化的,浓度是否从0开始升高,然后达到饱和状态后维持在一定浓度水平,最后降解再慢慢降低下来,这需要进一步研究。第二个指标是闪蒸温度。闪蒸温度是汽化设备的一个性能指标,闪蒸温度能使液体过氧化氢迅速汽化成气溶胶状态的过氧化氢,使消毒空间的汽化过氧化氢达到饱和状态并形成有效的消杀浓度,同时能尽最大程度减少过氧化氢分解,闪蒸温度的持续程度将会导致消毒空间温度的升高,这需要进行控制。第三个指标是环境温度。环境温度必须控制在相对较低的状态,才有利于汽化过氧化氢的微凝结,从而实现理想的消毒效果。第四个指标是环境相对湿度,环境相对湿度是消毒效果的一个重要影响因素。以上四个指标将在后续的研究中进行深入探索。

