QuEChERS/超高效液相色谱-串联质谱法测定禽蛋中90种禁用药物残留
陈 容,刘育形,王泽林,李澍才,张 晶*,邵 兵
(1.北京市疾病预防控制中心 食物中毒诊断溯源技术北京市重点实验室,北京 100013;2.四川省食品检验研究院,四川 成都 611731)
兽药是畜禽养殖过程中的关键投入品,在保障动物健康和确保食品产量方面发挥着重要作用。由于兽药的不规范使用、滥用或违禁使用,造成残留超标或违禁药物检出,可能会导致急性中毒、过敏反应、细菌耐药性等不良后果,不仅给消费者带来明显或潜在的健康威胁,而且会损害我国相关食品在国际贸易中的声誉,造成经济损失。因此,兽药残留一直是动物性食品安全的重点关注领域。GB 31650-2019《食品安全国家标准 食品中兽药最大残留限量》[1]等标准和法规规定了肉、蛋、奶等多种动物性食品的兽药残留限量,其中蛋类涉及的禁用药物种类最多,包括甲硝唑、氯丙嗪等不得检出的9种以及磺胺类、青霉素类、四环素类等产蛋期禁用的34 种;在农业农村部第250 号公告[2]中,禁用药物包括β-激动剂、万古霉素类及部分农药等33类。为保障消费者的健康,确保禽蛋产品质量安全,建立快捷、高通量、准确可靠的禁用药物同时分析方法十分必要。
目前关于动物性食品中药物残留的分析方法主要有酶联免疫法[3]、气相色谱法[4]、高效液相色谱法[5]以及液相色谱-串联质谱法(LC-MS/MS)[6-8]。LC-MS/MS 法具有高选择性、高灵敏度、低检出限的特点,是动物性食品药物残留分析的首选方法[9-10]。动物性食品药物残留分析应用较为广泛的前处理方法主要包括固相萃取法[11-13]和QuEChERS法[14-15]。前者需经过富集、分离、净化等步骤,耗时较长;固相萃取柱多是基于极性分离和离子交换分离原理,因此不适用于化合物数量多、性质差异大的分析场景;且固相萃取柱成本较高。QuEChERS 法具有快速、低成本、操作简单等优点,被广泛应用于动物性食品的药物残留分析中,可实现多种性质差异较大的化合物的高通量分析。关于药物残留分析的标准与研究主要针对一类药物或几类性质相似的药物,针对禽蛋中违禁药物的检测方法鲜有报道[16-18]。本文建立了禽蛋中包括磺胺类、β-激动剂类、四环素类、万古霉素类等90种违禁药物的QuEChERS/超高效液相色谱-三重四极杆串联质谱高通量分析方法,实现禽蛋中多种违禁药物的同时分析,为禽蛋产品的质量安全保障提供了技术支持。
1 实验部分
1.1 材料与试剂
实验样品购于当地超市;90 种标准品和29 种内标(纯度>90%)购自加拿大TRC 公司。十八烷基键合硅胶吸附材料(C18)、QuEChERS Z-sep/C18(120 mg Z-Sep+,300 mg Discovery DSC-18)净化管、N-丙基乙二胺键合固相吸附材料(PSA)购自美国Supelco 公司;多壁碳纳米管(MWNTs,8~15 nm)购自南京先丰纳米材料科技有限公司;QuEChERS dSPE EMR-lipid净化填料购自美国安捷伦公司。
除特殊说明外,所用试剂均为分析纯。甲醇(LC-MS 级)、乙腈和超纯水均购自迪马科技有限公司;甲酸(纯度>99%)购自美国Acros 公司;乙二胺四乙酸二钠盐(Na2EDTA)购于国药集团化学试剂有限公司;氟化铵(NH4F,纯度>99.99%)购自上海阿拉丁试剂有限公司;实验用水由Milli-Q 超纯水净化处理系统制备。
1.2 仪器与设备
ACQUITYTM超高效液相色谱仪-Xevo®TQ-XS 串联质谱仪(美国Waters 公司);Allegra X-30R Centrifuge 冷冻离心机(美国Beckman 公司);Vortex-Genie 2涡旋振荡器(美国Scientific Industries 公司);Milli-Q超纯水器(美国Millipore公司)。
1.3 标准溶液配制
分别称取适量标准品及其内标于10 mL 容量瓶中,用含0.1%甲酸的甲醇溶液配制成1 000 mg/L 的混合标准储备液,-20 ℃保存;用甲醇将90种标准储备液配制成1 mg/L 的混合标准中间液,将29种内标储备液配制成1 mg/L的混合内标中间液,再用10%甲醇水稀释至所需浓度。
1.4 样品前处理
准确称取鸡蛋样品2 g(精确至0.01 g)于50 mL 聚丙烯离心管中,分别加入50 µL 100 µg/L 的混合标准溶液和混合内标溶液,加入10 mL 0.2%甲酸-乙腈水溶液(3∶1,体积比)作为提取溶剂,涡旋30 s后加入25 mg乙二胺四乙酸二钠盐,涡旋15 s,超声提取30 min,4 ℃下10 000 r/min 离心10 min。准确称取50 mg(精确至0.0001 g)QuEChERS dSPE EMR-lipid 净化填料于2 mL 聚丙烯离心管中,加入1 mL上述上清液,涡旋1 min,4 ℃下14 000 r/min离心5 min,将上清液转至进样瓶中待测。
1.5 色谱条件
色谱柱:ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 µm);柱温:40 ℃;进样量:5 µL;流速:0.35 mL/min。正离子模式流动相:A 相为0.1%甲酸水,B 相为甲醇;梯度洗脱程序:0~1 min,3%~10% B;1~2.5 min,10%~15% B;2.5~5 min,15% B;5~7 min,15%~30% B;7~10.5 min,30%~50% B;10.5~12.5 min,50%~100% B;12.5~13.5 min,100% B;13.5~14 min,100%~3% B;14~14.5 min,3% B。负离子模式流动相:A 相为水,B 相为乙腈;梯度洗脱程序:0~1 min,10%~15% B;1~2.5 min,15%~50% B;2.5~6 min,50%~65% B;6~7.5 min,65%~95% B;7.5~8 min,95%~100% B;8~8.5 min,100% B;8.5~8.6 min,100%~10% B。
1.6 质谱条件
离子源:电喷雾离子源(ESI),正、负离子模式;扫描方式:多反应监测(MRM)模式;毛细管电压:2.5 kV;锥孔电压:30 V;离子源温度:150 ℃;脱溶剂气温度:400 ℃;脱溶剂气(N2)流速:800 L/h;碰撞室压力:15.9 Pa。
2 结果与讨论
2.1 质谱条件的确定
将500 µg/L的单个标准品依次进行质谱条件优化。分别在正、负离子模式下进行一级质谱全扫描,在最优碰撞电压条件下,确定目标物母离子的m/z 值;然后进行二级质谱全扫描,通过优化碰撞能,选择响应最高的碎片离子作为目标物的定量离子,响应次高的碎片离子作为定性离子,质谱参数如表1。
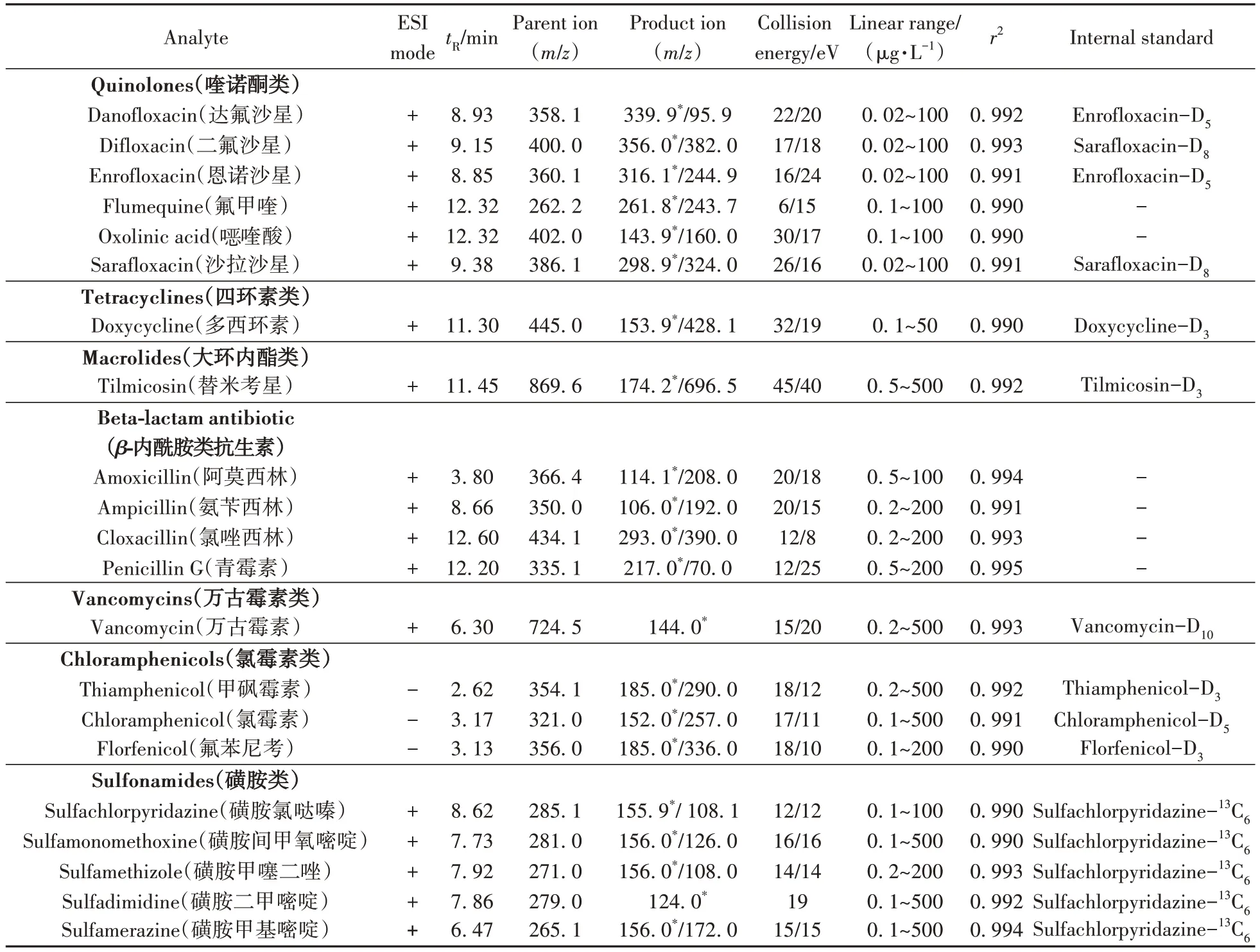
表1 90种目标物及29种内标物的质谱参数、线性范围及相关系数Table 1 Mass spectrometry parameters,linear ranges and correlation coefficients of 90 target drugs and 29 internal standards
2.2 色谱条件的优化
由于本实验的化合物数量较多,且各化合物的理化性质差异较大,为达到更好的响应值和分离度,比较了ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 µm)、ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 µm)、SHIMADZU C18-AQ(2.1 mm×100 mm,1.9 µm)、Epic Biphenyl(2.1 mm×100 mm,1.8µm)不同类型反相色谱柱的分离效果。结果表明,使用HSS T3 色谱柱时所有物质均可得到较好的峰形,且分离度和响应值优于其他3 种色谱柱,推测是因为T3 柱的键合疏水相比例较低,除常规的反相机制外,还可对极性物质达到较好的保留效果。因此实验选择ACQUITY UPLC HSS T3色谱柱,进一步对流动相进行了优化。
正离子模式下,以甲醇为有机相,考察了0.1%甲酸水溶液、0.1%甲酸-0.5 mmol/L NH4F 水溶液2 种水相对目标物分离效果的影响。发现在0.1%甲酸-0.5 mmol/L NH4F 水溶液条件下,福莫特罗、达氟沙星、硝呋烯腙等目标物的峰形较宽,存在拖尾;而在0.1%甲酸水溶液条件下,目标物的响应值更高,且峰形较尖锐对称。以0.1%甲酸水溶液为水相,比较了甲醇和乙腈2 种有机相的分离效果,如图1 所示,在乙腈体系下,硝呋烯腙、毒杀芬、丙酸睾酮等目标物的峰形展宽,而在甲醇体系下目标化合物的峰形、响应值和分离度均较好,可满足分析要求。因此,正离子模式下选择0.1%甲酸水溶液-甲醇作为流动相。负离子模式下分别比较了乙腈、甲醇两种有机相,研究表明水相中加入NH4F 可改变雌二醇等目标物的响应值[19],因此实验比较了水、1 mmol/L NH4F 两种水相的分离效果。结果显示,乙腈-水体系下目标物的响应值更高、峰形更好,因此负离子模式下选择水-乙腈作为流动相。
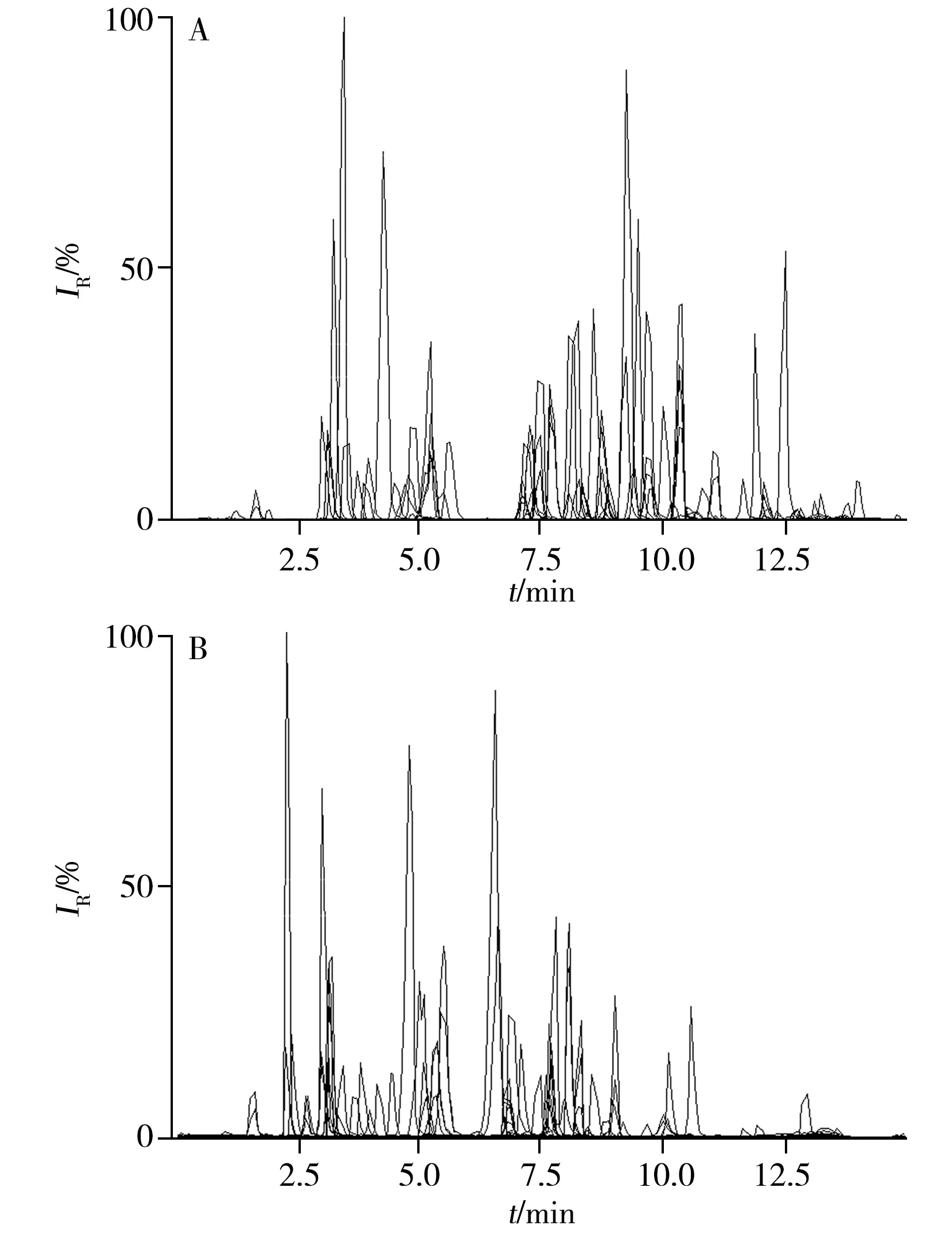
图1 正离子模式不同有机相条件下目标物的总离子流图Fig.1 Total ion chromatograms of targets under different organic phase conditions in positive ion mode A:methanol;B:acetonitrile
2.3 样品前处理优化
2.3.1 提取溶剂的选择乙腈是动物性食品兽药残留提取常用的有机溶剂,在乙腈中加入一定比例的水和酸可以提高提取效率,减少共沉淀造成的目标物损失。研究表明,随着甲酸含量的增加,磺胺类等碱性物质的回收率降低,当甲酸含量为0.2%时,提取效果较好[20-21]。因此本文选择0.2%甲酸-乙腈为提取溶剂并进行了优化。称取2 g禽蛋样品,分别加入10 mL 0.2%甲酸-乙腈水溶液(1∶1)、0.2%甲酸-乙腈水溶液(3∶1)和0.2%甲酸-乙腈溶液,加入50 µL 混合标准溶液(100 µg/L),超声离心。从表观看,0.2%甲酸-乙腈水溶液(1∶1)产生的上清液较混浊,另两种溶液的提取液均很澄清;取上清液进行分析,结果表明以0.2%甲酸-乙腈水溶液(3∶1)提取时大部分目标物的峰面积大于其他两种提取溶剂,以0.2%甲酸-乙腈提取时目标物的峰面积最小,这可能是由于高比例的乙腈使得样品发生团聚,目标物被包裹在样品基质中。综上,本实验选用0.2%甲酸-乙腈水溶液(3∶1)作为提取溶剂。
2.3.2 Na2EDTA 对目标物回收率的影响由于四环素、喹诺酮等药物易与基质中的金属离子和蛋白质结合,导致提取率偏低。研究表明,提取溶液中加入EDTA 可使金属离子与之发生螯合,从而使目标物解离[22-23]。因此考察了Na2EDTA 对目标化合物提取率的影响。向2 g 鸡蛋中加入25 mg Na2EDTA,用10 mL 0.2%甲酸-乙腈水溶液(3∶1)超声提取30 min,离心后取上清液进行分析。结果显示,加入Na2EDTA 后有48 种目标物的回收率增加,其中多西环素的平均回收率提高了24%,喹诺酮类药物的平均回收率增加了16.4%~21.4%。
2.3.3 样品净化复杂的样品基质会对目标物的回收率和色谱行为造成不良影响,为提升分析效果,延长色谱柱寿命,通常需对样品提取液进行净化以去除干扰成分。目前QuEChERS 法因高效、快捷和操作方便常用于动植物食品残留检测的前处理[24-25]。本研究比较了C18、PSA、增强型除脂材料(EMRlipid)、MWNTs、Z-Sep/C18净化管 5 种净化材料的处理效果。分别称取50 mg C18、20 mg PSA、50 mg EMR-lipid、50 mg Z-Sep/C18、10 mg MWNTs 填料,考察鸡蛋基质的加标回收率和基质效应(图2)。由图2 可知,采用MWNTs 填料净化时回收效果最差,有27 种物质的回收率在60%以下,其中恩诺沙星、二氟沙星等7 种目标物的回收率低于10%,这可能是MWNTs 对目标物产生不可逆吸附所致;采用EMR-lipid 填料净化时,目标化合物的回收率为53.2%~134%,其中85 种药物的回收率为60%~120%,从基质效应来看,使用EMR-lipid 填料时,仅氟苯尼考有基质增强效应,其他化合物无显著影响或有轻微抑制效应。这可能是由于EMRlipid 净化填料能够选择性去除鸡蛋提取液中的脂质等干扰成分,且不会对分析物造成显著影响。因此选择EMR-lipid 填料作为净化材料。
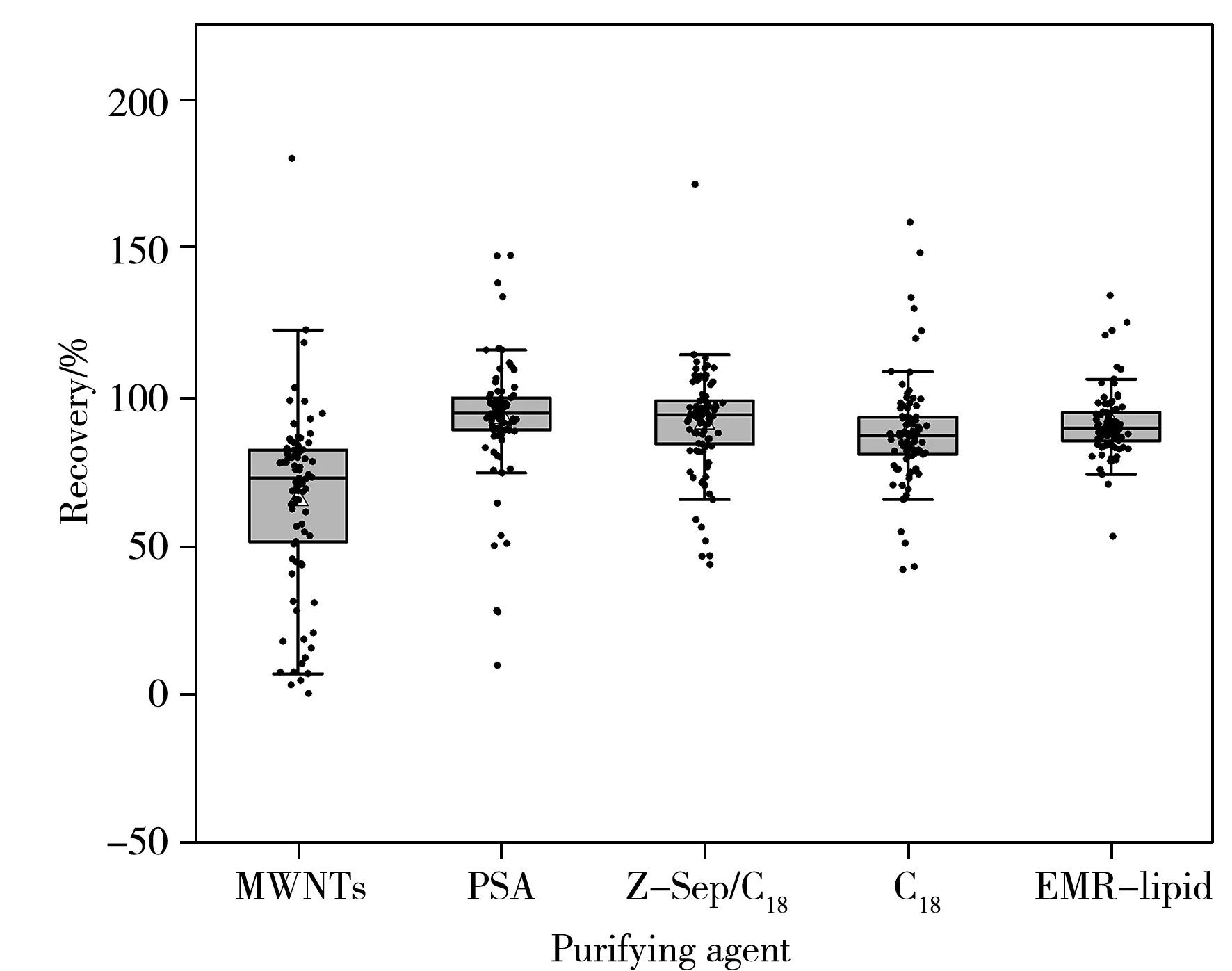
图2 采用不同净化材料时鸡蛋基质中目标物回收率的分布情况Fig.2 Distribution of target recovery in egg matrix with different purifying agents
2.4 方法确证
本研究通过基质标准曲线斜率与溶剂标准曲线斜率的比值考察了各目标物的基质效应。如表2 所示,目标物的基质效应为55.7%~138%,因此采用内标校正曲线或基质空白提取液配制标准曲线以消除基质效应的影响。采用基质空白提取液配制标准曲线溶液,在优化条件下进行分析。硝呋烯腙、呋喃苯烯酸钠、水杨酸、毒杀芬、呋喃丹等12种物质因未获得同位素内标,故采用基质外标曲线法校正,其余物质使用内标曲线法校正。以目标物的质量浓度为横坐标(x,µg/L),相应峰面积与内标峰面积比为纵坐标(y)进行线性回归。结果显示,90 种目标物在对应质量浓度范围内呈良好的线性关系,相关系数(r2)不小于0.99(表1)。对空白基质进行加标分析,以信噪比(S/N)≥3 为检出限(LOD),S/N≥10 为定量下限(LOQ),得到本方法的检出限为0.05~1 µg/kg,定量下限为0.1~3 µg/kg(表2)。
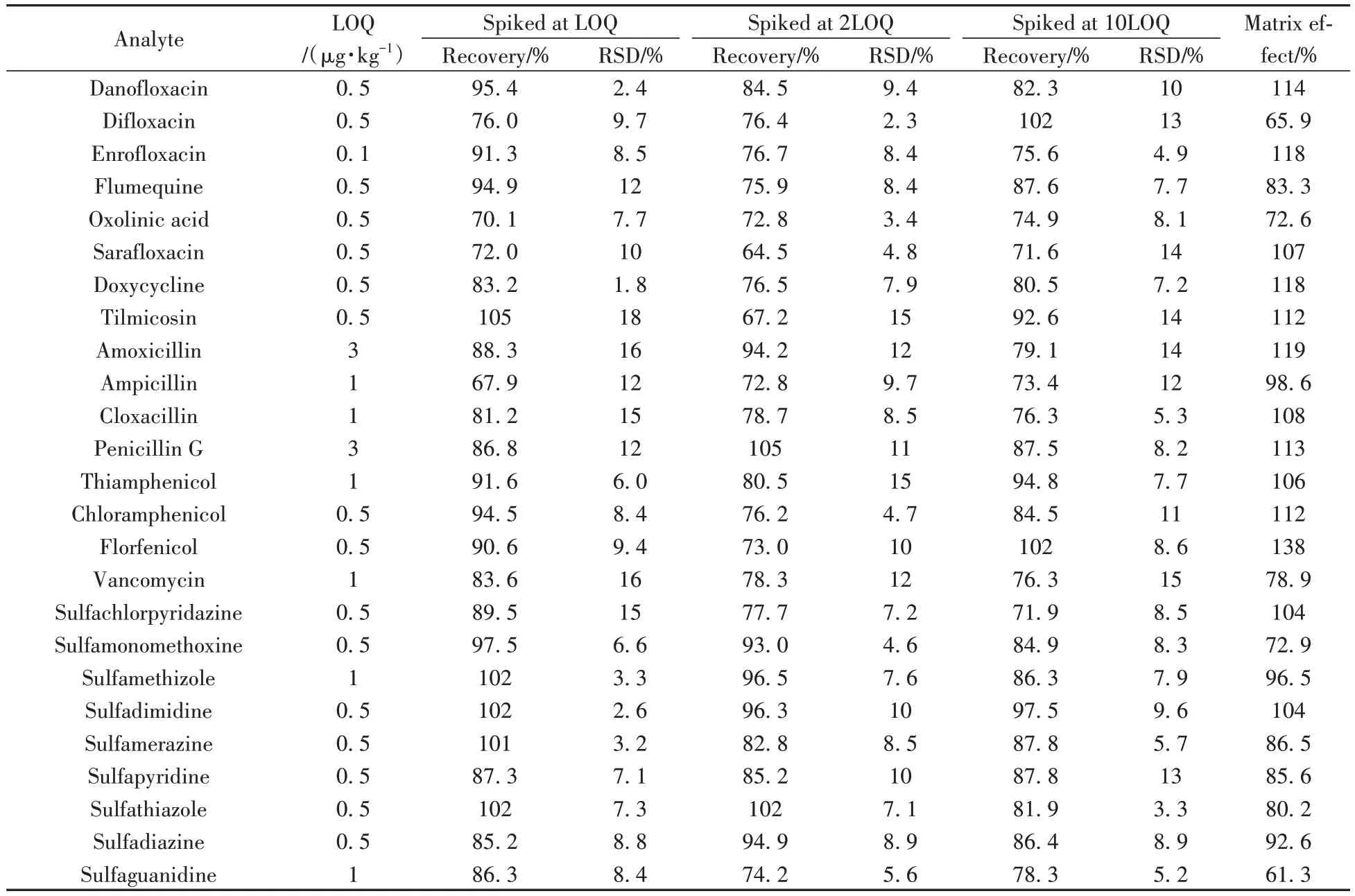
表2 鸡蛋中90种目标物的定量下限、平均加标回收率、RSD及基质效应(n=6)Table 2 Limits of quantitation(LOQs),average recoveries,RSDs and matrix effects of 90 targets in eggs(n=6)
对鸡蛋空白基质进行LOQ、2倍LOQ、10倍LOQ 3个水平的加标实验,每个浓度设6个平行,在优化条件下进行分析,计算目标物的平均回收率及相对标准偏差(RSD)。如表2 所示,鸡蛋中90 种目标物的平均回收率为60.8%~111%,RSD 为1.6%~18%。同时还考察了鸭蛋和松花蛋的加标回收率,90 种目标物在二者中的平均回收率分别为58.6%~118%、61.4%~120%,RSD 分别为0.90%~13%、1.2%~17%,符合药物多残留分析的要求。
2.5 方法应用
应用此方法对超市采集的106 件禽蛋样品(包括80 件鸡蛋、18 件咸鸭蛋、7 件皮蛋、1 件鹌鹑蛋)进行了检测,结果如表3所示。共有12件样品检出7种禁用药物,检出量为0.49~22.30 µg/kg;咸鸭蛋中检出甲硝唑、沙丁胺醇、恩诺沙星、磺胺喹啉4 种禁用药物,检出量为0.49~19.07 µg/kg。GB 31650-2019[1]规定甲硝唑允许作治疗用,但不得在动物性食品中检出;磺胺类药物(含甲氧苄啶)、喹诺酮类、多西环素等在产蛋期禁用,GB 31650.1-2022[26]规定这几类药物在禽蛋中的最大残留限量为10 µg/kg,因此7件样品存在药物残留超标现象。
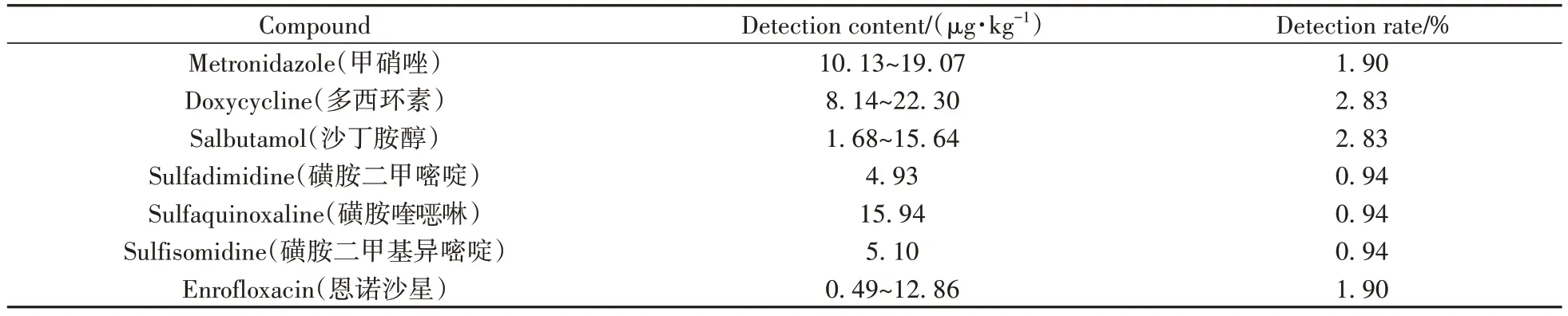
表3 106件禽蛋样品中违禁药物的检出情况Table 3 Detection of prohibited drugs in 106 poultry egg samples
3 结 论
本文建立了禽蛋中90 种违禁药物的QuEChERS/超高效液相色谱-串联三重四极杆质谱法。通过对前处理过程的优化,有效降低了基质中干扰物的影响。与现有方法相比,本方法实现了禽蛋中禁用药物的高通量检测,降低了检测成本,并应用于实际样品检测中。该方法可用于日常禽蛋产品中违禁药物的监测,为相关产品的质量安全保障提供技术支持。

