超早产儿临床特征及死亡危险因素分析
张 烨 齐 敏 施春燕 杨世炳 姜 舟
浙江大学医学院附属邵逸夫医院新生儿科(浙江杭州 310016)
超早产儿(extremely preterm infant,EPI)是指胎龄<28周的活产新生儿。近年随着辅助生殖技术的发展,EPI 的出生率越来越高。EPI 因为各系统发育不成熟,导致其死亡率很高。目前随着产前护理和新生儿监护水平的进步,这部分婴儿存活率已有所提高,然而不同医疗中心之间存在差异[1-3]。为进一步了解EPI的临床状况及影响其出院时临床结局的相关危险因素,本文对本院2018年1月至2021年12月期间收治的EPI的临床资料进行回顾性分析。
1 对象与方法
1.1 研究对象
回顾性分析2018 年1 月1 日至2021 年12 月31日在浙江大学医学院附属邵逸夫医院新生儿科住院的EPI的临床资料。纳入标准:①年龄<28天;②符合EPI诊断标准[2]。排除标准:①放弃治疗并于出生24小时内死亡;②临床资料不完整。
根据出院时结局将研究对象分为存活组和死亡组。
1.2 方法
1.2.1 临床资料收集 采集母婴相关临床资料。母体因素包括:产妇年龄、分娩方式、有无妊娠期糖尿病、胎膜早破、产前使用糖皮质激素、产前使用抗生素等;患儿因素包括:胎龄、出生体重、Apgar评分、新生儿急性生理学评分围生期补充Ⅱ(SNAPPE-Ⅱ)(简称为SNAPPE-Ⅱ重症评分)、新生儿呼吸窘迫综合征(NRDS)、动脉导管未闭(PDA)、呼吸支持、感染性休克、出院时结局等。
1.2.2 相关指标定义 EPI指出生时胎龄<28周的活产新生儿。NRDS、PDA、高血糖的诊断标准参照第5 版《实用新生儿学》[4];严重NRDS 定义为胸片改变达Ⅲ~Ⅳ级[4];SNAPPE-Ⅱ重症评分评价内容包括出生体重、5分钟Apgar评分、平均血压、最低体温、动脉氧分压(PO2)/吸入氧浓度百分比(FiO2)、最低pH 值、尿量、抽搐以及小于胎龄儿,评分越高提示病情越重[5]。高龄产妇为年龄≥35 岁的产妇。产前糖皮质激素使用定义:产前为促胎肺成熟而应用糖皮质激素,无论是否足疗程[6]。
1.3 统计学方法
采用SPSS 24.0 统计软件进行数据分析。计量资料符合正态分布的以均数±标准差表示,两组间比较采用两独立样本t检验;非正态分布的以中位数(M)(P25~P75)表示,组间比较采用秩和检验。计数资料以例数(百分比)表示,组间比较采用χ2检验。采用二分类多因素logistic 回归分析影响EPI 死亡的危险因素。以P<0.05 为差异有统计学意义。
2 结果
2.1 一般情况
研究期间共收治EPI 118例,排除放弃治疗且出生24 小时内死亡者4 例,最终纳入114 例。其中男性58例(50.9%);中位胎龄27.0(26.0~27.6)周,最小胎龄23+1周;平均出生体重(921.0±179.0)g,体重最低490 g,最高1 340 g;体外受精和胚胎移植65 例,双胎57 例。存活组90 例,中位住院时间107.0(84.8~125.3)d,死亡组24 例,中位住院时间17.5(7.5~23.8)d。23~24、24~25、25~26、26~27、27~28 周胎龄组的存活率分别为0%(0/1)、16.7%(1/6)、80.0%(12/15)、71.9%(23/32)、90.0%(54/60)。
2.2 两组EPI母亲临床情况比较
两组EPI母亲之间高龄产妇、宫颈机能不全、合并妊娠期糖尿病、胎膜早破、产前使用糖皮质激素、产前使用抗生素、剖宫产比例的差异均无统计学意义(P>0.05)。见表1。
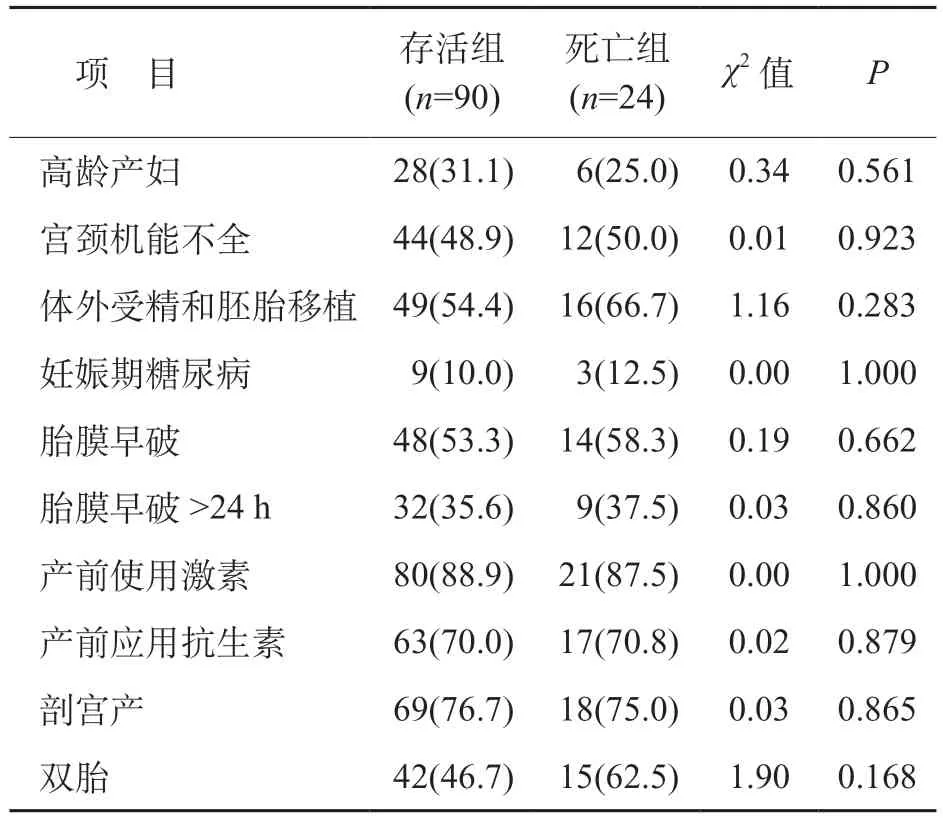
表1 两组EPI之间母亲情况比较[n(%)]
2.3 两组EPI临床特征比较
与存活组相比,死亡组胎龄、出生体重较低,出生体重≤750 g,1 分钟和5 分钟Apgar 评分≤7 分,严重NRDS,生后第1 天机械通气,生后1 周内肺出血、高血糖、使用胰岛素,感染性休克比例较高,SNAPPE-Ⅱ重症评分较高,差异均有统计学意义(P<0.05)。见表2。
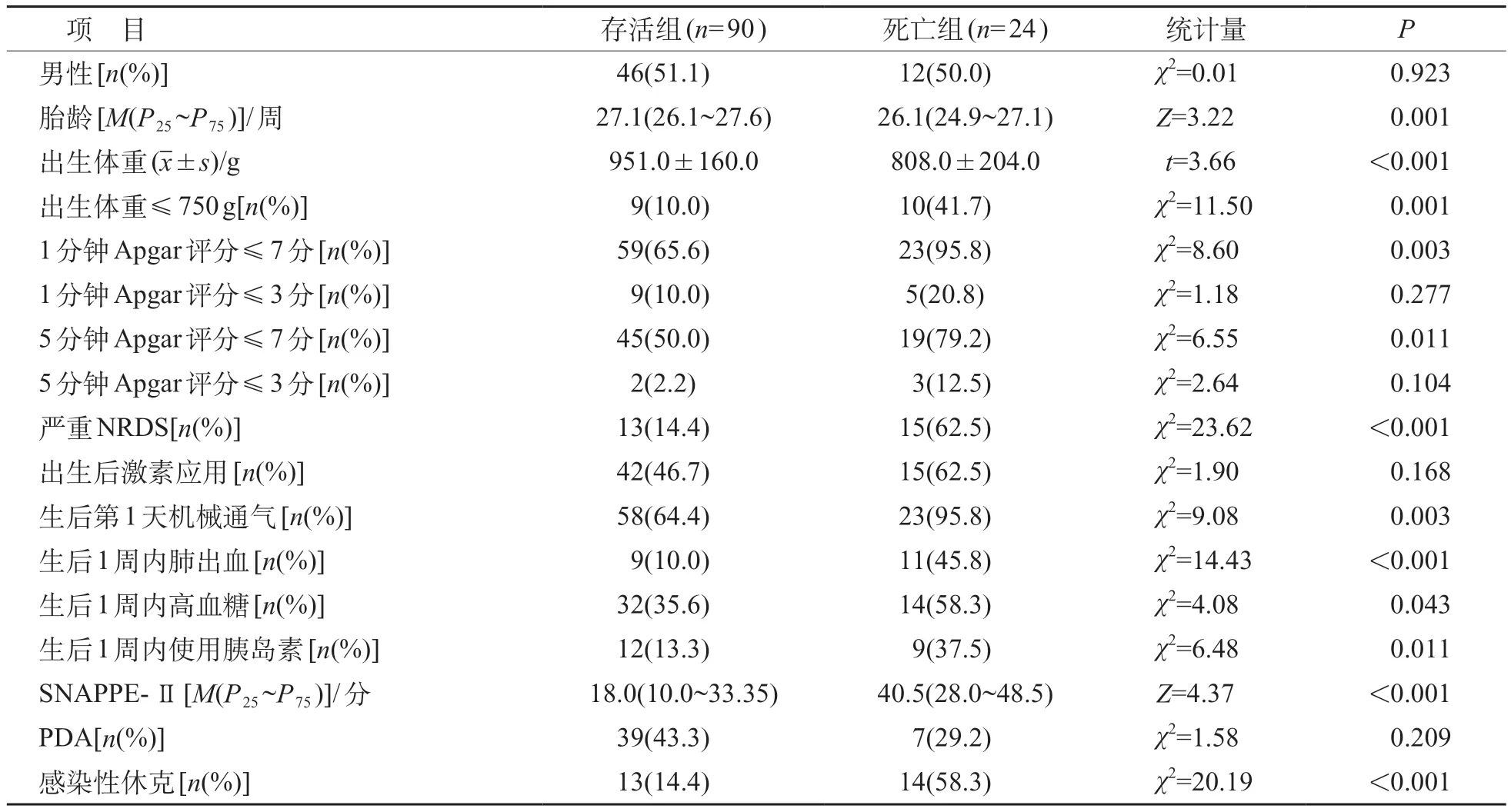
表2 影响EPI死亡的单因素分析
2.4 影响EPI死亡的多因素logistic回归分析
将单因素分析有统计学意义的变量纳入多因素logistic 回归模型,结果显示出生体重≤750g、严重NRDS、生后1周内肺出血、生后1周内使用胰岛素、感染性休克是EPI死亡的独立危险因素(P<0.05)。见表3。
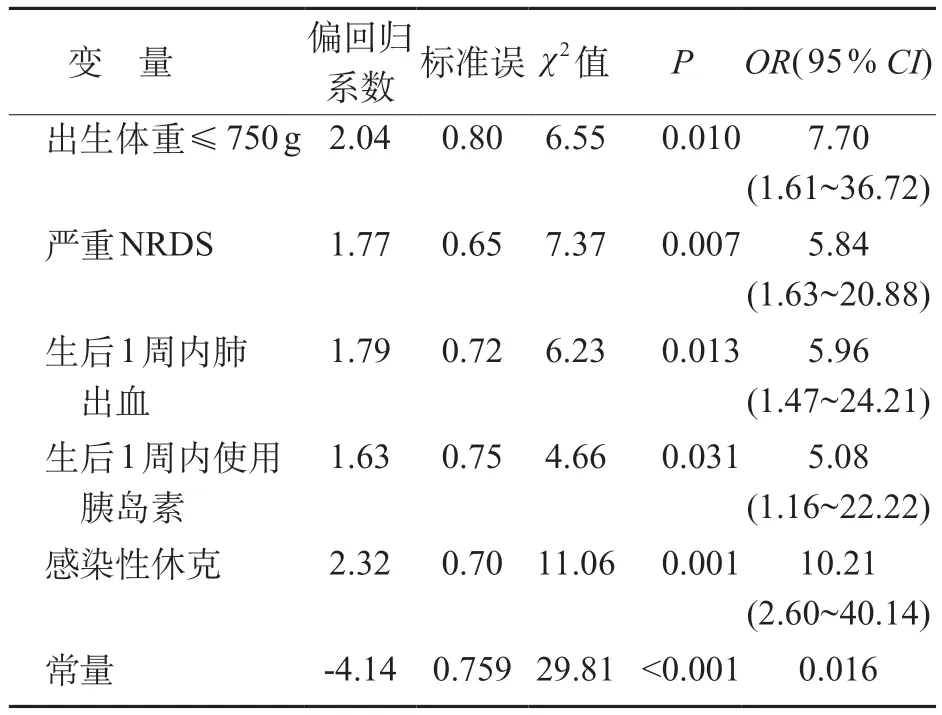
表3 影响EPI死亡的多因素logistic回归分析
3 讨论
随着新生儿重症监护技术的开展及推广应用,EPI 存活率明显提高。美国新生儿研究网(neonatal research network,NRN)对2013—2018年的EPI进行统计,显示其存活率为78.3%,其中胎龄23~27 周的存活率分别为55.8%、71.4%、79.9%、88.1%和90.8%[3]。加拿大的多中心研究显示,EPI在2010—2017 年的存活率为82.1%,其中胎龄23~27 周的存活率分别为47.0%、68.0%、81.0%、88.0%和94.0%[7]。我国近些年EPI的存活率较前有所提高,但仍低于发达国家,研究显示我国EPI 的在院存活率为60.0%~78.6%,<25周胎龄EPI的存活率更是低于30.0%[8-10]。本研究中EPI的存活率为78.9%,但≤24周胎龄者存活率明显低于发达国家,≥25周胎龄者存活率和发达国家相似,提示对于胎龄≤24周患儿的管理仍需继续努力。
EPI死亡率和其出生体重相关[8,11]。本研究中死亡组的出生体重明显低于存活组,对出生体重进一步分层发现出生体重≤750g是EPI死亡的独立危险因素,提示出生体重对EPI预后十分重要。另外胎龄是影响EPI 死亡的重要危险因素[3,11]。本研究中死亡组的中位胎龄明显低于存活组,但并非独立危险因素,考虑本研究对象的胎龄主要集中在26~27周,而这部分患儿的存活率高,也可能与样本量较小有关,未来需要纳入更多样本进行研究。
严重NRDS 是早产儿早期死亡的重要危险因素[8,12]。本研究中严重NRDS是EPI住院期间死亡的危险因素,但因病例数有限并未将早期及晚期死亡病例分开分析,因此并不能确定NRDS在EPI早期及晚期死亡中的作用,今后将继续收集病例作进一步研究。本研究发现生后1周内发生肺出血是EPI死亡的独立危险因素,生后1 周发生肺出血患儿的死亡率高达55.0%,和其他研究结果相近[13-14]。肺出血常发生于极早产儿,可增加其死亡率,肺出血高危因素包括缺氧窒息、NRDS、PDA及感染等[13],提示在EPI的早期管理中需及时处理并避免这些高危因素。
高血糖是EPI 生后1 周常见表现,发生率波动于30.0%~80.0%[15],本研究中的高血糖发生率为40.0%。多项研究显示生后1 周高血糖是早产儿死亡的独立危险因素[15-16]。本研究中死亡组的高血糖发生率高于存活组,但并不是独立危险因素。高血糖可能影响早产儿长期代谢和神经发育,在高血糖持续存在、葡萄糖输注速率受到限制时需要胰岛素治疗[12]。然而胰岛素的作用和影响目前仍存在争议[15],有研究显示在发生高血糖的EPI中,使用胰岛素治疗可降低其死亡率[16],而另外的研究则显示生后1周内使用胰岛素增加了死亡率[17]。本研究显示生后1周内使用胰岛素增加了EPI的死亡风险,分析原因可能和胰岛素使用的时机、剂量及治疗阈值存在差异有关。
感染性休克是引起早产儿死亡的重要原因[18],致死率可高达70.0%。由于EPI住院时间长、需要长期静脉置管、肠道发育不成熟等原因,其感染发生率及病死率显著高于足月儿[18]。本研究显示感染性休克是引起EPI 死亡的重要危险因素,出现感染性休克的EPI死亡风险是无感染性休克患儿的10倍左右,提示临床上需尽量预防感染发生,尽早发现感染性休克并给予及时有效的治疗。
Apgar评分对早产儿预后有重要意义,研究显示生后5分钟以及10分钟仍有重度窒息的早产儿预后更差[19]。本研究发现死亡组1分钟、5分钟 Apgar评分≤7分比例显著高于存活组,但并不是影响EPI死亡的独立危险因素,考虑原因为本研究中EPI在生后5分钟时基本复苏成功,减少了其死亡风险,另一方面由于生后5分钟仍重度窒息的患儿很少,限制了进一步分析其对EPI死亡的影响;并且由于EPI的特殊性,Apgar评分并不能很好判断该部分新生儿的预后[20]。
多项研究证实产前糖皮质激素使用是改善早产儿预后的有效方法[21-23]。本研究中并未发现产前糖皮质激素应用是EPI 死亡的保护因素,考虑和其应用率高有关,本研究中产前糖皮质激素使用率高达91.0%,明显高于国内其他研究中的使用率[14,23],和发达国家接近[22,24]。结合本研究中的产前激素的高使用率及相对较低的死亡率,提示按照循证依据进行临床管理,可更好改善患儿结局。
SNAPPE-Ⅱ重症评分可预测新生儿预后情况,本研究中死亡组EPI的评分明显高于存活组,但并非EPI 死亡的独立危险因素,考虑原因为SNAPPE-Ⅱ重症评分系统纳入的为出生12小时内的情况,对于EPI 的早期死亡预测能力更佳[25-26]。本研究加入了出生后的情况如有无严重NRDS,出生1周内有无肺出血、有无应用胰岛素,以及有无感染性休克,结合SNAPPE-Ⅱ重症评分可以更好帮助临床医师进行EPI的管理,提高其存活率。
本研究局限性在于:①为单中心研究,病例数偏少,且胎龄主要集中在26~27周,存在偏倚误差;②研究中纳入病例约一半为双胎及体外受精和胚胎移植的新生儿,人群存在特异性。因此未来需进一步扩大样本量,进行更深入研究,为临床精细化管理EPI提供依据。
综上所述,EPI 的死亡危险因素是出生体重≤750 g、严重NRDS、生后1 周内肺出血、生后1 周内使用胰岛素及感染性休克。在EPI的临床管理中,需高度警惕这些情况,并进行及时有效地治疗,进一步提高EPI的存活率。

