3D打印技术定制化覆膜支架精准治疗Stanford B型主动脉夹层临床研究
彭 栋,刘石琳,阿拉法特·艾尔肯,沙尔娜,张棋鑫,段 磊
(1.新疆医科大学第二附属医院介入诊疗科,新疆 乌鲁木齐 830054;2.新疆医科大学第二附属医院体检中心,新疆 乌鲁木齐 830054)
主动脉夹层是一种突发性疾病,常伴严重的并发症,对患者的生命造成严重的威胁[1]。该病的发病率为1/10万,由于发病急骤,临床表现较为复杂,发病后若患者未经及时有效的治疗则病死率高达50%,约70%的患者1周内死亡[2]。以往的研究指出[3],胸主动脉腔内修复手术是治疗主动脉夹层的微创手术,其能够降低主动脉夹层患者的病死率。胸主动脉腔内修复手术与其他介入微创手术相同,需借助术前及术中影像学辅助手术,术前手术医师处于非直视操作中,需充分掌握患者主动脉夹层的解剖结构,便于术中操作。由此可得出,术前影像学评估能够辅助主动脉夹层的手术治疗,对临床具有重要的应用价值[4]。3D打印技术定制化覆膜支架精准治疗是通过3D打印技术精准复制病变部位的主动脉弓部,从多角度、多方位了解病变部位主动脉弓部的解剖结构,全面掌握主动脉弓部夹层特点,并根据3D技术检查结果制定覆膜支架精准治疗,不仅能够明确手术过程及细化手术方案,而且能够为患者提供精准的支架,从而有效提高手术成功率,降低患者病死率,对临床具有重要意义[5-6]。但目前临床关于3D打印技术定制化覆膜支架精准治疗Stanford B型主动脉夹层的研究甚少。基于此,本研究将探讨3D打印技术定制化覆膜支架精准治疗Stanford B型主动脉夹层的临床应用。
1 资料与方法
1.1 一般资料 将2021年2月至2023年3月于新疆医科大学第二附属医院收治的23例Stanford B型主动脉夹层患者为研究对象,其中男18例,女5例;年龄29~65岁,平均(43.29±13.28)岁;合并糖尿病3例,合并高血压6例。病例纳入标准:经CT血管造影(CTA)诊断为Stanford B型主动脉夹层患者;患者精神正常,认知功能正常;符合胸主动脉腔内修复手术适应证;既往无手术治疗史者;患者均知情同意并签订知情同意书。排除标准:存在免疫系统疾病;合并凝血系统疾病;夹层逐渐累及升主动脉或已破裂需紧急手术者;存在恶性肿瘤患者;病例资料、影像资料缺失;不愿意参加本次研究者。本研究方案符合《世界医学协会赫尔辛基宣言》的相关要求。
1.2 研究方法
1.2.1 术前检查:所有研究对象术前均进行超声心动图、心电图、血液常规等检查,再次采用CTA诊断明确鉴别,患者的病情情况采用多模态影像学评估。
1.2.2 术前3D打印:采用德国西门子公司生产的双源CT,禁饮禁食2 h,将尿液排空,调整呼吸,设置扫描参数,以500 mA的电流,120 kV的管电压,0.625 mm的层厚,0.625 mm的间隔,800 HU的窗宽,观察窗位200 HU。扫描范围从主动脉弓到耻骨联合,扫描层厚7.0 mm,重建层厚0.75 mm。扫描时经肘静脉团注非离子型对比剂(300 mgI/ml)100 ml,注射流速为3.0 ml/s。扫描数据以DICOM格式导出,并导入MIMIC16.0软件进行胸主动脉三维重建,提取范围从升主动脉开口到腹主动脉腹腔干动脉,模型表面光滑修饰,并以STL格式导出模型。STL模型导入Magic软件进行模型表面修饰后,模型外表面加壳厚度2 mm,提取出中空的血管厚度2 mm的胸主动脉夹层模型;打印材料选择以光敏树脂软性材料,以便有良好拉伸和弯曲能力;打印成型主动脉夹层Stanford B型。采用光固化打印技术(第三方提供),测量数据后24 h内制作。
1.2.3 3D打印评估:①胸腹主动脉CTA三维重建结果与3D模型比较,对比主动脉重要分支及破口的位置,并观察其测量值是否一致。②掌握主动脉弓具体位置,确定头臂干、左颈总动脉、左锁骨下动脉各分支开口对应主动脉弓的部位。③对真腔大小进行测量,评估选择支架的直径(覆膜支架外径较相应动脉直径大10%~15%)。评估方式:全方位观察主动脉夹层的解剖条件,拉伸破口演示支架。两位影像科副主任以上级别医师在CT图像后处理工作站测量CT数值,DSA造影测量由副高技术职称医师和技师共同完成,使用导管校正技术测量。
1.2.4 手术及定制化覆膜支架:局部麻醉及常规消毒后,取仰卧位,一组人员选择无菌薄膜覆盖在制备好的术前3D打印模型上,将弓上分支的部位标记清楚并测量,根据标记的位置,在主动脉弓主支架上烧灼出对应的侧孔,选择与分支血管内径相应的覆膜支架;另外一组人员对右股动脉和左桡动脉进行穿刺,放置6F和5F动脉鞘管。肝素通过静脉输注,将猪尾导管经左侧桡动脉放置至升主动脉造影,主动脉真腔通过导管、导丝及Lunderquist导丝到达破口处,将上述选择的支架及合适的双球囊导管置入狭窄处释放,观察支架释放情况,获得满意的压差后,将输送系统撤出,缝合包扎。
1.3 观察指标 比较术前常规CT测量;术前DSA造影测量;术前3D模型测量左颈总后缘直径、动脉瘤近端直径、动脉瘤直径、动脉瘤远端直径、远端锚定直径。

2 结 果
2.1 不同检查颈总后缘直径、动脉瘤近端直径、动脉瘤直径、动脉瘤远端直径、远端锚定直径比较 所有Stanford B型主动脉夹层患者均完成术前3D打印、术前DSA及术前CT检查。术前3D打印测定的动脉瘤近端直径、动脉瘤远端直径与术前DSA比较,术前3D打印测定的左颈总后缘直径、左锁骨后缘直径、动脉瘤近端直径、动脉瘤远端直径、远端锚定直径与术前CT比较,术前DSA测定的左颈总后缘直径、动脉瘤近端直径、动脉瘤直径、动脉瘤远端直径、远端锚定直径与术前CT比较,差异有统计学意义(均P<0.05);术前3D打印测定的左颈总后缘直径、左锁骨后缘直径、动脉瘤直径、远端锚定直径与术前DSA比较;术前3D打印测定的动脉瘤直径比较,差异无统计学意义(均P>0.05)。见表1(图1)。
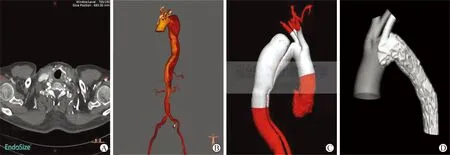
注:男,54岁,主动脉夹层Standford B型,A为术前CT,B为CT血管三维成像,C为术前3D打印血管三维成像,D为术后3D打印

表1 不同检查颈总后缘直径、动脉瘤近端直径、动脉瘤直径、动脉瘤远端直径、远端锚定直径比较 (mm)
2.2 不同检查真假腔/瘤体最大直径比较 术前3D打印测定的假腔最大直径、真腔最大直径与术前CT比较,术前DSA测定的假腔最大直径、真腔最大直径与术前CT比较,差异有统计学意义(均P<0.05);术前3D打印测定的假腔最大直径、真腔最大直径与术前DSA比较,差异无统计学意义(均P>0.05)。见表2。

表2 不同检查真假腔最大直径比较 (mm)
2.3 stanford B型主动脉夹层患者手术情况分析 23例Stanford B型主动脉夹层患者手术时间为318~587 min,平均(518.381±37.298)min;术中出血量为2789~4198 ml,平均(3187.873±145.982)ml;术中停循环时间5~11 min,平均(8.321±2.018)min;体外循环时间126~156 min,平均(143.283±34.298)min。
2.4 Stanford B型主动脉夹层患者并发症发生情况及死亡情况比较 随访12个月,平均(11.87±1.37)个月。术后ICU监护时间5~8 d,平均(6.19±1.56)d;住院时间16~27 d,平均(23.28±3.28)d;苏醒延迟1例,无死亡患者。
3 讨 论
主动脉夹层的主要病理特征为主动脉壁内膜撕裂,血液从主动脉壁内膜和中膜间的通道或主动脉和二级血管主通道(真腔)流出,不同近端破口位置可区分不同类型的主动脉夹层[7]。主动脉夹层患者血液沿真假腔流动,会影响正常血流改变原有的血流动力学,诱发主动脉壁出现动脉瘤或重要器官灌注,造成主动脉瘤劈裂[8]。主动脉夹层的治疗仍是心血管急症的一个难点,每年因主动脉夹层死亡的患者约1%~3%,严重威胁到患者的生命健康。随着血管外科学、超声医学、影像学的不断发展,其诊断率会不断提高[9-10]。其中CT影像学对Stanford B型主动脉夹层的确诊及制定手术策略能够提供一定的帮助,但其存在直观感较差,缺乏立体感,诊疗过程中存在失误的情况发生[11]。近年来,3D打印技术又称快速成型技术,其在数字、堆积、分层、直接、快速制造等方面具有独特的优越性,如今该技术已经可以应用到心血管疾病术前诊断,通过其模型能够清晰地观察到目标部位的解剖结构及病变部位,根据其打印的模型进行模拟手术,方便与患者沟通及进行相关动物研究等[12-14]。
针对Stanford B型主动脉夹层而言,破口的部位、大小及解剖条件与手术方案的选择密切相关;另外,覆膜支架与主动脉管壁的力学“博弈”结果是主动脉夹层腔内治疗的近远期效果实质,在主动脉弓的不同位置放置相同的覆膜支架的效果并不相同(即便不覆盖头臂干动脉、左颈总动脉左锁骨下动脉),如远期支架源性新破口及破口逆向撕裂[15-16]。本研究采用光固化打印技术制作Stanford B型主动脉夹层模型,通过CT等影像学数据,构建一个直观、立体的三维模型,在二维断层影像基础上进行三维重建,且主动脉根部和弓部呈不规则走形,会造成在CT上测量该层面的主动脉直径,非此层面主动脉的真实直径;另外无法对锚定区直接测量,根据左锁骨下动脉根部的破口层面的投影,对投影距离与破口距离进行计算和投影在根据其根部与病变部位间的层数估算支架的锚定区,与术中存在的差异;影像科医师和手术团队医师在对疾病关注点上也存在不同的认知,造成其测量结果与实际情况存在一定的差异。以往的研究指出[17],3D打印在Stanford B型主动脉夹层中应用能够直观地反映主动脉重要分支的空间位置关系,有利于设计血管岛,对根大动脉的位置进行标定,更便于手术操作,从而降低并发症的发生。本研究结果显示,术前3D打印测定的动脉瘤近端直径、动脉瘤远端直径与术前DSA比较,术前3D打印测定的左颈总后缘直径、左锁骨后缘直径、动脉瘤近端直径、动脉瘤远端直径、远端锚定直径与术前CT比较,术前DSA测定的颈总后缘直径、动脉瘤近端直径、动脉瘤直径、动脉瘤远端直径、远端锚定直径与术前CT比较差异有统计学意义(均P<0.05),术前3D打印测定的假腔最大直径、真腔最大直径与术前CT比较,术前DSA测定的假腔最大直径、真腔最大直径与术前CT比较差异有统计学意义(均P<0.05),提示术前3D打印的数据与术前DSA基本接近,其存在的误差在临床中属于可以接受的范围;另外,术前3D打印及术前DSA与术前CT的数据比较存在明显的差异,这可能是由于术前CT测定支架的锚定区,贴合在主动内,是在主动脉弓内的一个弧形距离,术前评估的锚定区仅为大致结果,并不能算作一个直接测量的精准数据;而锚定区域的估算与手术方案的选择密切相关,若锚定区域估算不准确则需更换手术方式。而3D打印技术制作出的三维实体模型,能够辅助手术医师分析Stanford B型主动脉夹层主动脉根部受累情况,指导其对疾病的分型及手术的选择[18-19]。
术前3D打印能够将CT三维重建模型直观反映出来,能够全方位地观察主动脉夹层及破口部位和真假腔的形态、真假腔的比例;同时收集测量的各项数据,进行主体支架入路选择,从而考虑病变部位与支架的力学问题,有利于模拟支架放置在不同部位后对主动脉弓影响及选择远端限制性支架,同时能够发现可能存在的问题如支架释放角度发生改变,是否影响到支架锚定位置和周围贴壁的关系,是否需要增加放置支架,为其制定针对性的手术方案[20-21]。以往的研究指出[20],3D打印技术辅助手术治疗Stanford B型主动脉夹层疗法良好,其能够应用于术前评估、模拟手术,可减少术后并发症的发生情况,提高手术的安全性。
综上所述,术前3D打印的数据与术前DSA基本接近,且术前3D打印定制化覆膜支架精准治疗Stanford B型主动脉夹层能够改善手术情况,降低相关并发症的发生,对临床具有重要意义及价值,但远期疗效仍需更多样本量进行研究与观察。

