沉积电压对Ni-Fe-Sn镀层组织结构及析氢性能的影响
袁绍武,吴艺辉,王宇鑫,张 原,孙泽生,何 震
(江苏科技大学 材料科学与工程学院,镇江 212100)
近年来,Ni-Fe合金因其制备成本低和良好的电化学稳定性,是一种良好的析氢催化剂材料,但其仍存在析氢过电位较高的不足[3].研究表明[4],在合金中引入锡(Sn)可以增大镀层的比表面积,调整电子结构,增加暴露的活性位点数量和电导率,增强合金的析氢性能.文献[5]采用在铜箔表面合成的Ni-Fe-Sn镀层,其在30% KOH 溶液中的析氢过电位仅为333 mV,Tafel斜率低至47.3 mV·dec-1.
电沉积[6]是一种操作简单、成本低廉、沉积速率快、环境友好的镀层沉积技术.相比传统的恒电流电沉积,恒电位电沉积法得到的合金成分更稳定、分布更均匀.文中采用恒电位电沉积法在泡沫镍表面制备Ni-Fe-Sn镀层,研究了沉积电位对镀层表面形貌、组织成分和电催化析氢性能的影响.
1 实验
1.1 电极制备
采用传统的三电极体系制备Ni-Fe-Sn镀层,其中饱和甘汞电极(SCE)为参比电极,泡沫镍(10 mm×10 mm×1 mm)为工作电极,纯石墨板为对电极.利用CS Studio5电化学工作站(武汉科思特仪器有限公司)在温度40 ℃、电镀时间60 min的条件下进行电镀.制备Ni-Fe-Sn镀层的镀液配方为:100 g·L-1NiSO4·6H2O,30 g·L-1FeSO4·7H2O,5 g·L-1SnCl2·2H2O,40 g·L-1H3BO3,35 g·L-1NaCl和70 g·L-1Na3C6H5O7·6H2O,镀液的pH值为4.0.沉积时,电沉积电位为-0.7、-0.8和-0.9 V vs.SCE.电沉积后将样品取出,用超纯水多次冲洗,60 ℃真空干燥箱中烘干后备用.
1.2 材料的表征和电催化性能
使用TD-6000 X射线衍射仪(XRD,日本岛津公司)分析样品的物相组成,其中辐射源为Cu Kα(λ=0.154 18 nm);扫描电子显微镜(SEM,ZEISS EVO18,德国)和能谱仪(EDS,Oxford Instrument X-maxN,英国)分析Ni-Fe-Sn镀层的表面形貌和元素组成;X射线光电子能谱仪(XPS,Thermo Scientific Escalab250Xi,美国)分析镀层的价态.使用CS Studio5电化学工作站在标准三电极体系下(石墨板为对电极,SCE为参比电极)测试Ni-Fe-Sn镀层的电化学性能.所有测试均在25 ℃的N2饱和的1 mol·L-1KOH溶液中进行.采用线性扫描伏安法(LSV)测试电极析氢极化曲线,扫描速率为2 mV·s-1.电化学阻抗谱(EIS)测试频率范围为100 000~0.01 Hz,交流幅值为5 mV.
2 结果与讨论
图1为在不同沉积电位下制备的Ni-Fe-Sn镀层XRD图谱.在2θ=44.8°、52.3°、76.7°处存在3个强衍射峰,分别对应着FeNi3(PDF:38-0419)的(111) (200) (220)晶面.随着沉积电位的增大,2θ=44.8°衍射峰往低角度偏移,这是由于Sn原子的引入造成了Ni-Fe晶胞膨胀所致[7].此外,XRD谱图中并未观察到含Sn相的衍射峰,这可能是Sn固溶进入Ni-Fe晶胞所致,这与文献[8]观察到的现象一致.

图1 Ni-Fe-Sn镀层的XRD图谱
图2为不同沉积电位条件下制备样品的SEM图.
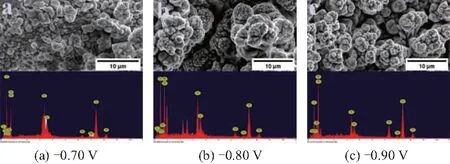
图2 不同沉积电位制备的Ni-Fe-Sn镀层的表面SEM图和能谱图
从图中可看出,随着沉积电位的下降,Ni-Fe-Sn镀层表面逐渐生成了菜花状结构.这是因为随着电位的下降,泡沫镍的极化程度增高,阴极表面析氢反应加剧,产生的氢气泡附着在材料表面,阻碍了离子在材料表面的均匀还原,从而产生了菜花状结构.这种菜花状结构增加了材料的比表面积,暴露更多的活性位点,从而促进HER性能.同时,从图2能谱图中可以看出Ni、Fe、Sn元素对应的能量峰,表明3种元素均成功沉入电极中.表1为不同沉积电位条件下制备样品的元素含量.由表可知,样品中Ni和Fe含量随着沉积电位的下降而增加,而Sn的含量则呈下降趋势,表明沉积电位的变化可显著地影响镀层中各组成元素含量.

表1 Ni-Fe-Sn镀层的元素含量
通过X射线光电子能谱(XPS)技术分析Ni-Fe-Sn镀层表面元素价态.图3(a)的全谱数据显示Ni-Fe-Sn镀层中含有Ni-Fe-Sn镀层的C,O,Ni,Fe和Sn元素的信号,进一步表明Ni,Fe和Sn元素已经成功沉积到镀层中.C和O可能是镀层表面轻微氧化或材料表面吸附的少量CO2.在Ni 2p(图3(b))的XPS谱图中,结合能为855.5和873.2 eV处的两个主峰,其结合能相差17.7 eV,分别属于Ni 2p1/2和Ni 2p3/2的特征峰,说明镀层中含有+2和+3两种价态,另外在861.1和879.2 eV为其相应的卫星峰.此外,结合能为851.6 eV处的峰表明镀层表面存在金属态镍.Ni-Fe-Sn镀层中Fe 2p谱(图3(c))在706.0、711.2、714.8和724.9 eV处的峰分别对应着Fe02p3/2、Fe3+2p3/2、卫星峰和Fe3+2p1/2.Sn 3d的XPS光谱(图3(d))在484.1 eV和493.0 eV处的峰分别归属于Sn 3d5/2和Sn 3d3/2,表明镀层中存在着金属Sn.486.5 eV和495.0 eV处的峰对应Sn4+3d5/2和Sn4+3d3/2.

图3 Ni-Fe-Sn镀层的XPS谱图
图4(a)为Ni-Fe-Sn镀层在1 mol·L-1KOH溶液中的极化曲线.由图可知,当电流密度为10 mA·cm-2时,沉积电位-0.7,-0.8,-0.9 V条件下合成的Ni-Fe-Sn镀层的过电位分别为127,81,62 mV,表明当沉积电位为-0.9 V时具有较高的析氢催化活性.Tafel斜率是催化剂的一个内在参数可以揭示析氢过程中的反应动力学.从图4(b)可知,沉积电位-0.7,-0.8,-0.9 V条件下合成的Ni-Fe-Sn镀层的Tafel斜率分别为103.3、90.4、109.7 mV·dec-1,表明Ni-Fe-Sn镀层的HER反应是一个Volmer-Heyrovsky动力学过程,即吸附H的过程起控制作用。

图4 Ni-Fe-Sn镀层析氢性能
图5(a)对比了Ni-Fe-Sn镀层经过2 000次CV循环后的极化曲线与初始极化曲线的对比图.CV测试条件为:扫描电压范围为-200~100 mV vs RHE,扫描速率为100 mV·s-1.

图5 Ni-Fe-Sn镀层的电化学性能
由图可知,经过2 000次CV循环后,Ni-Fe-Sn镀层的过电位从62 mV轻微增加到94 mV (@10 mA·cm-2),表明其具有较好的稳定性.同时,在10 mA·cm-2电流密度条件下,对Ni-Fe-Sn镀层进行了长时间的电解.如图5(b)可知,经过24 h电解后,镀层的电解电位基本不变,表明其在1 mol·L-1KOH中具有良好的电催化析氢稳定性电化学阻抗谱(EIS)是研究不同催化剂材料的电子转移和反应动力学的有效方法.图5(c)是不同沉积电位制备Ni-Fe-Sn镀层的Nyquist图(测试电位为-100 mV vs RHE)及其相应的等效电路.等效电路图中Rs代表电解液、电极以及仪器之间的欧姆电阻,Rct是电极与电解液之间的电荷转移电阻,CPE表示恒相位元件.沉积电压-0.7、-0.8,-0.9 V条件下合成的Ni-Fe-Sn镀层的Rct值分别为1.03、0.88和0.68 Ω,表明沉积电位为-0.9 V时,Ni-Fe-Sn镀层的电荷转移速度更快、效率更高,具有更高的本征催化活性,这与图4(a)的阴极极化曲线的结论是一致的.
一般电化学活性面积(ECSA)越大往往意味着催化活性越大.ECSA通常采用双电层微分电容法获得.ECSA与双电层电容(Cdl)成线性关系:ECSA=Cdl/Cs,Cs是光滑平面样品的比电容,大小通常取0.04 mF·cm-2.图6(a)~(c)为不同沉积电压条件下合成Ni-Fe-Sn 镀层在电压-0.468~-0.540 V vs.SCE不同扫描速率下的循环伏安曲线.
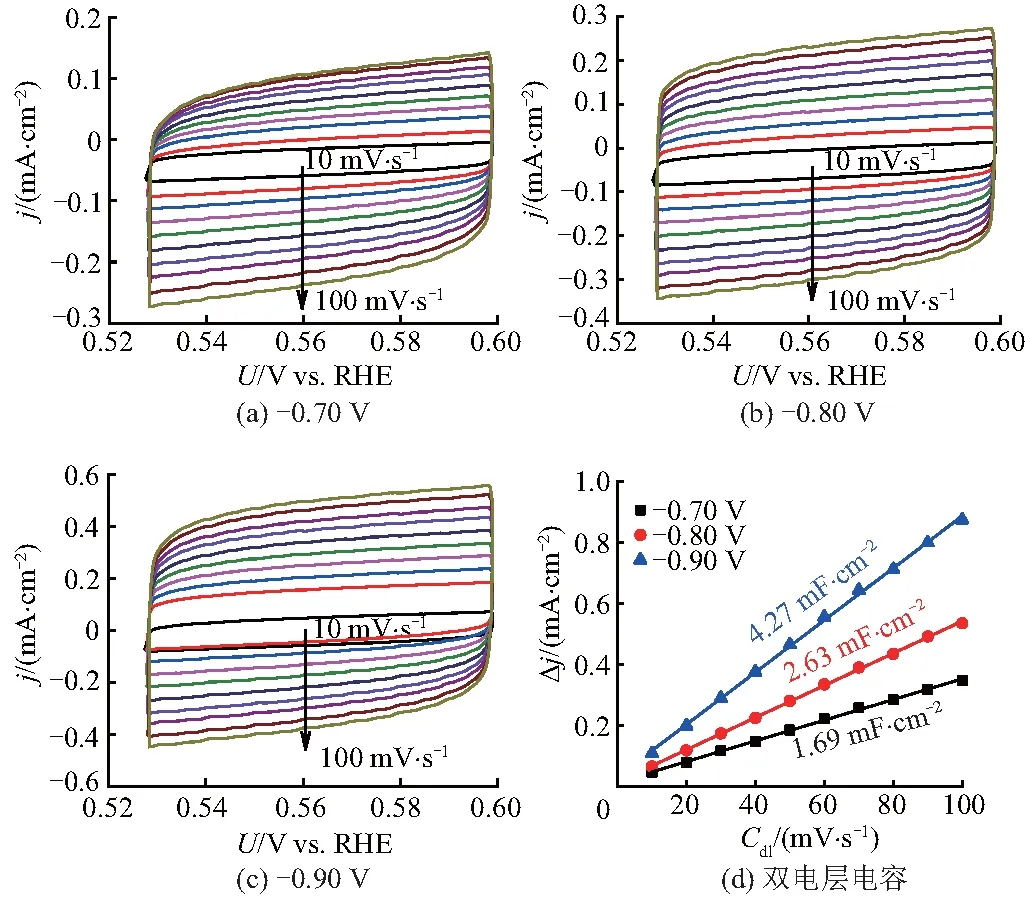
图6 不同扫描速率下Ni-Fe-Sn镀层的CV曲线及双电层电容值
图6(d)为Ni-Fe-Sn 镀层在-0.014 V时的电流密度(Δj=ja-jc)与扫描速率的关系曲线,曲线斜率值的一半即为Cdl值.由图可知,在-0.7,-0.8,-0.9 V 沉积电位条件下的Cdl值分别为1.69,2.63和4.27 mF·cm-2,表明当沉积电压为-0.9 V时,Ni-Fe-Sn镀层具有较大的ECSA,拥有更多的活性位点,这与图2中的SEM结果一致.
3 结论
文中以泡沫镍为载体,采用恒电位电沉积法制备了不同沉积电位条件下的Ni-Fe-Sn镀层,通过SEM、EDS、XRD、XPS和电化学测试技术等方法研究了镀层的微观形貌、晶型结构以及不同沉积电压条件下制备的镀层对其催化活性的影响.
Ni-Fe-Sn镀层具有良好的析氢性能.在1 mol·L-1KOH电解液中的过电位仅为62 mV(@10 mA·cm-2),并且表现出良好的电化学稳定性.表征结果表明:其优异的催化性能主要归因于大的电化学活性比表面积,暴露了更多的活性催化位点,促进电催化过程中的电子传递,从而增强了HER活性.研究结果将为探索具有更高活性的非贵金属基电解水催化剂的设计、构建提供新的思路和解决方案.

