CuO-CeO2/TiO2高效催化CO低温氧化反应性能
李润蕾,王子彦,王志苗,李芳,薛伟,赵新强,王延吉
(1 河北工业大学化工学院,天津 300401;2 中国船舶重工集团公司第七一八研究所,河北 邯郸 056027)
随着工业的飞速发展和人类社会生产活动的多样化,CO 排放量随之急剧增加,并成为了空气中的主要污染物之一。目前,CO的消除有直接燃烧、催化氧化[1-2]、超重力吸收[3]和固体吸附等方法,其中催化氧化法反应条件温和、净化能力强、绿色无二次污染、应用广泛,是最具发展潜力的CO 消除方法,催化氧化法的关键是催化剂的选择,因此选择和制备高活性的催化剂是研究的重点[3]。
CO 催化氧化反应使用的催化剂有贵金属和非贵金属两大类。目前,贵金属催化剂主要包括Au[4-6]、Pt[7]和Pd[8]等。贵金属催化剂虽具有优异的催化活性,但贵金属资源稀缺,成本较高,限制了其广泛应用。与贵金属催化剂相比,非贵金属催化剂价格便宜,且具有较好的催化活性和热稳定性,因而一直受到人们高度关注。目前,Co、Cu[9-10]、Ce[11-12]、Mn[13]等元素的氧化物被广泛应用于CO 催化氧化反应中,其中CuO-CeO2被认为是最有潜力替代贵金属的催化剂[14]。CuO-CeO2催化剂的高活性源于铜铈之间协同效应,有利于Cu2+/Cu+和Ce3+/Ce4+之间的氧化还原循环,这个循环被认为是CO 氧化反应的关键步骤[15-17]。此外,CeO2中存在的氧空位能够产生更多的活性氧,从而有利于氧化反应的进行[18]。
CuO-CeO2的制备方法有柠檬酸络合法、溶胶凝胶法[19]、浸渍法[19-20]、共沉淀法[19]和金属有机框架(MOFs)衍生法[21-27]等,不同制备方法会影响到其催化性能。与其他方法相比,MOFs 衍生法制备的CuO-CeO2催化剂具有较好的催化性能。这是由于在MOFs 中,金属离子被有机配体很好地分离,焙烧后有利于金属氧化物的分散,更利于CuO 和CeO2之间的相互作用,进而促进CO 氧化反应[21]。Zhang等[21]利用浸渍法将Ce(NO3)3浸渍在Cu3(BTC)2上,然后经焙烧制得CuO-CeO2。当Cu质量分数为5%、焙烧温度为600℃时,催化剂具有较好活性,100℃时可将CO[空速18000mL/(g·h)]完全转化。Gong等[25]利用水热法制备了CuxCe1-xBTC,将其在高温下焙烧制得CuO-CeO2。在650℃下、焙烧4h 所制得的Cu0.3Ce0.7O2活性最好,反应温度为80℃时,CO[空速60000mL/(g·h)]转化率为87%。
对于负载型催化剂而言,载体可提供较大的比表面积和适宜的孔结构,有助于活性组分的分散,此外,载体和活性组分的相互作用也会在一定程度上提高催化剂的活性。将活性组分负载在可还原金属氧化物(如TiO2、Fe2O3和CeO2)上通常表现出较高的CO 催化氧化性能,这是由于反应中载体被CO 部分还原,导致了金属-载体强相互作用所致。Huang 等[28]以TiO2为载体,制备了负载型CuO/TiO2催化剂,研究发现,以TiO2作为载体,CuO的活性得到增强,当CuO 负载量(质量分数,下同)为30%、煅烧温度为300℃时,催化剂表现出了最高的催化活性,可于140℃将CO 完全氧化。梁飞雪等[29]采用溶胶-凝胶法制备了一系列CeO2-TiO2复合氧化物,考察了其对CO 氧化反应的催化性能。1% CO 完全转化的温度高于260℃,并且复合氧化物催化活性要比单独CeO2或TiO2高。迄今为止,尚未有文献对TiO2负载CeO2-TiO2催化CO氧化反应进行研究。Li等[30]以TiO2为载体,制备了负载型催化剂CuO-CeO2/TiO2用于NO+Hg0氧化还原反应,发现在空速54000mL/(g·h),温度200~250℃条件下,NO 和Hg0的转化率均在85%以上。并根据一系列表征发现TiO2载体较小的晶粒尺寸可以更好地分散Cu 活性组分,并提升CeO2的储氧效果,使得催化剂具备较高的催化活性。且TiO2的引入使得催化剂更加稳定,反应后不易失活。
本文以TiO2为载体,利用等体积浸渍法制备了CuO-CeO2/TiO2催化剂用于催化CO氧化反应,考察了制备条件对其催化CO氧化反应性能的影响。
1 材料和方法
1.1 化学原料和试剂
Ce(NO3)3·6H2O,分析纯,天津市科密欧化学试剂有限公司;Cu(NO3)2·3H2O,分析纯,天津市科密欧化学试剂有限公司;纳米TiO2(锐钛矿),分析纯,上海麦克林生化科技有限公司;石英砂(350~833μm),分析纯,天津市百伦斯生物技术有限公司。
1.2 催化剂的制备
采用等体积浸渍法制备CuO-CeO2/TiO2催化剂。具体步骤如下:分别称取一定量的Cu(NO3)2·3H2O、Ce(NO3)3·6H2O 放入烧杯,加入蒸馏水,超声15min 使溶液充分混合溶解。取一定量的纳米TiO2装入梨形瓶中,逐滴加入上述溶液,静置24h。浸渍结束后,将样品置于旋转蒸发仪中在70℃下干燥1.5h,最后在马弗炉中焙烧制得CuO-CeO2/TiO2催化剂。
1.3 催化剂的表征
1.3.1 X射线衍射(XRD)
使用德国Bruker 公司生产的D8 FOCUS 型X 射线衍射仪进行催化剂及试剂样品的物相结构表征分析,仪器的测试条件为:使用Cu 靶;石墨单色滤光片;狭缝条件为SS/DS=1°,RS=0.15mm;工作管电压40kV,管电流40mA;扫描角度2θ=5°~90°;扫描速度为1°/min。采用Scherrer 公式计算催化剂样品的晶粒尺寸。采用TOPAS 精修软件来计算样品中CeO2的晶格常数。
1.3.2 N2等温吸附-脱附测试
采用美国Micromeritics 公司生产的ASAP 2020 M+C 型吸附仪测定催化剂的织构性质。样品的比表面积采用BET 方法计算,样品的平均孔容、平均孔径大小及分布数据使用BJH方法计算。
1.3.3 X射线光电子能谱(XPS)
使用美国Thermo Scientific 公司所生产的Escalab 250Xi型X射线光电子能谱仪对催化剂表面元素组成、价态分布及相对含量进行测定。使用Al Kα射线(hν=1486.6eV)作为测试激发源,采用200W功率及14.6kV电压。扫描结果以C 1s(284.8eV)进行校正。
1.3.4 程序升温还原(H2-TPR)
使用美国Micromeritics 公司生产的AutoChemⅡ-2920 型号装置进行样品的氢气程序升温还原(H2-TPR) 测试。在室温下将样品于Ar 气氛(50mL/min)中预处理10min,等待仪器平稳运行;随后转化使用H2/Ar混合气(50mL/min,10%/90%),采用10℃/min 的升温速率,对样品进行500℃范围内的程序升温还原测试,采用热导检测器(TCD)采集样品的H2消耗量数据。
1.4 催化剂的活性评价
采用常压固定床反应装置来进行CO 催化氧化反应测试,反应器内径11mm。将350~833μm的催化剂(0.5g)与350~833μm 的石英砂(0.5g)均匀混合,填入反应管固定测温区域,反应管其他部分填入350~833μm 的石英砂。使用混合气(CO 1%、O29%、N290%)为原料气体,流量为200mL/min,空速为24000mL/(g·h)。
使用配备TCD 的北分瑞利SP-3420A 型气相色谱仪进行在线气体分析。通过双色谱柱对气体产物进行分析:柱A 为5A 分子筛填充柱用于分离O2、N2和CO,柱B为Porapak Q填充柱用于分离CO2。
2 结果与讨论
2.1 负载量对CuO-CeO2/TiO2催化剂活性的影响
当nCe/nCu=1.6 时,考察了负载量对催化剂催化性能的影响,结果如图1所示。由图可知,负载量对催化剂的活性影响十分显著,随着负载量的提高,催化剂的催化性能提高,当负载量达到30%时,CuO-CeO2/TiO2催化剂的催化性能最佳,继续提高负载量,催化剂的催化活性反而下降,因此,最佳的负载量为30%。
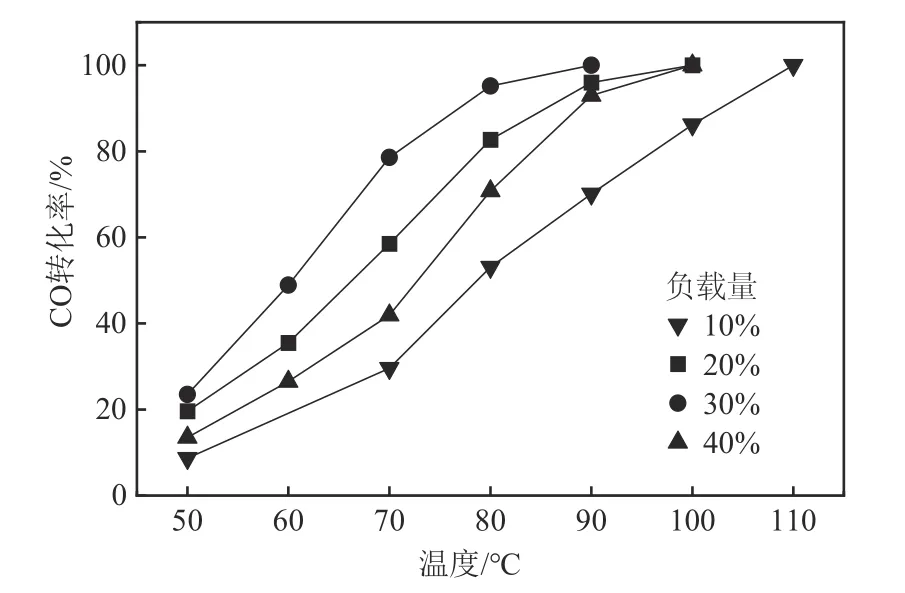
图1 不同负载量的CuO-CeO2/TiO2催化剂催化CO氧化反应性能
图2是不同负载量催化剂的XRD谱图。可以看出,谱图中出现了锐钛型TiO2衍射峰(PDF-#73-1764)和萤石CeO2的衍射峰(PDF-#34-0394),随着负载量的提高催化剂仍未出现CuO 的衍射峰,说明CuO高度分散在催化剂中[31]。计算了催化剂中CeO2的晶格常数及平均晶粒尺寸,结果列于表1(编号1 和编号2),结果表明,CeO2的晶粒尺寸随着负载量的增大呈现出增大的趋势,这说明低负载量时,CeO2可更好地分散在载体表面。此外,随负载量提高,CeO2的晶格常数随之下降,说明铜离子进入了CeO2晶格中产生了晶格收缩,表明CuO和CeO2之间相互作用增强。
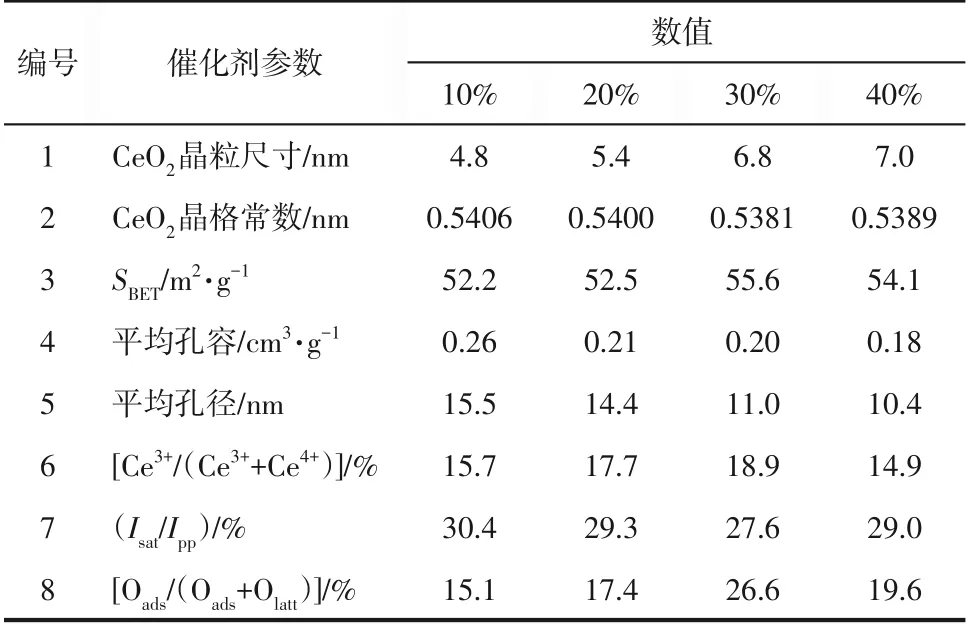
表1 不同负载量CuO-CeO2/TiO2催化剂的物化性质
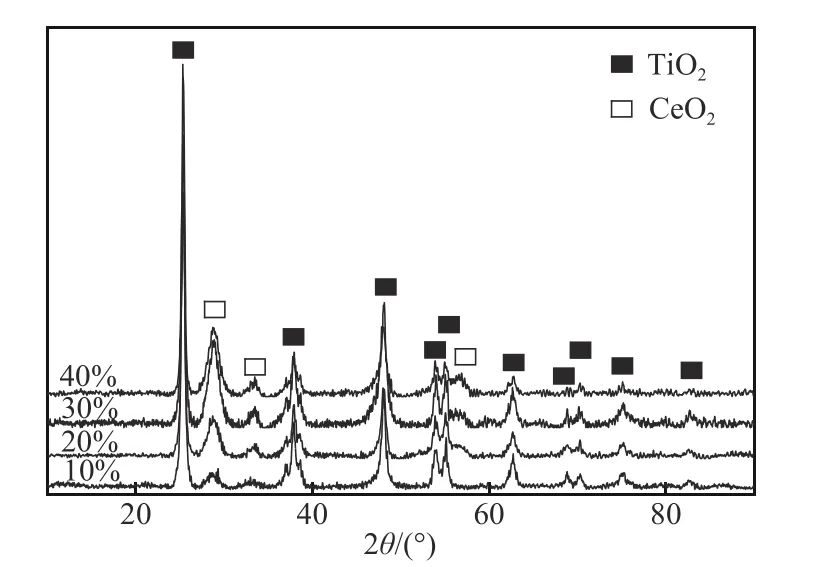
图2 不同负载量的CuO-CeO2/TiO2催化剂XRD谱图
对不同负载量催化剂的物化性质进行了表征,结果见表1(编号3~编号5)。可以看出,随着负载量的增大,催化剂的平均孔径有所下降,而比表面积和平均孔容变化不明显。由图1可知,不同负载量催化剂的催化活性具有明显差异,这说明比表面积的大小并不是影响该催化剂活性的主要因素。
为探究催化剂活性差异原因,进一步对催化剂进行XPS表征。图3(a)为催化剂的Ce 3d谱图,估算了催化剂表面Ce3+含量,结果见表1(编号6)。可以看出,催化剂表面的Ce3+含量首先随着负载量的增加而增加,负载量为30%的催化剂其表面的Ce3+元素含量最高,继续增加负载量到40%,催化剂表面的Ce3+含量明显降低。图3(b)为不同负载量的催化剂的Cu 2p谱图,计算了卫星峰强度与主峰强度的比值(Isat/Ipp)来判断Cu物种的化学价态[32],结果列于表1(编号7)。若Isat/Ipp小于0.55,表明催化剂表面存在Cu+物种,该比值越小,则催化剂表面Cu+的含量越高。由结果可知,负载量为30%的催化剂其Isat/Ipp比值最小,说明其表面具有更多Cu+。图3(c)是催化剂的O 1s 谱图,图中出现了晶格氧(Olatt)和表面吸附氧(Oads)的特征峰,计算了催化剂表面吸附氧含量,结果列于表1(编号8)。可以看出,催化剂的负载量对其表面吸附氧含量影响显著,随催化剂负载量的提高,其表面吸附氧含量明显提高,当负载量为30%时,催化剂表面吸附氧含量最高,继续增加负载量,表面吸附氧含量反而有所下降。
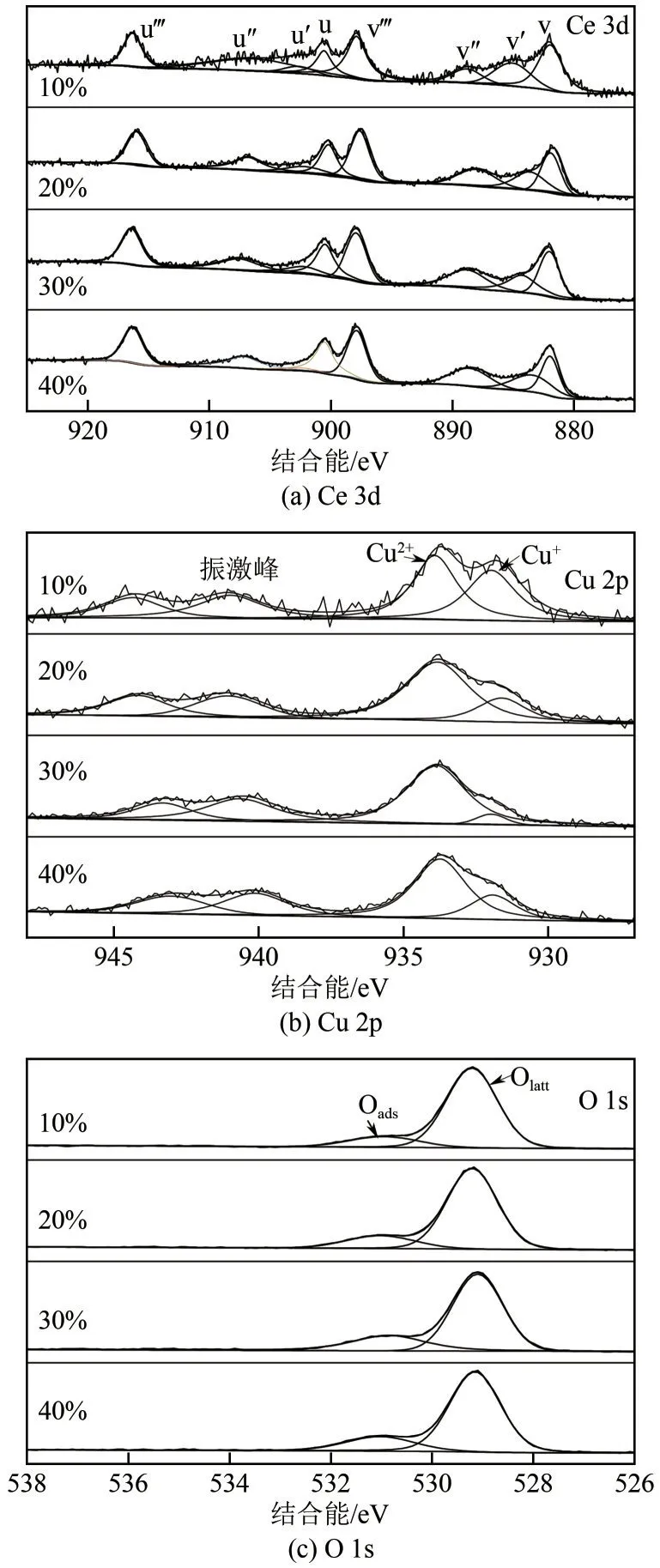
图3 不同负载量催化剂XPS谱图
图4 为不同负载量催化剂的H2-TPR 曲线。可以看出,图中也出现了Cu 物种的α、β 两个还原峰,并且随着负载量的增大,α、β 两个还原峰向低温移动,当负载量为30%时,其还原温度最低,负载量升至40%时,α、β 两个还原峰反而向高温移动。由此可知,负载量为30%的CuO-CeO2/TiO2催化剂还原温度最低,这说明该催化剂更容易还原。同时由XPS 表征可知,其表面吸附氧以及Cu+和Ce3+含量也最高,因此具有较好的催化性能。
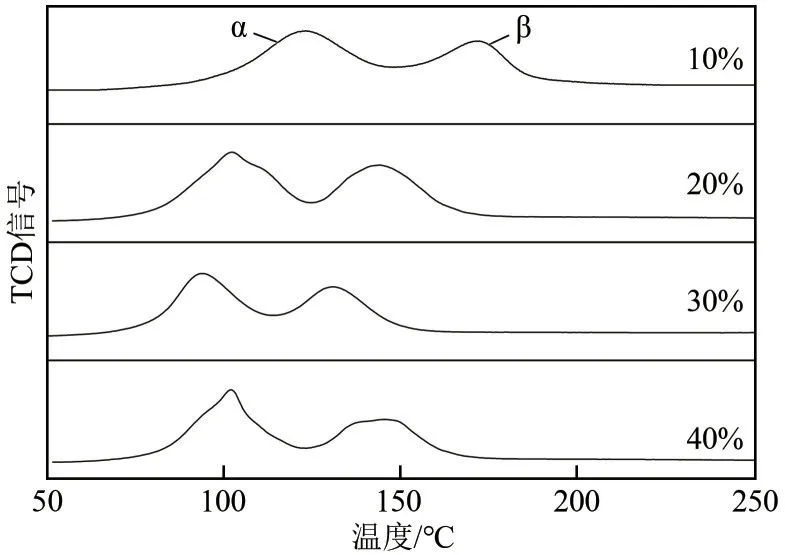
图4 不同负载量催化剂的H2-TPR曲线
图5为不同负载量CuO-CeO2/TiO2催化剂的O2-程序升温脱附(TPD)曲线。图中α、β 峰分别为过氧物种O2-(ad)和表面吸附氧O-(ad)的特征峰[33]。可以看出,随着负载量的增加,两个氧物种的脱附温度向低温偏移,在负载量为30%时,氧物种脱附温度最低,负载量升至40%时,O2-(ad)和O-(ad)脱附峰反而向高温区域移动。低温脱附氧物种的存在以及O2-和O-的低温脱附能力,更有利于表面氧的吸附,氧化还原反应也更易进行[34],这是负载量为30%催化剂具有优异的催化性能的原因之一。

图5 不同负载量催化剂的O2-TPD曲线
2.2 焙烧温度对CuO-CeO2/TiO2 催化剂活性的影响
考察了焙烧温度对催化剂催化CO 反应性能的影响,结果如图6所示。可以看出,随着焙烧温度的提高,催化剂的催化活性随之提高,当焙烧温度为500℃时,催化剂具有最佳的催化活性;在90℃,就可将CO 完全转化;继续升温到600℃,催化剂的催化活性反而降低。
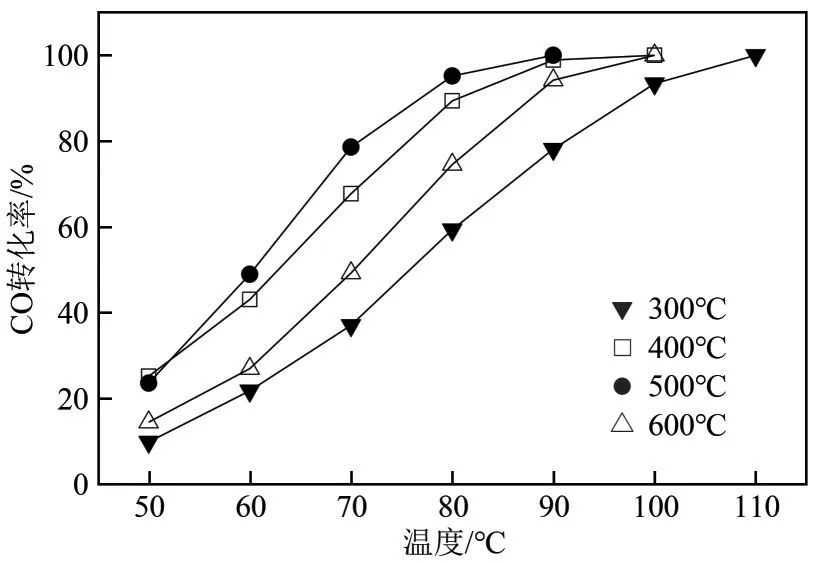
图6 不同焙烧温度的CuO-CeO2/TiO2催化剂催化CO氧化反应性能
图7为不同焙烧温度下催化剂的XRD谱图。可以看出,谱图中均出现了锐钛型TiO2衍射峰(PDF-#73-1764)和萤石CeO2的衍射峰(PDF-#34-0394),并且仍未发现CuO 的衍射峰。计算了催化剂中CeO2的晶格常数及平均晶粒尺寸,结果见表2(编号1、编号2)。可以看出,当焙烧温度在300~500℃时,CeO2的晶粒尺寸变化不大,当焙烧温度提升至600℃后,CeO2的晶粒明显变大。此外,随着焙烧温度的提高,CeO2的晶格常数随之降低,这说明升高焙烧温度会使得更多Cu2+掺杂到CeO2晶格中,从而产生晶格收缩[35-36]。
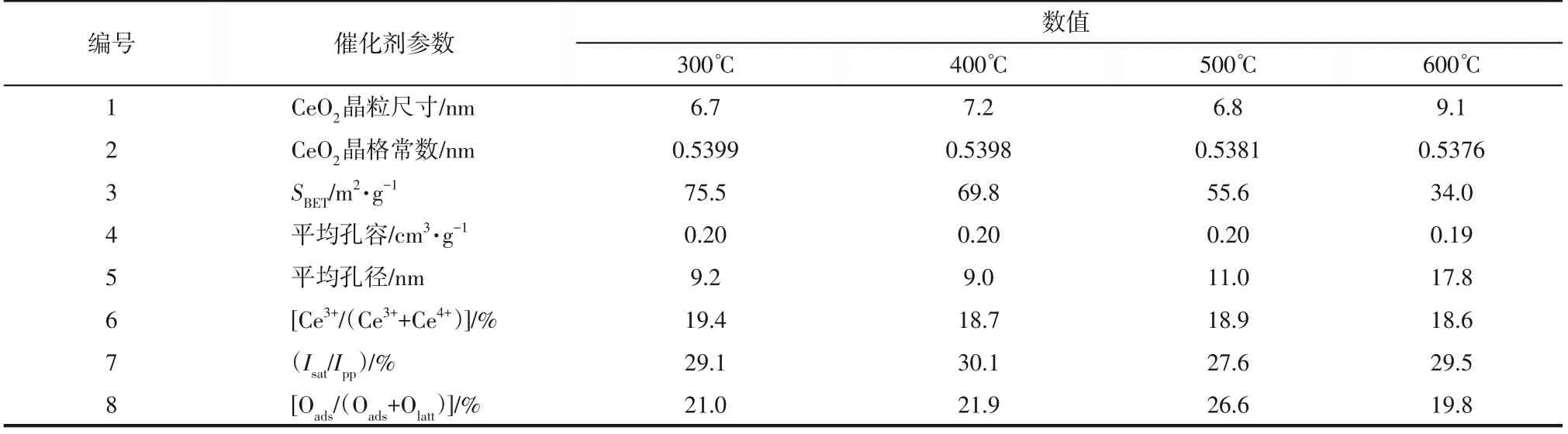
表2 不同焙烧温度CuO-CeO2/TiO2催化剂的物化性质
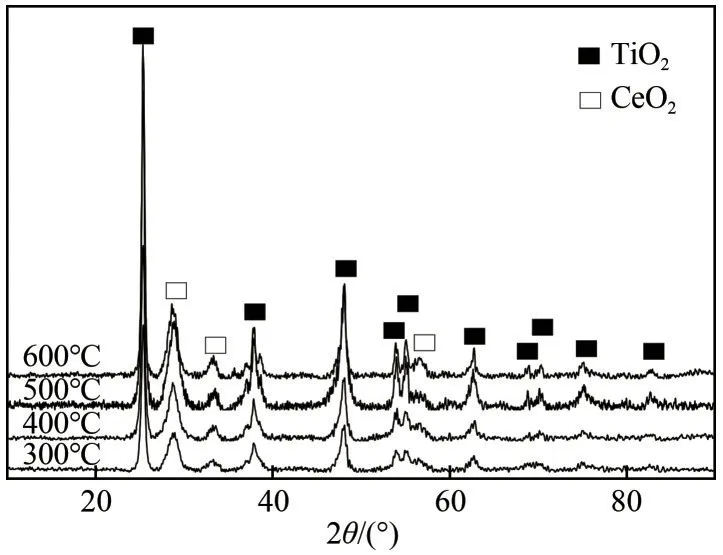
图7 不同焙烧温度的CuO-CeO2/TiO2催化剂XRD谱图
由表2(编号3~编号5)可以看出,随焙烧温度的提高,催化剂的比表面积减小,催化剂的平均孔径明显变大,而平均孔容无明显变化。500℃下焙烧的催化剂比表面积并非最高,却具有最佳的催化活性,这也同样说明了比表面积和孔结构并不是影响该催化剂活性的主要因素。
图8为催化剂的XPS谱图,分别计算了催化剂表面Ce3+含量、Isat/Ipp比值和表面吸附氧的含量,结果见表2(编号6~编号8)。可以看出不同焙烧温度下制备的催化剂表面Ce3+含量接近,这说明焙烧温度对催化剂Ce3+含量影响不明显。此外,500℃下焙烧的催化剂Isat/Ipp较小,说明其表面Cu+的含量相对较多,同时其表面吸附氧含量也较高。
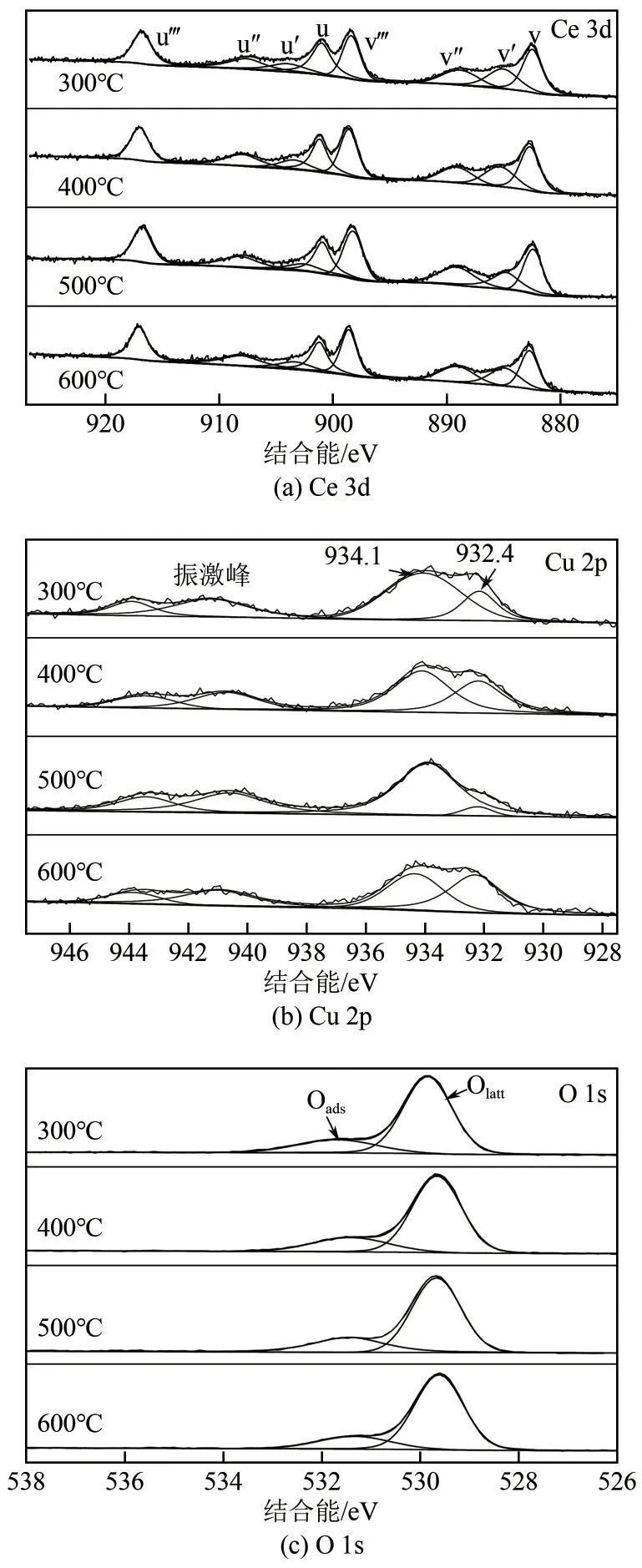
图8 不同焙烧温度催化剂XPS谱图
XPS测定的吸附氧的含量和90℃反应条件下催化剂表面吸附氧的含量有一定的差异,具体表现在XPS 测定的为新鲜催化剂表面吸附氧的含量。在CO氧化反应过程中,表面吸附氧参与了CO氧化的过程,同时原料气中氧气也会转化形成吸附氧。在反应过程中,表面吸附氧的含量是变化的,这就导致了上述差异的发生。
图9为不同焙烧温度下催化剂的H2-TPR曲线。可以看出,随着焙烧温度的提高,催化剂中α和β峰的还原温度向低温移动,500℃下焙烧的催化剂还原峰的还原温度最低,当焙烧温度升温至600℃,催化剂的还原温度明显上升,并且其α 峰面积减少,β峰峰面积增大。这说明焙烧温度过高,高分散铜物种含量明显变少,由表2(编号2)的结果可知,更多的铜物种进入CeO2晶格。上述结果表明,焙烧温度可以显著影响铜物种在催化剂中的分散,500℃焙烧的催化剂中铜物种的分散程度更好,更容易还原,同时由XPS 表征可知,500℃焙烧的催化剂其Cu+的含量和表面吸附氧含量也较高,故具有较好的催化活性。

图9 不同焙烧温度催化剂的H2-TPR曲线
2.3 nCe/nCu对CuO-CeO2/TiO2催化剂活性的影响
当催化剂的负载量为30%时,考察了不同铈铜摩尔比(nCe/nCu)对CuO-CeO2/TiO2催化活性的影响,结果如图10所示。可以看出,随着nCe/nCu的增加,催化剂活性随之增强,当nCe/nCu=1.6 时,其催化活性最好,继续增大nCe/nCu,催化剂的活性反而下降。
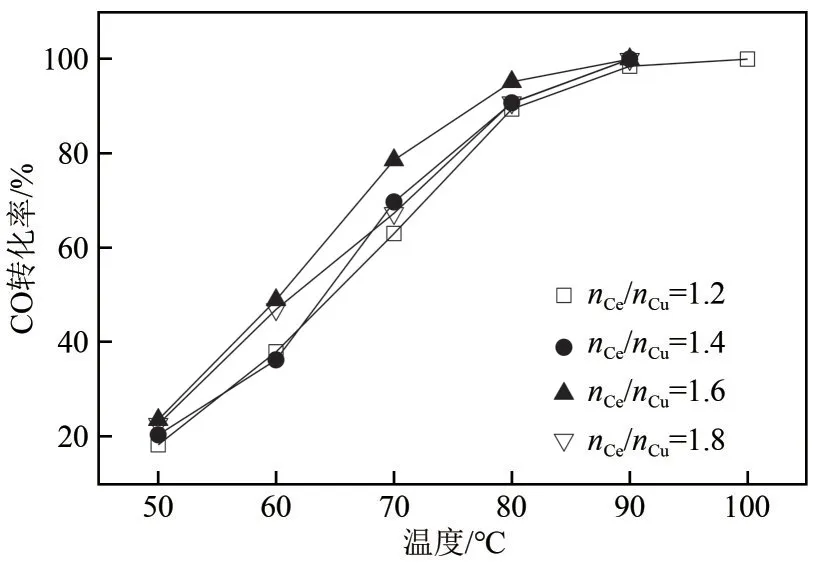
图10 不同nCe/nCu的CuO-CeO2/TiO2催化剂催化CO氧化反应性能
表3(编号3~编号5)列出了不同铈铜摩尔比催化剂的结构性质。可以看出,当nCe/nCu=1.2 时,催化剂的比表面积和孔容最小,孔径最大;当nCe/nCu=1.4时,催化剂的比表面积和孔容有所增大,孔径变小,继续增大nCe/nCu,催化剂的比表面积、孔容和孔径变化不明显。
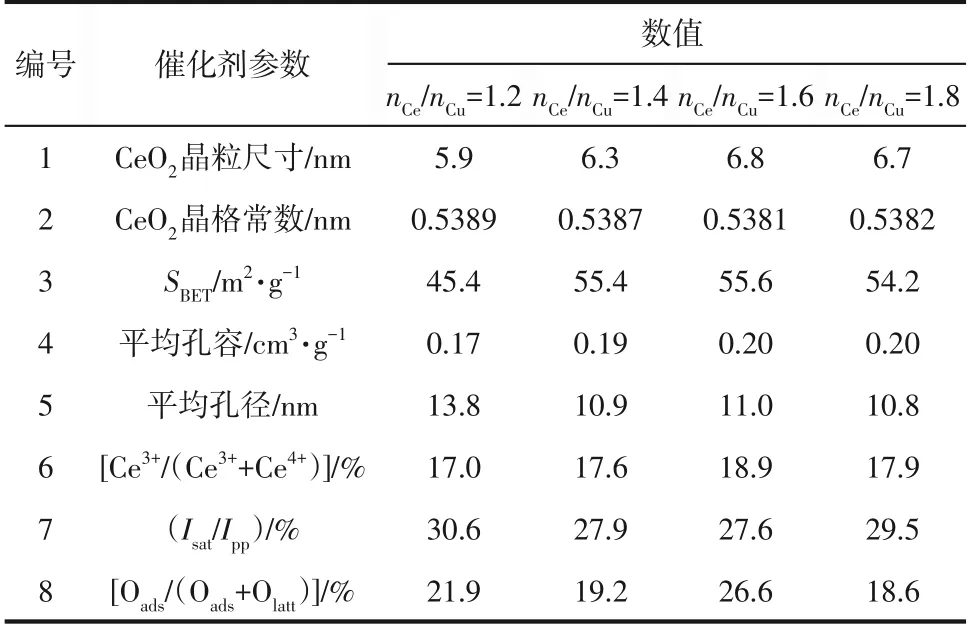
表3 不同nCe/nCu的CuO-CeO2/TiO2催化剂的物化性质
图11 为不同nCe/nCu的CuO-CeO2/TiO2催化剂的XRD 谱图。可以看出,催化剂均出现了锐钛型TiO2(PDF-#73-1764) 和萤石型CeO2的衍射峰(PDF-#34-0394),并且均未观察到CuO 衍射峰,这表明CuO 在上述催化剂中都高度分散。根据XRD谱图分别计算了不同nCe/nCu催化剂中CeO2的平均晶粒尺寸及晶格常数,结果列于表3(编号1、编号2)。可以看出,nCe/nCu对催化剂中CeO2晶粒尺寸的影响不大,均在6nm左右;不同铈铜摩尔比的CuO-CeO2/TiO2催化剂,其CeO2的晶格常数接近,且均小于纯净CeO2的晶格常数(0.5414nm)[37]。这是由于Cu2+半径(0.073nm) 小于Ce3+(半径为0.110nm)或Ce4+(半径为0.097nm),部分Cu2+可掺杂到CeO2晶格中,取代了部分Ce3+或Ce4+,导致晶格收缩[37]。

图11 不同铈铜摩尔比的CuO-CeO2/TiO2催化剂XRD谱图
利用XPS 对催化剂进行表征,结果如图12 所示。图12(a)为催化剂的Ce 3d谱图,将Ce 3d谱图分为两组共8 个峰,一组标记为v、v′、v″、v‴对应于Ce 3d5/2轨道峰;一组标记为u、u′、u″、u‴对应于Ce 3d3/2轨道峰,谱图中明显出现的v′和u′峰表示催化剂表面Ce3+元素的存在[38],Ce3+产生的原因可能为CeO2与周围金属氧化物的相互作用,导致晶格氧的转移,进而产生晶格缺陷[39],通过v′和u′峰面积所占总峰面积比来估算催化剂表面Ce3+质量分数,如式(1)。
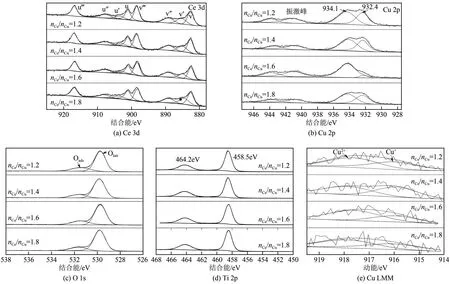
图12 不同nCe/nCu催化剂XPS谱图
式中,∑S(u)+(v)为v、v′、v″、v‴与u、u′、u″、u‴8 个峰的峰面积之和;S(v′)与S(u′)分别对应v′和u′峰的峰面积。
表3(编号6)给出了不同铈铜摩尔比催化剂表面Ce3+的质量分数。可以看出,当nCe/nCu在1.2~1.8 之间变化时,催化剂表面的Ce3+质量分数变化不大。纯CeO2中Ce3+的质量分数为6.75%,上述催化剂表面的Ce3+质量分数均远高于其CeO2中Ce3+的量,Ce3+的质量分数高会利于形成更多的Ce3+与Ce4+的配对来参与的氧化还原循环,产生更多的氧空位,提高催化剂储存-释放氧的能力,进而提升催化剂催化氧化消除CO 反应的性能[18]。
图12(b)为催化剂的Cu 2p XPS 谱图,结合能在934.1eV 出现的谱峰以及946~938eV 范围内出现的卫星峰,说明催化剂中存在CuO[37]。而结合能为932.4eV的谱峰则说明催化剂中还存在低价态的Cu+或Cu0物种,因二者的特征峰位置比较接近,为了区分二者,需要借助X 射线激发的俄歇电子谱线Cu LMM,结果如图12(e)所示,916eV左右的特征峰归属于Cu+,而917.5eV 左右的特征峰则归属于Cu2+,这说明催化剂中低价态的Cu 物种为Cu+。而Cu+的存在主要归因于氧化还原平衡向右移动[40]。此外,催化剂表面Cu 物种的还原程度可以通过计算卫星峰与主峰强度的比值(Isat/Ipp)进行比较,该比值越小,则催化剂表面Cu+的含量越高。由表3(编号7)给出的计算结果可知,nCe/nCu=1.6 的催化剂其Isat/Ipp比值最低,这说明其表面含有更多的Cu+。
图12(c)为催化剂的O 1s 谱图,图中529~530eV 范围的谱峰对应于催化剂表面晶格氧(Olatt)的特征峰,530~531eV范围的峰则为催化剂的表面吸附氧(Oads)的特征峰[40-41]。计算了催化剂表面吸附氧占总氧含量(Olatt+Oads)的比值,结果列于表3。可以看出,nCe/nCu=1.6 时,催化剂的表面吸附氧含量最高,而与晶格氧相比,表面吸附氧更容易发生迁移,在氧化还原反应中性质更加活泼,更容易参与反应的进行,从而大大提高催化剂催化CO 氧化反应的性能[42]。
图12(d)为催化剂的Ti 2p 谱图。结合能为464.2eV 和458.5eV 的谱峰分别对应于Ti4+的Ti 2p1/2和Ti 2p3/2,图中并未观察到Ti3+或Ti2+的特征峰,这说明不同nCe/nCu并未对催化剂表面Ti 的价态产生影响。
图13为不同催化剂的H2-TPR曲线,从图中可以看出CuO-CeO2/TiO2催化剂具有α、β 两种Cu 物种的还原峰,还原温度较低的α还原峰归属于催化剂中高度分散的铜物种;β还原峰归属于进入CeO2晶格或与CeO2有弱相互作用的铜物种[10],其中高度分散的铜物种可与CeO2产生强烈的相互作用,使得CuO-CeO2/TiO2催化剂具有更好的氧化还原活性[32]。由图13 可以看出,当nCe/nCu=1.6 时,催化剂的还原温度最低,这说明该催化剂更容易还原。结合XPS表征可知该催化剂还含有更多的表面吸附氧以及更多的Cu+,因此具有较好的催化性能。
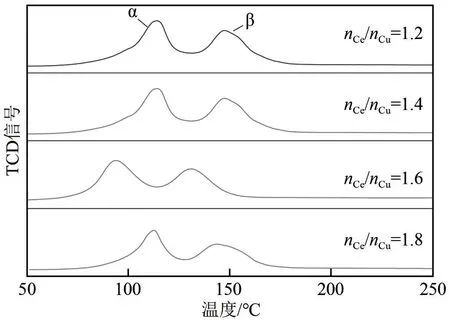
图13 不同nCe/nCu催化剂的H2-TPR曲线
2.4 催化剂对比
将本研究中的催化剂与近三年文献中催化剂进行对比,各项数据列于表4中。尽管每种催化剂的评价条件不同,但本研究中的CuO-CeO2/TiO2催化剂可以在90℃将CO 完全转化,显示出较高的催化活性。

表4 不同催化剂催化氧化CO的性能表现
3 结论
(1)以锐钛型TiO2为载体,利用等体积浸渍法制备了CuO-CeO2/TiO2催化剂,发现当nCe/nCu为1.6,负载量为30%,经500℃焙烧4h后制得的催化剂活性最佳,当空速为24000mL/(g·h),该催化剂可在90℃将CO完全氧化。
(2)探究了制备条件对CuO-CeO2/TiO2催化剂的影响,发现负载量对催化剂表面Ce3+、Cu+和表面吸附氧含量的影响较为明显,而nCe/nCu和焙烧温度仅影响催化剂表面Cu+和吸附氧的含量。活性评价结果显示,CuO-CeO2/TiO2催化剂表面较高的Ce3+、Cu+和表面吸附氧含量有利于CO 氧化反应的进行。
(3)与文献中的非贵金属催化剂进行了对比,本研究中CuO-CeO2/TiO2催化剂活性更高,有望替代成本高昂的贵金属催化剂,用于大气污染治理。

