重组人血管内皮抑制素注射液联合同步放化疗治疗晚期非小细胞肺癌患者的疗效和安全性*
黄小平,范运秀
(重庆大学附属三峡医院肿瘤中心,重庆 404100)
肺癌是我国乃至全球男性发病率和死亡率均位居第1位的恶性肿瘤,严重威胁人们健康和生命[1-2]。肺癌有非小细胞肺癌(NSCLC)和小细胞肺癌2种主要的病理类型,其中NSCLC约占84%,且恶性程度高、预后差[3-4]。抗血管生成治疗的特异性和选择性使其成为近年来肿瘤治疗中发展最迅速的研究领域之一。1997年O′REILLY等[5]发现内皮抑素能特异性地抑制血管内皮细胞增殖,从而抑制肿瘤生长。
重组人血管内皮抑制素注射液由内皮抑素肽链于N 端加9个氨基酸组成。有研究表明,重组人血管内皮抑制素注射液与化疗联合使用显著提高了晚期NSCLC的疗效[6-7]。陈明等[8]研究结果显示,重组人血管内皮抑制素注射液使用后5~7 d,荷瘤小鼠移植瘤血管出现正常化现象,移植瘤乏氧细胞比例降低,以第3~7天显著,但持续使用重组人血管内皮抑制素注射液9 d后,肿瘤血管退化,血管正常化现象不明显。进一步的研究结果显示,经重组人血管内皮抑制素注射液处理后肿瘤出现的血管正常化时间窗内,联合放疗能为NSCLC患者带来最佳获益。近年来,重组人血管内皮抑制素注射液联合同步放化疗用于局部晚期肺癌、食管癌、鼻咽癌等肿瘤的研究已初步取得一定的临床进展[9-11]。本研究采用重组人血管内皮抑制素注射液联合同步放化疗治疗晚期NSCLC者,旨在探讨其临床疗效及安全性,现报道如下。
1 资料与方法
1.1资料
1.1.1一般资料 选取2019年9月至2021年11月重庆大学附属三峡医院肿瘤中心收治的分期为Ⅲa~Ⅳa期的NSCLC患者42例,按随机数字表法将其分为对照组和观察组,各21例。观察组年龄20~70岁,平均(55.81±2.94)岁;病理类型:鳞癌7例,腺癌13例,腺鳞癌1例;NSCLC癌分期:Ⅲa期7例,Ⅲb期6例,Ⅲc期5例,Ⅳa期3例。对照组年龄19~59岁,平均(54.93±3.10)岁;病理类型:鳞癌6例,腺癌14例,腺鳞癌1例;NSCLC癌分期:Ⅲa期6例,Ⅲb期7例,Ⅲc期5例,Ⅳa期3例。本研究获医院伦理委员会批准,2组一般资料比较,差异无统计学意义(P>0.05)。
1.1.2纳入与排除标准 纳入标准:(1)经病理组织学、细胞学确诊的初治NSCLC患者;(2)第8版AJCC/UICC临床分期Ⅲa~Ⅳa期;(3)年龄18~70岁,性别不限,预计生存期12周及以上;(4)所有患者都应该有可测量的或可评估的目标病灶;(5)能进食流质饮食以上;(6)体力状况评分(PS评分)0~1分;(7)正常的器官功能:血小板大于100 000/mm3,血红蛋白高于10 g/dL,中性粒细胞高于1.5×103/mm3,血清肌酐低于2.5 mg/dL,胆红素及谷丙转氨酶(AST)或谷草转氨酶(ALT)低于正常上限的2倍,肺功能第1秒用力呼气容积(FEV1)≥1 L,且超过健康人群相应值的40%;(8)签署知情同意书。排除标准:(1)有明确的紫杉醇过敏史;(2)曾患其他恶性肿瘤(除了非黑色素性皮肤癌或子宫颈原位癌);(3)孕妇或哺乳妇女及治疗观察期内拒绝避孕的女性;(4)患者临床上有明显的肝脏疾病;(5)有严重肺部或心脏疾病病史者;(6)拒绝或不能签署知情同意书;(7)滥用药物或酒精成瘾者;(8)有体格或精神疾患,无民事行为能力或限制民事行为能力者;(9)患有难以控制的严重感染;(10)既往使用过其他抗表皮生长因子受体(EGFR)单抗者;(11)在30 d内接受过其他的临床试验药物者。剔除标准:(1)试验期未按规定用药及未能完成计划80%的患者;(2)违反研究方案的要求;(3)数据记录质量差,资料不完整、不准确。
1.2方法
1.2.1治疗方法 对照组采用同步放化疗,治疗方案为患者入院5~6 d后给予放疗60 Gy/30F,放疗采用三维适形或调强技术;从放疗第1天同步化疗,具体方案:紫杉醇150 mg/m2静脉滴注d1+顺铂75 mg/m2静脉滴注或d1~2,分2次给药,每个周期间隔3周。研究组采用同步放化疗联合重组人血管内皮抑制素注射液治疗,放化疗方案同对照组,具体使用方案为105/5d W0、2、4、6给予重组人血管内皮抑制素注射液静脉滴注,静脉泵24 h持续滴注,连续5 d,隔9天继续使用,首次化疗在使用重组人血管内皮抑制素注射液5 d后。对照组同步放化疗后休息3周后继续行巩固化疗2个周期,方案同上,每个周期间隔3周。观察组化疗联合重组人血管内皮抑制素注射液 15 mg/(m2·d7)隔3周1次,2周期,化疗方案同对照组。巩固化疗结束后4周行颈部+胸部+上腹部增强CT等检查评价最终疗效。此后随访:第1年每3个月进行1次,第2年每4个月进行1次,第3年以后每6个月进行1次。
1.2.2观察指标 疗效评估标准:所有患者接受同步放化疗及巩固治疗2周期后,根据实体瘤的疗效评价标准(RECIST 1.1)评估近期疗效,包括完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),其中总有效率(RR)=(CR例数+PR例数)/总例数×100%,无效率=(SD例数+PD例数)/总例数×100%;局部/区域无进展生存期(PFS)定义为从治疗开始日至记录到肿瘤局部/区域进展或随访截止时的时间;肿瘤局部/区域进展日期是指检查(包括影像学、活检等)确定肿瘤局部/区域进展的日期。不良反应评估标准:参照国际通用不良反应标准3.0版[11]评估各组患者治疗中、后不良反应发生情况。
1.3统计学处理 应用SPSS20.0软件进行数据分析,近期疗效及不良反应发生率的比较采用χ2检验或Fisher′s精确检验。无疾病进展生存率和总生存率的估计采用Kaplan-Meier法分析,计算并报告具有临床反应的患者比例及其95%可信区间。P<0.05为差异有统计学意义。
2 结 果
2.12组患者近期疗效比较 观察组近期疗效总有效率为95.24%(20/21),显著高于对照组的66.67%(14/21),差异有统计学意义(χ2=5.559,P=0.018)。见表1。
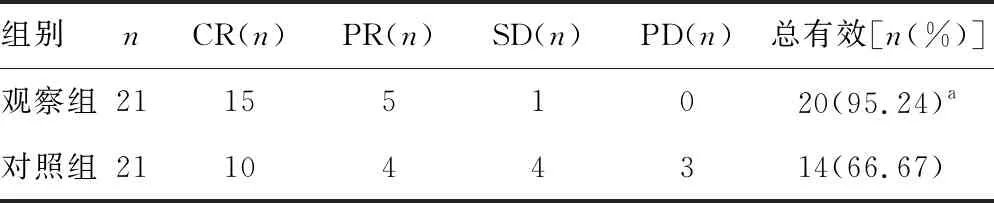
表1 近期疗效比较
2.22组患者远期疗效对比 观察组显著改善肺癌的生存及治疗预后,其中位PFS较对照组延长6.1个月,差异有统计学意义(P<0.05)。中位总生存期(OS)尚未达到。见图1。

图1 2组患者远期疗效对比
2.32组患者不良反应发生率比较 观察组不良反应发生率为14.29%,对照组为42.86%,差异有统计学意义(P<0.05),其中观察组恶心呕吐、过敏反应发生率较对照组低。见表2。

表2 2组患者不良反应发生率比较
3 讨 论
肺癌是一个全球性的健康问题,根据全球癌症统计数据,肺癌是目前发病率第2和死亡率第1的恶性肿瘤,每年估计有超过200万人被新诊断为肺癌,其中NSCLC占80%~85%[12]。约一半的新肺癌病例发生在亚洲,而中国肺癌新发病例数持续上升[13]。NSCLC的确诊主要依靠X射线和CT,而超过70%的NSCLC患者确诊时已为晚期(Ⅲa期以上),对于这部分患者而言,手术治疗机会渺茫,好在NSCLC对于化疗较为敏感。但随着时代的发展,人们对于个性化治疗的需求越来越高,在保证疗效的同时,还要提高患者的生存质量。
诱导血管生成是癌症的标志之一,因此,抗肿瘤血管生成已成为当前癌症研究的一个重要领域。1997年,O′REILLY等[5]首次报道了一种新蛋白,称为内皮抑素,是胶原X型Ⅷ羧基末端的20×103内部片段,在血管内皮瘤细胞的条件培养基中作为抗血管生成分子。重组人血管内皮抑制素注射液是一种重组人内皮抑素,几项临床试验已证明,重组人血管内皮抑制素注射液联合铂类化疗可以提高NSCLC疗效[14]。也有研究表明,在NSCLC中使用重组人血管内皮抑制素注射液联合同步放化疗可获得更好的生存率和局部控制,且无严重不良事件[9]。HELPER STUDY共入组了73例不可手术切除的Ⅲa及Ⅲb期NSCLC患者,揭示了静脉输液泵注重组人血管内皮抑制素注射液联合同步放化疗治疗局部晚期NSCLC(不可切除的Ⅲ期NSCLC)具有较好的近期疗效,且其不良反应发生率较低[9]。在局部晚期NSCLC患者使用重组人血管内皮抑制素注射液联合同步放化疗已有相关报道,然而局晚期NSCLC外,更晚期的患者是否能获益尚鲜有报道。本研究结合真实世界情况,参考HELPER STUDY的基础上,扩大入组患者分期至Ⅲa~Ⅳa期,且在同步放化疗结束后增加重组人血管内皮抑制素注射液再联合化疗巩固治疗,旨在探索重组人血管内皮抑制素注射液联合放化疗与单纯标准放化疗治疗晚期NSCLC患者的疗效和安全性。
研究表明,在Lewis肺癌中,重组人血管内皮抑制素注射液可通过调节血管内皮生长因子与血小板反应素-1之间的平衡来提高化疗的抗肿瘤疗效[15]。同时,重组人血管内皮抑制素注射液也被证明是治疗NSCLC的有效和安全的药物[16]。荟萃分析也表明,重组人血管内皮抑制素注射液联合化疗可改善晚期NSCLC患者的疗效和预后,而不会增加毒性风险[17]。在本研究中,观察组患者在采取同步放化疗联合重组人血管内皮抑制素注射液治疗后的近期疗效为95.24%,显著高于仅行同步放化疗的对照组患者的66.67%。观察组患者的长期疗效——中位PFS相比于对照组患者延长6.1个月(P<0.05)。本研究中,观察组患者治疗后的不良反应发生率(14.29%)显著低于对照组(42.86%)。不良反应中较为严重的是放射性肺炎,一项系统综述表明,在接受同步放化疗的不能切除的Ⅲ期NSCLC患者中,严重和致命放射性肺炎的发生率在3.62%~7.85%[18]。尽管在本研究中未观察到放射性肺炎,但根据总体不良反应发生率可估计使用重组人血管内皮抑制素注射液联合同步放化疗可降低放射性肺炎发生率。同时本研究结果还显示,观察组患者恶心呕吐、血小板减少等不良反应也显著降低,大大提高了肺癌患者的生存质量。
综合上述研究结果,晚期NSCLC患者可以从重组人血管内皮抑制素注射液联合同步放化疗治疗中的获益显著优于仅行同步放化疗,具有重要的临床价值,值得进一步探索和推广。此外,本研究仍存在样本量较小、单中心取样等局限性,后期将扩大样本量,探究相关生物标志物变化,深入研究重组人血管内皮抑制素注射液联合放化疗治疗晚期NSCLC的作用机制,为临床用药提供参考。

