程序升温热解过程中高挥发分煤对高硫焦煤硫迁移的影响
张晋玲,郑雨嘉,元宁
(清华大学山西清洁能源研究院,山西 太原 030032)
煤炭的清洁高效利用,对于实现双碳目标意义重大[1-2]。热解是煤炭利用的重要技术[3],煤在高温环境下发生反应,生成煤气、焦油和焦炭[4-5]。硫是煤炭中的一种重要元素[6-7],了解硫元素的迁移转化机理,指导煤热解过程中硫迁移行为的调控,对煤炭的清洁高效利用尤为重要[8]。
升温速率和方式会影响热解产物的产率[9-11]。程序升温煤的一次热解产物与煤粒接触时间变长,增加活性挥发物二次反应的机会[12]。我们前己研究了在快速升温热解过程中,硫的迁移行为[13]。本研究将通过程序升温-恒温热解实验,考察高硫煤在不同配比下热解过程中的硫变迁基本规律。
1 实验部分
1.1 材料与仪器
高有机硫焦煤(Coal A新阳煤);高挥发分低硫烟煤(Coal B,大同煤);其工业分析、元素分析及形态硫分析分别见表1、表2。

表1 实验所用煤的工业分析和元素分析Table 1 Proximate and ultimate analyses of samples used in experiment
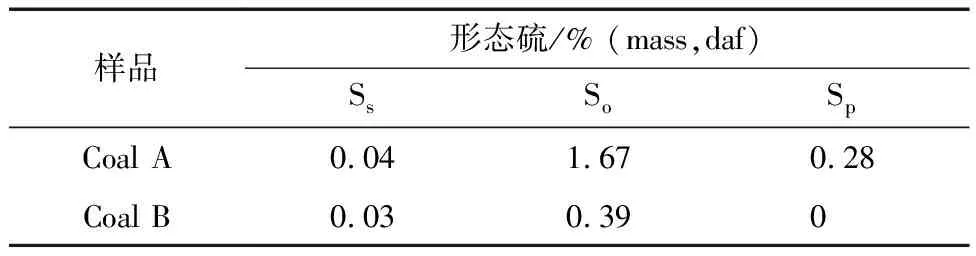
表2 实验用煤形态硫分析Table 2 Sulfur forms of coal samples by chemical analyses
Hiden QIC-20四极质谱分析仪;GC-950气相色谱仪;HCS系列高频红外碳硫分析仪。
1.2 实验方法
煤样经过破碎、研磨、筛分后,选择粒径0.106~0.150 mm的两种样品开展实验。实验采用固定床石英反应器,见图1。该反应器结构为两段式三管,可以用于解析两种煤共热解过程对硫迁移的影响。
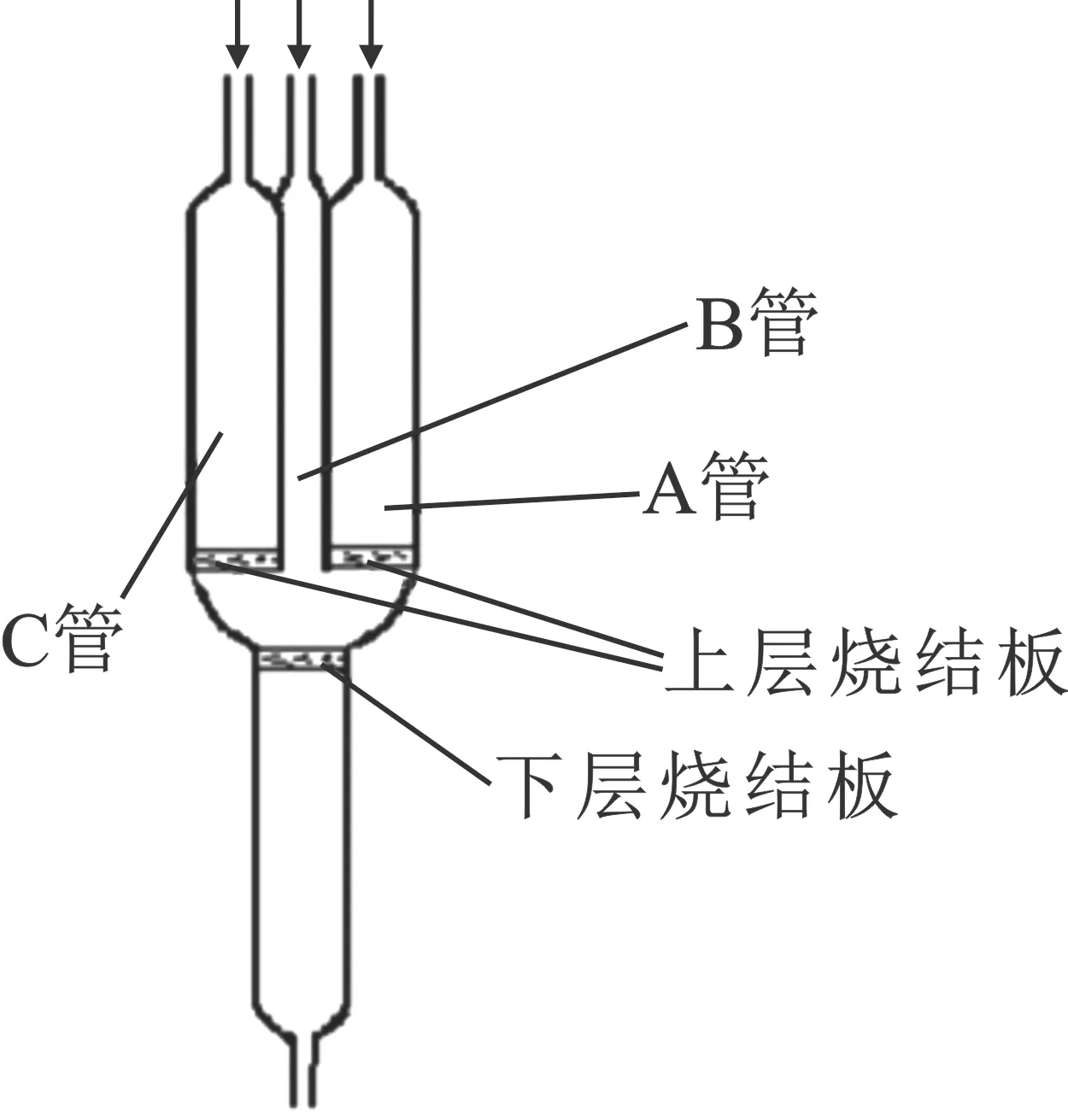
图1 固定床石英反应器示意图Fig.1 A schematic diagram of the fixed-bed quartz reactor
对Coal A和Coal B以不同比例进行混合,得到混合煤样“BL”(Coal A∶Coal B分别为,0∶1,1∶1,1.5∶1,2∶1,3∶1,5∶1,1∶0)。将约2 g的样品通过B管进样至下层烧结板,以10 ℃/min的升温速率从室温升至1 000 ℃。用质谱进行在线检测,并用气相色谱对气体中的H2S,COS的含量进行定量分析检测。
为了进一步揭示Coal A和Coal B在程序升温热解过程中对硫迁移影响的机制,按照不同配比的BL中Coal A和Coal B的质量,将一定质量的Coal A和Coal B分别放置到上层烧结板和下层烧结板上,进行程序升温热解实验,以考察Coal A的挥发分对Coal B的热解行为的影响(记为“ATB”);反之,改变Coal A和Coal B的位置,将Coal B放置到上层烧结板上,Coal A放置到下层烧结板上,记为”BTA”;最后,将一定质量的Coal A和Coal B分别放置在上层两个烧结板上,进行程序升温热解实验(记为“AAB”),试图揭示Coal A和Coal B在热解过程中挥发分的相互作用。
2 结果与讨论
2.1 程序升温共热解过程对总挥发分和焦油产率的影响
图2为两种煤不同比例混合下进行程序升温热解过程半焦和焦油的产率。以单独热解Coal A 和Coal B时半焦和焦油产率的加权值作为计算值。
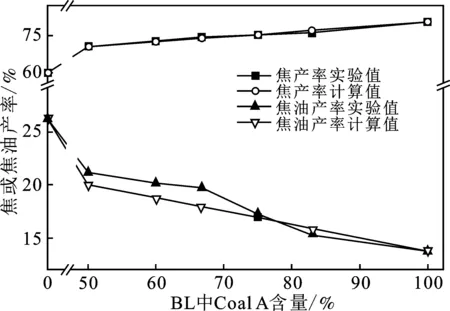
图2 Coal A和Coal B混合物共热解焦样和焦油产率Fig.2 Yields of char and tar during co-pyrolysis of BL
由图2可知,Coal A 含量在66.7%时,焦油产率与计算值差值最大,表明Coal A和Coal B的混合物在共热解的过程中发生了相互作用,使得Coal A 含量在50%~66.7%时,增加了焦油的产率,且Coal A 含量为66.7%时,这种促进作用最明显。
2.2 程序升温共热解过程对含氢气体释放的影响
2.2.1 程序升温共热解过程H2S释放趋势 煤中挥发分的释放随着温度的升高而增加,煤中的含硫化合物随着挥发分的释放而释放,同时使不同形态的硫分解而释放出来。图3是在程序升温共热解过程中,不同配比的混合煤样共热解过程中H2S的释放强度随温度变化的曲线。
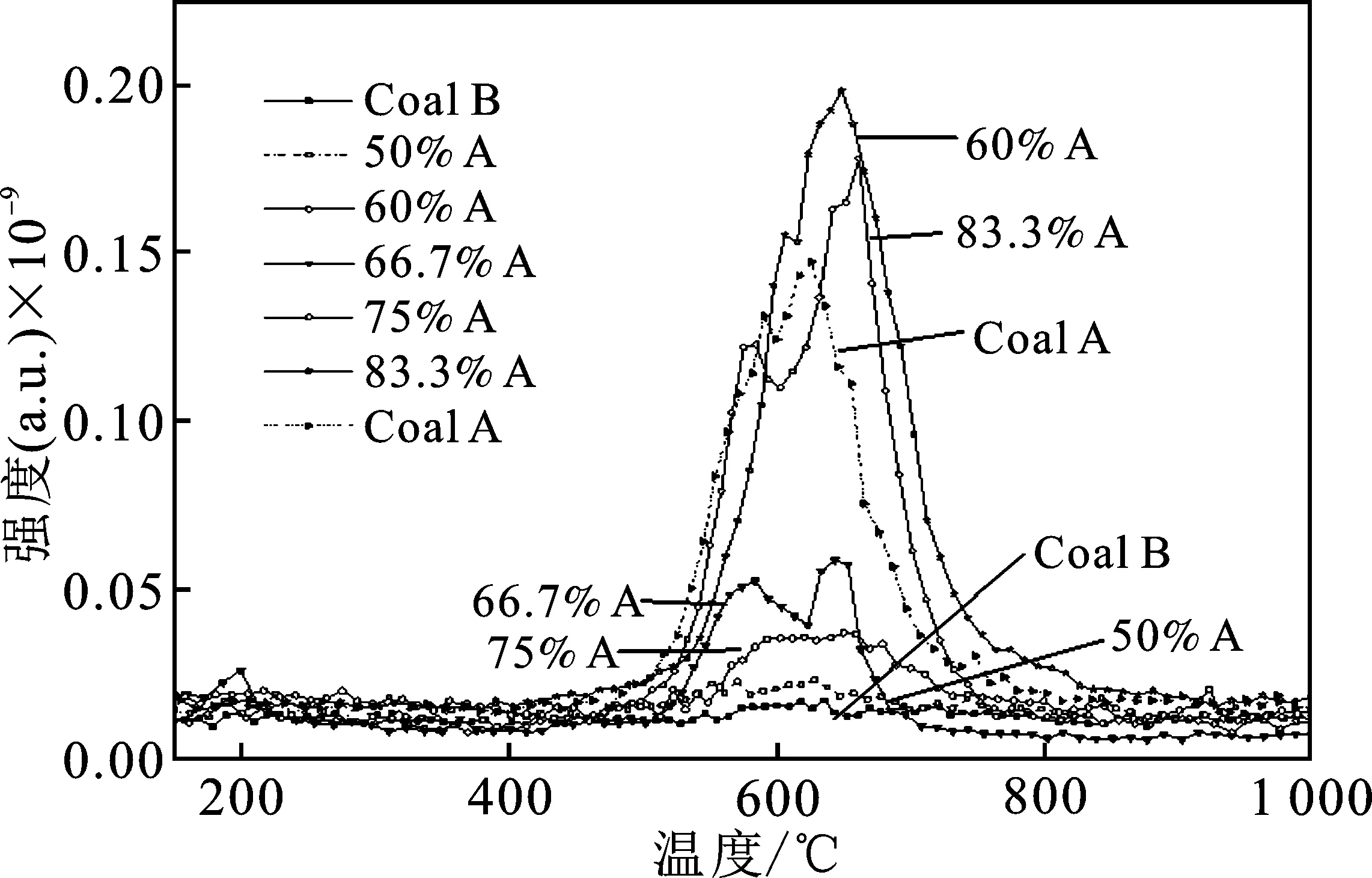
图3 Coal A与Coal B混合共热解过程中H2S的释放曲线Fig.3 Releasing curves of H2S during coal pyrolysis of BL experiment
由图3可知,程序升温热解过程中,Coal A 的H2S释放量远大于Coal B。Coal A 在500 ℃ 时H2S开始释放,而且在650 ℃时释放量达到最大,共热解过程中Coal A含量为60%时H2S的释放达到最大值。
由图4气相色谱测得含硫气体的量可知,H2S 的最大释放值出现在Coal A含量为60%时。H2S是由含氢自由基与煤中的含硫化合物分解的含硫基团结合而成,所以H2S的含量与热解过程挥发分中可以释放出的含氢自由基多少以及能结合的含硫基团数量有关。
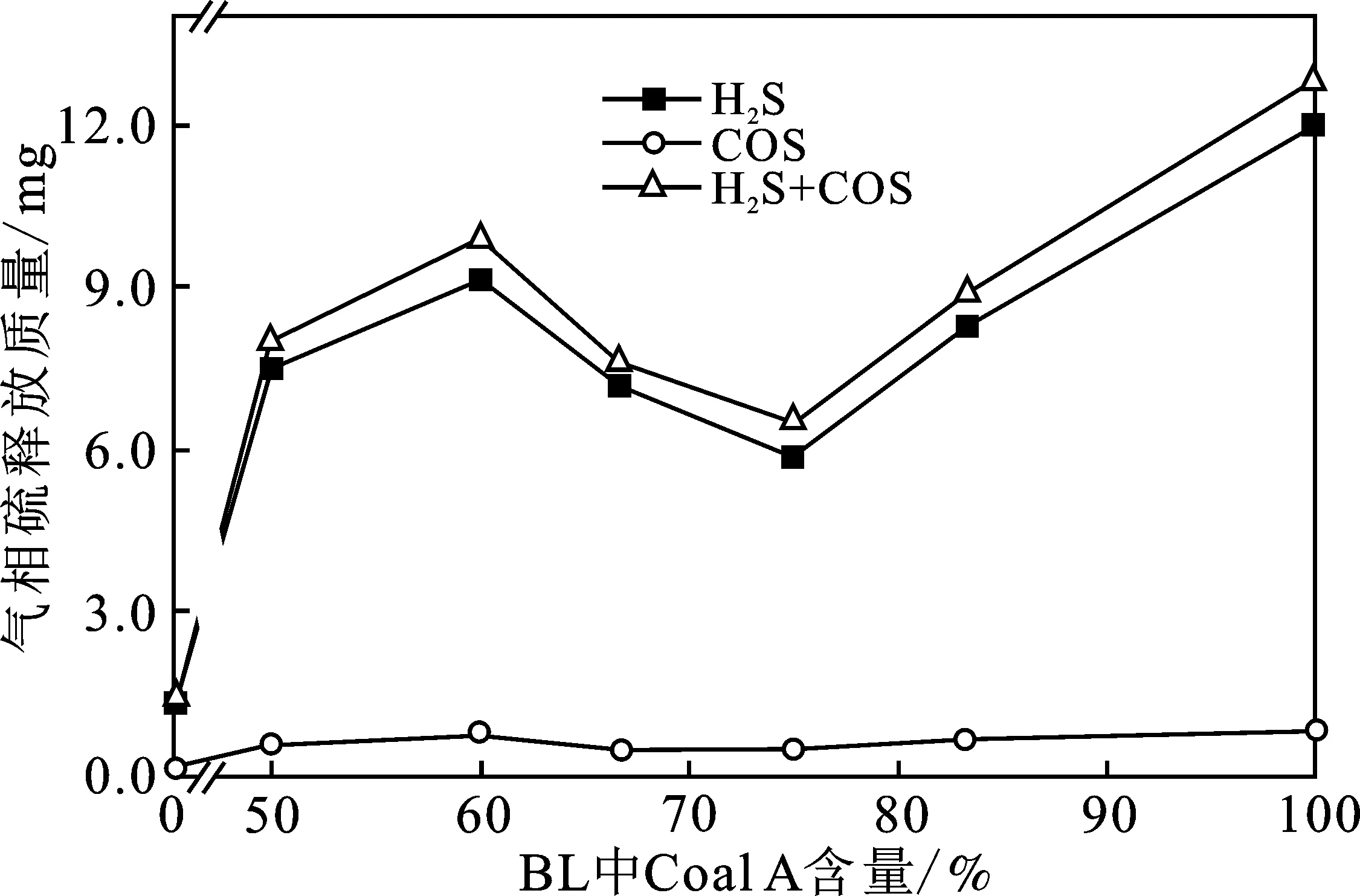
图4 BL共热解实验过程中H2S和COS释放质量Fig.4 Releasing amount of H2S and COS during co-pyrolysis of BL
2.2.2 程序升温共热解过程H2/CH4的释放趋势 H2一部分来源于高温下Coal A 以及Coal B 大分子结构的芳环缩聚反应,一部分来源于挥发分中重质大分子碳氢液相产物和轻质碳氢气相产物之间的二次反应[14-15]。图5是热解过程中氢气和甲烷的释放曲线。
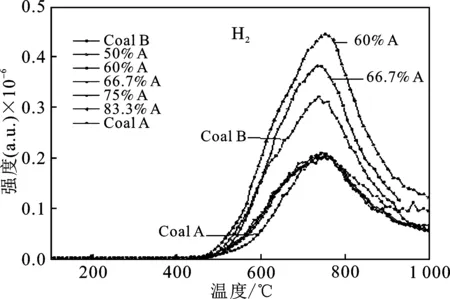
图5 BL程序升温共热解中H2和CH4的释放曲线Fig.5 Releasing curves of H2 and CH4 during co-pyrolysis of BL
由图5可知,Coal A 和Coal B 的H2释放曲线只有一个峰值,500 ℃时开始有H2的释放,在750 ℃ 左右出现最大释放峰,到1 000 ℃仍然有H2释放。
Coal B的H2释放量明显大于Coal A,CH4在400 ℃左右开始释放,500 ℃左右出现最大释放峰,800 ℃基本没有CH4的释放。Coal B的CH4释放量明显大于Coal A 的CH4释放量。
由图6可知,H2和CH4的积分面积图趋势相似,对比图4可知,H2/CH4半定量与H2S的释放趋势图一致,这表明共热解过程中H2S的释放量的大小与含氢气体H2和CH4的释放行为有关。
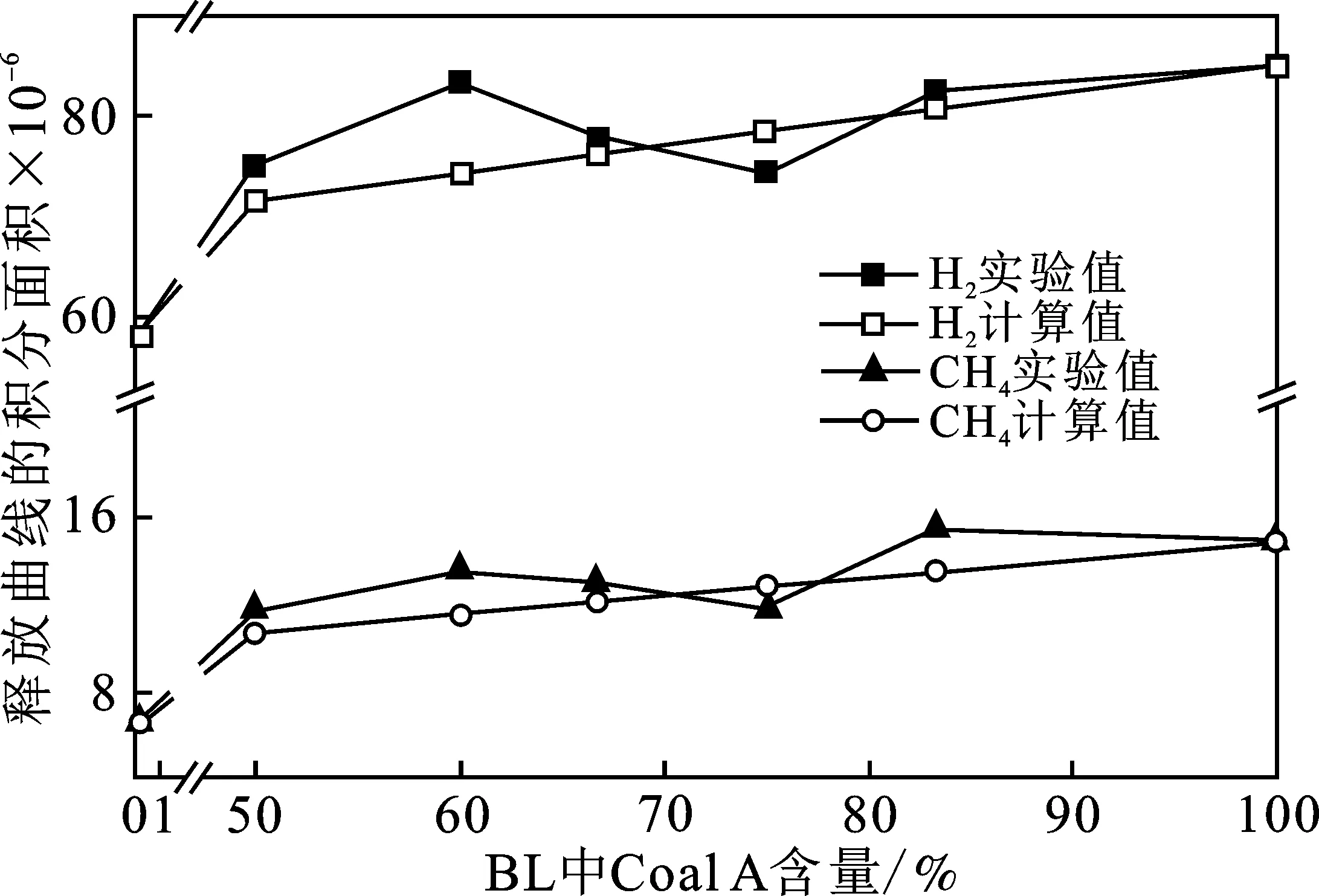
图6 BL程序升温共热解中H2和CH4的释放曲线Fig.6 Intergral areas of H2 and CH4 during co-pyrolysis of BL
2.3 程序升温共热解过程对含氧气体释放的影响
2.3.1 程序升温共热解过程COS的释放趋势 图7为BL热解过程中Coal A 与Coal B的COS释放曲线图。
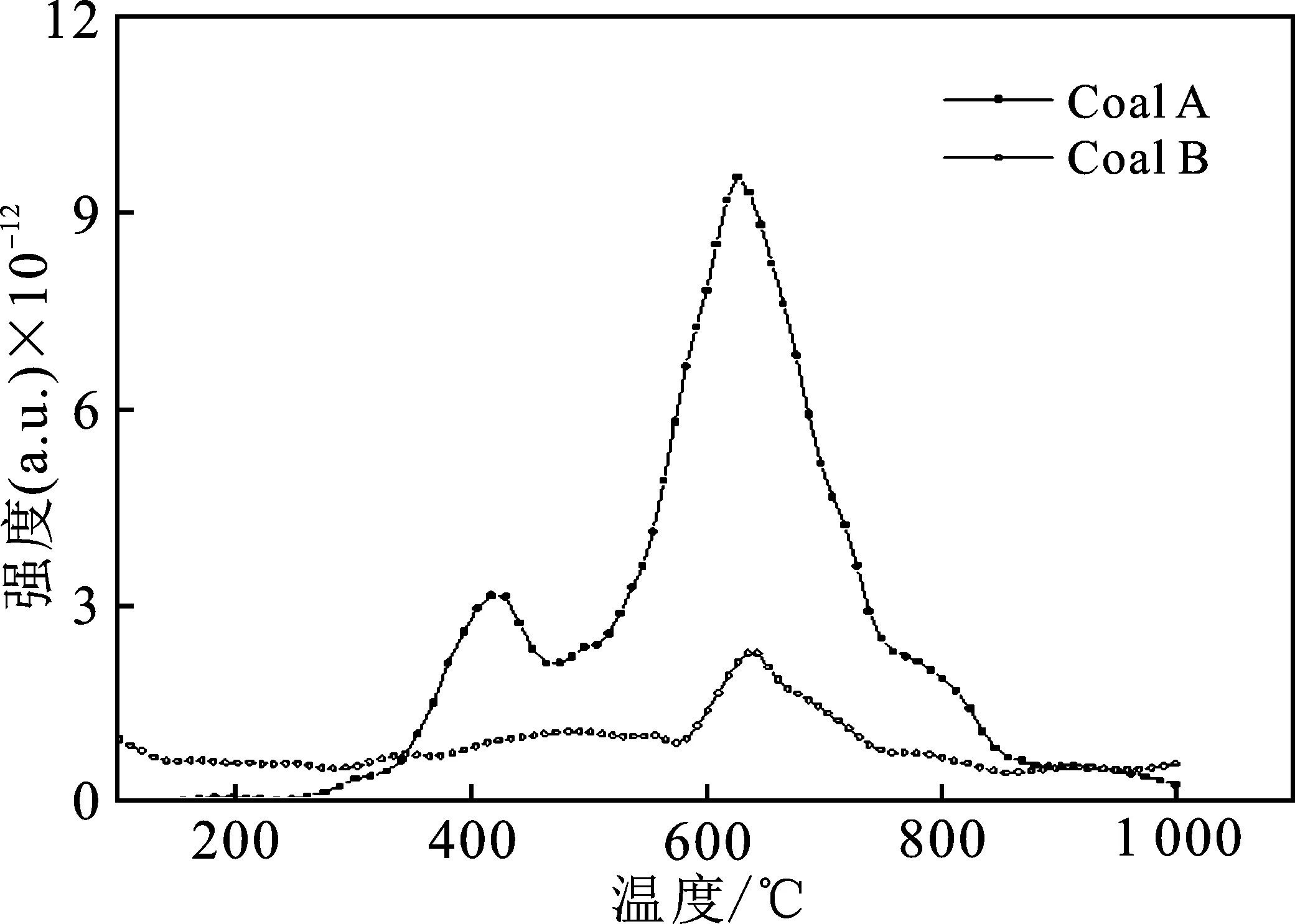
图7 BL热解过程中Coal A和Coal B的COS释放曲线Fig.7 COS releasing curves of Coal A or Coal B during BL pyrolysis
由图7可知,Coal A 有两个COS的峰,400 ℃时有一个小峰,650 ℃左右有一个大峰;Coal B仅在650 ℃左右呈现一个COS峰。对比图7与图3可知,Coal A在400 ℃没有H2S释放峰,然而存在COS释放峰,而Coal B在400 ℃没有COS峰,此处的COS释放峰应归因于分解的硫铁矿与CO或CO2的反应所生成,由于Coal B中不含硫铁矿,因此在400 ℃ 没有出现COS的释放峰。Coal A和Coal B在650 ℃都有COS峰和H2S峰,这表明COS主要来自于H2S与含氧基团或者含氧气体的二次反应。
2.3.2 程序升温共热解过程CO/CO2的释放趋势 含氧基团可以促进COS的生成,为了进一步观察含氧基团对热解过程中硫变迁的影响,对CO和CO2的释放进行了研究。煤中的CO和CO2主要来自于煤中的含氧官能团,比如羟基、羧基、酮类、醚类以及酯类。图8为BL热解过程中CO和CO2的释放曲线。
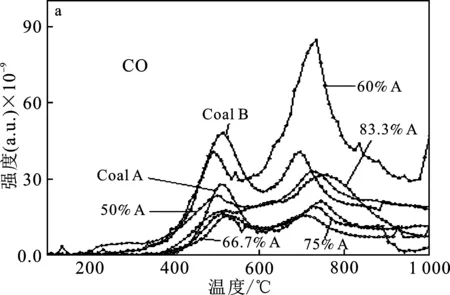
图8 BL共热解过程中CO和CO2的释放曲线Fig.8 Releasing curves of CO and CO2 during co-pyrolysis of BL
由图8可知,Coal A和Coal B都有两个CO释放峰,Coal A从400 ℃左右开始有CO的释放,第1个CO峰位置在550 ℃左右,第2个CO释放峰也是最大释放峰在700 ℃左右;Coal B的两个CO释放峰,位置与Coal A的峰位置相同,只是Coal B在低温区550 ℃处的释放峰高于第2个释放峰,且Coal B的两个峰大于Coal A的对应峰,这表明两种煤的CO 应该是来源于同种含氧基团。
由图8b BL混合热解过程中CO2释放随温度的变化趋势可知,Coal A呈现两个CO2峰,第1个峰在500 ℃左右,该峰值较低,在700 ℃出现最大释放峰。Coal B从200 ℃热解开始释放CO2,到800 ℃基本释放完全,峰值出现在500 ℃左右。很明显,Coal B的CO2释放量远大于Coal A。
为了进一步说明热解过程中释放的CO与CO2量与热解释放COS的关系,对图8中CO和CO2的释放曲线图进行积分处理,结果见图9。
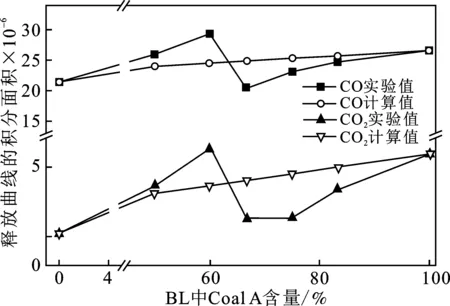
图9 BL共热解过程中CO和CO2的释放曲线Fig.9 Intergral areas of CO and CO2 during co-pyrolysis of BL
由图9可知,Coal A 含量在50%~60%时,实验过程中释放的CO和CO2大于计算值。
对比图4中COS的释放量曲线,可知与CO和CO2释放趋势基本相同,且COS的释放趋势基本与H2S的释放趋势类似,热解过程中COS的量远低于H2S的量。
2.4 程序升温共热解过程中硫在气相和固相中的分布
图10为BL共热解过程中硫在气相和固相中的分布。煤中的硫含量是通过元素分析计算而得到,通过Coal A和Coal B的元素分析加权计算得到它们不同配比的硫含量;焦中的硫则是通过碳硫分析仪测得。

图10 BL共热解过程中硫在气相和固相中的分布Fig.10 Sulfur distribution in gas and solid during co-pyrolysis of BL
由图10可知,气相与固相中硫的分布均与计算值不同,而且焦中的硫都比计算值低,这说明在BL热解过程中,硫的迁移使硫更多以挥发分释放。
Coal A含量在50%~66.7%时,BL在程序升温热解过程中硫在气相中的分布大于计算值,这是由于在热解过程中高挥发Coal B提供的含氢自由基与Coal A中的含硫基团结合,生成气相硫释放;随着Coal A含量的继续增加,Coal B减少,硫在气相以及半焦中的分布都小于计算值,这应该是由于硫以大分子形式存在没有分解而冷凝在焦油中引起的。
2.5 Coal A与Coal B程序升温共热解过程的解析实验
2.5.1 两种煤程序升温共热解解析实验中气体硫含量的分析 从前面分析可知,Coal A与Coal B之间发生的相互反应使得硫在气相、焦油以及焦中的分布不同于它们的计算值。BL共热解过程中除了煤本身的热解以外,存在着3种可能导致硫迁移的相互影响的反应:(1)Coal A的挥发分与Coal B煤本体的反应(ATB);(2)Coal B的挥发分与Coal A煤本体的反应(BTA);(3)Coal A 的挥发分与Coal B的挥发分之间的反应(AAB)。针对这些反应过程,设计了三组对比解析实验。虽然热解解析实验与BL共热解过程不能等同,但是也可以从这些实验数据中获得一些引起硫迁移反应机理的一些重要依据。图11为不同解析实验和BL实验中H2S的释放量,前面已经提到H2S为热解过程产生的主要含硫气体,因此H2S释放量基本可以表明含硫气体的分布规律。
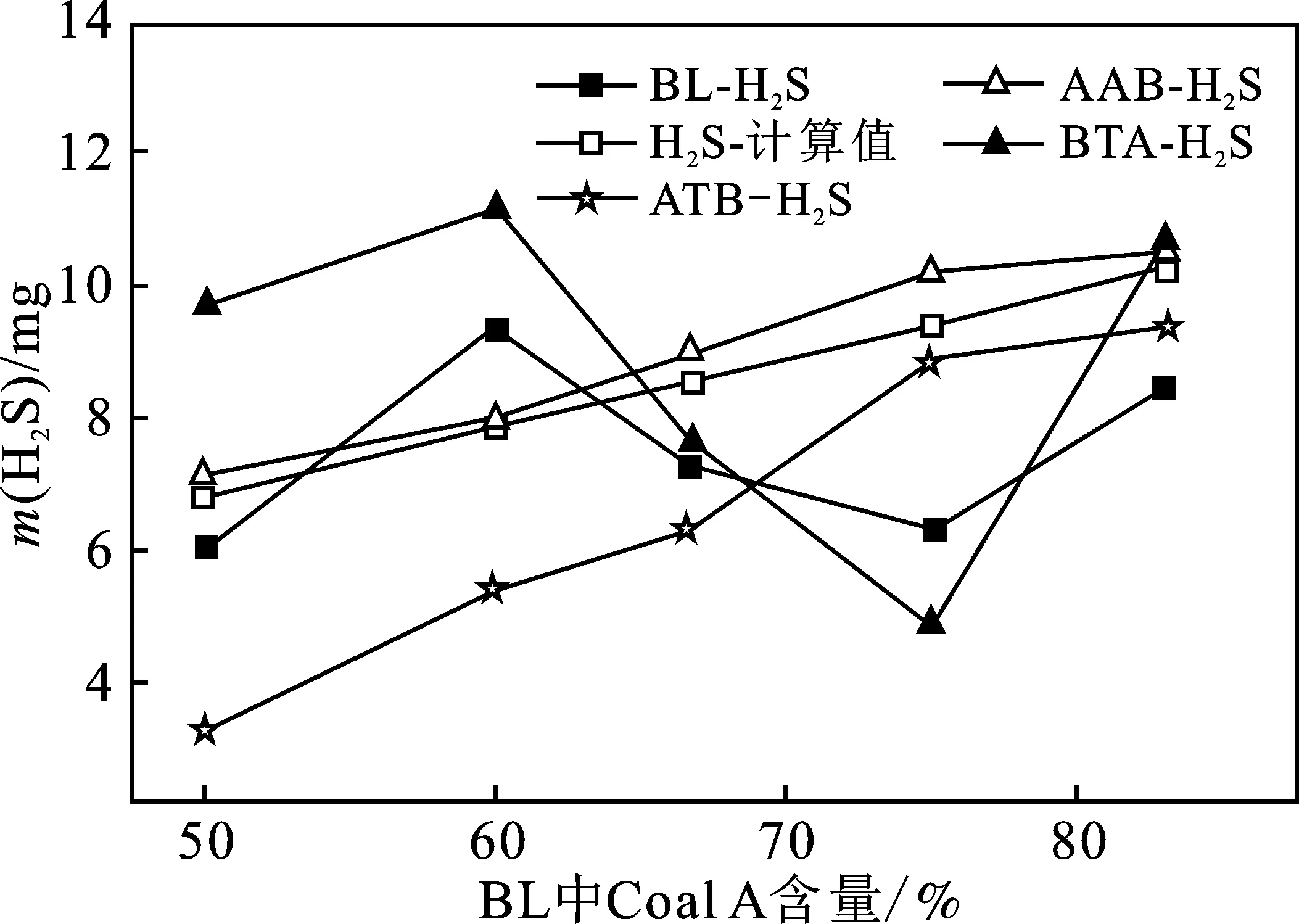
图11 BL,BTA,AAB和ATB 程序升温热解过程中释放的H2S的量 Fig.11 Amount of H2S of BL,BTA,AAB and ATB during temperature programmed pyrolysis
由图11可知,BL-H2S与计算值-H2S不同,如前面所述,这是由于共热解过程两种煤之间的基团重组对硫迁移产生影响。BTA-H2S与BL-H2S呈现出相同的趋势。当Coal A含量在50%~60%时,高挥发分的Coal B含量为40%~50%,可以提供足够的含氢自由基,当Coal B热解产生的挥发分在载气的作用下,吹扫到下层烧结板时与Coal A中的含硫基团结合成为含硫气体释放。当Coal A增加到75%时,此时Coal B的含量减少到25%,无法提供足够的含氢自由基,从而使得含硫基团更多迁移到半焦或者焦油中;当Coal A 含量增加到75%~83.3%时,BTA-H2S和BL-H2S又呈现出增加的趋势,这应该是高硫含量的Coal A本身分解产生出的含硫气体对硫在气相中的分布起到了主导作用。
随着Coal A含量的增加,ATB-H2S的量呈现逐渐增加的趋势,这表明程序升温共热解过程中,Coal A含量的多少是影响H2S释放量的主要因素。Coal A 含量在50%~66.7%时,ATB-H2S低于BL-H2S,这是由于在ATB解析实验中,Coal A焦中的硫不能与高挥发分的Coal B接触,使得硫仍然存在于焦中。随着Coal A含量增加到大于75%时,ATB-H2S高于BL-H2S而低于计算值,这是由于在BL的共热解过程中,生成的含硫气体会与Coal A以及Coal B发生二次发应,而ATB解析实验Coal A热解产生的含硫气体在载气的作用下带到下层烧结板,减少了Coal A热解产生的含硫气体与自身的二次反应。同时,Coal A热解产生的含硫气体与Coal B热解产生的焦进行反应,将热解产生的硫固定在Coal B中。
程序升温热解过程中AAB-H2S的释放量呈现增加的趋势,增加的幅度较小,而且与计算值差别不大,这说明Coal A与Coal B的挥发分之间的作用对BL在程序升温热解过程中气相硫的迁移没有产生重要影响。
综上所述,引起BL在程序升温热解过程中硫迁移的反应主要为高挥发的Coal B与Coal A焦之间的作用,一方面将Coal A焦中的硫更多以气体的形式释放,另一方面生成的含硫气体与Coal A的二次作用,降低含硫气体的释放。综合作用下,使得混合配比为60% A时,气体释放量最大。
2.5.2 两种煤程序升温共热解解析实验中固体硫含量的分析 图12为不同热解过程产生的焦中硫的含量。
由图12可知,BTA-S在Coal A含量为50%~66.7% 时小于计算值,这表明热解过程中,载气将上层烧结板Coal B产生的含氢气体吹到下层烧结板Coal A 的半焦上,促使了Coal A中含硫基团形成H2S而释放。图11中显示在这个比例处气相含硫量增加;随着Coal A 含量的继续增加,BTA-S与计算值-S接近,这应该是由于少含量的Coal B 无法提供足够的挥发分,从而使得焦中的硫就相当于煤自体热解后的结果。
ATB-S热解过程中高于计算值-S,可能由于热解过程中载气将Coal A自身热解产生的含硫气体吹扫到底层烧结板,从而Coal B与其发生反应,生成H2S,又与Coal B焦中的有机质发生反应,生成了结构复杂的大分子含硫结构。Coal A的挥发分与Coal B的挥发分反应对焦中硫应该不会有影响,图中也显示AAB-S与计算值在实验误差范围内基本一致。
为了进一步解释在不同解析实验过程中引起固相中硫的迁移,分别对Coal A以及Coal B焦中的硫进行计算,见图13。
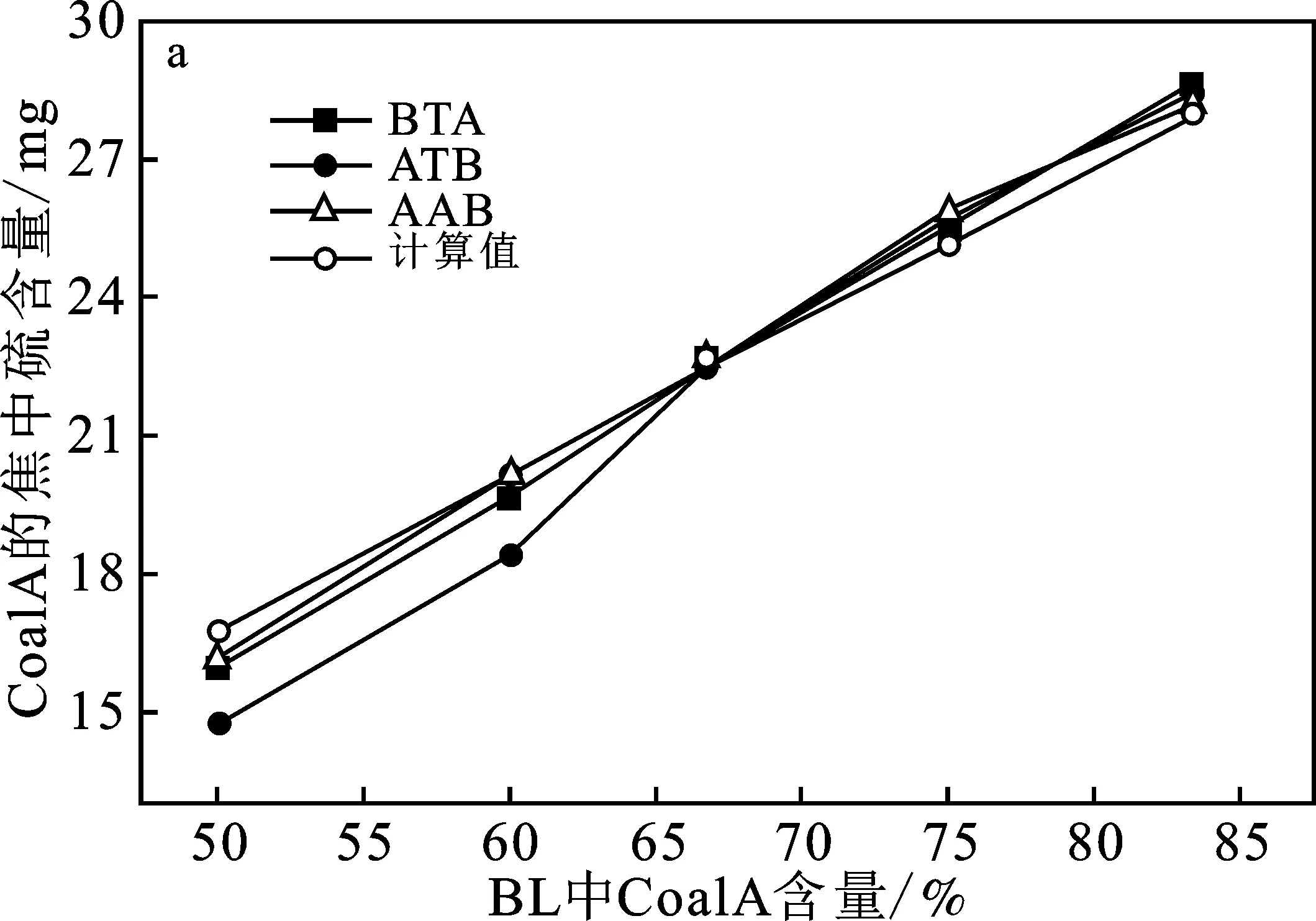
图13 BL,BTA,AAB and ATB热解后Char A和Char B中硫含量Fig.13 The amount of sulfur in Char A or Char B of BL,BTA,AAB and ATB during pyrolysis
由图13可知,Coal A 含量为50%~66.7%时,BTA中的Char A硫含量低于计算值,这主要是因为高挥发分Coal B促进了Coal A中硫转移到气相中,从而降低焦中的硫含量。当Coal A 含量增加到60%~83.3%时,BTA中的Char A硫含量与计算值相当,这表明热解过程固相硫的产生主要来源于Coal A本身。AAB,ATB实验中的Char A中的硫都与计算值相当,这进一步表明AAB实验主要是A的挥发分与B的挥发分的反应,而ATB主要是A的挥发分与B的焦的反应,从而它们对Char A中的硫不会产生影响,相当于煤本身热解的结果。
由图13b Coal B焦样中的硫含量可知,ATB实验Char B的硫含量都高于相应配比的计算值,这个原因前面也已经提到过,应该是由于载气将Coal A本身热解产生的含硫挥发分吹扫到下层烧结板上,从而与Coal B发生反应,产生了更加稳定的含硫化合物而固定在Char B中。
3 结论
(1)高硫含量焦煤Coal A与高挥发分煤Coal B热解行为不同,不同比例的混合煤样程序升温热解时,挥发分产率以及焦样的产率不同于相对应比例的计算值,表明共热解过程中存在相互作用。
(2)Coal A和Coal B热解过程释放的含硫气体H2S和COS受不同因素的影响,H2和CH4等含氢气体的形成促进了H2S的释放,CO和CO2等含氧气体的释放促进了COS的释放。
(3)Coal A的挥发分与Coal B的挥发分之间的反应对焦中硫的分布没有影响;Coal A的挥发分与Coal B焦之间的反应会增加焦中的硫含量;Coal A含量在50%~66.7%范围时,Coal B的挥发分与Coal A的焦反应可以降低焦中硫含量,与计算值相比Coal A含量为50%时可以使焦中硫含量降低12.4%。

