磁固相萃取-气相色谱-质谱法测定饮料中罂粟碱
田洁,曹淑瑞,苏泓滔,巫端浩,刘正宏
(1.西南政法大学鉴定中心,重庆 401120)(2.西南政法大学鉴定中心,刑事侦查学院,重庆 401120)
罂粟壳俗称大烟,是罂粟的干燥成熟果壳。虽然具有药用价值,例如敛肺、涩肠和止痛等,但久服产生依赖性和成瘾性[1]。罂粟碱是罂粟壳的主要生物碱之一,其分子结构见图1。长期食用会产生精神失常,出现幻觉,甚至因呼吸停止而引起死亡[2]。饮料作为大众消费品,在国内占有很大市场,不法商贩为谋取利益在饮料中添加过量的罂粟碱,长期低剂量饮用会有成瘾性和依赖性,大剂量服用甚至危及生命[2]。
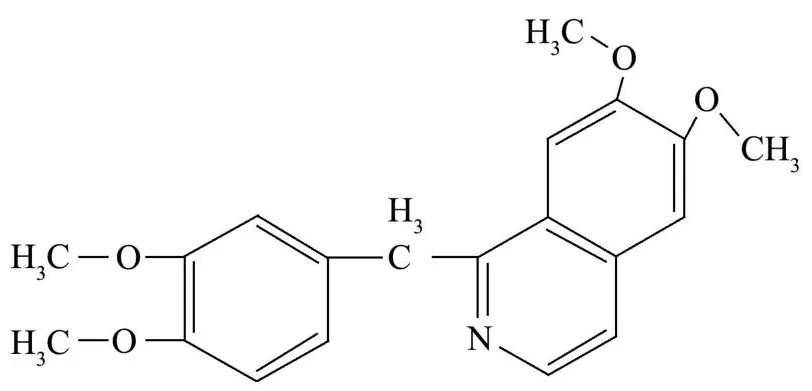
图1 罂粟碱的分子结构Fig.1 Molecular structure of papaverine
在国内,检测罂粟碱的方法有气相色谱法[3,4]、高效液相色谱法[5]、液相色谱-质谱法[6-8]等。对罂粟碱样品进行分析检测前均需要对样品提取、净化、浓缩等操作。磁性固相萃取(MSPE)属于固相萃取法中的一种新型方法。其原理是将磁性吸附剂添加到样品溶液中,目标组分经分子扩散快速地从溶液中被吸附到吸附剂中,然后利用外部磁场,目标组分同吸附剂一同被迁移,最终选取合适洗脱溶剂洗脱目标组分,实现分离[3]。与传统的固相萃取法相比,MSPE既具有磁性强,可重复利用,萃取操作简单等特点,而且可以避免繁琐的离心等操作[9,10]。此外,气相色谱-质谱法具有灵敏度高、回收率好的优点。二者联用对样品进行分析,可使分析过程更加简单快速,准确。
吸附剂材料是磁性固相萃取技术的重要组成部分之一。目前磁性纳米材料有壳聚糖[11]、离子液体[12]、聚多巴胺[13]、氧化石墨烯(Graphene Oxide,GO)[14]等。其中,GO具有大比表面积和丰富的官能团,可以使目标物固定在结合位点上[15,16],通过π-π相互作用和氢键作用吸附芳香族有机分子。Fe3O4基纳米材料由于其优异的磁性能而备受关注,其除了具有磁性的优良特性外,还具有隧道效应、小尺寸效应以及表面效应等特点[17]。Fe3O4与GO的复合使得GO的结合位点充分暴露且具有磁性,有利于目标分子的选择性吸附和分离。在复合材料的合成过程当中,修饰特定的官能团,与目标物通过非共价键作用实现高效吸附,再通过选择合适的洗脱溶剂从而实现高效分离。本研究旨在合成一种磁性强、吸附性能好的磁性氧化石墨烯材料(Fe3O4@GO),通过单因素法和响应面法优化实验中的吸附和解吸条件,再结合GC-MS法检测;从而建立饮料中罂粟碱的快速高效的MSPE-GCMS检测方法。
1 材料与方法
1.1 主要材料与仪器
氧化石墨烯(GO),山东利特纳米技术有限公司;罂粟碱标准品,纯度99.8%,CFW Laboratories Inc;HCl、FeCl3·6H2O、FeCl2·4H2O、NaOH,成都市科隆化学品有限公司;甲醇、乙醇、乙腈,霍尼韦尔(中国)有限公司。
主要仪器:ISQ 7000气相色谱-质谱仪,美国赛默飞世尔科技有限公司;S-024氮吹仪,上海仪电科学仪器股份有限公司;Quanta Q400扫描电子显微镜、FEI TECNAI G2 F20透射电子显微镜,美国FEI公司;IRTracer-100傅里叶变换红外光谱仪,日本岛津有限公司;HR800拉曼光谱仪,法国JobinYvon公司;MPMS(SQUID)XL-7振动样品磁强计,美国量子设计公司。
1.2 实验方法
1.2.1 Fe3O4@GO的制备
采用化学共沉淀法制备材料。具体制备过程如下:溶液A:称取0.15 g的GO粉末于100 mL的超纯水中,超声处理1 h得到均匀分散的GO分散液。溶液B:在氮气流下,将1.8 g的FeCl3·6H2O和0.8 g的FeCl2·4H2O分散在装有50 mL超纯水的三颈烧瓶中。再将溶液A快速加入到装有溶液B的三颈烧瓶中,在80 ℃下用磁力搅拌器剧烈搅拌1 h后,加入10 mL 8 mol/L的氨水,剧烈搅拌30 min后等待自然冷却。所得黑色产物用外部磁体进行收集并用乙醇和超纯水多次洗涤以除去未反应的化学物质,然后在60 ℃的烘箱中干燥样品。所得产物为磁性氧化石墨烯(Fe3O4@GO)。
合成磁性四氧化三铁的反应如下(式1):
1.2.2 磁性固相萃取过程
量取2 mL的含罂粟碱待测液于10 mL的离心管中,用适量浓度的盐酸和氢氧化钠溶液调节pH值至7,加入15 mg的Fe3O4@GO纳米材料,水平振荡仪振荡30 min,通过外部磁场收集溶液中的磁性材料,弃除上清液,向离心管中加入2 mL解吸溶液,振荡解吸6 min,用永久磁铁吸引富集,移取所有上清液进行氮吹操作;近干后用2 mL正己烷溶液进行复溶,最后样品溶液用0.22 μm滤膜过滤后再上机检测。
1.2.3 GC-MS检测条件
色谱柱:TG-5MS(30 m×0.25 mm×0.25 μm);
升温程序:起始温度70 ℃保持1 min,然后升温至280 ℃(升温速率20 ℃/min)保持5 min,再升温至300 ℃(30 ℃/min)保持2 min。
仪器条件:温度的设定为进样口260 ℃,传输线250 ℃,离子源300 ℃;进样量2.0 μL;不分流进样;扫描方式:SIM。
1.2.4 Fe3O4@GO的表征
使用扫描电子显微镜、透射型电子显微镜、傅里叶变换红外光谱仪、振动样品磁强计及拉曼光谱仪对磁性吸附剂Fe3O4@GO的形貌、官能团及磁化性质进行表征。
1.2.5 吸附条件的优化
以罂粟碱回收率为指标,考察单因素对测定罂粟碱的回收率的影响,考察的因素水平如表1所示。

表1 单因素实验设计Table 1 Single factor experimental design
1.2.6 响应面优化实验
根据单因素优化实验的结果,以pH值(A)、萃取剂剂量(B)、解吸时间(C)为变量,以罂粟碱的回收率为考察指标,设置三因素三水平的设计实验,见表2。
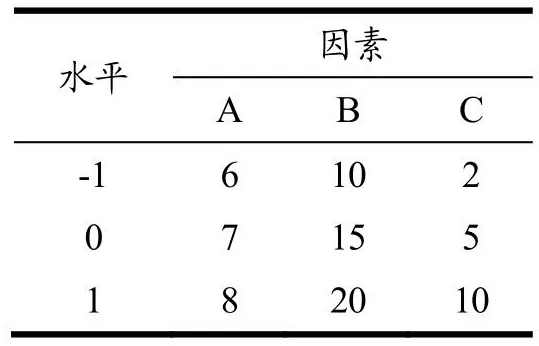
表2 响应面优化实验表Table 2 Response surface optimization experiment
1.2.7 样品回收率的分析
在过滤后的待测样品溶液中,加入1 mL已知浓度的罂粟碱溶液,混合均匀后再经过萃取净化。回收率的计算方法(式2):
式中:
R——加标回收率,%;
C0——加标浓度,μg/mL;
V0——加标体积,mL;
C——加标后测定浓度,μg/mL;
C'——加标前浓度,μg/mL;
V——加标后总溶液体积,mL。
2 结果与讨论
2.1 Fe3O4@GO的表征分析
2.1.1 扫描电镜分析
从图2a可观察到GO呈片状二维结构,表面伴有许多褶皱。这些褶皱能够使磁性纳米粒子(Fe3O4)更容易负载在其结构中。由图2c可观察到GO表面结合了很多粒径较小的纳米粒子,结合图2b可知是这些粒子正是Fe3O4,可以表明Fe3O4已经成功负载于氧化石墨烯上,磁性氧化石墨烯纳米材料(Fe3O4@GO)被成功合成。

图2 扫描电镜图(a)GO,(b)Fe3O4,(c)Fe3O4@GOFig.2 SEM (a) GO; (b) Fe3O4; (c) Fe3O4@GO
2.1.2 透射电镜分析
由图3a可清楚地观察到Fe3O4@GO中氧化石墨烯的片层结构和褶皱,图中颜色较深的粒子为Fe3O4纳米粒子,透射电镜分析再次证明了Fe3O4纳米粒子已经成功负载在氧化石墨烯中,其粒径约为10~20 nm。
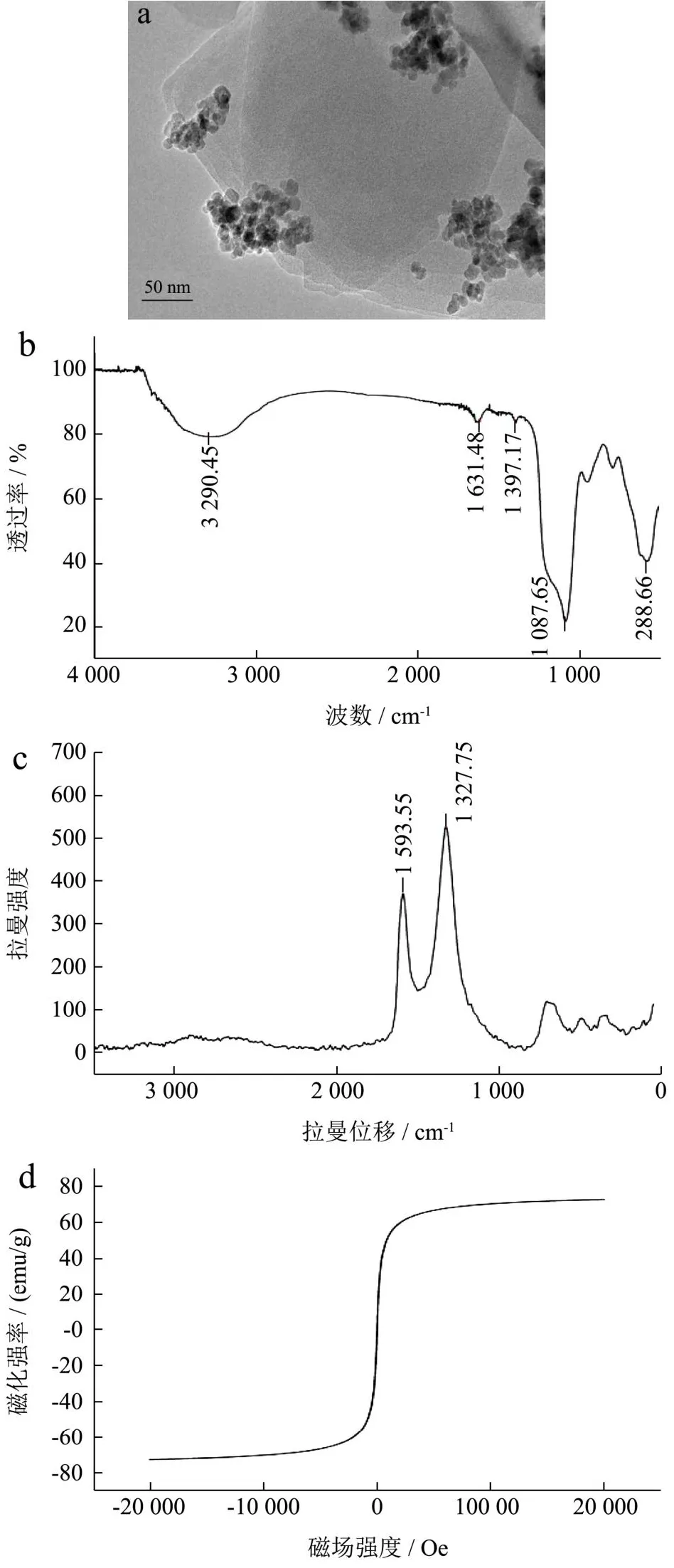
图3 (a)透射电镜图、(b)红外光谱图、(c)拉曼光谱图、(d)磁滞回线Fig.3 (a) TEM; (b) FT-IR; (c) Raman; (d) VSM
2.1.3 红外光谱分析
红外光谱作为材料常见的表征方法之一,从红外图谱中可以获取有关化学键合和官能团的相关信息。由图3b可知,GO和H2O中羟基的伸缩振动显示在3 290 cm-1宽峰处[18],1 631、1 397、1 087 cm-1分别是芳香基C=O、C=C、C-O-C的伸缩振动峰[19],说明GO结构中含有-OH、C=O、C=C和C-O-C等官能团。在588 cm-1处为Fe-O的伸缩振动峰[20],说明Fe3O4@GO已成功合成。
2.1.4 拉曼光谱分析
由图3c可见,Fe3O4@GO的拉曼光谱图中在波长为1 327 cm-1和1 593 cm-1位置出现两个峰。在1 327 cm-1处出现的为D吸收峰,1 593 cm-1的峰为G吸收峰。D峰为一种非对称性的声学振动峰,是由sp3杂化的碳原子呼吸振动产生的,用来表示物质内部的结构缺陷情况[21];G峰的对称性高,是因为碳原子的sp2杂化,其表示结构的对称性[22]。D峰的出现表明Fe3O4@GO具有一定的缺陷结构。
2.1.5 振动样品磁强计
图3d为Fe3O4@GO的磁滞回线。磁滞回线通过并以原点为中心,呈光滑的S形,零矫顽力,无剩磁现象。其饱和磁化强度为72.5 emu/g,强的磁化强度说明制备的材料具有强磁性,能够满足磁性分离的要求。
2.2 萃取条件的优化
为了能够高效率的实现吸附剂对样品溶液的解吸和萃取,本实验对吸附剂用量、溶液pH值、萃取时间、解吸时间四个条件进行了优化。
2.2.1 吸附剂用量的优化
吸附剂用量的影响是吸附过程中需要考虑的主要因素。在不改变其他条件的情况下,设计Fe3O4@GO用量分别为5、10、15、20、25 mg,按照1.3.2方法进行实验。如图4a所示,结果表明,罂粟碱的回收率会随着吸附剂用量的增加而增大,最终当用量增加到15 mg,回收率基本稳定。这是因为Fe3O4@GO纳米吸附材料提供了更多的活性吸附位点,萃取回收率随着Fe3O4@GO纳米吸附剂的增加而增加。而当进一步增加Fe3O4@GO吸附剂的用量,由于活性位点的饱和,罂粟碱的回收率没有显著提高。因此,确定吸附剂用量为15 mg。
2.2.2 溶液pH值的优化
由于溶液的pH值对分析物的存在形式(质子化或去质子化)和吸附剂表面的电荷密度有很大影响,因此溶液的pH值在吸附过程中对萃取效率起着关键作用[23]。通过NaOH溶液和HCl溶液调节溶液pH值来考察pH值对萃取结果的影响。通过查阅文献可知,最佳pH值在呈中性左右[24,25],因此实验只考察pH值在4~8的范围内对罂粟碱回收率的影响,如图4b所示,pH值为7时吸附性能最佳,当pH值从4增加到7时,回收率增大;当pH值进一步增加时,回收率又逐渐降低。
2.2.3 萃取时间的优化
要达到良好的萃取效果需要足够的时间。其余实验条件不变,选择振荡时间分别为从5、10、20、30、40、50、60 min。按1.3.2实验方法,实验结果如图4c所示,萃取时间在30 min时回收率最大,说明此时吸附剂与目标组分之间吸附达到动态平衡。随后延长吸附时间,回收率反而略有下降。这是因为Fe3O4@GO吸附位点已被完全占据,在30 min时获得饱和吸附量,之后有少量分析物因为吸附不牢固从而从吸附剂表面脱离重新进入样品溶液。因此,为使罂粟碱在吸附剂上吸附完全,选择30 min为最佳吸附时间。
2.2.4 解吸时间的优化
解吸时间也是影响萃取效率的重要因素。根据查阅相关文献[26,27],含有一定的氨的解吸剂有利于提高罂粟碱的回收率,所以甲醇:氨水=99:1被选为解吸剂。为了促进罂粟碱的转移和均匀分布,采用振荡技术从Fe3O4@GO吸附剂中分离罂粟碱。其余实验条件不变,在2~20 min范围内检测振荡时间对回收率的影响。结果图4d表明,在5 min时解吸效率最佳,随后随着时间的增加,效率开始降低,因此选择5 min为最佳解吸时间。
2.3 响应面优化
综合分析单因素实验结果,以pH值(A)、吸附剂剂量(B)和解吸时间(C)3个因素为自变量,以罂粟碱的回收率为响应值,进行响应面优化。响应面实验结果见表3。
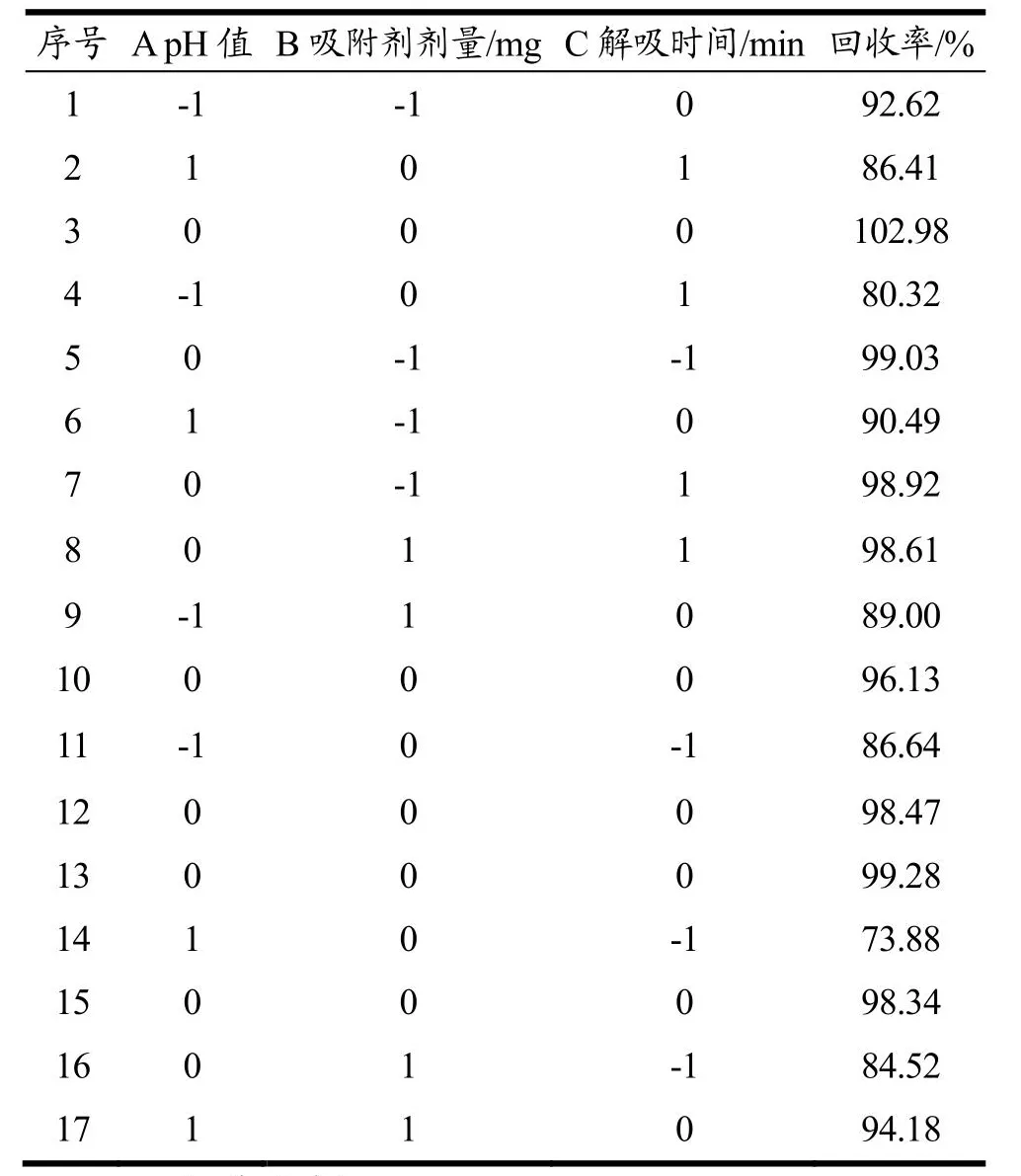
表3 响应面实验设计及结果Table 3 The experimental design and results of response surface optimization
2.3.1 方差分析
根据表3结果,进行方差分析,结果见表4。对实验数据进行拟合,建立回归模型,其线性方程(式3):
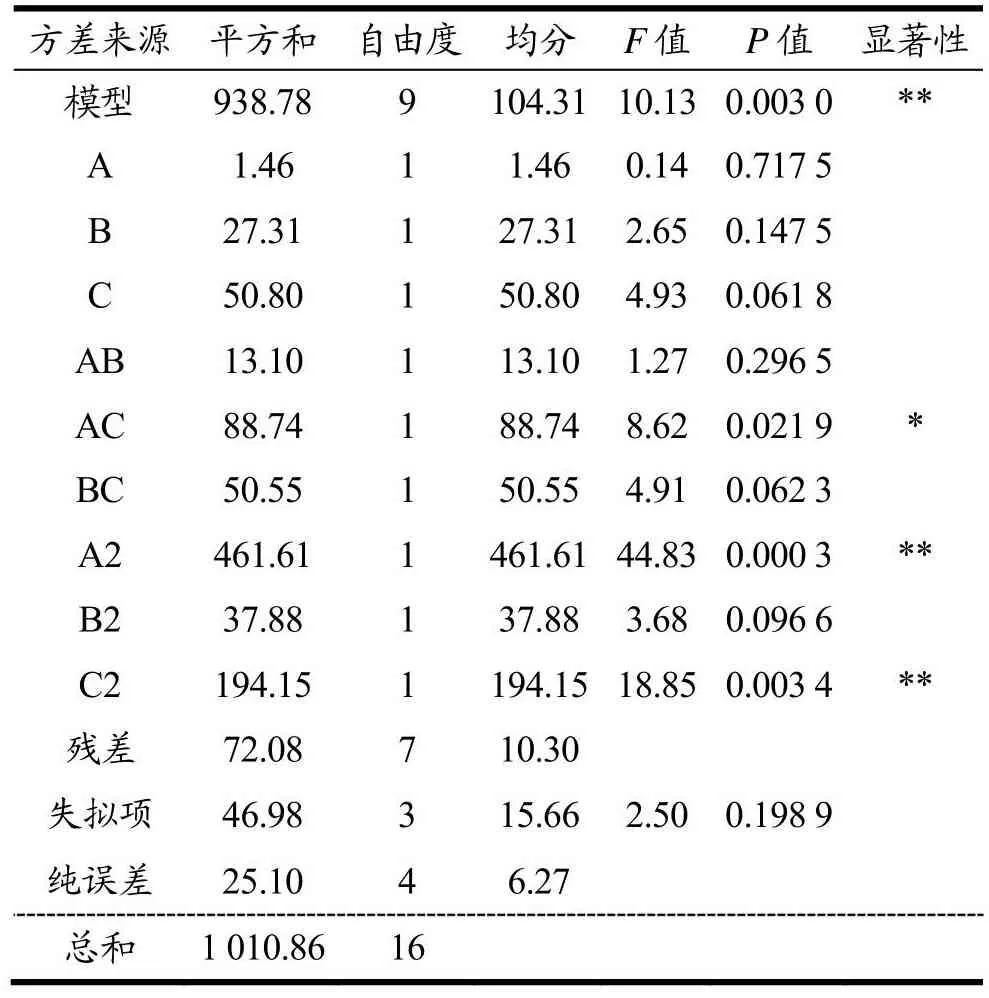
表4 方差分析Table 4 Analysis of variance
该模型的P值小于0.01,表明差异极显著,此次建模成功,可以被利用。失拟项P值为0.198 9,表明差异不显著,进一步说明所得建立的回归模型方程与实际实验过程中拟合中的非正常误差所占比例较小,可以用该回归方程取代实验中的真实点对实验结果进行建模分析。
2.3.2 各因素交互作用分析
图5是根据回归分析结果作出的有关溶液pH值、磁性纳米材料用量、解吸时间3因素对罂粟碱回收率影响的响应面图和等高线图,展现了各因素交互作用对回收率的影响。由图5a~b、e~f可看出,pH值与吸附剂剂量、吸附剂剂量与解吸时间的响应面图不呈凸形曲面且分别对曲线最高点影响均较小,等高线图交互作用都不显著。而图5c~d曲面较为陡峭且等高线图呈现出椭圆形的形态,表明解吸时间和pH值对回收率的交互作用较为明显,方差分析佐证交互关系显著。通过统计软件Design-Expert对所模拟的模型进行优化和求解,得到检测液体中罂粟碱的最佳实验条件是:溶液pH值为7,磁性纳米材料用量为15 mg,解吸时间为6 min。
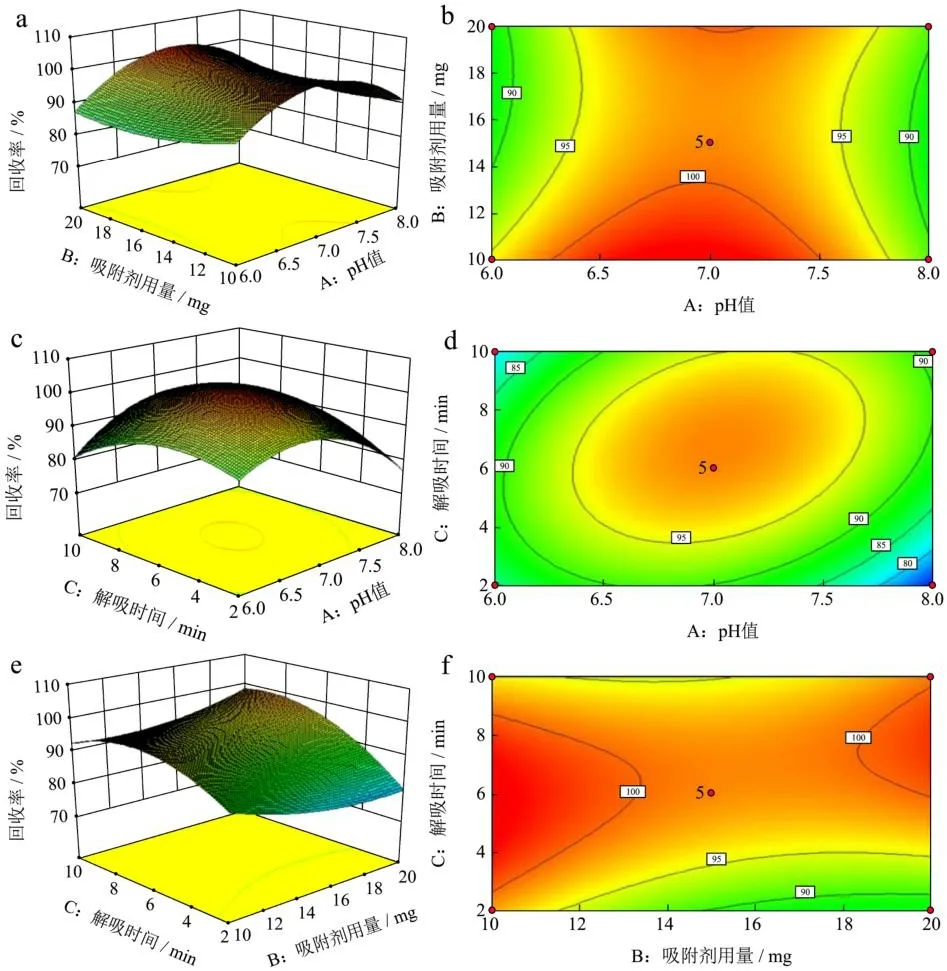
图5 溶液pH值与吸附剂剂量(a、b)、溶液pH值与解吸时间(c、d)、吸附剂剂量与解吸时间(e、f)交互作用对罂粟碱回收率的响应面图及等高线图Fig.5 The response surface plot and contour map of the interaction between solution pH and adsorbent dosage (a, b),solution pH and desorption time (c, d), adsorbent dosage and desorption time (e, f) on the recovery rate of papaverine
2.4 标准工作曲线、相对标准偏差及检出限
在最优条件下:溶液pH值为7,磁性纳米材料用量为15 mg,萃取时间30 min,解吸时间6 min,评估所建立的方法。实验结果总结在表5。在0.10~2.00 μg/mL范围内,罂粟碱的峰面积与浓度有着良好的线性关系,R2为0.999 3。以3倍信噪比计算检测限,检测限为0.038 μg/mL;质量水平1.0 μg/mL进行6次重复实验,获得的方法回收率在97%~103%范围内,RSD为1.96%,表明该方法准确度和重复性良好。

表5 线性方程、相关系数、线性范围、相对标准偏差和检测限Table 5 Regression equation, correlation cofficient, linear range and detection limits
2.5 实际样品分析
在实际样品分析中,按照建立的检测方法对所购买的三种饮料(冰红茶、脉动、红牛)进行分析检测。每个样品平均做3次,均未检测出罂粟碱。为了验证方法的准确度,在这三种饮料中分别加入浓度为0.1、1.0、2.0 μg/mL的罂粟碱标液进行分析。检测结果总结于表6,其加标回收率在98.4%~105.0%范围内,相对标准偏差为0.6%~3.5%,表明此方法具有良好的准确度,可以用于检测饮料中罂粟碱的含量,能够满足实际检测需求。
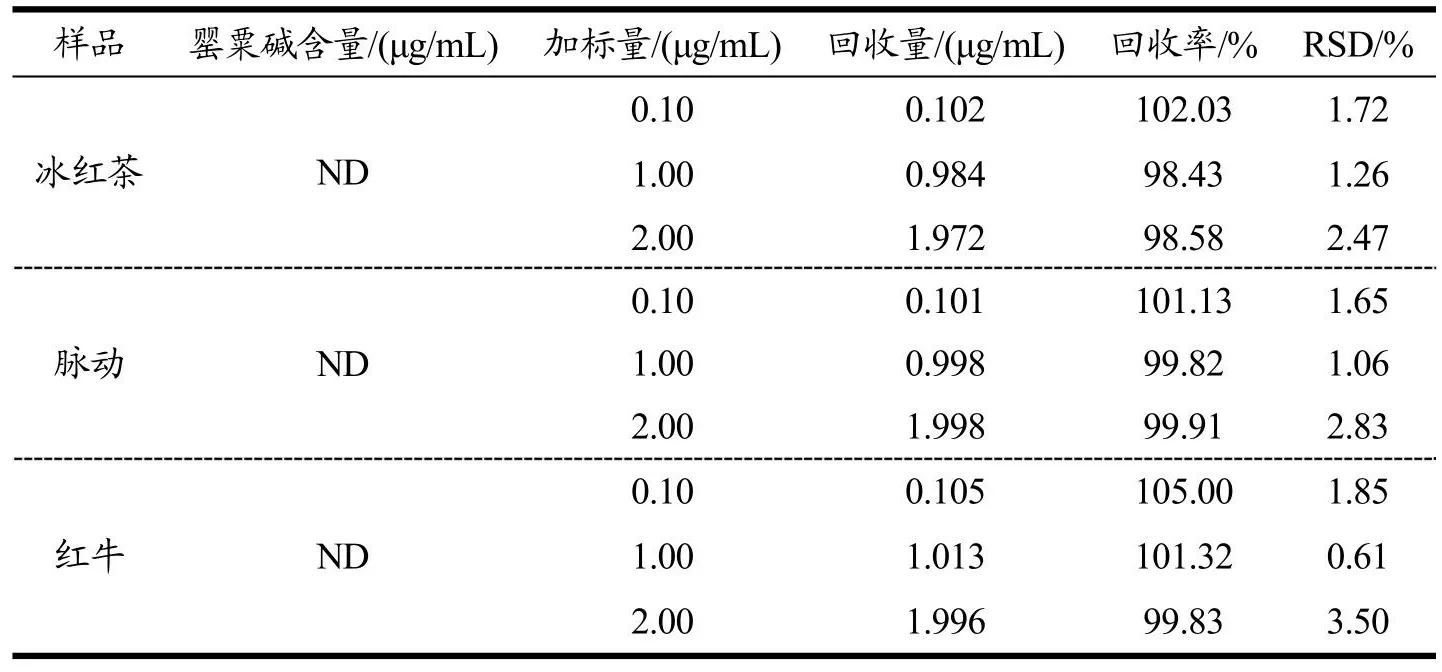
表6 实际样品测定结果表Table 6 The actual sample measurement results (n=3)
3 结论
采用简单的化学共沉淀法制备了磁性氧化石墨烯复合纳米材料,材料具有良好的磁性,可以实现快速分离,是一种良好的吸附剂。本研究将Fe3O4@GO作为吸附剂,萃取饮料中的罂粟碱,再结合气相色谱-质谱进行测定,最终实验方案为:样品溶液pH值7、吸附剂用量为15 mg、萃取时间30 min、甲醇:氨水=99:1(V/V)、解吸剂体积2 mL、解吸时间6 min。结果表明,建立的方法具有良好的重复性和准确度。该方法不仅操作简单,快速准确,而且灵敏度较高,回收率满足检测的要求。有望应用于实际,为质检部门对食品监管、打击食品中非法添加物和禁毒工作提供一定的技术参考。

