长方案促排卵晚卵泡期孕酮升高对胚胎质量及累积活产率的影响
李丹阳,张 亚,董孝贞,徐 影,杨如雪,黄江笛,张俊韦,胡继君,管一春,孙丽君*
(郑州大学第三附属医院 a.生殖医学中心;b.超声科,郑州 450052)
长方案作为体外受精/卵胞浆内单精子注射-胚胎移植(in vitro fertilization/intra-cytoplasmic sperm injection-embryo transfer,IVF/ICSI-ET)技术中控制性超促排卵(controlled ovarian hyperstimulation,COH)的主导方案,具有卵泡发育同步性好、抑制早发黄体生成素(luteinizing hormone,LH)峰以及增加获卵数和胚胎数等优点[1],可提高卵巢储备良好患者的新鲜周期种植率、临床妊娠率及累积活产率(cumulative live birth rate,CLBR)[2-3]。但是,仍有13%~46%的促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRH-a)周期会出现晚卵泡期血清孕酮(progesterone,P)提前升高[4],对患者的子宫内膜容受性造成一定损害,导致新鲜胚胎移植(embryo transfer,ET)周期的种植率、临床妊娠率和活产率降低[5-6]。因此,患者HCG注射日(HCG injection day)孕酮升高时,多数生殖中心会选择全胚冷冻策略以规避这一风险,随后选择合适的时机解冻移植[7-8]。目前,HCG日孕酮升高对患者的胚胎质量是否造成影响尚有争议[8-11],而累积活产率作为评价IVF/ICSI治疗效果和安全性的指标较单次胚胎移植的成功率更全面、更准确[11-12]。因此,本研究主要探讨长方案促排卵晚卵泡期孕酮升高对IVF/ICSI助孕患者的胚胎质量及累积活产率(cumulative live birth rate,CLBR)的影响。
1 材料与方法
1.1 研究对象及分组 本研究为单中心回顾性队列研究,选取2015年10月至2021年12月在郑州大学第三附属医院生殖中心行IVF/ICSI助孕长方案促排卵的7001个周期的临床资料。参考文献[10,13],HCG日孕酮升高定义为P≥2.0ng/mL。研究组纳入标准:助孕方式为IVF/ICSI;促排卵方案为早卵泡期长效长方案/黄体中期长效长方案;女方年龄≤38岁[12];窦卵泡数(antral follicle counting,AFC)≥5个;抗苗勒管激素(anti-Müllerian hormone,AMH)≥1.2ng/mL;基础促卵泡生成素(follicle-stimulating hormone,FSH)<10U/L;因HCG日孕酮升高行全胚冷冻者的首个冻胚移植周期。纳入同期以相同促排卵方案但HCG日P<2.0ng/mL行鲜胚移植的患者为对照组。排除标准:患子宫内膜异位症、子宫肌瘤、子宫腺肌病、畸形子宫、宫腔粘连、子宫内膜息肉或输卵管积水者;复发性流产或反复种植失败者;有不良孕产史者;供精或供卵周期;行未成熟卵母细胞体外成熟(in vitro maturation,IVM)者;HCG日雌二醇(estradiol,E2)≥10000ng/L或获卵数>25个或合并不同程度的腹胀、少尿、腹水等症状和体征者;移植日子宫内膜厚度<7.0mm者;冷冻胚胎移植内膜准备方案为降调+人工周期者。依据患者HCG日P水平分为低孕酮组(6331例)和高孕酮组(670例)。本研究经郑州大学第三附属医院伦理委员会批准(伦理批号为2022-218-01)。
1.2 临床促排卵方案及胚胎实验室操作方法
1.2.1 促排卵方案 早卵泡期长效长方案:月经周期第2~4d给予长效GnRH-a(达菲林,法国益普生)3.75mg降调节30~40d;黄体中期长效长方案:前一月经周期的黄体中期给予长效GnRH-a 1.5~1.875mg降调节14~16d,达到垂体降调节标准(LH<5U/L,E2<183.5pmol/L,子宫内膜厚度<5mm,无卵巢功能性囊肿)时,根据患者年龄、体质量指数(body mass index,BMI)和卵巢储备等给予促性腺激素(gonadotropin,Gn)促排卵(75~300U/d启动),用药过程中根据卵巢反应性及激素水平调整Gn用量。
1.2.2 取卵、授精和胚胎培养 当至少1枚主导卵泡直径≥20mm,或3枚卵泡直径≥18mm时,停用Gn,采用电化学发光免疫法测血清LH、E2和P水平(根据制造商的说明进行质控,各试剂盒变异系数小于10%),当晚皮下注射重组HCG(艾泽,瑞士默克雪兰诺)250μg扳机。36~38h后行阴道超声监测下取卵术。根据男方精液及患者情况,行常规IVF/ICSI,受精后第3d(D3)观察胚胎形成情况,卵裂期胚胎质量评分标准见参考文献[14]。若继续培养至第5~6d(D5~D6),发育至囊胚阶段,参照Gardner评分标准进行囊胚评分[15]。
1.2.3 胚胎移植与黄体支持 取卵后3~5d根据患者情况和胚胎质量进行移植。若HCG日P<2.0pg/mL,取卵术后给予常规黄体支持,于取卵后第3d或第5d进行新鲜卵裂期胚胎或囊胚移植。若HCG注射日的孕酮升高则取消新鲜周期移植行全胚冷冻。根据患者的具体情况,至少间隔1个月经周期,制定不同的冻融胚胎移植方案,包括自然周期、激素替代周期和刺激周期,移植后给予常规黄体支持。
1.3 观察指标 (1)主要观察指标:CLBR=每取卵周期中形成的胚胎(新鲜+冻融胚胎)移植后首次活产的周期数/取卵周期总数×100%,CLBR的统计时间截止为2019年12月,随访至2年。(2)次要观察指标:可利用胚胎率=可利用胚胎数/2PN卵裂数×100%,优质胚胎率=优质胚胎数/2PN卵裂数×100%,囊胚形成率=2期及2期以上囊胚数/行囊胚培养的卵裂期胚胎总数×100%,种植率=B超下见孕囊数/移植胚胎数×100%,临床妊娠率=临床妊娠周期数/移植周期数×100%,活产率=活产周期数/移植周期数×100%。
1.4 统计学方法 采用SPSS 22.0软件。采用Kolmogorov-Smirnov检验对定量资料进行正态分布检验。非正态分布的定量资料以中位数(第25百分位数,第75百分位数)[M(P25,P75)]表示,组间定量资料比较采用秩和检验。定性资料采用构成比或率(%)表示,组间定性资料比较采用卡方检验或Fisher精确检验。采用多重线性回归及二分类logistic回归分析校正混杂因素,以低孕酮组为参照,计算高孕酮组校正后的偏回归系数/比值比(partial regression coefficient/adjusted odds ratio,β/aOR)及95%置信区间(confidence interval,CI)。与P水平上升的相关因素分析采用logistic多元逐步回归。P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者的一般资料比较 高孕酮组的年龄、不孕年限及继发不孕占比显著高于低孕酮组,而AFC、AMH及患多囊卵巢综合征(polycystic ovary syndrome,PCOS)占比则显著低于低孕酮组,差异均有统计学意义(P均<0.05)(表1)。

表1 低孕酮组与高孕酮组的一般资料比较[M(P25,P75),%]
2.2 两组患者的促排卵情况及实验室指标比较 高孕酮组的Gn总量、Gn天数、HCG日E2水平、HCG日P水平及获卵数显著高于低孕酮组,而HCG日黄体生成素(luteinizing hormone,LH)水平则显著低于低孕酮组,差异均有统计学意义(P均<0.05)(表2)。采用多重线性回归校正混杂因素,结果显示高孕酮组的可利用胚胎率与囊胚形成率显著低于低孕酮组(P均<0.05)(表3)。
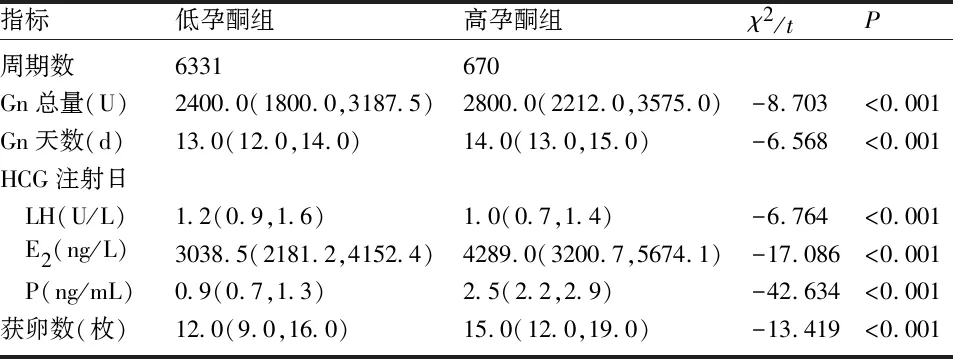
表2 低孕酮组与高孕酮组的促排卵情况比较[M(P25,P75)]

表3 高孕酮组与低孕酮组的实验室指标比较(n/N)
2.3 两组患者首个胚胎移植周期临床结局和累积活产率的比较 高孕酮组首个胚胎移植周期的移植胚胎数及移植日内膜厚度显著低于低孕酮组,移植囊胚占比显著高于低孕酮组(P均<0.05)(表4)。采用多重线性回归及多因素logistic回归校正混杂因素,结果显示,高孕酮组首个胚胎移植周期的种植率、临床妊娠率、多胎妊娠率、活产率和累积活产率均显著低于低孕酮组,而早期流产率与晚期流产率则显著高于低孕酮组,差异有统计学意义(P均<0.05)(表5)。

表4 低孕酮组与高孕酮组首个胚胎移植周期相关指标比较[M(P25,P75),%(n/N)]

表5 两组患者首个胚胎移植周期临床结局及累积活产率比较[%(n/N)]
2.4 HCG注射日P水平的相关因素分析 采用最大似然法进行多因素逐步logistic回归分析HCG日P水平的影响因素,结果显示,年龄、AMH、Gn总量、获卵数、HCG日LH水平和HCG日E2水平为HCG日孕酮水平提前上升的相关因素,见表6。

表6 logistic逐步回归分析结果HCG日P影响因素
3 讨 论
HCG日孕酮升高对新鲜胚胎移植患者的妊娠结局产生不良影响已在临床达成共识[16]。晚卵泡期血清孕酮升高可诱导子宫内膜组织学成熟[17]和显著的子宫内膜表观遗传表达变化,进而影响子宫内膜容受性[18]及其免疫耐受[19]。然而,HCG日孕酮升高是否对患者的胚胎质量造成影响尚有争议。研究表明,HCG日孕酮升高未对冻胚复苏周期及赠卵周期结局产生不利影响,即HCG日孕酮升高不影响卵母细胞及胚胎质量[20-21]。但也有学者认为,HCG日孕酮升高会影响卵母细胞和胚胎质量,降低周期优质胚胎率和可利用胚胎率[10,22],对CLBR不利[11]。本研究结果显示,高孕酮组患者的可利用胚胎率与囊胚形成率均显著低于低孕酮组,这表明晚卵泡期孕酮升高可能对患者的胚胎质量产生负面影响。
Shimada等[23]对敲除孕酮受体基因小鼠的颗粒细胞的研究发现,在卵丘细胞的扩张中发挥关键作用的表皮生长因子样因子的mRNA和蛋白水平降低,表明孕酮在卵母细胞的成熟中发挥着重要作用。Urrego等[24]研究则表明,在牛卵母细胞的体外成熟过程中,孕酮水平较低的卵母细胞发育潜力更好。本研究发现,晚卵泡期孕酮水平升高与患者胚胎质量的下降相关。然而,是孕酮水平的升高影响了卵母细胞质量还是卵母细胞提前成熟导致孕酮水平的提前升高,尚待进一步研究。
随着玻璃化冷冻的引入,冻存人类胚胎的能力较程序化冷冻有了显著的改善,既往有研究表明玻璃化冷冻并不会对患者的胚胎质量造成影响[25]。为了避免不同移植周期胚胎选择带来的偏差,本研究对低孕酮组和高孕酮组的患者均选择首次胚胎移植进行研究,即高孕酮组的首个冻胚移植周期和低孕酮组的鲜胚移植周期。采用二分类logistic回归校正混杂因素后,发现高孕酮组首个冻胚移植周期的种植率、临床妊娠率、多胎妊娠率及活产率均显著低于低孕酮组的鲜胚移植周期,而早期流产率与晚期流产率则显著高于低孕酮组,高孕酮组的累积活产率亦显著低于低孕酮组。这也间接支持晚卵泡期孕酮升高可能对患者胚胎质量产生负面影响,进而影响其随后的临床结局。
既往研究认为,晚卵泡期血清孕酮的升高可能与成熟卵泡数多、高剂量Gn以及卵巢刺激时间延长相关,HCG日孕酮升高时,HCG日E2和获卵数随之增加[11,26-27]。本研究结果显示,Gn总量、获卵数和HCG日E2与HCG日孕酮升高呈正相关,与上述研究相一致,这提示在临床促排卵过程中可通过控制患者的促排卵药物剂量及获卵数来预防晚卵泡期孕酮升高。
综上所述,长方案促排卵晚卵泡期孕酮升高可能对患者的胚胎质量产生负面影响,进而影响其累积活产率。Gn总量及获卵数与晚卵泡期孕酮升高呈正相关。在临床上,应在患者的COH过程中加以关注,控制患者的促排卵药物剂量及获卵数,减少因孕酮升高而取消移植的几率,增加患者的鲜胚移植机会,提高卵母细胞质量,以增加累积活产率。然而,晚卵泡期孕酮水平升高导致不良临床结局的机制仍待进一步研究。

