达格列净对初诊2型糖尿病患者肠道菌群、胰岛素抵抗和胰岛β细胞功能的影响
刘丽琴,陈桃生
福建省汀州医院药剂科,福建长汀 366300
糖尿病作为终身的慢性内分泌代谢性疾病,据《中国2 型糖尿病防治指南》最新流行病学调查数据,我国糖尿病患病率升高了11.2%,而90%以上都为2 型糖尿病[1]。糖尿病患者患病后因机体长时间保持高血糖水平,会增加蛋白质、脂质等代谢异常风险,随病情进展侵损脏器、血管而诱发并发症,影响患者机体健康及预后[2]。研究指出,环境因素以及遗传因素等共同作用下是导致胰岛素抵抗、胰岛β 细胞功能缺陷的主要原因,而胰岛素抵抗以及胰岛β 细胞功能缺陷是引起2 型糖尿病的主要病理原因,改善胰岛素抵抗和胰岛β 细胞功能有助于提高治疗效果[3]。2 型糖尿病发病与肠道菌群的关系越来越受到临床研究者高度重视,研究发现,肠道菌群在2 型糖尿病发生及发展过程中起到了重要作用,肠道菌群失调可以通过增加胰岛素抵抗而影响糖代谢。因此,对于2 型糖尿病患者而言,调节肠道菌群失调具有重要临床价值[4]。研究发现,达格列净能够对小鼠肠道菌群进行调节,并可改善血糖代谢[5]。基于此,本研究选便利选取2021 年6 月—2022 年5 月在福建省汀州医院接受治疗的56 例初诊2 型糖尿病患者为研究对象,分析了达格列净对初诊2 型糖尿病患者肠道菌群、胰岛素抵抗和胰岛β 细胞功能的影响,并与二甲双胍进行了对照分析。现报道如下。
1 资料与方法
1.1 一般资料
便利选取在本院接受治疗的56 例初诊2 型糖尿病患者为研究对象,以患者就诊顺序进行编号,根据随机数表法分为对照组和研究组,每组28 例。两组一般资料对比,差异无统计学意义(P>0.05),具有可比性,见表1。本研究符合《赫尔辛基宣言》要求,并与患者及家属签署知情同意书。
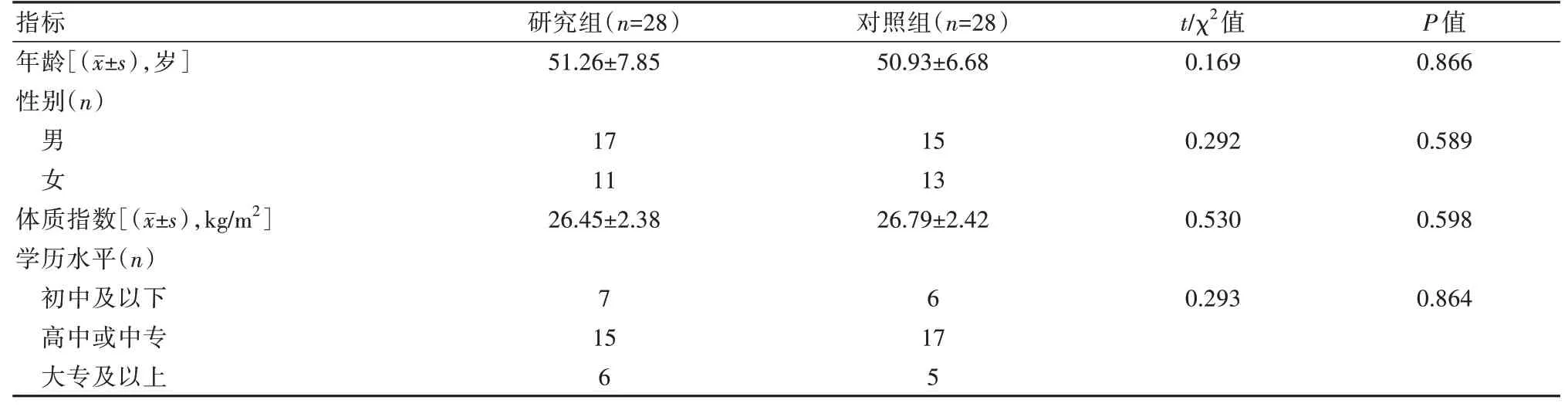
表1 两组患者一般资料对比
1.2 纳入与排除标准
纳入标准:符合临床诊断标准;年龄18~75 岁患者;均为初诊2 型糖尿病患者;患者及家属对本研究知情。
排除标准:乙醇滥用患者;入组前个月3 内存在黄连素、培菲康等肠道菌群调控药物或者使用抗生素类药物患者;存在严重肝肾功能障碍或者心脑血管疾病患者;合并严重语言功能障碍或者认知功能障碍患者;对本研究用药存在过敏反应患者;存在酮中毒等严重糖尿病并发症患者;伴有严重感染性疾病或者恶性肿瘤患者。
1.3 方法
所有患者入院后均接受运动干预、饮食干预及胰岛素强化治疗,在血糖控制达标1 周之后停用胰岛素。对照组给予二甲双胍片(国药准字H20023370)治疗,0.5 g/次,3 次/d。研究组给予达格列净(国药准字H20170117)治疗,10 mg/次,1 次/d。两组患者均连续治疗3 个月。
1.4 观察指标
比较两组患者治疗前后肠道菌群数量、血糖、血脂及胰岛素功能,并比较不良反应发生率。①肠道菌属丰度。于治疗前及治疗后收集患者新鲜粪便2.0 g,放置于无菌EP 管中待用;通过光冈法检测患者粪便标本当中肠道菌群数量,包括酵母菌、肠球菌、肠杆菌、乳杆菌、拟杆菌以及双歧杆菌,其中酵母菌、肠球菌和肠杆菌属于需氧菌群,在37℃温箱中进行培养,时间为24 h;乳杆菌、拟杆菌和双歧杆菌属于厌氧菌群,在厌氧箱中进行培养,时间为48 h;观察菌落的生长形态并记录菌群数量,计量单位为log N/湿便重量(g);培养基均购自青岛海博生物技术有限公司。②胰岛素功能及血糖血脂检测。采集患者空腹静脉血5 mL,静置30 min 后进行离心处理,离心速度为3 500 r/min,时间为10 min,在离心完成后提取上层血清,放置于-20℃冷冻箱内保存待检;通过德国西门子公司生产的Atellica CH930 全自动生化分析仪测定患者的空腹血糖、糖化血红蛋白、高密度脂蛋白胆固醇(high density lpoprotein cholesterol, HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol, LDL-C)、三酰甘油、总胆固醇及空腹胰岛素水平,并计算胰岛素β细胞功能指数(homeostasis model assessment- β,HOMA-β)和胰岛素抵抗指数(insulin resistance index, HOMA-IR)。③不良反应。记录患者治疗过程当中不良反应的发生情况,包括乏力、头痛、头晕以及恶心呕吐等。
1.5 统计方法
采用SPSS 20.0 统计学软件处理数据,计量资料符合正态分布,以(±s)表示,组间差异比较采用t检验;计数资料以例数(n)和率表示,组间差异比较采用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者治疗前后肠道菌群数量比较
治疗前,两组患者酵母菌、肠球菌、肠杆菌、乳杆菌、拟杆菌以及双歧杆菌数量比较,差异无统计学意义(P>0.05);治疗后,两组患者酵母菌、肠球菌、肠杆菌数量均明显低于治疗前,乳杆菌、拟杆菌以及双歧杆菌数量均明显高于治疗前,且研究组的上述指标均明显优于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者治疗前后肠道菌群数量比较[(±s),log N/湿便]

表2 两组患者治疗前后肠道菌群数量比较[(±s),log N/湿便]
?
2.2 两组患者治疗前后血糖及血脂指标比较
治疗后,两组患者空腹血糖、糖化血红蛋白、空腹胰岛素、LDL-C、三酰甘油、总胆固醇均低于治疗前,HDL-C 高于治疗前,差异有统计学意义(P<0.05),但治疗前后的组间比较,差异无统计学意义(P>0.05),见表3。
表3 两组患者治疗前后血糖及血脂指标比较(±s)
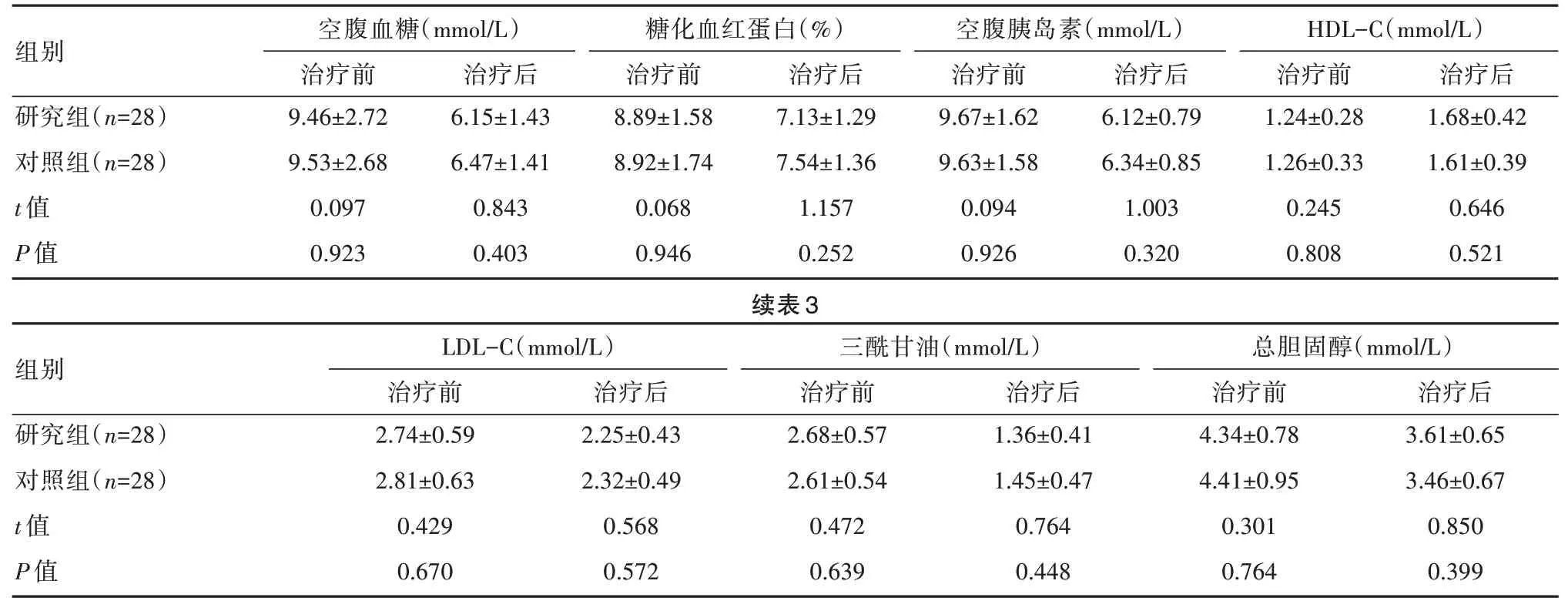
表3 两组患者治疗前后血糖及血脂指标比较(±s)
?
2.3 两组患者治疗前后胰岛素功能比较
治疗后,两组患者HOMA-β 高于治疗前,HOMA-IR 低于治疗前,且研究组均优于对照组,差异有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后胰岛功能比较(±s)
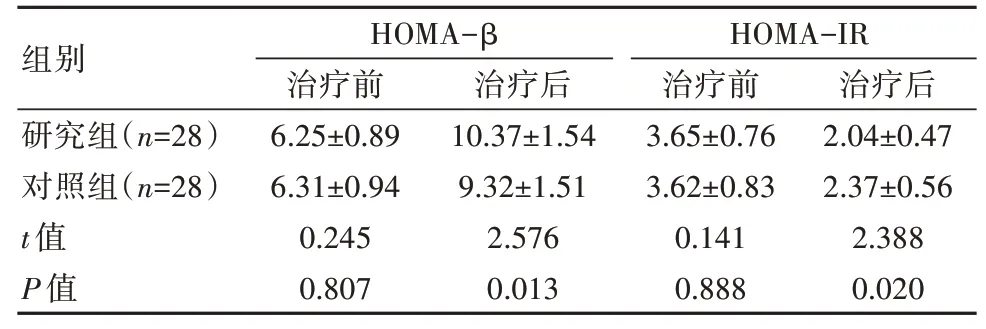
表4 两组患者治疗前后胰岛功能比较(±s)
?
2.4 两组患者不良反应发生情况比较
两组不良反应发生率比较,差异无统计学意义(P>0.05),见表5。

表5 两组患者不良反应发生情况比较
3 讨论
达格列净是一种高效、可逆和选择性的钠-葡萄糖协同转运蛋白2 抑制剂,在世界范围内用于治疗2 型糖尿病。在欧盟,当单独的饮食和运动不能提供足够的血糖控制时,1 次/d 口服达格列净被批准用作2 型糖尿病的单一疗法(用于二甲双胍不耐受的患者)和附加联合疗法(与其他降糖药,包括胰岛素等)。达格列净通过抑制位于近曲小管的高容量葡萄糖转运蛋白钠-葡萄糖协同转运蛋白-2,减少葡萄糖在肾脏中的重吸收,并促进其在尿液中的排泄,从而降低葡萄糖水平。
3.1 达格列净对初诊2 型糖尿病患者肠道菌群的影响
临床相关研究指出,2 型糖尿病患者肠道微生物组成变化可能会对降糖药物的疗效及代谢造成一定影响,肠道微生物组成不同患者对降糖药物血糖反应性并不一致[6-7]。达格列净为临床新型药物,是可逆和选择性的钠-葡萄糖协同转运蛋白2抑制剂,在降低血糖水平的同时,还降低了低血糖发生风险[8]。本研究结果显示,治疗后,两组患者酵母菌、肠球菌、肠杆菌数量均明显低于治疗前,乳杆菌、拟杆菌以及双歧杆菌数量均明显高于治疗前(P<0.05),说明二甲双胍与达格列净均可有效对初诊2型糖尿病患者肠道菌群进行调节,能够提升有益菌群数量;同时,研究组患者酵母菌、肠球菌、肠杆菌数量明显低于对照组,乳杆菌、拟杆菌以及双歧杆菌数量明显高于对照组(P<0.05),说明达格列净可进一步改善初诊2 型糖尿病患者肠道菌群数量,其调控效果优于二甲双胍。不过目前对于钠-葡萄糖共转运蛋白2 抑制剂对肠道菌群影响研究较少,大多数研究为动物试验,如Lee DM 等[9]的研究显示,达格列净可明显改善糖尿病模型大鼠的肠道菌群组,双歧杆菌等益生菌含量增加,而有害菌含量降低。
3.2 达格列净对初诊2 型糖尿病患者胰岛素抵抗和胰岛β 细胞功能的影响
胰岛素抵抗在临床上被定义为已知量的外源性或内源性胰岛素无法像健康人群增加个体的葡萄糖摄取和利用,此时机体会代偿性增加胰岛素分泌,从而出现高胰岛素血症,进而维持血糖水平稳定性[10]。有研究指出,胰岛素抵抗可能由胰岛素信号传导缺陷、葡萄糖转运蛋白缺陷或脂毒性引起;胰岛β 细胞功能障碍被认为是由胰岛淀粉样蛋白沉积、氧化应激、过量脂肪酸或缺乏肠促胰岛素作用引起的[11-12]。临床上,胰岛素抵抗往往会贯穿疾病整个发展过程,HOMA-IR、HOMA-β 反映了糖尿病患者的胰岛素功能,其中HOMA-β 降低说明患者体细胞对胰岛素受体敏感性的降低[13-14]。本研究结果显示,治疗后两组患者HOMA-β 高于治疗前,HOMA-IR 低于治疗前(P<0.05),说明二甲双胍与达格列净均可提高患者周围组织对胰岛素敏感性,而研究组HOMA-β 以及HOMA-IR 指标情况优于对照组(P<0.05),说明达格列净可进一步改善患者胰岛素功能。达格列净可促进葡糖激酶合成及降血糖素分泌,进而改善胰岛β 细胞功能;同时,达格列净还可以抑制糖毒性所诱导的氧化应激反应,从而起到保护残存胰岛β 细胞的再生功能作用[15-16]。本研究中,两组患者治疗后血糖及血脂水平均得到改善(P<0.05),说明二甲双胍与达格列净均可改善患者血糖及血脂代谢。
综上所述,达格列净对初诊2 型糖尿病患者肠道菌群、胰岛素抵抗和胰岛β 细胞功能有显著影响,可调节菌群失衡及提升有益菌群数量,并可改善其胰岛素抵抗、胰岛β 细胞功能及糖脂代谢。但本研究亦存在一定不足,如样本量偏少、单中心研究等,随后可扩大样本量,开展多中心及前瞻性研究,进一步验证达格列净的疗效。

