无导线起搏与传统起搏对三尖瓣反流短期影响的对比研究
郭雨龙 付明鹏 刘晨 乔宇 郭金锐 刘可 郭涛
650102 昆明,云南省阜外心血管病医院心律失常中心
心脏起搏是严重心动过缓最有效的治疗方式。传统心脏起搏器由脉冲发生器及相连接的电极导线构成,电极导线一般通过上腔静脉途径植入心腔内,右心室起搏电极导线跨过三尖瓣进入右室内固定。但是在以机械机制为主的多种机制介导下,传统心脏起搏会有加重恶化三尖瓣反流风险。无导线起搏是近年来最新的心脏起搏技术,与传统起搏器不同,无导线起搏器体积仅有胶囊大小,可通过特殊的输送装置,经下腔静脉途径植入右心室内,植入成功后输送装置可完全撤除,具有创伤小、恢复快,以及避免了囊袋并发症等特点。其心腔内留存的无导线起搏器仅在右心室内,不会遗留跨三尖瓣的电极导线。但是,无导线起搏对患者三尖瓣反流影响的临床研究数据较少,且尚无直接比较无导线起搏与传统起搏的报道。因此,我们通过纳入无导线起搏与匹配的传统起搏患者,在术前与术后短期通过经胸超声心动图评估三尖瓣反流情况,比较两组之间三尖瓣反流恶化的发生率,以此评估无导线起搏对三尖瓣反流的影响,希望能为无导线起搏的进一步推广应用提供有价值的临床信息。
1 对象和方法
1.1 研究对象
回顾性队列研究。纳入2020年1月至2022年11月在云南省阜外心血管病医院新植入起搏器患者,分为无导线起搏组和传统起搏组。纳入标准:(1)无导线起搏组符合无导线起搏适应证,且成功完成无导线起搏器植入手术者;(2)传统起搏组按照年龄、性别进行1∶1匹配,纳入同期就诊的符合传统起搏适应证且成功完成植入者。排除标准:(1)因传统起搏感染、电极故障或电池耗竭而转用无导线起搏者;(2)仅植入心房电极单腔起搏器者;(3)原有起搏器更换或升级者。本研究符合医学研究伦理学要求(编号:2022-94)。所有患者均知情同意。
1.2 方法
1.2.1 无导线起搏器植入手术 采用美敦力无导线起搏器(型号MicraTMMC1VR01或MicraTMAV MC1AVR1),所有操作均在导管室血管造影机透视指导下完成。穿刺右股静脉,置入导引钢丝,逐级扩张;若右股静脉穿刺或置入导丝不顺则换用左股静脉,沿导引钢丝置入输送装置,应用输送装置将无导线起搏器送至右心室内;多体位投照(至少三个体位:右前斜30°、左前斜45°及正位)确认跨过三尖瓣到达右心室中下间隔部,造影确认与心肌贴靠情况满意后,施加一定压力推送输送系统,并释放无导线起搏器,稍微回退输送鞘管,通过牵拉试验证实无导线起搏器头端勾挂满意,且测试阈值、阻抗、感知等参数满意后方可剪断拉绳;若不满意,则回收后重新定位释放。整个手术过程中,静脉推注3 000 U肝素,输送鞘管持续肝素盐水冲洗,最后撤除输送装置、缝合伤口,最后加压包扎。
1.2.2 传统起搏器植入手术 采用传统起搏器,所有操作均在导管室血管造影机透视指导下完成。穿刺左锁骨下静脉或腋静脉,置入导引钢丝,若穿刺或置入导丝不顺则改为右侧植入,沿锁骨下做4~5 cm皮肤切口,逐层分离至深筋膜层,制作合适大小的皮下囊袋,应用可撕开鞘管置入起搏电极,右房电极定位固定至右心耳,右室电极定位固定至右室间隔部或心尖部(均使用主动固定电极),测试阈值、阻抗、感知等参数满意后,拔除可撕开鞘管,电极尾端连接脉冲发生器并埋置于囊袋内,充分止血、冲洗后逐层缝合,最后加压包扎。
1.3 观察指标和随访
所有患者在植入术前1周内及术后6个月内完成经胸超声心动图对三尖瓣反流情况进行评估。使用GE或飞利浦超声探头,在彩色血流多普勒下测量三尖瓣反流束面积与右心房面积比和(或)缩流颈宽度综合评估三尖瓣反流情况的变化。其中,面积比<10%为微量反流,10%~20%为少量或轻度反流,21%~40%为中量或中度反流,>40%为大量或重度反流;缩流颈宽度<3 mm为少量或轻度反流,缩流颈宽度3~7 mm为中量或中度反流,缩流颈宽度>7 mm为大量或重度反流。此外,三尖瓣反流恶化定义为与术前相比,术后面积比增加超过5%和(或)缩流颈宽度增加超过1 mm。
1.4 统计学方法

2 结果
2.1 两组的基线临床资料比较
如表1所示,两组的诊断差异有统计学意义,表现为无导线起搏组诊断为≥Ⅱ度房室传导阻滞的比例显著低于传统起搏组,而诊断为心房颤动伴RR长间歇的比例显著高于传统起搏组(P=0.005)。其余基线临床资料相似,差异均无统计学意义(均为P>0.05)。
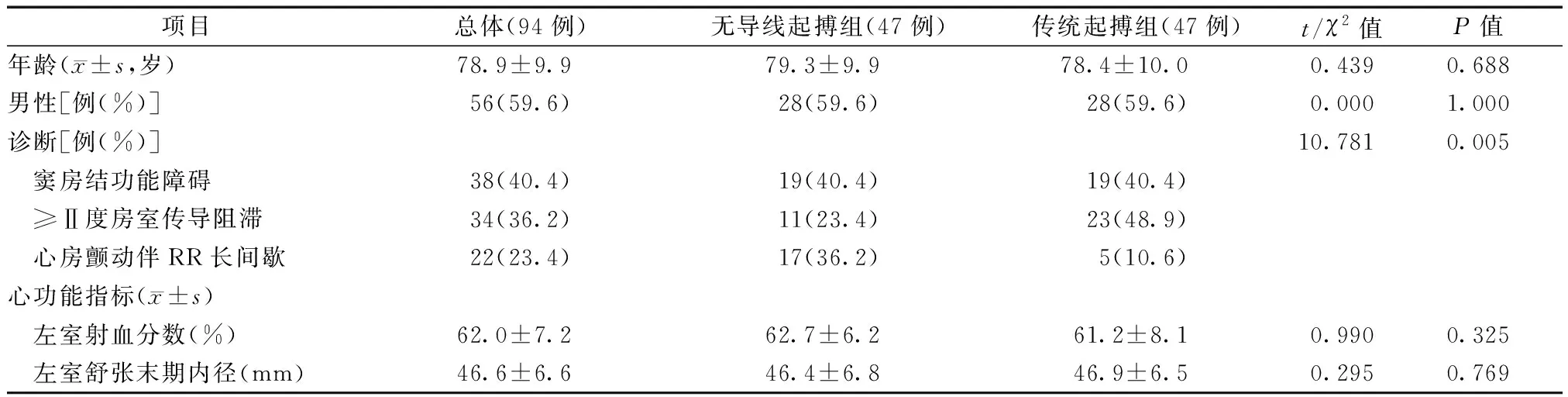
表1 两组的基线临床资料比较
2.2 两组的起搏器植入术后即刻右室电极参数比较
无导线起搏组中,38例(80.9%)使用MicraTM
MC1VR01(起搏模式VVI),9例(19.1%)使用MicraTMAV MC1AVR1(起搏模式VDD),所有无导线起搏器均位于右室中低位间隔部。传统起搏组中,9例(19.1%)使用单腔起搏器(模式VVI),38例(80.9%)使用双腔起搏器(模式DDD);右室电极导线在心尖部3例(6.4%),在间隔部44例(93.6%)。如表2所示,两组起搏器植入术后右室电极的即刻参数均相似,差异无统计学意义(均为P>0.05)。
表2 两组起搏器植入术后即刻右室电极参数比较
2.3 两组术前和术后的三尖瓣反流情况比较
如表3所示,两组术前的三尖瓣反流情况差异有统计学意义(P=0.002),表现为无导线起搏组的无或微量三尖瓣反流率明显低于传统起搏组(P=0.009),而大量/重度三尖瓣反流率明显高于传统起搏组(P=0.003)。

表3 两组术前和术后的三尖瓣反流情况比较[例(%)]
两组术后的三尖瓣反流情况差异也有统计学意义(P=0.003),表现为无导线起搏组的无或微量三尖瓣反流率明显低于传统起搏组(P=0.002),而大量/重度三尖瓣反流率明显高于传统起搏组(P=0.007)。与术前比较,术后新增的有临床意义的三尖瓣中大量反流有12例,其中无导线起搏组6例(12.8%),传统起搏组6例(12.8%),组间比较差异无统计学意义(χ2=0.000,P=1.000)(图1)。

图1 两组发生三尖瓣反流情况比较
三尖瓣反流恶化者共29例(30.9%),其中无导线起搏组14例(29.8%),传统起搏组15例(31.9%),组间比较差异无统计学意义(χ2=0.050,P=0.823)(图1)。
2.4 术前三尖瓣反流程度对术后发生三尖瓣反流恶化的影响
进一步研究显示,术前三尖瓣无或微少量反流者在术后出现反流恶化的比例为29.3%(22/75),而术前三尖瓣中、大量反流者在术后出现反流恶化的比例为36.8%(7/19),两者之间比较差异无统计学意义(χ2=0.401,P=0.527)。
2.5 Logistic回归分析结果
采用二元logistic回归分析(Wald后退法),分析术后新增三尖瓣中、大量反流的影响因素,无导线起搏组纳入因素为年龄、性别、起搏适应证诊断、术前左室射血分数、舒张末期内径及术前三尖瓣反流情况,传统起搏器纳入因素除上述外,增加右室电极位置及起搏器类型(单腔或双腔)。最终在无导线起搏组中未发现影响术后新增三尖瓣中、大量反流的有统计学意义相关因素(均为P>0.05);而在传统起搏患者中,发现起搏器类型[Exp(B)=35.589,P=0.01]是独立影响因素,其中单腔起搏器患者术后出现新增三尖瓣中、大量反流的比例远高于双腔起搏器患者[4例比2例,44.4%(4/9)比5.3%(2/38),χ2=10.031,P=0.002]。
3 讨论
本研究发现,无导线起搏器与传统起搏器相比,术后短期发生三尖瓣反流恶化及新发中、大量三尖瓣反流的比例无统计学差异,故无导线起搏可能并不能够减少对三尖瓣反流的负面影响。
三尖瓣反流是右心室起搏的常见并发症。国外研究报道术后三尖瓣反流的发生率7%~21%,三尖瓣反流恶化或加重的比例为10%~45%[1]。一般认为,导致或加重三尖瓣反流的机制以机械损伤为主,机械机制主要包括植入过程中起搏电极导线直接损伤瓣叶导致穿孔或撕裂、导线嵌顿于瓣叶之间、导线与瓣叶粘连或与腱索缠绕等。与普通电极导线相比,更粗、更硬的除颤电极导线导致三尖瓣反流的概率更高;此外,长期高比例右室非生理性起搏、慢性右心扩大及三尖瓣环扩张也是远期三尖瓣反流发生及加重的因素。其中,术中电极导管对三尖瓣的直接机械损伤是短期发生三尖瓣反流的主要机制。使用的电极越硬、越粗或暴力操作等均是潜在的危险因素,而慢性电极导线粘连、高比例右室非生理起搏及右心扩大瓣环扩张则是远期发生三尖瓣反流的主要机制[1-3]。国内关于三尖瓣反流的报道的例数较少且还有争议,赵波等[4]发现长期右室心尖部起搏仅导致轻微反流,引起有临床意义的三尖瓣反流恶化的比例更低。邹宝明等[5]发现无论右室心尖部还是间隔部起搏都不会在短期内明显加重三尖瓣反流。
无导线起搏是最新的心脏起搏技术,与传统右室起搏不同,无导线起搏在植入后并不会长期遗留跨三尖瓣的电极导线,因此其对三尖瓣的影响及机制可能会不同。目前国外关于无导线起搏对三尖瓣反流作用的研究报道有限,而国内尚无相关报道。2019年Beurskens等[6]报道无导线起搏术后1年三尖瓣反流加重的比例为43%。2022年一项关于无导线起搏器的真实世界研究,纳入植入心房感知、心室起搏的无导线起搏器患者,发现中度以上的三尖瓣反流发生率为48.8%(21/43)[7]。因此,无导线起搏器导致或加重三尖瓣反流的风险依然存在,甚至可能比传统起搏器高。
此项研究发现,在起搏器植入术后短期内,总体三尖瓣反流恶化发生概率为30.9%,无导线起搏组为29.8%,传统起搏组为31.9%,考虑到本研究中我们为了更早地发现短期影响效果,所定义的三尖瓣反流恶化的超声心动图指标较为敏感,远比临床症状更早出现变化,因此该比例应该会高于真实世界中有临床症状的三尖瓣反流发病率。我们发现两组间差异无统计学意义,可认为无导线起搏并不能够减少对三尖瓣的负面影响。表1中两组间的入院诊断有统计学差异,无导线起搏组的心房颤动伴RR长间歇患者比例更高,这是其最早及最强的植入适应证,很可能对结果造成一定影响。由表3中可看出,本研究无导线起搏组术前的中、大量三尖瓣反流者更多,这是由于我们在开展无导线起搏器植入术初期误以为其对三尖瓣反流的影响较小,因此在病人选择上有了偏差,而后续统计分析发现术前反流程度并未影响其术后恶化情况,故这种差异并不影响本文的主要研究结论。而经过本研究之后,我们对无导线起搏与三尖瓣的相互作用又有了更多认识,将进一步优化及改善今后对患者的处理决策,希望能更好改善预后。
从表面上看,由于无导线起搏器并不会长期遗留跨瓣导线,从理论上来说慢性三尖瓣粘连及腱索缠绕的发生率可能会低于传统起搏器,似乎避免了传统起搏引发三尖瓣反流的一些机制。但是,无导线起搏器植入须使用更粗、更硬的输送装置,操作中对三尖瓣的损伤可能会大于传统起搏,发生瓣膜穿孔的风险是否增加尚无报道。另外,国外有学者发现,无导线起搏器植入后对三尖瓣瓣下复合体的干扰较大,瓣下复合体是个解剖概念,主要指与瓣膜、腱索连接的乳头肌,三尖瓣下一般有三组乳头肌,前组在右室游离壁,下组及间隔组分别在下壁及右室间隔面,下组及后组乳头肌可能表现不完全而腱索就直接连接到间隔面或心室壁[8]。固定于间隔面的无导线起搏器虽然无跨瓣导线,但可能会显著影响间隔侧的三尖瓣瓣下复合体功能,由此加重三尖瓣反流。然而,目前对于无导线起搏器与三尖瓣相互作用的认识有限,还需要进一步的研究及临床实践来明确,尤其需要心脏外科及心脏结构专业与起搏电生理专业的合作。
本研究有一些局限性。本研究仅为临床观察性研究,例数较少,并非严密设计的随机对照研究,而且三尖瓣反流的可能影响因素较多,本研究也未能完全排除无导线/传统起搏选择以外的其他可能干扰因素,结论的说服力有限。总之,与传统起搏器相比,无导线起搏器可能并不减少术后短期发生三尖瓣反流的风险。
利益冲突:无