无阿片化全身麻醉在甲状腺次全切术中的应用效果▲
伍国芳 谢海龙 罗玉金
(湖南省娄底市中心医院麻醉科,湖南省娄底市 417000)
阿片类药物是全身麻醉诱导及麻醉维持的常用药物,可以减轻麻醉所致的应激反应,维持机体血流动力学平稳。临床上常以芬太尼或舒芬太尼作为麻醉诱导,并以瑞芬太尼静脉泵注作为麻醉维持。研究发现,术中静脉泵注瑞芬太尼不但可以减少镇静催眠药物的用量,还能缩短患者术后苏醒时间[1]。虽然目前阿片类药物的镇痛效果及优势确切,但仍可能发生不良反应,如呼吸抑制、恶心、呕吐、痛觉过敏、免疫抑制、皮肤瘙痒、肌阵挛等。近年来为了控制阿片类药物的用量和加速患者的康复,有学者提出了无阿片类药物麻醉(opioid-free anesthesia,OFA)的概念。OFA指为了避免阿片类药物的不良反应,在术中联合应用其他药物(如非甾体抗炎药、右美托咪定、利多卡因、氯胺酮等)或联合区域阻滞技术,为手术患者提供有效的镇痛效果,促进患者术后的快速康复[2]。作为新的麻醉方式,OFA目前只用于一些特定手术,有关OFA应用于甲状腺次全切手术的报告较为少见。本研究探讨基于艾司氯胺酮复合右美托咪定的无阿片化全身麻醉应用于甲状腺次全切手术中效果,以期为临床麻醉方案的优化提供参考。
1 资料与方法
1.1 临床资料 选择2021年10月至2022年6月在湖南省娄底市中心医院进行甲状腺次全切除术的80例患者作为研究对象。纳入标准:(1)符合甲状腺次全切手术指征;(2)行择期手术;(3)年龄30~60岁;(4)美国麻醉医师协会分级Ⅰ~Ⅱ级;(5)无心、脑、肾等重要器官及重要系统严重疾病。排除标准:(1)术前1个月使用过α受体激动剂或α受体拮抗剂的患者;(2)手术前48 h内服用过阿片类药物、非甾体抗炎药及其他影响研究结果药物的患者;(3)有艾司氯胺酮、丙泊酚、右美托咪定使用禁忌证或对上述药物过敏的患者;(4)有阿片类药物、艾司氯胺酮药物成瘾史的患者。根据随机数字表法将患者分为无阿片化全身麻醉组(A组)和基于阿片类药物的全身麻醉组(B组),每组40例。两组患者的性别、年龄、体质指数、手术时间比较,差异均无统计学意义(均P>0.05),具有可比性,见表1。本研究经湖南省娄底市中心医院医学伦理委员会批准,并与患者及其家属签署知情同意书。

表1 两组患者一般资料的比较
1.2 麻醉方法 (1)麻醉前常规处理:所有患者术前禁食8 h、禁饮4 h。入手术室后立即开放外周静脉通路,静脉持续输注乳酸林格氏液,同时通过心电监护仪监测心电图、无创血压、心率、脉搏血氧饱和度(pulse oxygen saturation,SpO2)、呼气末二氧化碳分压(partial pressure of end-tidal carbon dioxide,PetCO2)及脑电双频指数(bispectral index,BIS)。对患者行Allen试验(检查手部的血液供应,桡动脉与尺动脉之间的吻合情况),Allen试验阴性后在局部麻醉下行右侧桡动脉穿刺置管,实时监测有创动脉压的变化。(2)麻醉方法:A组患者在麻醉诱导前10 min静脉泵注右美托咪啶(江苏恒瑞医药股份有限公司,国药准字H20090248,规格为100 μg/支)0.5 μg/kg(用生理盐水配制成50 mL),随后以0.4 μg/(kg·h)的速度持续静脉泵注[3]。麻醉诱导采用丙泊酚(西安力邦制药有限公司,规格为20 mL ∶200 mg,国药准字H19990282)1.5 mg/kg、艾司氯胺酮(江苏恒瑞医药股份有限公司,规格为2 mL ∶50 mg,国药准字H20193336)0.4 mg/kg[4]、罗库溴铵(浙江仙琚制药股份有限公司,规格为5 mL ∶50 mg,国药准字H20123188)0.6 mg/kg,麻醉维持采用0.4 mg/(kg·h)艾司氯胺酮和6~12 mg/(kg·h)丙泊酚持续静脉泵注。B组患者在麻醉诱导前10 min静脉泵注50 mL生理盐水。麻醉诱导采用丙泊酚1.5 mg/kg、舒芬太尼(宜昌人福药业有限责任公司,规格为1 mL ∶50 μg,国药准字H20054171)0.4 μg/kg、罗库溴铵0.6 mg/kg,麻醉维持采用6~12 μg/(kg·h)瑞芬太尼(宜昌人福药业有限责任公司,规格为1 mg/瓶,国药准字H20030197)和6~12 mg/(kg·h)丙泊酚持续静脉泵注(具体用量根据术中体循环情况适时调整)。(3)麻醉后处理:麻醉诱导后3~5 min在可视喉镜下行经口气管插管。若插管时患者BIS超过60,或血压上升幅度超过20%,则追加丙泊酚0.5 mg/kg。若患者出现体动,则追加丙泊酚1 mg/kg。两组患者均根据术中BIS调整丙泊酚输注速度,使BIS维持在40~60之间。密切观察术中患者生命体征,当心率<50次/min时静脉注射阿托品0.5 mg,必要时可重复使用阿托品;若收缩压升高或降低幅度超过基础值的20%,可酌情使用血管活性药物,维持患者体循环稳定。设定潮气量6~8 mL/kg,呼吸频率为12~20次/min,维持PetCO2在35~45 mmHg之间。两组患者均在术毕停用所有麻醉药物,同时追加舒芬太尼0.01 μg/kg。
1.3 观察指标 (1)监测患者入手术室时(T0)﹑气管插管即刻(T1)﹑切皮时(T2)、切皮后30 min(T3)及手术结束时(T4)的平均动脉压(mean arterial pressure,MAP)、心率。MAP=舒张压+(收缩压-舒张压)/3。(2)记录患者术中丙泊酚用量、拔管时间(手术结束到气管导管拔除的时间)、定向力恢复时间(手术结束至患者定向力完全恢复的时间,患者能正确回答自己名字和当日日期即认定为定向力恢复)。(3)应用疼痛视觉模拟量表(Visual Analogue Scale,VAS)[5]评定患者术毕30 min后(T5)、术毕1 h后(T6)、术毕4 h后(T7)时的疼痛程度,量表总分为10分,0分为无痛,1~3分为轻微疼痛,能忍受,4~6分为疼痛较严重,但尚能忍受,并影响睡眠,7~10分为疼痛剧烈,难以忍受,影响日常生活。(4)记录两组患者术后24 h内呼吸抑制、头昏、躁动、恶心/呕吐的发生情况。
1.4 统计学分析 应用SPSS 19.0软件进行统计学分析。满足正态分布的计量资料以(x±s)表示,组间比较采用两独立样本t检验;重复测量计量资料的比较采用重复测量方差分析;计数资料以例数(百分比)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 不同时点两组患者MAP﹑心率的比较 两组患者的MAP、心率比较,差异均有统计学意义(F组间=135.940,P组间<0.001;F组间=120.692,P组间<0.001),MAP、心率均有随时间变化的趋势(F时间=18.976,P时间<0.001;F时间=19.180,P时间<0.001),MAP、心率的分组与时间均有交互效应(F交互=8.249,P交互=0.001;F交互=7.699,P交互=0.003)。两组患者T1、T2时的MAP均高于T0,且A组患者的MAP均高于B组(均P<0.05);两组患者T1时的心率均高于T0,且A组患者的心率高于B组(均P<0.05)。见表2。
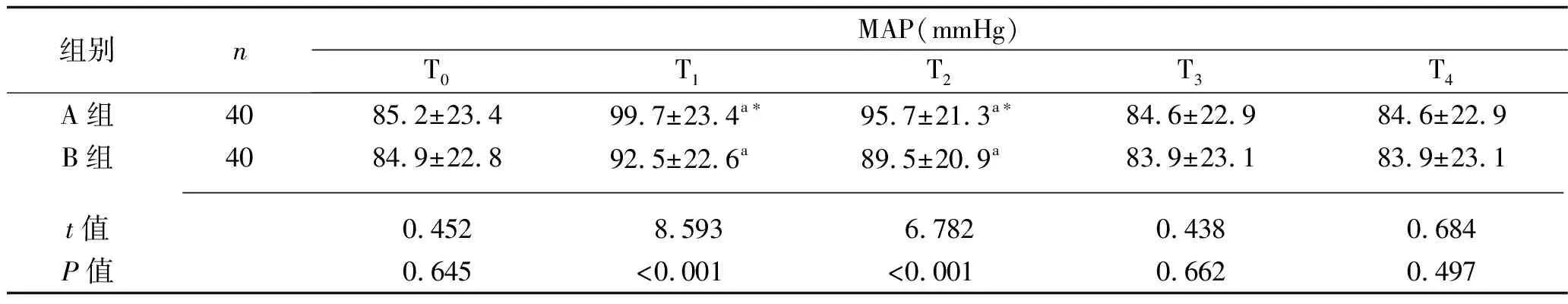
表2 不同时点两组患者MAP﹑心率的比较(x±s)
2.2 两组患者术中丙泊酚用量、拔管时间、定向力恢复时间的比较 A组患者术中丙泊酚用量多于B组,定向力恢复时间长于B组(均P<0.05)。两组患者拔管时间差异无统计学意义(P>0.05)。见表3。

表3 两组患者丙泊酚用量﹑拔管时间﹑定向力恢复时间的比较(x±s)
2.3 不同时点两组患者疼痛VAS评分的比较 两组患者疼痛VAS评分比较,差异有统计学意义(F组间=43.601,P组间<0.001),疼痛VAS评分有随时间变化的趋势(F时间=105.671,P时间<0.001),分组与时间有交互效应(F交互=62.810,P交互<0.001)。两组患者T6、T7时的疼痛VAS评分均高于T5,且A组患者T7时的疼痛VAS评分低于B组(P<0.05)。见表4。

表4 不同时点两组患者疼痛VAS评分比较(x±s,分)
2.4 两组患者术后不良反应发生率的比较 A组术后恶心/呕吐、呼吸抑制的发生率均低于B组(均P<0.05)。两组术后头昏、躁动的发生率差异均无统计学意义(均P>0.05)。见表5。

表5 两组患者术后不良反应发生率的比较[n(%)]
3 讨 论
随着“舒适化医疗及快速康复”概念的提出,临床医师在诊疗时对患者的疼痛管理及快速康复更加重视,希望可以在有效镇痛的前提下,尽量避免或减少镇痛药物引起的不良反应。OFA是一种结合多种非阿片类药物和/或多种技术的多模式麻醉策略,其目的是在不使用阿片类药物的情况下获得更高质量的麻醉效果,减少麻醉镇痛药物不良反应的发生,促进患者的早日康复[6]。然而,目前的研究集中于探究OFA的优势,对其不足之处的探讨比较少见[7-11]。基于此,本研究对比无阿片化全身麻醉和阿片化全身麻醉的效果及安全性,以期更深入地了解无阿片化麻醉的临床应用价值。
阿片类药物作为全身麻醉的首选镇痛药物,不但镇痛作用强,还可通过抑制交感神经起到稳定血流动力学的作用。研究表明,OFA不易维持血流动学稳定,术中血流动力学不良事件的发生率较阿片化麻醉显著增多,因此目前OFA一般应用于手术时间短、出血少及血流动力学相对稳定的特定手术[12-13]。甲状腺次全切除术具有手术时间短、出血少、术后恢复快、住院时间短、治愈率高及并发症少等特点[14]。笔者认为将OFA应用于甲状腺次全切术,术中发生不良反应的概率低、安全性较高,具有一定的可行性。
临床实施 OFA 时常用的非阿片类药物包括右美托咪定、非甾体抗炎药、利多卡因、氯胺酮、盐酸可乐定、地塞米松等。每种药物作用机制不同,合理配伍可为患者提供良好的镇静和镇痛效果,为手术创造更好的条件。右美托咪定是常用的一种麻醉辅助药物,具有镇静、镇痛、调节应激反应及减少术中麻醉药物用量的作用,但右美托咪定会降低交感神经系统兴奋性,导致血浆皮质醇和儿茶酚胺浓度降低,从而引起心动过缓及血压下降。艾司氯胺酮是氯胺酮的纯右旋异构体,通过与多个受体结合,如N-甲基-D-天冬氨酸受体、阿片受体、M胆碱受体、单胺受体等,发挥催眠、镇静、镇痛的作用,与氯胺酮比较,其镇痛镇静作用更强、代谢更快、副作用更少,并且可以防止术后痛觉过敏的发生,在临床麻醉中的应用性更强[15]。但艾司氯胺酮会使交感神经兴奋,引起患者血压升高、心率增快及心排量增加。研究显示,右美托咪定与艾司氯胺联合应用,可以发挥协同作用,具有更强的镇痛镇静作用,使得患者血流动力学更平稳[13]。因此,笔者认为右美托咪定联合艾司氯胺酮在OFA技术中具有广阔的应用前景,但目前相关报道少见。本研究选用右美托咪定与艾司氯胺作为OFA方案的药物,观察其麻醉效果及安全性。
患者术中的循环状况间接反映了麻醉药物的镇痛作用及控制应激反应的效果,这是因为皮肤和气管黏膜周围分布着丰富的感觉神经末梢,当受到切割和牵拉时,交感-肾上腺髓质系统高度兴奋,大量儿茶酚胺被释放,从而引起患者心率加快、血压急剧升高,血流动力学发生明显变化,因此,合理应用麻醉药物能维持循环的相对稳定[16-17]。本研究结果显示,T1、T2时A组患者的MAP均高于B组,T1时A组患者的心率高于B组(P<0.05)。分析其原因:(1)阿片类药物的镇痛及抑制应激反应的作用比艾司氯胺酮联合右美托咪定更强,阿片类药物在维持术中循环稳定方面具有明显优势;(2)术中维持应用的艾司氯胺酮剂量不足,镇痛效果欠佳;(3)艾司氯胺酮本身具有兴奋交感神经的作用,导致患者血压升高、心率加快。在本研究中,A组患者术后恶心/呕吐、呼吸抑制的发生率低于B组(P<0.05),说明无阿片化全身麻醉能避免阿片药物的不良反应,在临床应用中具有一定的优势。本研究结果还显示,术毕4 h后A组患者疼痛VAS评分低于B组(P<0.05),笔者认为可能与长时间输注瑞芬太尼引起患者的爆发性疼痛有关,长时间输注瑞芬太尼出现的爆发性疼痛一般在停止输注后4 h或24 h出现[18]。此外,本研究中,A组的丙泊酚用量多于B组(P<0.05),可能是因为艾司氯胺酮兴奋交感神经导致BIS检测值高于实际值,如需将BIS维持在一定的范围会导致丙泊酚的输注量比实际需要量多。本研究中,A组患者的定向力恢复时间长于B组(P<0.05),可能与艾司氯胺酮代谢时间比瑞芬太尼相对更长有关。但笔者认为,如果在手术结束前提早停药,患者苏醒时间和定向力恢复时间可能不受艾司氯胺酮影响。
综上所述,与传统基于阿片类药物的全身麻醉相比,基于右美托咪定复合艾司氯胺酮的无阿片化全身麻醉能满足甲状腺次全切除术的手术要求,可有效减轻患者术后4 h的疼痛感,对术后拔管时间无明显影响,术后恶心/呕吐、呼吸抑制发生率低,但术中血流动力学变化较大、定向力恢复较迟,基于右美托咪定复合艾司氯胺酮的无阿片化全身麻醉的临床应用效果尚需进一步观察。另外,本研究中艾司氯胺酮的麻醉诱导剂量为相关文献[4]中推荐的剂量,麻醉维持剂量为药品说明书所规定的剂量,笔者认为应在今后的研究中进一步探讨艾司氯胺酮的最佳剂量。

