纳米流体用于二氧化碳吸收分离研究进展
娄宝辉,吴贤豪,张驰,陈臻,冯向东
(1 浙江大学材料科学与工程学院,浙江 杭州,310027;2 浙能技术研究院有限公司,浙江 杭州 311121;3 浙江省火力发电高效节能与污染物控制技术研究重点实验室,浙江 杭州 311121)
在过去的十年内,我国的二氧化碳排放量平均以每年1.8%的速率递增,2021 年达到120.4 亿吨,占全球二氧化碳排放总量的30.9%[1]。由于二氧化碳是引发全球变暖的重要原因之一,联合国政府间气候变化专门委员会提出2050 年全球平均气温增长不超过2℃,与之对应的需减少50%的二氧化碳排放量。为了应对二氧化碳排放对全球气候变化的影响,大量的减碳技术应运而生,其中碳捕获、利用与封存(CO2capture storage and utilization,CCUS)由于具有减排规模大、减排效益明显的特点成为减碳技术的研究重点之一。然而,CCUS 技术目前还面临一些技术和经济壁垒因此无法实现在电厂的实际应用。CCUS 技术中关键一步是二氧化碳的捕集,目前燃煤电厂二氧化碳捕集技术按照二氧化碳吸收装置的安装位置可以分为燃烧前捕集、燃烧中捕集、燃烧后捕集三种[2-4]。其中燃烧后捕集被认为是目前最具有工业化潜力的技术。吸附、吸收、低温和膜分离是用于CO2捕获的主要技术。在过去几十年的研究中,对于CO2的气液吸收已经取得了很多进展。此技术也可以应用于其他可再生能源领域对二氧化碳的吸收。通常情况下,使用溶剂的新型吸收方法得益于物理和/或化学现象,以改善吸收过程,这种技术不仅捕集效率高装置简单,同时在低浓度的CO2中具有更高的效率与选择性,因此它在从含有低浓度CO2的燃烧后工艺的烟气混合物中分离CO2方面具有更好的性能[5-6],其缺点是吸收剂再生过程中需要消耗大量蒸汽,再生能耗较高[7]。因此,未来该技术的发展主要侧重于对吸收剂配方的优化来进一步降低能耗以获得技术推广。
纳米流体是Choi 等[8]提出的一种由纳米颗粒以预先指定的比例分散在无机或有机液相中产生的具有稳定均匀性的胶体分散系统。对于气体吸附分离领域,纳米材料可以增强吸收剂的传热和传质性能[9-10],提高解吸速率同时降低解吸能耗,进而提升其气体吸附分离效果。相比于传统的二氧化碳有机胺吸收剂,纳米流体具有传热传质性能优异、高热稳定性、饱和蒸气压低、吸收速率快、解吸能耗低等优点。针对纳米流体在二氧化碳化学吸收领域的研究,本文主要论述纳米颗粒与有机胺合成的纳米流体吸收剂强化二氧化碳吸收的相关进展。
1 纳米流体的分类
根据纳米颗粒与基液之间的作用力不同,可以将纳米流体分为纳米颗粒-基液混合吸收剂和纳米颗粒-基液复合吸收剂两种。前者主要通过物理作用相结合,后者则依赖于化学键的相互作用。
1.1 纳米颗粒-基液混合吸收剂
纳米颗粒-基液混合吸收剂(nanoparticle amine mixing solvents,NAMSs)是通过物理方法将纳米颗粒均匀分散到有机胺吸收剂基液中而形成的稳定流体。常用的纳米颗粒主要有Al2O3[11-12]、ZnO[13]、TiO2[14]、SiO2[15]、Fe3O4[16]、NiO2[17]等 氧 化 物纳米颗粒。表1列出了一些常用纳米颗粒的热物理性质。
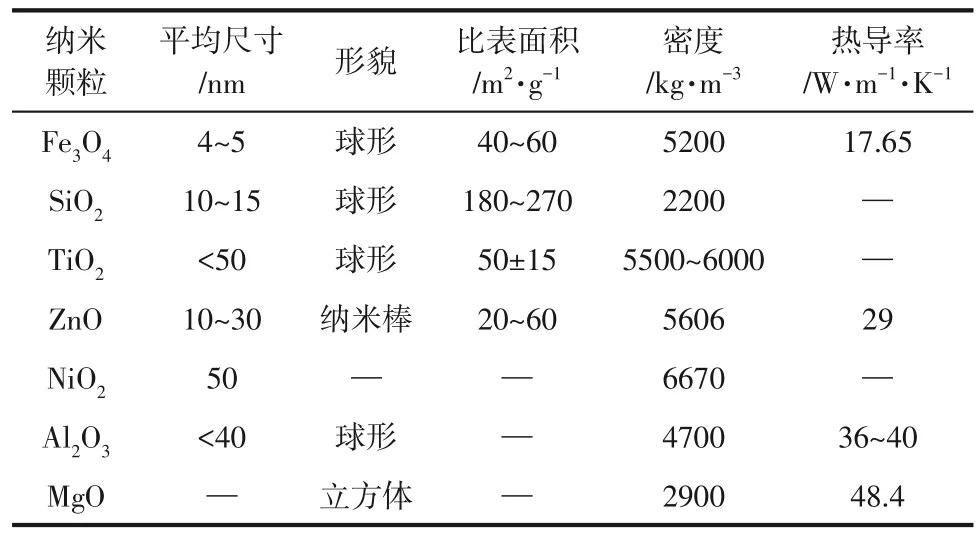
表1 常见纳米颗粒的热物理性质
在二氧化碳燃烧后捕集工艺中,有机胺类吸收剂是最为广泛利用的,其具有较高的二氧化碳吸收容量、高热稳定性以及与二氧化碳分子的高反应率[18]。空间位阻胺和烷醇胺是两类最常见的胺类吸收剂。一乙醇胺(MEA)、二乙醇胺(DEA)、甲基二乙醇胺(MDEA)分别属于简单烷醇胺的一级、二级、三级胺。不同种类的胺在对二氧化碳的吸收能力、反应动力学以及副反应是有区别的。其中,MEA具有捕集效率高、反应迅速、传质快等优点,被认为是最适合于工业化的吸收剂。与之相对应的纳米流体可采用有机胺类作为基液,将合成好的纳米颗粒与基液充分混合,通过物理相互作用形成稳定的纳米流体用于二氧化碳的吸收。
1.2 纳米颗粒-基液复合吸收剂
纳米颗粒-基液复合吸收剂(nanoparticle organic hybrid materials,NOHMs)是表面功能化的纳米颗粒,无需添加其他溶剂就能表现出类似液体的行为[19]。NOHMs 的制备方法主要是通过将聚合物链以离子键或共价键嫁接到纳米颗粒的表面[20],并能够将进行二氧化碳吸收的有机胺类通过化学键的方式结合在纳米材料表面[21]。相比于单纯的有机胺吸收剂,NOHMs 的传热传质性能更好,同时由于有机物的种类比较多,因此NOHMs 具有广泛的原料来源,可以针对不同的二氧化碳吸收场景进行调控。
NOHMs 主要有三部分组成,即纳米材料、基液以及耦合剂,三者的质量比约为14∶5∶1,根据作用力的不同,可以分为离子键和共价键两种类型。吸收剂基液可以直接与纳米材料相连也可以通过耦合剂的作用链接。如图1所示是典型的纳米颗粒-有机胺复合吸收剂的分子结构,其形成机制为将纳米级的SiO2与基液相混合,之后引入耦合剂得到[19]。合成NOHMs 常用的纳米颗粒主要包括SiO2、TiO2、碳纳米管(carbon nanotube,CNT)、Fe2O3、笼 型 聚 倍 半 硅 氧 烷 (polyhedral oligomeric silsesquioxane,POSS)等。在之前的研究中用于合成NOHMs 的CO2吸收剂一般为带有氨基或者醚基等碱性基团的有机物。
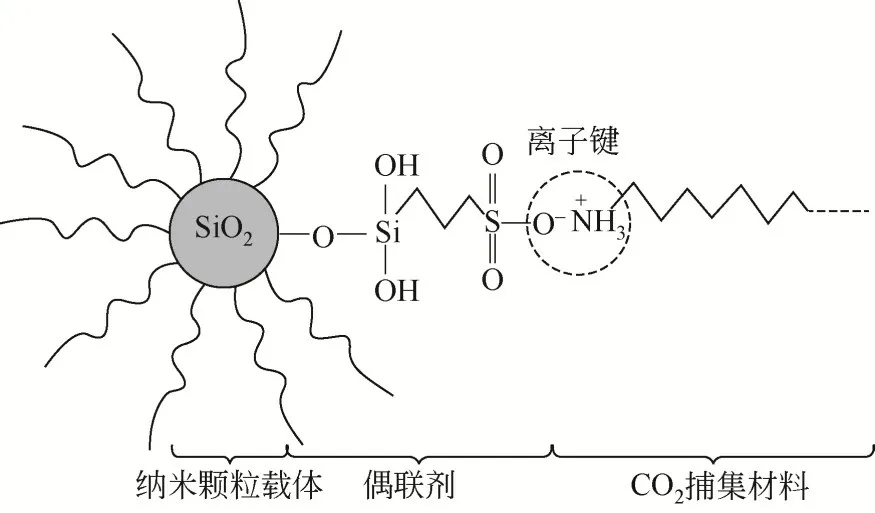
图1 典型的纳米颗粒-有机胺复合吸收剂的分子结构
2 纳米流体的制备方法
纳米流体优异的二氧化碳吸收性能依赖于其制备方法[22]。纳米流体中的纳米颗粒是完全分散的且不能发生团聚沉淀的,因此纳米颗粒的引入不改变基液本身的物化性质。如图2 所示,纳米流体的合成方法包括一步法和两步法两种。一步法的操作较为简单,采用磁力搅拌及蒸发沉淀的方式同时借助等离子体、微波辅助或激光手段在基液中直接生成纳米颗粒,得到纳米流体[23]。而两步法制备过程首先将纳米颗粒分散在基液中,然后通过辅助手段制备得到。尽管两步法制备的纳米流体具有小尺寸的纳米颗粒,表面活性高,但它们很容易结块,因此需要引入表面活性剂或利用超声波辅助来增加所获得的纳米流体的稳定性,并产生可分散的纳米颗粒悬浮液。

图2 纳米流体的合成方法
2.1 一步法制备纳米流体
纳米流体的一步法制备是在基液中直接制备纳米颗粒的方法,不涉及纳米颗粒的储存与分散步骤[24]。图3 为典型的一步法制备二氧化硅-基液纳米流体示意图,可以看出一步法能同时实现纳米颗粒在基液中的合成与分散,从而避免纳米颗粒被氧化。合成过程需要借助等离子体、微波辅助、激光等辅助手段将纳米颗粒均匀分散到基液中形成纳米流体。
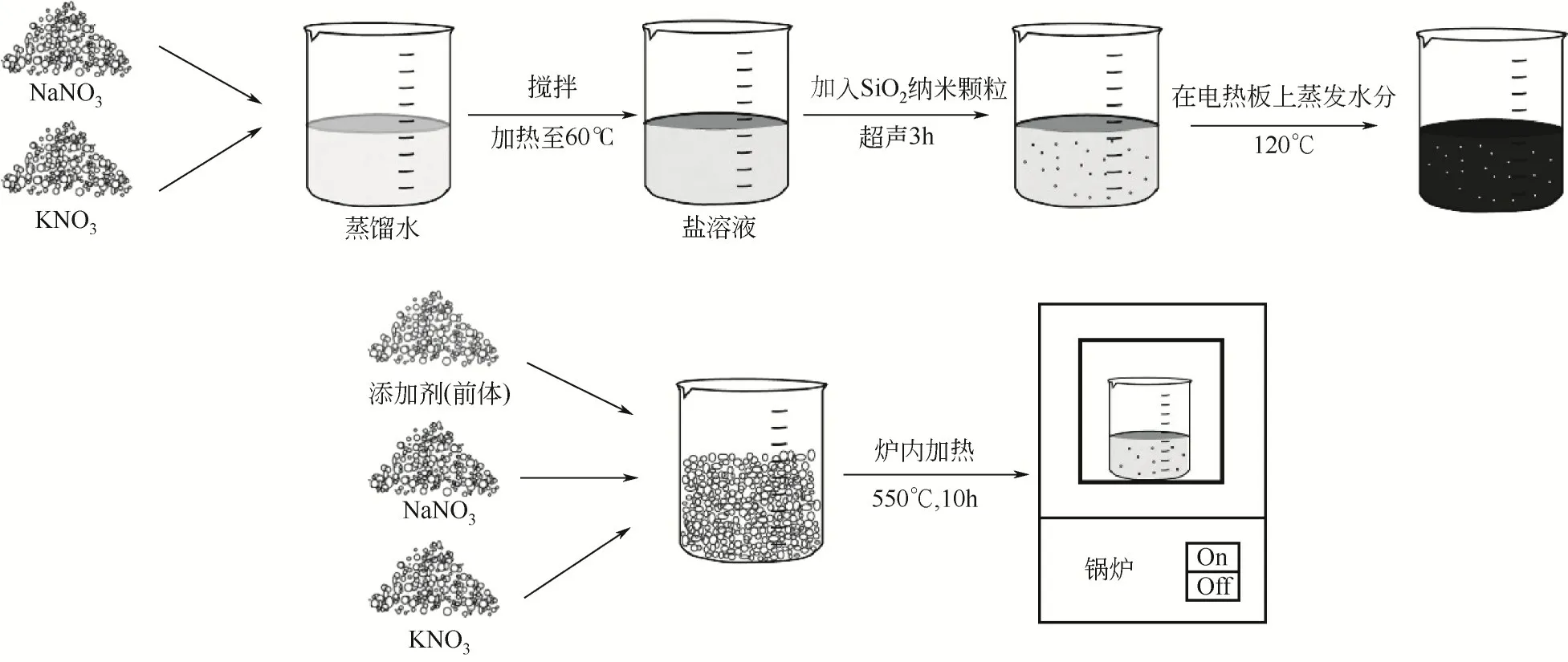
图3 一步法制备二氧化硅纳米流体示意图
2.2 两步法制备纳米流体
两步法制备纳米流体是将不同的纳米材料,如纳米颗粒等,通过物理、化学和机械方法加以利用[25]。直接应用的方法包括首先将纳米颗粒分散在基液中,然后使用稳定的方法,如利用超声波来增加所获得的纳米流体的稳定性,并产生可分散的纳米颗粒悬浮液。两步法的一些优点是成本低、工艺简单,可大规模制备纳米流体,并有望实现工业化[26]。然而,用这种方法预制备的纳米流体的稳定性很弱,而且使用表面活性剂在高温下也不适用。因此,在某些情况下,一些分散方法,如使用超声振动、添加表面活性剂、基液的pH 变化和超声处理相结合,以达到具有更好分散性能的悬浮液[27-28]。
3 纳米流体的结构与表征
纳米流体通常是由陶瓷(聚丙烯、氮化铝、纤维素等)、碳质材料(富勒烯、石墨烯、碳纳米管等)、金属(金、铜、铝等)和无机氧化物(二氧化硅、氧化梓、氧化铁等)在基液中分散制备的[29-30]。制冷剂、矿物油、高黏度的液体(如乙二醇)和低黏度的液体(如水),或各种液体的混合物(丙烯/水、水/乙二醇等)都可以作为基液使用。
3.1 纳米流体的结构
纳米流体可以通过离子键或共价键接枝聚合物链与纳米颗粒来合成[19]。因此,与传统的胶体悬浮液相比,纳米流体可以显示出一些优势[21]。首先,接枝聚合物与纳米流体中的纳米颗粒化学键合,而液体介质和纳米颗粒只是传统胶体悬浮液中的物理离散组分[31]。因此,纳米流体显示出与传统胶体悬浮液不同的热力学特性。图4 为二氧化硅-聚合物枝接纳米流体合成示意图,其中一个纳米流体单元由纳米级核心和聚合物链组成。可以有选择地设计这两个组件,以获得针对给定应用程序的特定功能[19]。此外,由于聚合物链与纳米流体中的纳米颗粒结合,因此可以防止聚合物链的损失,从而降低其蒸气压。因此,纳米流体也被认为是一类新的聚合物纳米复合材料和聚合物胶体[32]。

图4 二氧化硅-聚合物枝接纳米流体合成示意图
相比于吸收剂基液,NOHMs 纳米流体的密度略有增加。Park等[33]研究了以聚醚胺为基液的纳米流体的水溶液以及聚醚胺的水溶液密度变化,结果表明,纳米流体的密度相比之下提升了12.5%。图5 为纳米流体的结构示意图及实拍图。此外,Park等[34-35]对合成得到的纳米流体进行了二氧化碳吸附分离实验,结果表明NOHMs 在吸收CO2之后的体积膨胀率有所降低,与吸收剂基液相比,纳米流体的作用力更强,导致其黏度较高[36]。测试数据表明温度为30℃时,聚醚胺的黏度为260.2mPa·s,然而纳米流体的黏度却超过了1.0×104mPa·s。
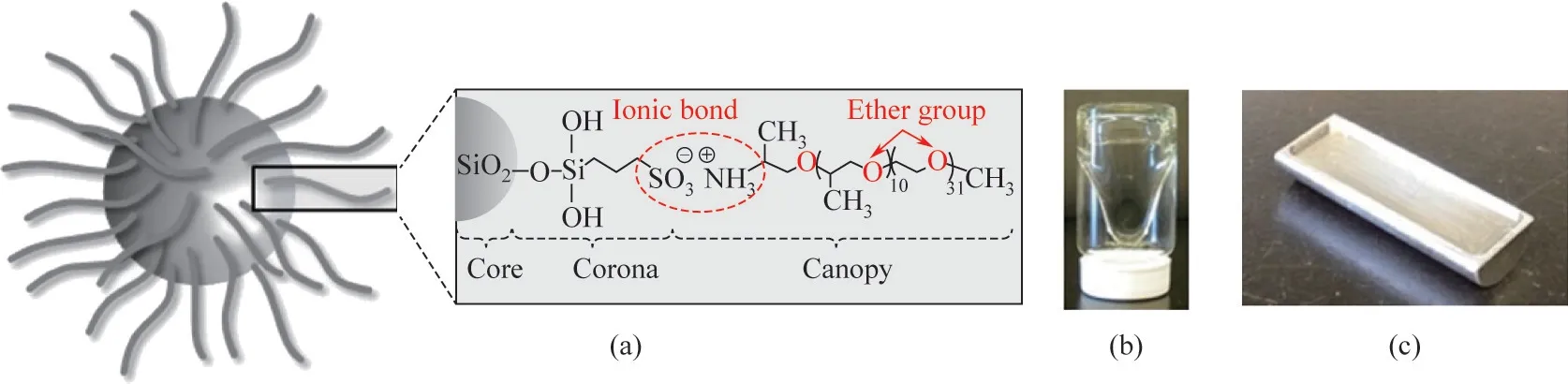
图5 二氧化硅-聚醚胺纳米流体的结构示意图及实拍图
3.2 纳米流体的稳定性
稳定性是影响纳米流体性能的重要技术指标[37-39]。由于范德华力的存在以及纳米颗粒布朗运动导致的碰撞加剧易造成纳米颗粒的团聚和沉淀[36,40]。具有悬浮颗粒的液体在受到范德华力、重力、浮力和静电排斥力等各种力的作用下容易失稳并形成沉积物。范德华吸引力和静电排斥力不利于任何胶体悬浮液的稳定性。用于各种应用的纳米流体(纳米颗粒在基础流体中的悬浮液)的功能和性能高度依赖于其稳定性[41]。悬浮液中存在的纳米颗粒相互碰撞并引起悬浮颗粒的团聚,从而形成较大的团簇。在引力、静电排斥力、范德瓦耳斯吸引力和浮力的影响下,纳米流体很容易失稳并生产沉淀。引力和范德华吸引力是任何胶体悬浮液不稳定的重要因素[42]。这意味着这些力有助于分散的颗粒相互粘连,并因此形成更大尺寸的聚合体。这些大颗粒会在引力的作用下从悬浮液中沉淀出来,并在容器底部形成沉淀。由于其高表面活性,纳米颗粒悬浮液显示出团聚倾向[43]。为了提高纳米流体的稳定性,悬浮在基础流体(水、油、酒精等)中的纳米颗粒应避免形成导致纳米颗粒从基础流体沉淀的大 聚 集 体。根 据DLVO (Derjaguin、Landau、Vewey 和Overbeek)理论,当范德华吸引势高于静电排斥势时,粒子往往会团聚并最终导致沉降[44]。纳米颗粒的沉降会导致微通道堵塞,会阻碍其在热交换器(增加污垢系数)、生物医学应用、提高采油率等多种应用中的性能。基于此研究人员在维持纳米流体的稳定性方面做了大量研究,如图6 所示,纳米流体的稳定方法总体上可以分为物理法和化学法两类[41]。
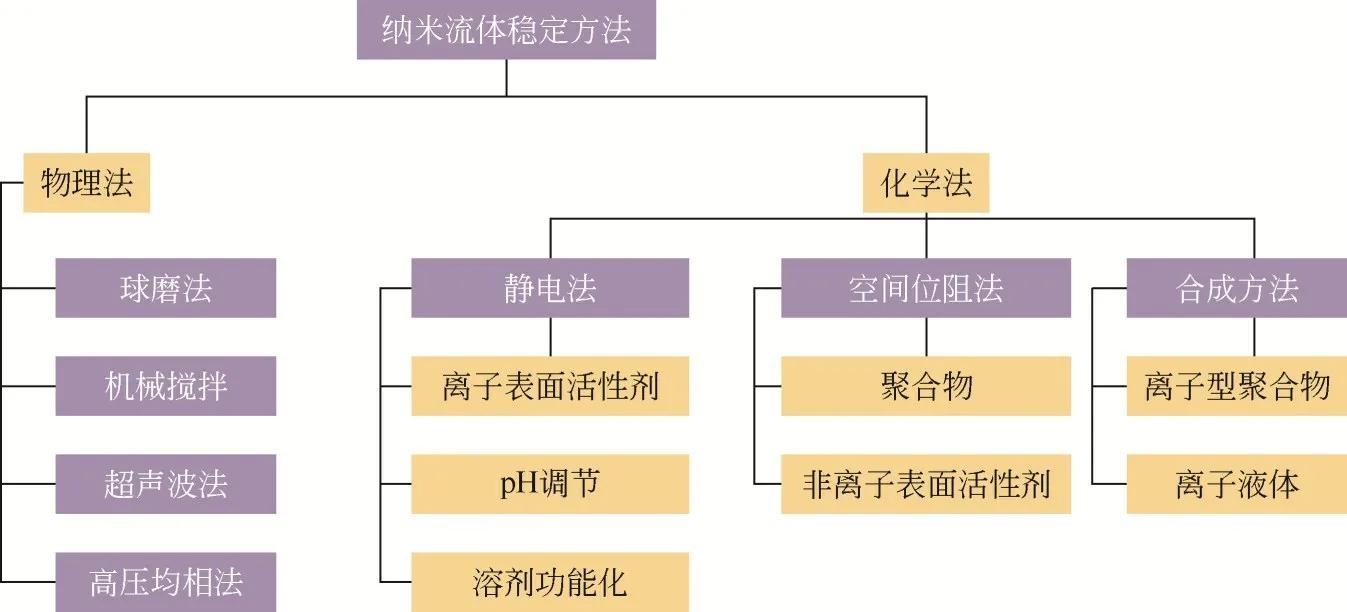
图6 纳米流体的稳定方法
此外,胶体悬浮液的稳定性也可以使用DLVO理论来解释。该理论基于以下假设:①粒子分散是稀释的;②范德华吸引力和静电力是唯一作用在悬浮粒子上的两个力;③重力和浮力被忽略;④胶体悬浮液本质上是均匀的;⑤整个胶体系统中的离子分布取决于三个因素,即静电力、布朗运动和熵诱导分散[45]。
3.3 纳米流体稳定性的评价方法
目前最常用的纳米流体稳定性评估方法是沉降法,这种方法的基础是纳米颗粒在重力作用下从纳米流体中沉降出来[46]。沉淀物的体积或重量是纳米流体稳定性的评价指标。如果上清液颗粒的浓度随着时间的推移保持不变,那么纳米流体被认为是稳定的[47]。因此,该方法处理的是观察容器中的纳米流体中的纳米颗粒随时间沉降的情况。一般来说,大多数研究认为稳定的时间框架是指在纳米流体中不发生明显的沉降,或者至少可以忽略沉降时间[48],但沉淀技术不是一种高效率的方法[49]。为了克服这个问题,研究人员采用了离心法,这是一种更省时的评估纳米流体稳定性的方法。在这种方法中,沉淀是在离心力的影响下加速的,而离心力比重力强得多,因此大大提高了评估效率[50]。
另一种确定纳米流体稳定性的方法是使用zeta电位测试,其中具有相同电荷的纳米颗粒之间发生相互排斥,因此具有高表面电荷的颗粒之间在碰撞中几乎没有聚集的趋势[51]。这种方法可以帮助描述一些实验数据的差异,其中悬浮液的结构和纳米粒子的表面电荷因使用表面活性剂的不同而改变[52]。zeta电位技术是确定纳米流体稳定性的一个基本测试,其原理基于电泳理论[53]。根据电泳理论,zeta电位可测量两个颗粒之间的排斥力[54]。根据稳定理论,当zeta电位出现高值表明颗粒在悬浮液中的溶解度高,这是由于颗粒之间的静电排斥力增加[55]。有人认为zeta电位为5mV或更低的悬浮液是不稳定的,会出现团聚现象,20mV 的悬浮液稳定性有限,但大于30mV的悬浮液具有物理稳定性,如果zeta 电位大于60mV,表明纳米流体具有极佳的稳定性[56]。
3.4 纳米流体的传热传质性能
纳米流体在理论上被归类为胶体分散系统,其特性与纳米颗粒的特性有关,如纳米颗粒的形状、特性、规模、含量,或其化学/物理特性[57]。与毫米级或微米级大小的颗粒相比,纳米流体更稳定,具有更高的热导率,使用纳米流体时压降和侵蚀更低,特别是在微通道中,因此被广泛应用于诸多行业,如化学工业、电子和机械、航空航天、生物医学、能源和电力等。此外,由于纳米流体具有较高的传质和传热系数,其作为传质和传热介质的应用已经引起了特别的关注[44]。
由于传质和传热的基本原理相似,纳米颗粒也能影响流体的传质。研究人员认为,使用少量的可溶性颗粒将大大增加气体吸收率。Ruthiya 等[58]证明了传质率的提高,评估了四种可能的机制来改善气液系统的传质。Krishnamurthy等[59]是最早研究纳米流体中传质改进的小组之一。他们比较了荧光素染料液滴在去离子水和水中的纳米流体混合物中的扩散性。目前,有关纳米流体的传热传质性能的研究重点是利用纳米颗粒来提高纳米流体的吸收率、传质率和碳的负载率,从而降低液体和气体相之间的传质阻力[60]。应用纳米流体作为CO2的吸收剂,可以通过提高吸收率来降低CO2捕获系统的能源成本。例如,得益于气体水合物的形成过程,在CO2捕集和封存(CCS)回收中利用纳米氧化石墨烯(NGO)来减少CO2捕集厂的能源消耗和成本[61]。纳米颗粒在吸收溶剂中的分散可以改善吸收性能,因为这些颗粒的高比表面积会产生布朗运动、微对流和传输效应。与尺寸较大的相同颗粒相比,小尺寸的纳米颗粒也能提高CO2的吸收速度和能力[62]。然而,如果纳米颗粒的浓度超过了最佳点,纳米颗粒就会结成团簇,阻止气体被吸收到液相中[63-64],进而降低二氧化碳的吸收效率。
4 纳米流体在二氧化碳气体分离的应用与机理
4.1 纳米流体在二氧化碳气体分离的应用
影响纳米流体CO2吸收效果的主要因素有:气体流速,初始气体CO2浓度,纳米颗粒的类型、形态、尺寸和在基液中的浓度,以及基液的类型、流速、压力、温度等[44]。
4.1.1 纳米颗粒类型的影响
为了定义纳米流体的二氧化碳吸收增强性能,增强因子(E)用于评估和比较不同纳米颗粒的效果,可以根据CO2吸收率或CO2捕获能力(Eu)的增加来计算。基于速率的增强因子可以定义为在一定时间内平均吸收率(Er)的增加比率,或者在假设纳米颗粒不存在的情况下液体侧传质系数(El)的增加比率。Eu、Er和El通常分别使用平衡池(EC)、鼓泡反应器(BR)和湿柱(WWC)进行测量。CO2捕获能力的增加是由于纳米颗粒对CO2的额外吸附。因此,Eu通常随着纳米颗粒质量分数的增加而增加。
各种金属、金属氧化物和非金属纳米颗粒,例如SiO2、TiO2、Al2O3、MgO、Cu、CuO、Fe3O4和CNT,已被用于增强CO2的吸收[65]。研究表明,与使用纯胺溶剂相比,纳米流体可将CO2吸收量提高20%以上[66],并将CO2捕获率提高2%~93%[67]。
Jiang等[60]研究了TiO2和Al2O3纳米颗粒对CO2吸收的影响,结果表明0.06%(质量分数)TiO2-MEA 和0.06%(质量分数)Al2O3-MEA 溶液的CO2吸收分别增加了0.7%和0.02%。Kim 等[68]用哌嗪/K2CO3溶液研究了SiO2纳米颗粒对CO2吸收的影响,并实现了12%的CO2吸收量提升。Ganapathy等[69]在鼓泡反应器上利用纳米颗粒加强纳米流体CO2吸收时,结果表明每种类型的纳米颗粒加强效果不同。当气液系统平衡时,气体浓度在液相中略有增加。Carcia 等[70]采用胺类鼓泡反应器来研究TiO2、CuO、SiO2纳米颗粒对CO2捕集效率的影响,CO2捕集效率依次为TiO2>CuO>SiO2。Lu 等[12]在搅拌式反应器上研究了含有CNT 和Al2O3纳米颗粒的CO2捕集效率,结果表明,在吸附溶剂中使用碳纳米管时,CO2的捕集量大大增加。Pineda 等[71]将TiO2、SiO2、A12O3纳米颗粒添加到吸收溶剂中,利用设有托盘的吸收塔研究CO2捕集效果,研究表明,当使用TiO2、SiO2和A12O3纳米颗粒时,吸收率分别提高了5%、6%和10%。Zhang 等[72]使用搅拌式反应器考察了TiO2纳米颗粒的加入对碳酸丙烯酯CO2捕集率的影响,并分析了颗粒大小和纳米颗粒最佳浓度的影响。Golkhar 等[73]使用中空纤维膜气液反应器,用含有SiO2纳米颗粒和碳纳米管的纳米流体捕集CO2,结果表明CNT 纳米流体在捕集CO2方面有更好的表现,效率高达40%。
4.1.2 纳米颗粒担载量的影响
Haghtalab等[74]在的准静态等温高压搅拌反应器上研究水基纳米流体中ZnO和SiO2纳米颗粒的温度和浓度对CO2吸收的影响。结果表明,温度的提高略微降低了CO2的吸收,而添加0.1%(质量分数)的ZnO 和SiO2可分别提高CO2的吸收率14%和7%。Nabipour 等[75]研究了添加剂MWCNTs 的影响,结果表明,与原始基液比,在Sulfinol-M 吸收液中添加0.02%(质量分数)的带羧基功能的MWCNTs,CO2的平衡溶解度提高了23.2%。Kim等[76]利用鼓泡吸收器系统评估了含有SiO2纳米颗粒的纳米流体对CO2的吸收性能,与原始基液纯水相比,0.21%(质量分数)的纳米颗粒提高了纳米流体CO2吸收性能24%。Pang等[77]研究了在水/NH3混合物中加入Ag 纳米颗粒对吸收柱传质性能的影响,发现当溶液中加入0.02%(质量分数)的Ag 纳米颗粒时,CO2的吸收率增加了55%。Lee 和Kang[78]用一个鼓泡反应器研究了在NaCl 溶液中加入Al2O3纳米颗粒对系统CO2吸收性能的影响,并观察到0.01%(体积分数)的Al2O3纳米颗粒即可改善CO2的溶解度。Darvanjooghi 等[15]最近研究了含有Fe2O3纳米颗粒的纳米流体的CO2吸收能力,结果表明,在Fe2O3质量分数为1%时,最大平均CO2流量可达到2.8×10-5mol/(m2·s)。Irani 等[79]研究了含有40%(质量分数)聚乙烯亚胺宫能团HKUST-1 的水溶液的CO2吸收能力,表明0.2%(质量分数)的纳米颗粒即可提高水溶液16%的CO2吸收能力。Manikandan等[80]研究Al2O3纳米颗粒对水基纳米流体CO2传质的影响,研究表明0.6%(体积分数)Al2O3纳米颗粒可使水基纳米流体CO2吸收能力达到最大。上述研究都说明了在吸收液中加入少量的纳米颗粒可以提高其CO2吸收能力。Hwang 等[81]和Park 等[82-84]在MEA、DEA 和二异丙醇胺的混合溶液中加入SiO2纳米颗粒,评估其CO2吸收性能。随着纳米颗粒浓度的增加,CO2吸收率下降,这被认为与溶液的弹性有关[67]。根据这些研究,在溶液中加入少量的纳米颗粒,可以明显地提高纳米流体对CO2的吸收能力。
对于基于速率的增强因子,始终存在与最大增强因子相对应的最佳纳米颗粒,如图7所示。这是因为固体负载的进一步增加将导致液体黏度急剧增加,从而在二氧化碳吸收过程中阻碍物质的扩散。不同的纳米颗粒表现出不同的增强效果。从二氧化碳吸收的增强因子随纳米粒子的固体负载量的变化可以看出,TiO2增强因子要比其他的强得多,随着固体负载的增加而明显变化,MgO 和Al2O3纳米颗粒的增强因子随着固体负载的增加而变化不大。对于SiO2纳米颗粒,其增强因子明显弱于其他类型的纳米颗粒,而且SiO2纳米粒子甚至阻碍了某些固体负载的吸收[60]。

图7 纳米颗粒浓度对基于速率的增强因子的影响
4.1.3 纳米颗粒大小的影响
通过向溶液中添加不同类型的纳米颗粒可提高CO2的 传 质 效 率,如Al2O3、SiO2和TiO2纳 米 颗粒[85-86]。Nagy 等[87]通过在液体中加入10%(体积分数)65nm大小的正十六烷纳米颗粒,实现了200%以上的CO2传质增强效果,并发现当纳米颗粒浓度较低时,传质效率随纳米颗粒浓度增加而迅速提高,当纳米颗粒体积分数超过6%,传质效率增幅减缓。Lee和Kang[78]研究发现在NaCl溶液中加入小粒径的Al2O3纳米颗粒后,流体的CO2吸收能力有了明显提升。Zhu 等[88]在微型搅拌反应器中研究了不同粒径的二氧化硅颗粒的影响,相比1.4mm 和7mm 微型二氧化硅颗粒,含有平均粒径为250nm介孔二氧化硅材料(MCM41)的纳米流体在吸收CO2方面优势明显。
Kim 等[76,89-90]是仅有的研究纳米颗粒对纳米流体传质性能影响的研究小组。他们将平均粒径为30nm、70nm 和120nm 的二氧化硅纳米颗粒分散在水中,以达到0.021%(质量分数)的纳米颗粒浓度,其提高了纳米流体76%的CO2的吸收效率。在8min吸收过程中,第一分钟即增强了24%的CO2吸收效率。他们[76]研究了含有K2CO3纳米颗粒的纳米流体,分别为11%和12%。
Hwang 等[81]提出,体积传质系数的提高一直持续到颗粒粒径达到60nm,而粒径的进一步增加并不促进纳米流体对CO2的吸收效率。一股来说,增加纳米颗粒的体积分数会增加增强系数,而纳米颗粒粒径的增强会降低这一增强系数[27]。
4.1.4 温度的影响
温度在纳米流体对CO2的吸收效率中也起着关键作用。Lee 和Kang[78]介绍了一种新型的CO2吸收剂,含有Al2O3纳米颗粒的NaCl 水溶液,评估了在不同的温度和Al2O3浓度下CO2在这种纳米流体中的溶解度。如图8 所示,当Al2O3纳米颗粒在溶液中的体积分数为0.01%时,CO2溶解度在30℃、20℃和10℃时CO2的捕获率分别提高了11%、12.5%和8.7%。Lee 等[91]在鼓泡反应器中进行的另一项研究表明,在20℃和Al2O3体积分数为0.01%时,CO2的吸收率增加了4.5%;在相同的温度下,当Al2O3被SiO2纳米颗粒取代时,CO2吸收率提高了5.6%。Jung等[92]在Al2O3纳米颗粒体积分数为0.01%和10℃时,在鼓泡反应器中实现了8%的CO2吸收率的提升。
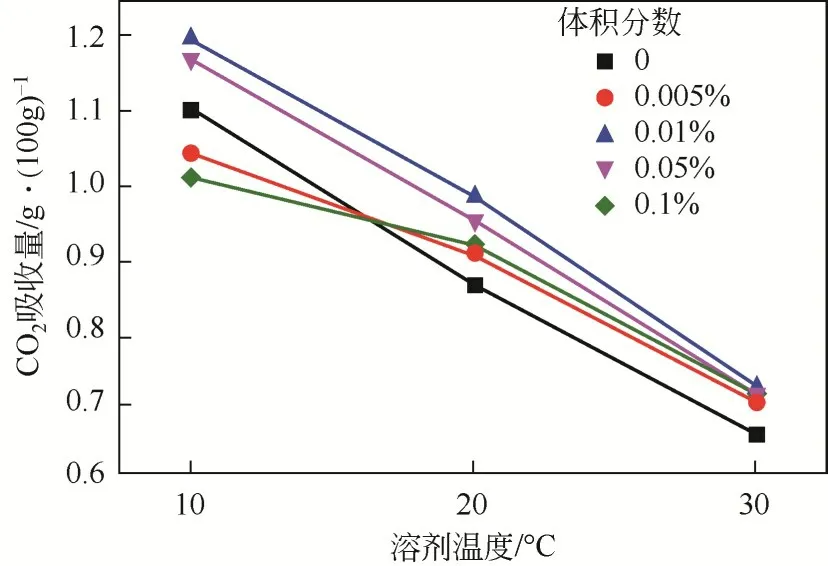
图8 不同纳米颗粒担载量、不同溶剂温度下纳米流体的二氧化碳吸收量
表2对纳米流体各类应用研究进行了汇总。
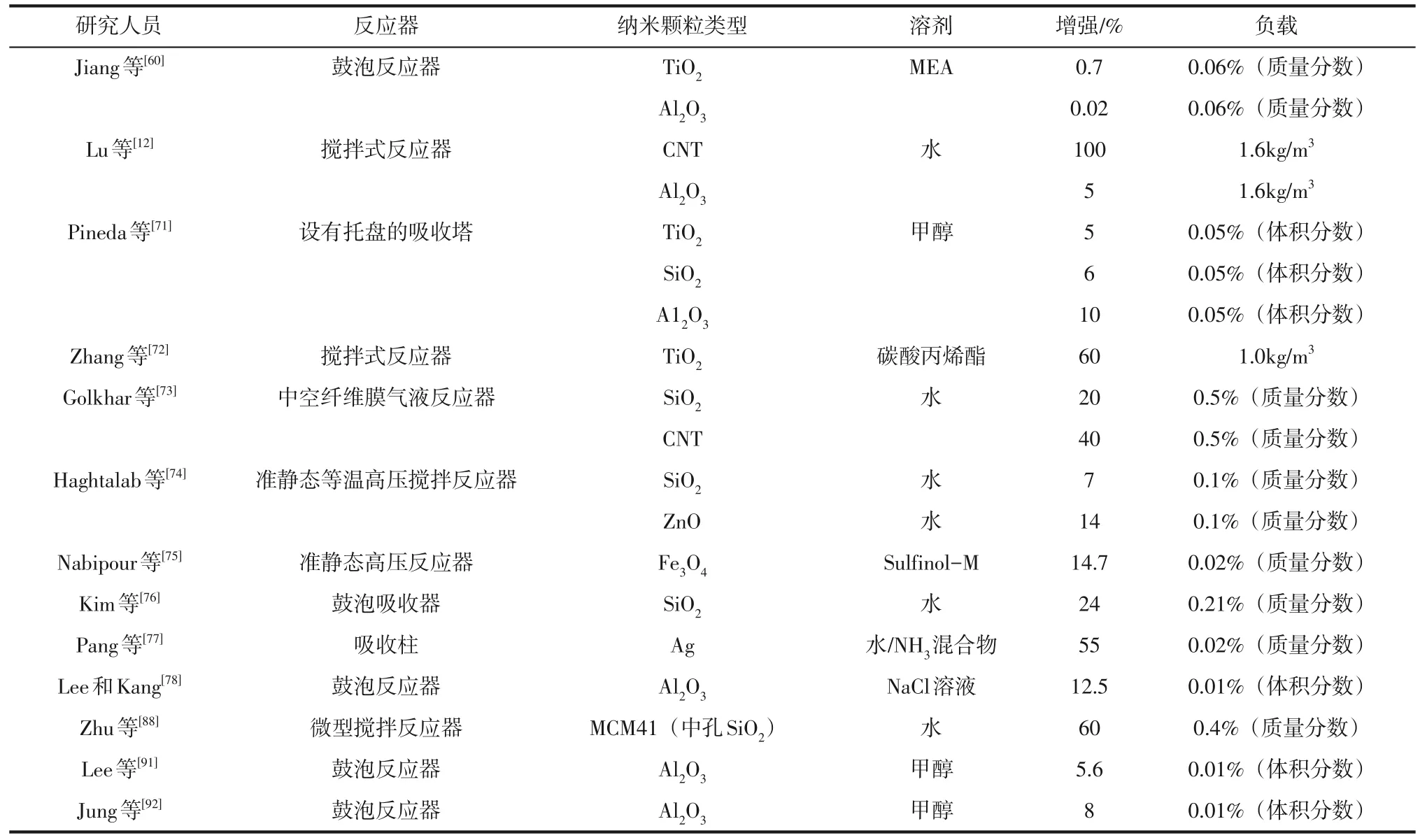
表2 不同纳米流体吸收特性
4.1.5 二氧化碳分压对纳米流体吸收效率的影响
除反应温度对纳米流体吸收效率的影响外,二氧化碳的分压同样会对纳米流体对二氧化碳的吸收效率产生影响。Haghtalab 等[74]首次利用静态气-液平衡法,测量了二氧化碳在使用二氧化硅和氧化锌的水基纳米流体中的溶解度。如图9所示,二氧化碳的吸收量随着二氧化碳压力的增大而增加,在不同温度下的实验结果表明升高温度会提升二氧化碳的吸收率。此外,压力越高,温度对于二氧化碳的吸收率提升就越明显,这种效应在更高的压力下得到加强,从而导致更多的二氧化碳溶解到在纳米流体中,导致更多的CO2被吸收,而在较低的压力下则会减弱。

图9 不同水相流体在不同温度下二氧化碳分压与吸收容量关系曲线(1bar=0.1MPa)
在以前的工作中,研究者们采用类似的方法研究了二氧化碳在纯水和其他基液中的溶解度[93-95]。Ali Haghtalab 等[74]的研究如图10所示,引入纳米颗粒后纳米流体中平均溶解度的提高在12%~16%之间,与水相比,ZnO的平均溶解度会随着温度的升高而慢慢降低。另外,在固定的二氧化碳压力下,使用SiO2纳米流体,二氧化碳的吸收率高于纯水(在不同的温度下,平均值为6%~10%),但低于ZnO纳米流体。因此,从这些结果中得出结论,氧化锌纳米流体对二氧化碳的吸收比二氧化硅纳米流体更加强烈。
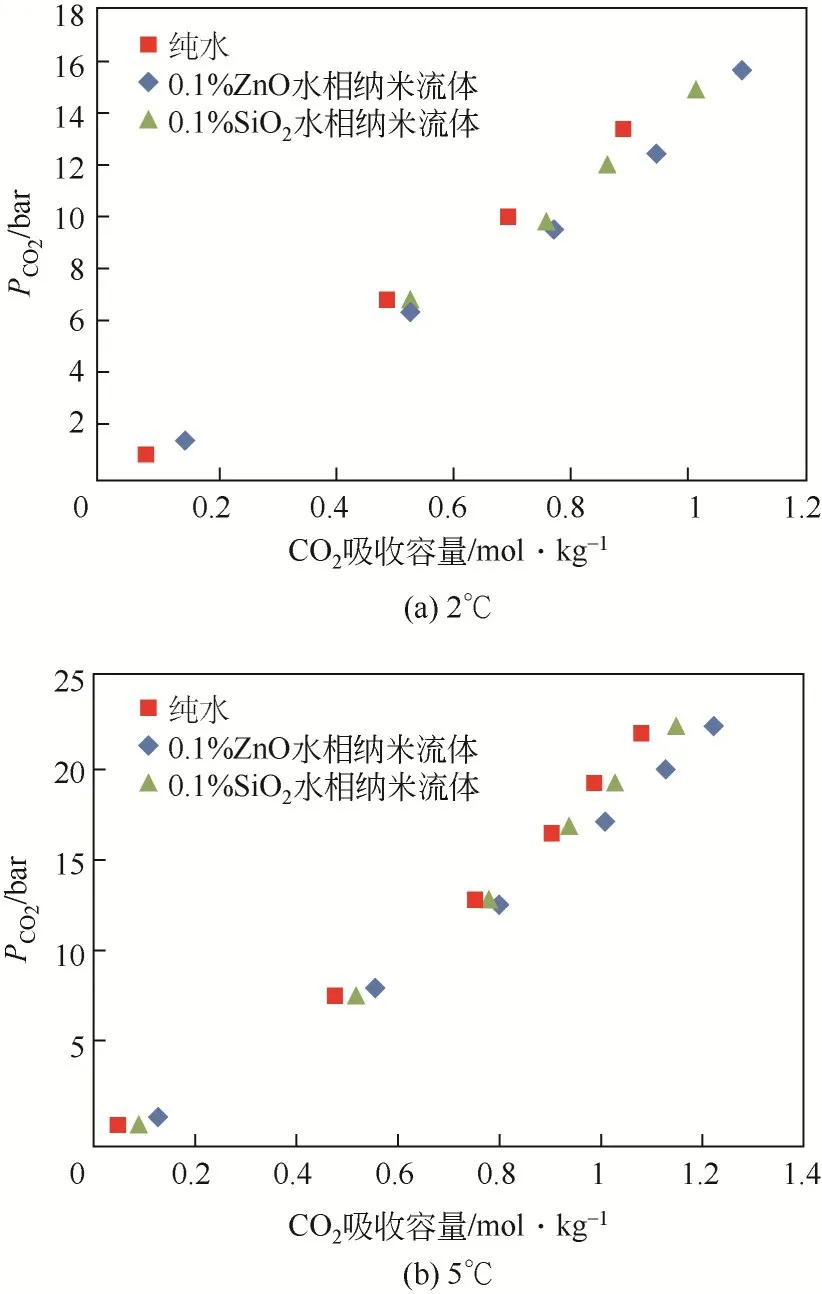
图10 0.1%(质量分数)SiO2/ZnO水相纳米流体不同温度下二氧化碳分压与吸收容量关系曲线(1bar=0.1MPa)
4.2 纳米流体强化二氧化碳气体分离机理
对于纳米流体强化二氧化碳吸附分离反应机理的研究工作重点集中在纳米颗粒在质量增强中的作用气液系统中的转移。研究表明分压增强会增加气体的吸收能力,同时温度增强会降低液相中的气体溶解度,符合理想气体定律[96]。在前人的研究基础之上,研究者们总结了纳米流体强化二氧化碳气体分离机制有以下几种:气泡破碎机理(bubble breaking effect)、传输机理(shuttle effect)和边界层 混 合 机 理(boundary mixing effect),如 图11所示。
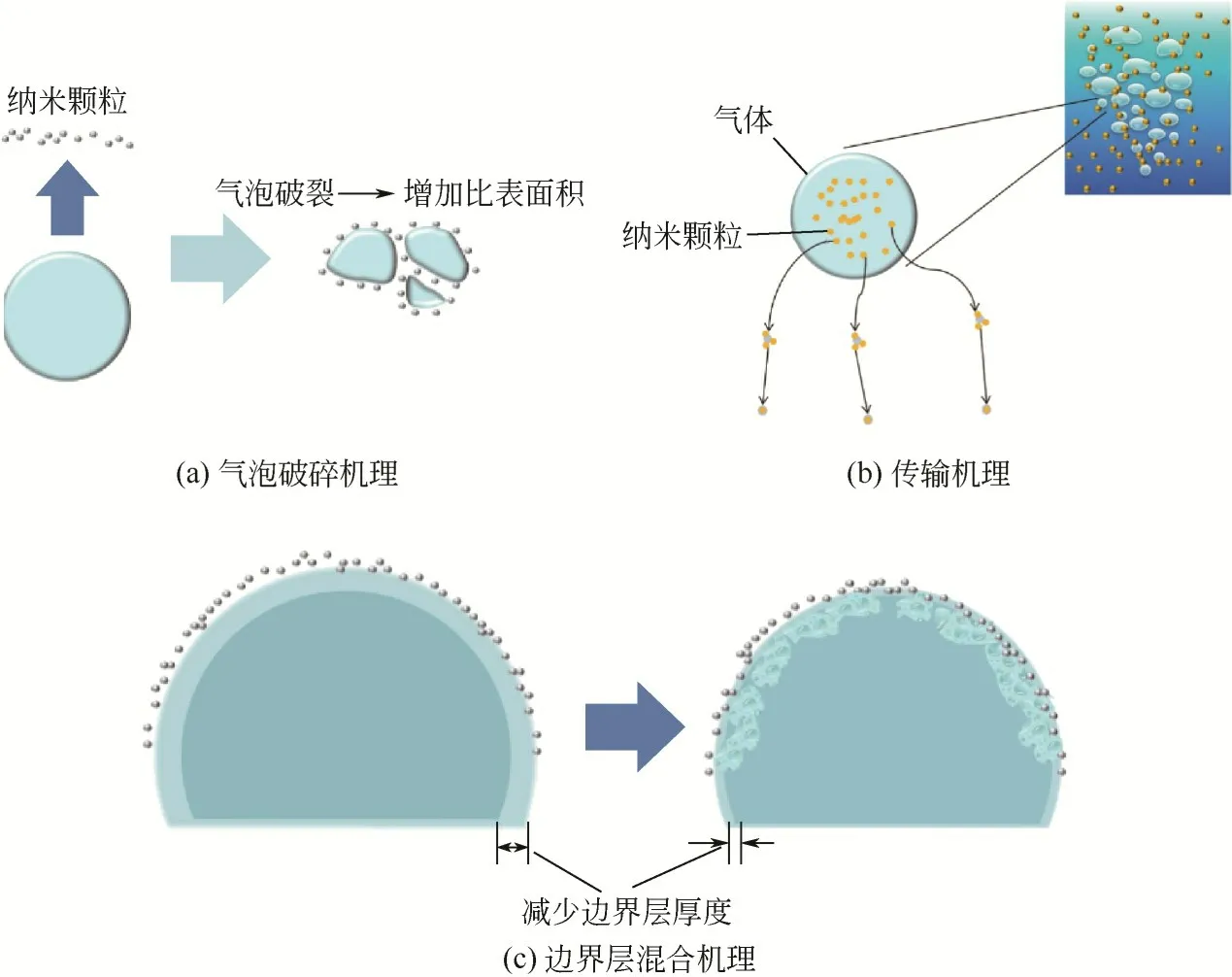
图11 纳米流体强化气体吸收机理
Krishnamurthy等[10]得出结论,速度扰动场是增强质量传递的诱因,这是由于纳米颗粒的运动而形成的。在气泡吸收过程中,纳米颗粒与纳米颗粒的碰撞出现气泡。当气泡向界面移动并形成动态运动时,纳米颗粒撞击气-液界面,导致气泡破裂[89],增加了比表面积。考虑到这种增强在特定的界面区域由于颗粒而发生,可以得出纳米颗粒可以增加整体传质系数的结论[97]。
传输机理是由Kars等[98]提出,讨论了固体颗粒在气-液-固三相体系中液体中的气体吸收理论模型,研究表明气体吸收过程可以通过穿透气液质量的纳米颗粒来增强从液体中分离的能力以吸收特定量的气体[99]。此外,传输机理认为纳米颗粒可以进入气液传质膜并吸收一定量的气体。而且由于浓度不同,携带吸收气体的颗粒返回本体液体,然后解吸[100]。由于分散相颗粒中扩散气相组分的强吸附,该气相反应物在界面附近液相中的浓度为减少,导致吸收率增加[101]。
此外还有边界层混合机理,也称作水利效应机理[102]。在流体动力学效应中,气泡周围的纳米颗粒破坏了扩散边界层并使其变薄。由于在气泡和液体之间的界面附近存在颗粒,因此扩散到液膜中会增加,因此也称之为“流体动力效应机制”。
5 结语
本文总结了纳米流体的独特性质及其在二氧化碳吸收中的广泛应用。在过去的几十年里,纳米颗粒由于其对吸收剂的传热传质增强效应,提供了一种有效的CO2吸收解决方案。在本文中,除了纳米流体本身性质外,从基液选择、稳定性、传质增强机制背后的机理阐述了纳米流体在二氧化碳吸收领域的应用。通过选取合适的纳米颗粒-基液,可增强二氧化碳的吸收效率,加速CO2反应动力学,同时解吸过程中溶剂再生所需的能耗较低。
(1)使用纳米流体吸收CO2取决于几个因素,即粒径、纳米颗粒类型、温度和基液类型。
(2)纳米颗粒的制备方法及其稳定性应考虑一些重要纳米流体的特性。由于纳米流体会随着时间的推移产生沉积物并沉降,为了解决这个问题,可以改造纳米颗粒的表面或添加低成本的分散剂,从而使纳米流体的稳定性增加。
(3)CO2吸收的机理主要有传输机理、气泡破裂和导致纳米颗粒微对流的布朗运动。
(4)纳米流体对CO2的吸收性能取决于具有大比表面积的纳米颗粒。由于纳米颗粒具有更大的比表面积,因此在基液中的分散性更好,吸收能力更强。
(5)由于成本较低,利用金属氧化物纳米颗粒,例如Fe3O4、ZnO、Al2O3、TiO2等,在工业应用中具有较大应用前景。
目前,由于纳米流体在二氧化碳吸收方面的优异性能,可替代当前单一液体吸收剂。另一方面,由于它们的新颖性,纳米流体需要进一步研究以了解参数的影响、纳米材料的性能,并分析过程以达到最佳吸收率。此外纳米流体的应用研究还存在一些挑战,包括沉淀、相位稳定性、缺乏足够的溶剂特性、泵功率和固体材料的成本数据。通过调控适当的纳米颗粒和基液的类型,加速传质和增加气相外,在这些系统中进行控制被固体颗粒吸收,可以解决吸收能耗及吸收效率两个问题。通过构效关系以及吸收机理的研究,实现纳米流体在二氧化碳吸收中的工业应用,为实现“碳达峰、碳中和”目标任务奠定基础。

