重难点创新题专练
金敖然 韩汝彩 陈洪义
(1.广西南宁市第三中学;2.河北衡水中学;3.湖北省恩施市第三高级中学)
1.中国古代有着璀璨的文明,明代科学家宋应星所著《天工开物》是一部百科全书,其中涉及很多化学知识,下列说法不正确的是
( )
B.(煤)入炉先用水沃湿,必用鼓鞲后红——该过程涉及置换反应
C.凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之——瓦属于硅酸盐材料
D.凡珠在蚌,如玉在璞。珍珠的主要成分是CaCO3,刚玉的主要成分是SiO2
【答案】D
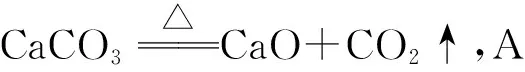
广西南宁市第三中学 金敖然

( )
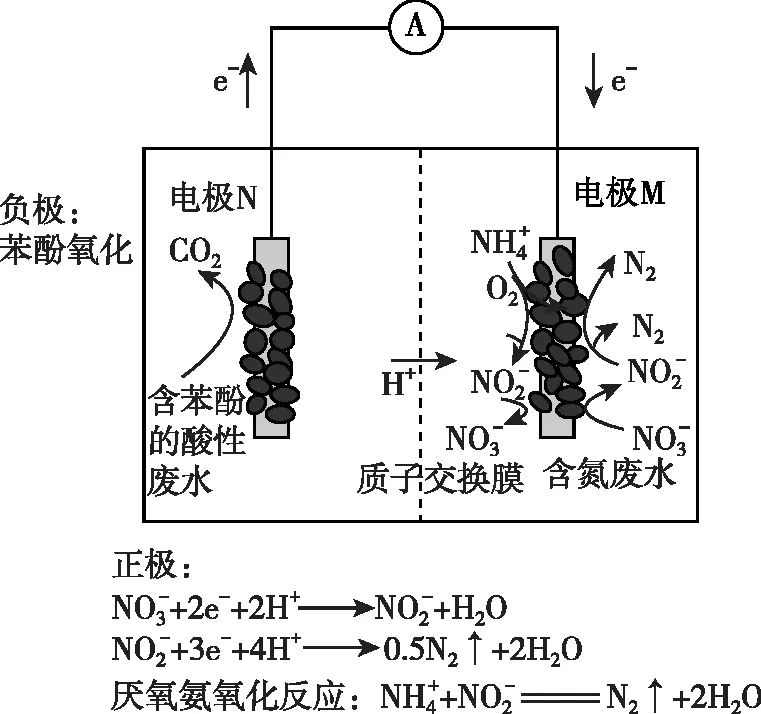
已知:
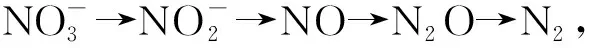

A.电极N的电势高于电极M
B.废水中氢离子通过质子交换膜由右室移向左室

【答案】CD
【图像分析】

河北衡水中学 韩汝彩
3.已知:把偏铝酸盐溶液逐滴加入到强酸溶液中至过量,依次发生如下两个反应:
在常温下,用0.1 mol·L-1NaAlO2溶液滴定某浓度的稀盐酸溶液,得到pH随时间的变化图像:
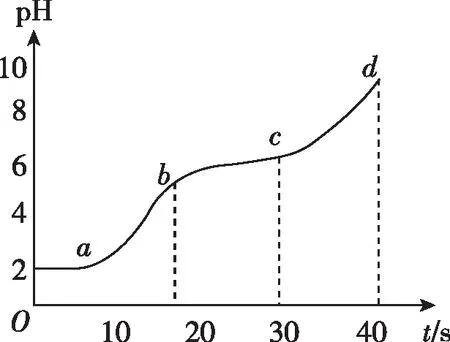
分析图像如下:

曲线段曲线趋势宏观现象主要微观粒子ab上升、斜率逐渐增大溶液无明显现象Na+、H+、Al3+、Cl-bc上升、斜率减小产生白色絮状沉淀略cd上升、斜率增大但比ab段斜率小,比bc段大溶液呈浑浊状态Na+、Cl-、AlO-2、Al(OH)3
则下列说法不正确的是
( )
A.稀盐酸的浓度为0.01 mol·L-1
B.b点溶液中的主要微观离子是Na+、Al3+、Cl-
C.在bc段的主要微观粒子有Na+、Cl-、Al3+、Al(OH)3
D.曲线ab、cd两段斜率增大程度不同的原因是反应消耗H+的速度不同
【答案】D
【图像分析】

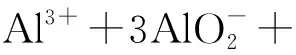
湖北省恩施市第三高级中学 陈洪义
4.铼(Re)具有优良的物理化学性能,适于超高温和强热震工作环境。回收铼金属主要是通过火法处理砷滤饼(含ReS2、CuS、As2S3等),具体过程如下:
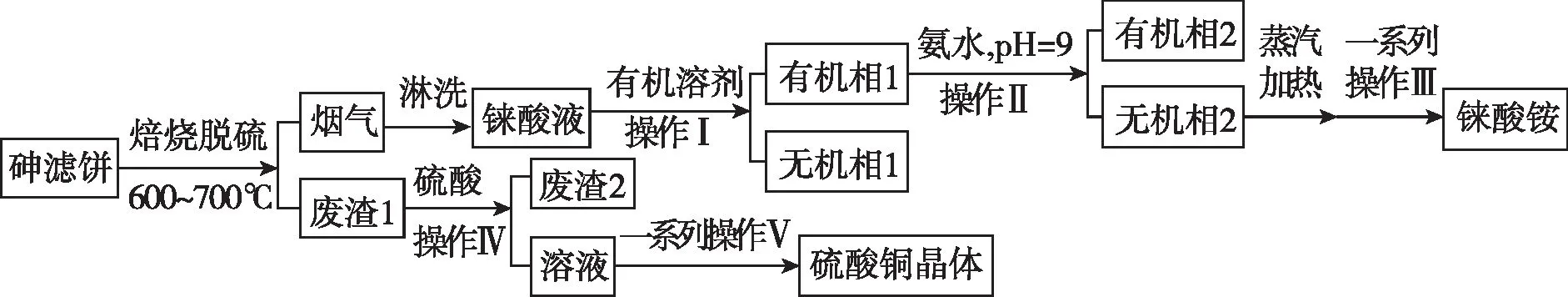
已知:
(1)As2S3焙烧后得到As2O3。As2O3是白色粉末,熔点312.3℃,193℃升华,微溶于水生成亚砷酸。
(2)Re2O7易挥发,溶于水生成铼酸(HReO4)。
(3)废渣中的其他成分均不与硫酸反应,且不溶于硫酸。
(4)铼酸液中加入有机溶剂后发生的主要反应:

请回答下列问题:
(1)焙烧脱硫中ReS2发生的化学反应方程式:________。
(2)下列说法错误的是
( )
A.淋洗过程采用逆流法可以提高效率
B.操作Ⅱ为分液、操作Ⅳ为过滤
C.从无机相1中可以提取亚砷酸
D.一系列操作Ⅲ、Ⅴ相同,均为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥
(3)操作Ⅰ所用到的玻璃仪器:________。
(4)加入氨水发生的化学方程式:。
(5)蒸汽加热的目的:。
(6)NH4ReO4在空气中用适当温度加热反应得到无污染的物质,化学方程式为________________。
(7)为了测定所得硫酸铜晶体的化学式CuSO4·xH2O,取少量所得晶体,称量质量为4.64 g,小心加热变成白色固体后,冷却、称量,得到固体 3.2 g,计算:x=。试分析没能得到CuSO4·5H2O的原因:________。

(2)D
(3)分液漏斗,烧杯

(5)浓缩铼酸铵溶液,防止铼酸铵分解
(7)4 加热过度(其他合理答案均可)
【命题意图】金属的回收流程分析
【思路分析】
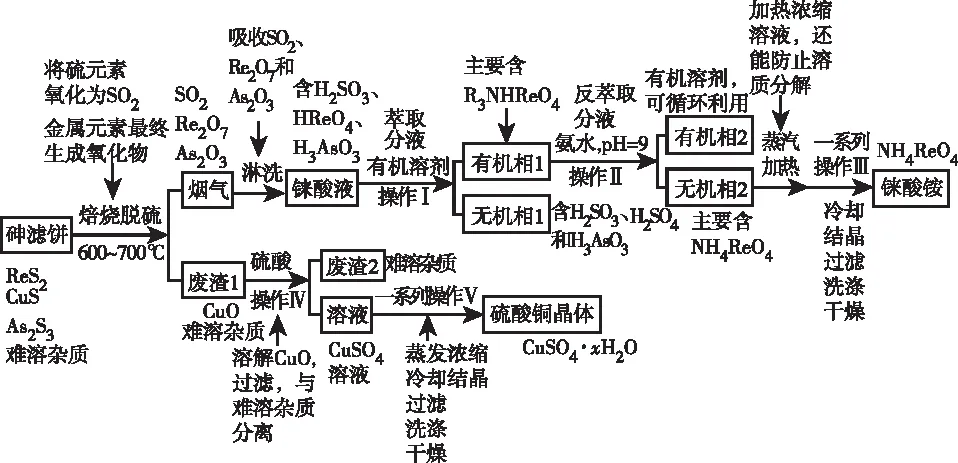
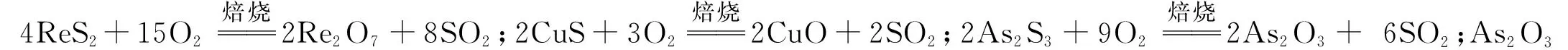
河北衡水中学 韩汝彩
5.赤泥是制铝工业产生的废料,我国作为世界第4大氧化铝生产国,每年排放的赤泥高达数百万吨。赤泥中含有丰富的钪元素,另含有Fe2O3、SiO2、Al2O3等氧化物。如图是从赤泥中提取氧化钪的工艺流程。(P204是一种磷酸酯萃取剂)。
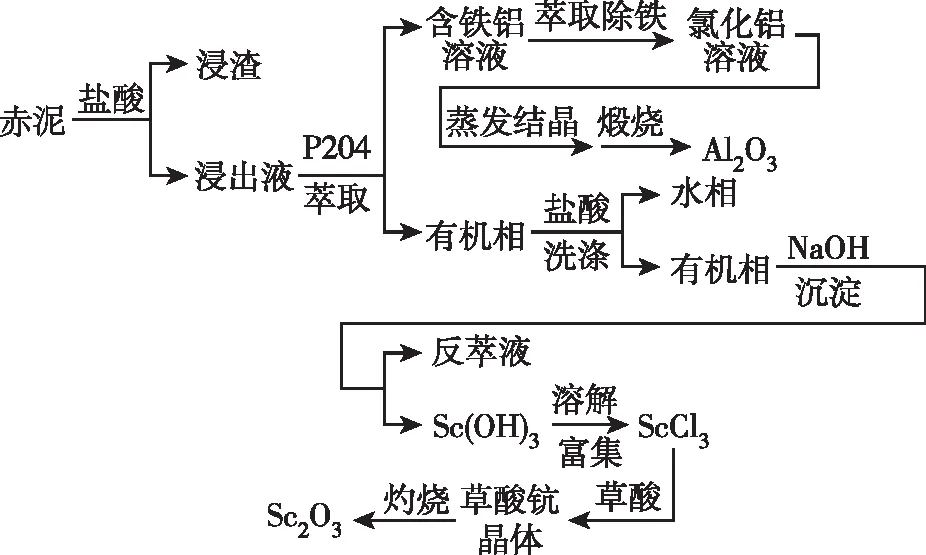
回答下列问题:
(1)赤泥经酸处理时,用盐酸不用硝酸的原因,写出浸渣主要成分的用途(写出一种)。
(2)有关获得Al2O3的一系列过程中下列说法正确的是
( )
A.“萃取除铁”中加入过量铝粉代替萃取剂,也可以到达除铁的目的
B.氯化铝溶液蒸发结晶的操作需在HCl的气流中进行
C.加水稀释氯化铝溶液,所有离子浓度都降低
D.蒸发结晶的副产品可以在工艺中循环利用
(3)“盐酸洗涤”后的分离操作为________。
(4)“NaOH沉淀”时,随着氢氧化钠加入,钪离子可以生成[Sc(OH)n]3-n(n=1~6)。写出n=5时此步骤反应的离子方程式________。
(5)钪是一种化学性质非常活泼的稀土金属,若要获得金属钪宜采用________法进行冶炼。
(6)生成草酸钪晶体Sc2(C2O4)3·xH2O的化学方程式为________。
(7)Sc2O3纯度的测定:称取Sc2O3样品10.0 g,加入稀盐酸中充分溶解,配制成100 mL溶液,取出10.00 mL溶液于锥形瓶内,加入20 mL水和少量抗坏血酸,以二甲基酚橙(0.1%溶液)为指示剂,用0.01 mol·L-1EDTA(H2Y2-)标准液滴定,当溶液由酒红色变为亮黄色,且半分钟不恢复原色,即为滴定终点,记下消耗的EDTA体积为VmL,(已知:Sc3+与EDTA反应的化学计量数之比为1∶1)。则Sc2O3的纯度为________。
【答案】(1)用硝酸酸浸可能会产生氮的氧化物污染环境 制光导纤维、光学镜片、玻璃、石英坩埚等
(2)AD
(3)分液

(5)电解

(7)0.138V%
【命题意图】从赤泥中提取氧化钪的工艺流程
【思路分析】
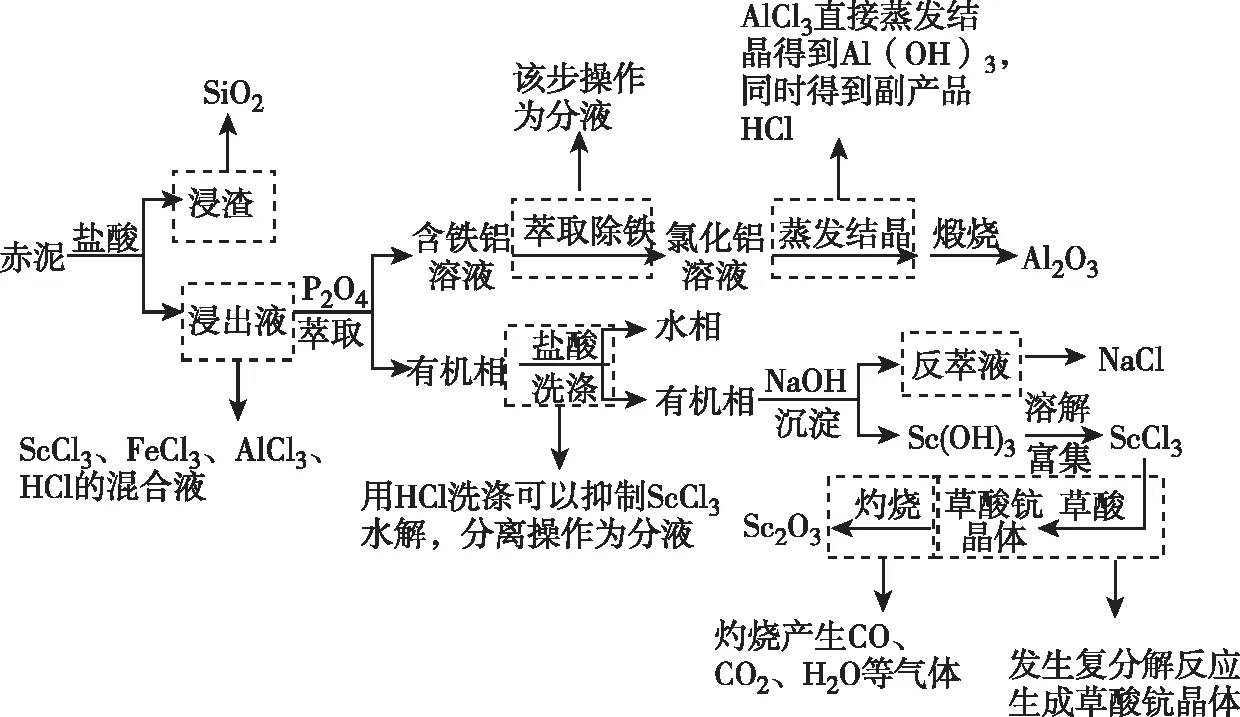

广西南宁市第三中学 金敖然

