石墨烯与导电聚合物PSS∶PEDOT 共包覆对LiCoO2 材料高电压电化学性能的影响
王继贤 ,彭思侃 ,王 晨 ,南文争 ,刘明良 ,燕绍九* ,戴圣龙
(1.中国航发北京航空材料研究院,北京,100095;2.北京石墨烯技术研究院有限公司,北京,100095;3.鲁东大学 物理与光电工程学院,山东 烟台 264025)
锂离子电池是一种将电能与化学能相互转换的电化学储能装置,通过锂离子在电极材料中的嵌入与脱出实现能量的传递与转换。自1991 年索尼公司将锂离子电池商业化以来,锂离子电池已经广泛应用于笔记本电脑、便携式电动工具及电动汽车等领域[1-3]。在军事领域,随着信息化作战装备的升级、无人机技术的发展及新式激光武器的问世,锂离子电池在高性能武器装备中也获得了广泛应用,但是,进一步提升无人机、单兵武器装备及电动车的性能,都对锂离子电池能量密度和功率密度提出了更高的要求。锂离子电池正极材料是决定电池性能的关键材料,开发高工作电压、高容量的锂离子电池正极材料刻不容缓。
纵观已商品化的锂离子电池正极材料LiCoO2、LiNixCoyMn1-x-yO2及LiFePO4,LiCoO2凭借其工作电压高、倍率性能好、振实密度高和生产工艺简单等优点,已经成为应用最广泛的正极材料[4-7]。当LiCoO2晶体结构中的Li+全部脱出时,其理论容量高达274 mAh/g,但目前实际应用中容量通常仅能发挥145 mAh/g。研究者通常认为,当超过0.5 个Li+脱出晶格结构时(对应充电截止电压为4.2 V),由于c轴方向的形变,将导致其晶格常数发生剧烈变化,晶格易失去氧使LiCoO2的晶体结构从六方晶系变成不具有电化学活性的单斜晶系[8-9]。除此之外,由于高价态的Co 具有强氧化性,与电解液之间发生的副反应会引起材料的界面结构稳定性下降和表面电阻增加,因此商业上通常把LiCoO2的充电截止电压限制在4.3 V 以下[10-12]。工作电压的限制使得LiCoO2损失了40%的理论容量,限制了该材料的进一步应用。对锂电产业界而言,开发高电压LiCoO2材料,能够大大节省设备更新及工艺开发成本,具有重大经济价值。因此,在>4.3 V 高工作电压下进一步提升LiCoO2材料的容量和循环稳定性一直是国内外的研究热点,主要围绕以下两方面开展:(1)提升电化学反应动力学;(2)提升界面稳定性。
表面包覆是提升LiCoO2界面结构稳定性的有效手段。金属氧化物诸如Al2O3[13]、ZrO2[14]及MgO[15]包覆都能够有效的提升材料的电化学性能,但是单纯的无机氧化物本征电子电导率较低,当包覆量过大时,会在颗粒表面形成一层阻碍电子和离子传输的界面层,从而导致容量的损失和电化学性能的下降[16],这种包覆方式较难实现界面稳定性和倍率性能的综合提升。在LiCoO2表面包覆导电聚合物也能够有效提升材料的电化学性能[17-20],导电聚合物包覆LiCoO2有以下优势:(1)导电聚合物具有较高的电子电导率,能够增加电极的电导率;(2)导电聚合物加工性能好,易于对正极材料形成均匀包覆,且其结构稳定性强,包覆结构在正极材料表面能够减缓正极材料与电解液之间的副反应;(3)其制备过程通常在常温下即可完成,且流程较为简单、成本较低,有利于大规模生产。
导电聚合物聚(3,4-乙基二氧噻吩)(PEDOT),因其电导率高,化学及电化学稳定性良好等特点,在锂离子电池高电压正极材料包覆改性中具有良好的应用前景[21-24]。然而PEDOT 作为不溶性高分子,必须加入聚(苯乙烯磺酸)(PSS)等水溶性有机物才能溶于水。但PSS 的加入在增加 PEDOT 水溶性的同时,会使其电导率降低[25],这阻碍了PEDOT 材料进一步的工程化应用。有研究表明,有机/无机复合是提高聚合物材料导电性能的有效方法,将PEDOT∶PSS 与高电导率的无机碳材料复合对提升其电导率有显著效果[26-27]。石墨烯作为一种新型sp2结构的碳纳米材料,相比于其他碳材料具有超轻薄、电导率高及载流子传输速度快等优势,在提升PEDOT∶PSS 电导率方面有明显效果[28-30]。并且,引入石墨烯改性锂离子电池正极材料,有望在电极中与传统导电剂Super P 构建新型复合导电网络,进一步缩短Li+扩散路径,优化电化学反应过程,在导电剂用量较低的情况下获得更加优异的电化学性能,这对于开发高能量密度和高功率密度电池具有重要意义[31-32]。为了综合利用PEDOT∶PSS和石墨烯改性LiCoO2的性能优势,本工作采用工艺路线较为简单的溶液法在LiCoO2表面进行石墨烯与导电聚合物PEDOT:PSS 的均匀共包覆,分析包覆后材料的形貌与微观结构,研究共包覆对LiCoO2电池电化学性能的改善机制。
1 实验材料及方法
实验所用LiCoO2购自湖南瑞翔新材料股份有限公司。聚(苯乙烯磺酸盐)(poly(sodium-pstyrenesulfonate),PSS)、3,4-亚乙 基二氧噻吩(3,4-ethylenedioxythiophene,EDOT)、过硫酸铵(ammonium persulphate,APS)、盐酸(hydrochloric acid,HCl)、氮-甲基吡咯烷酮(N-methyl pyrrolidone,NMP)、聚偏氟乙烯(Poly(vinylidene fluoride,PVDF)购自国药集团化学试剂有限公司,纯度为分析纯。
1.1 聚(3,4-亚乙基二氧噻吩):聚(苯乙烯磺酸盐)(PEDOT:PSS)的制备
称取2.2 g PSS 溶于100 mL 水中,之后加入0.75 g EDOT。将1.7 g APS 溶于200 mL 水中,并逐滴加入PSS 与EDOT 的水溶液中,之后用HCl 将pH 值调至2,将上述溶液放置在25℃反应24 h。将反应产物转移至截留分子量为3500 的透析膜袋中透析3 天,得到浓度为0.45%的PEDOT:PSS 水溶液。
1.2 石墨烯的制备
以膨胀石墨为原料,在NMP 溶剂中采用文献报道的机械剥离法[33]得到石墨烯纳米片溶液,烘干之后得到石墨烯粉体以备用。
1.3 石墨烯与PEDOT:PSS 共包覆LiCoO2 材料的制备
图1 为石墨烯与PEDOT:PSS 共包覆LiCoO2材料的制备工艺路线图。首先称取8.89 g 浓度为0.45%的PEDOT:PSS 水溶液,先加入0.02 g 石墨烯粉体,超声1.5 h,得到均匀的石墨烯分散液。将2 g LiCoO2加入上述石墨烯分散液中,在1000 r/min的转速下搅拌1 h 后,在120 ℃下缓慢搅拌,待浊液蒸干之后即得到包覆终产物,标记为GP-LCO。
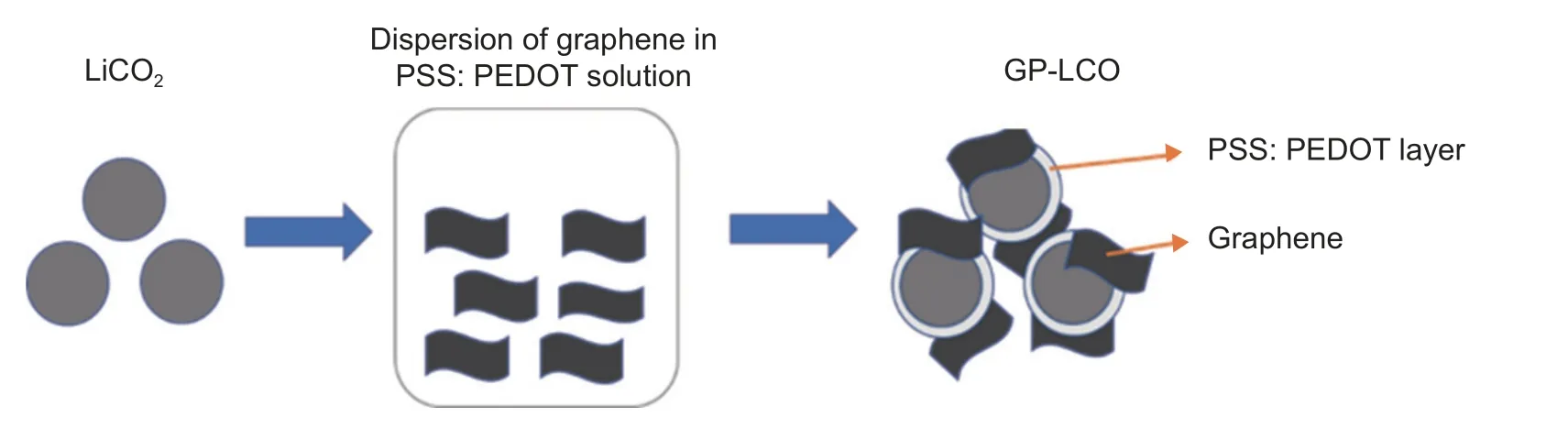
图1 石墨烯与PEDOT:PSS 共包覆材料制备工艺示意图Fig.1 Scheme diagram of fabrication of GP-LCO
1.4 材料物性表征
采用 D8 Advance(CuKα radiation)研究材料的晶体结构;采用 Nano SEM450 扫描电镜研究材料的微观形貌;采用 Tecnai G2 F30 透射电镜分析材料的微观结构。
1.5 电极制作及电池组装测试
电极极片制备过程如下:
(1)对于GP-LCO 材料,按照正极材料(GPLCO):导电炭黑(Super P)∶黏结剂(PVDF)质量比为91∶3∶6 分别称取材料;对于LCO 材料,按照正极材料(LCO)∶导电炭黑(Super P)∶黏结剂(PVDF)质量比为84∶8∶8 分别称取材料。加入适量NMP作为溶剂,控制固体在浆料中的质量分数为60%,磁力搅拌8 h,分别制备成两种均匀的正极浆料;(2)将正极浆料涂覆于铝箔上,自然干燥1 h 后转移至真空干燥箱于120 ℃干燥12 h 以完全去除NMP及残余水分;(3)将干燥后电极裁成直径为14 mm的圆片即制得工作电极。
扣式电池的组装过程如下:
选取CR2032 电池模具,负极选取锂片,隔膜选取Celgard2500 聚丙烯隔膜,采用1 mol/L LiPF6(溶剂为碳酸二甲酯∶碳酸乙烯酯=1∶1(体积比))为电解液,在充满干燥氩气的手套箱控制手套箱内水、氧浓度低于1×10−6,在手套箱中完成扣式电池装配。扣式电池在手套箱中封壳之后静置老化8 h后,使用蓝电电池测试系统对扣式电池进行充/放电测试,电压测试区间为2.5~4.5 V(vs.Li+/Li)。使用电化学工作站对扣式电池进行循环伏安(CV)测试及电化学阻抗(EIS)测试。
2 结果与分析
2.1 晶体结构分析
图2 为LCO 原始材料及包覆后样品GP-LCO的 XRD 图谱。从图2 可以看出,包覆后的样品和未包覆样品的XRD 衍射图谱基本一致,均可与α-NaFeO2结构相对应,且谱图中(006 )/(012)、(018)/(110 )两对分裂峰均分裂明显,这表明包覆前后材料都具有良好的层状结构有序度[5]。相比于包覆前样品,包覆后样品在26°附近可见一个微弱的突起峰,这标志着产物中少量石墨烯的存在[31]。除此之外,未见样品中有其他杂相产生,这说明包覆工艺并未对材料晶体结构产生明显影响,而PEDOT∶PSS 共聚物在包覆后产物中以无定形的形式存在。
2.2 形貌与微观结构分析
图3(a)、(b)和(c)分别是包覆实验所用LCO颗粒、石墨烯和包覆实验处理后的GP-LCO 样品的扫描电镜图。其中,图3(a)为LCO 原始颗粒的SEM 照片,可以看到,包覆实验所用的LCO 材料为多面体形貌,颗粒之间无明显团聚且表面光滑,说明材料的结晶度高,且颗粒之间分散性良好。图3(b)是包覆所用石墨烯纳米片的SEM 照片,石墨烯纳米片片径<10 μm,且纳米片的透明度较高,这说明本实验选用的是少层纳米石墨烯片。图3(c)为包覆后GP-LCO 颗粒的SEM 照片,由图3(c)可见,包覆后LCO 颗粒仍然保持了多面体形貌,但部分颗粒表面变得较为粗糙,颗粒之间仍然保持良好分散,且包覆后复合材料中未见明显石墨烯纳米片团聚体的存在,经过石墨烯及PEDOT∶PSS 包覆后,可以清晰的观察到贴附在颗粒表面的石墨烯纳米片。这表明本实验所采用的湿法包覆工艺能够实现LCO 颗粒及石墨烯的良好分散及石墨烯在LCO 表面的均一贴附。

图3 LCO 颗粒、石墨烯和GP-LCO 材料的形貌(a)LCO;(b)石墨烯片;(c)GP-LCOFig.3 SEM images of LCO,graphene and GP-LCO(a)LCO;(b)graphene ;(c)GP-LCO
图4(a)、(b)和(c)分别是LCO颗粒的TEM 照片、GP-LCO 颗粒的TEM 和HRTEM 照片。对比图4(a)及图4(b)可以看到,经过共包覆后,材料表面可以观察到一层2~3 nm 的非晶层,这进一步确认了颗粒表面有PSS∶PEDOT 导电聚合物的存在。需要说明的是,TEM 照片中观察到的钴酸锂颗粒表面的突起是因为本实验选用的商用钴酸锂进行了表面纳米氧化物包覆处理。为了进一步分析GP-LCO 材料的结构,图4(c)为GPLCO 颗粒的HRTEM 照片。从图4(c)中可以清晰的看出,LCO 颗粒本体、PSS∶PEDOT 和石墨烯三者之间存在着明显边界。PSS∶PEDOT 导电聚合物在LCO 颗粒表面以无定形状态存在,厚度约为2.5 nm,这与图4(b)得到的结果相吻合。在石墨烯与PSS:PEDOT 共存的区域内,PSS∶PEDOT 包覆在LCO 颗粒表面,石墨烯纳米片贴附在PSS∶PEDOT层外。在这种复合结构中,表面贴附的石墨烯与导电聚合物PSS∶PEDOT 共同作用,不仅有望大大降低材料的表面电阻,提升材料的倍率性能,还能够作为LCO 与电解液之间的惰性层,隔绝高电压下LCO 与电解液之间的副反应,改善LCO 在高电压下的循环性能。

图4 LCO 和GP-LCO 材料的微观结构图(a)LCO;(b)GP-LCO;(c)GP-LCOFig.4 TEM and HRTEM images of LCO and GP-LCO particle(a)TEM image of LCO;(b)TEM image of GP-LCO;(c)HRTEM image of GP-LCO
2.3 电化学性能分析
图5(a),(b)分别对比了LCO 和GP-LCO 材料在2.5~4.5 V(vs.Li+/Li)的电压范围内,0.1C 倍率下的循环性能和0.1C~10C 范围内的倍率性能。从图5(a)中可以看出,在0.1C 倍率下,未包覆的LCO 材料的放电容量自首次充/放电循环后即开始快速衰减,100 次循环后容量保持率仅为41.1%;而经过石墨烯纳米片和PSS:PEDOT 包覆处理后,GP-LCO 材料在0.1C 倍率下经过100 次循环后容量保持率提升至76.6 %,材料的循环稳定性得到了明显改善。图5(b)对比了LCO 和GP-LCO材料在0.1C 倍率下充电,分别在不同倍率(0.1C-10C)放电的容量,可以看出,包覆后材料GP-LCO在高倍率下展示出了更高的放电容量,尤其在5C 及10C 倍率下,GP-LCO 材料的放电容量分别为132.6 mAh/g 和118.0 mAh/g,均高于LCO 材料在5C(118.0 mAh/g)及10C(96.0 mAh/g)的放电容量,展示出了更加优异的高倍率性能。值得注意的是,在电极制备过程中,GP-LCO 的电极中总的碳导电剂含量仅有约3%(0.9% 石墨烯+2% Super P),但其首次放电容量仍与加入8% Super P 导电剂的LCO 材料相近,且在5C 及10C 更高倍率下,GPLCO 表现出更高的放电容量。由此可见,通过石墨烯与PSS:PEDOT 共包覆,所得的复合材料在降低导电剂添加量的条件下,依然能够展现出更高的倍率放电容量,这对于在电池中提升正极的活性材料载量进而大幅提升电池的能量密度及功率密度具有重要的意义。
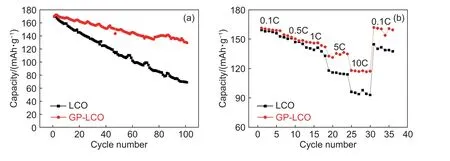
图5 LCO 和GP-LCO 材料的电化学性能(a)循环性能对比图;(b)倍率性能对比图Fig.5 Comparison of cycle performance and rate performance between LCO and GP-LCO(a)cycling performance at 0.1C;(b)rate performance at 0.1C-10C
为了进一步分析包覆前后材料的电化学性质差异,将所组装的扣式电池分别进行了循环伏安测试和电化学阻抗测试,如图6 所示。从图6(a)中可以看出,在2.5~4.5 V 的电压范围内,采用0.5 mV/s的扫描速率进行测试,GP-LCO 与LCO 的CV 曲线上都展示出一对氧化还原峰,对应于Li+在充放电循环过程中的脱出和嵌入反应。从峰位及峰强度的比较可以看出,GP-LCO 的氧化峰和还原峰的峰强更强,且二者之间的电位差更小,这表明经过包覆后,GP-LCO 具有更为对称的Li+脱/嵌电化学反应。对于LCO 材料而言,在>4.3 V 较高电压下,其晶格结构容易发生释氧,且高价态的Co 具有更高的氧化性,极易与不稳定的电解液发生副反应,这是导致循环性能的急速下降的主要原因[9,12]。而通过在GP-LCO 颗粒表层包覆石墨烯与PSS∶PEDOT,能够隔绝高电压下不稳定的LCO 颗粒界面与电解液之间的直接接触,进而提升循环稳定性[24]。氧化峰和还原峰的峰强代表着电化学反应的速率,与电极的电阻密切相关,图6(b)为未进行充放电的新鲜电池的电化学阻抗图谱。对于未进行充放电循环的新鲜电池,由于 SEI 膜尚未形成,一般认为其电化学阻抗主要由电荷转移电阻构成。经过计算可得,LCO 的电荷转移电阻约为270.4 Ω,而GPLCO 的电荷转移电阻约为154.8 Ω,这说明通过本研究所设计的石墨烯与PSS∶PEDOT 共包覆,在导电剂添加量较少的情况下,电极中由石墨烯与Super P 所构成的复合导电网络能够有效地降低电极的电荷转移电阻,这也是GP-LCO 电极在CV 测试中表现出更强的氧化/还原峰强的原因。综上可以看出,通过石墨烯纳米片与PSS:PEDOT 的共包覆,不仅能够改善电极的电化学反应动力学,还可以提升4.5 V 高截止电压下电化学反应过程的可逆性和稳定性,这是循环性能和倍率性能都得到提升的主要原因。
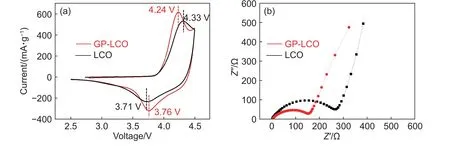
图6 LCO 和GP-LCO 电极的电化学性质(a)循环伏安(CV)曲线图;(b)电化学阻抗(EIS)曲线图Fig.6 Electrochemical characteristics of LCO electrode and GP-LCO electrode(a)cyclic voltammetry curves;(b)electrochemical Impedance Spectroscopy
3 结论
(1)通过简便的湿法包覆工艺设计并制备了石墨烯纳米片与PSS∶PEDOT 共包覆的LiCoO2材料,所制备的产品中未见LiCoO2颗粒团聚及石墨烯纳米片的团聚,且包覆工艺未对LiCoO2的晶体结构造成破坏,实现了石墨烯纳米片与PSS∶PEDOT对LiCoO2材料的均匀包覆。
(2)经过包覆后,在LiCoO2表面形成了厚度为2~3 nm 的PSS∶PEDOT 导电聚合物包覆层,石墨烯纳米片均匀的贴附在PSS∶PEDOT 层外,PSS∶PEDOT 与石墨烯纳米片形成了一种复合包覆结构,不仅改善了充/放电过程中的电极电化学反应速率,还提升了Li+脱嵌电化学反应的可逆性和稳定性。
(3)经过石墨烯纳米片与PSS∶PEDOT 共包覆,LiCoO2材料在2.5~4.5 V 的工作电压范围内,0.1C 倍率下100 次循环后的容量保持率从41.1%提升到76.6%,在5C 及10C 倍率下的放电容量分别从118.0 mAh/g 和96.0 mAh/g 提升到132.6 mAh/g和118.0 mAh/g,材料的循环容量保持率和倍率性能均得到了较大幅度的提升。

