维立西呱在心力衰竭中的研究进展
田师鹏 安慧 陈淑霞 谷剑 王立立
(河北省人民医院心血管内科,河北 石家庄050051)
心力衰竭(heart failure,HF)是多种原因导致心脏结构和/或功能的异常改变,使心室收缩和/或舒张功能发生障碍,从而引起一组复杂的临床综合征,主要表现为呼吸困难、疲乏和液体潴留(肺淤血、体循环淤血及外周水肿)等[1]。根据相关流行病学研究[2]统计,35岁以上中国成年人HF的患病率约1.3%,现有患者约890万,预计在未来15年内,中国HF的总体患病率将增加44%。目前国内外相关指南[1,3]多依据左室射血分数(left ventricular ejection fraction,LVEF),分为射血分数降低的心力衰竭(heart failure with reduced ejection fraction,HFrEF)、射血分数保留的心力衰竭(heart failure with preserved ejection fraction,HFpEF)和中间范围射血分数心力衰竭。随着对HF研究的不断进展,药物从早期“强心、利尿、扩血管”的血流动力学治疗策略,发展到目前以抑制交感神经和肾素-血管紧张素-醛固酮系统的神经内分泌治疗策略[4]。虽然HF在治疗方面取得了一定的进展,但患者的发病率、再住院率及死亡率仍较高,预后较差[5]。因此,迫切需新的药物来进一步改善患者的预后。一氧化氮(nitric oxide,NO)-可溶性鸟苷酸环化酶(soluble guanylate cyclase,sGC)-环磷酸鸟苷(cyclic guanosine monophosphate,cGMP)信号通路在心血管疾病的发生和发展中起重要作用。现就sGC刺激剂维立西呱在HF领域的最新临床研究做一综述。
1 NO-sGC-cGMP机制在HF中的作用
1.1 NO-sGC-cGMP信号通路
L-精氨酸在NO合成酶的作用下,生成具有高挥发性的NO分子,其通过自由扩散进入细胞,与胞质内sGC的血红素相结合[6-7],催化鸟苷三磷酸(guanosine triphosphate,GTP)生成cGMP,后者作为第二信使进一步激活蛋白激酶G(protein kinase G,PKG),从而对心脏、血管、肾脏等产生一系列作用[8]。有研究[9-10]表明在HF患者中,存在内皮功能障碍、氧化应激和炎症反应增强,从而导致NO的生物利用度下降以及sGC对NO的反应性降低,进一步引发cGMP生成减少,导致相关心血管疾病。此外,cGMP依赖的PKG活性受损,引发心肌细胞中肌联蛋白低磷酸化,致使心室重塑/硬化[11]。综上所述,NO-sGC-cGMP信号通路在血管内皮、心肌细胞和血管功能调节等方面起着关键作用,是慢性HF治疗的潜在靶点[10,12]。针对以上NO-sGC-cGMP信号通路在HF过程中遭受到不同程度的损坏,更多新型药物通过作用于sGC以增加cGMP浓度,包括sGC激活剂(如西那西呱)和sGC刺激剂(如维立西呱和利奥西呱)[8]。sGC激活剂通过模仿NO本身来靶向氧化型、功能不良、对NO无反应的酶。相反,sGC刺激剂作用于还原型、有作用的异构体,在存在内源性配体的情况下增强sGC的活性[13-14]。
1.2 维立西呱的作用机制
sGC激动剂维立西呱具有独特的双重作用机制,一方面通过稳定NO-sGC结合位点增加sGC对内源性NO的敏感性,另一方面作用于与NO无关的结合位点直接刺激sGC,使cGMP表达上调,修复受损的NO-sGC-cGMP信号通路,从而对心脏、血管和肾脏等器官产生多重保护作用(图1)[15-17]。
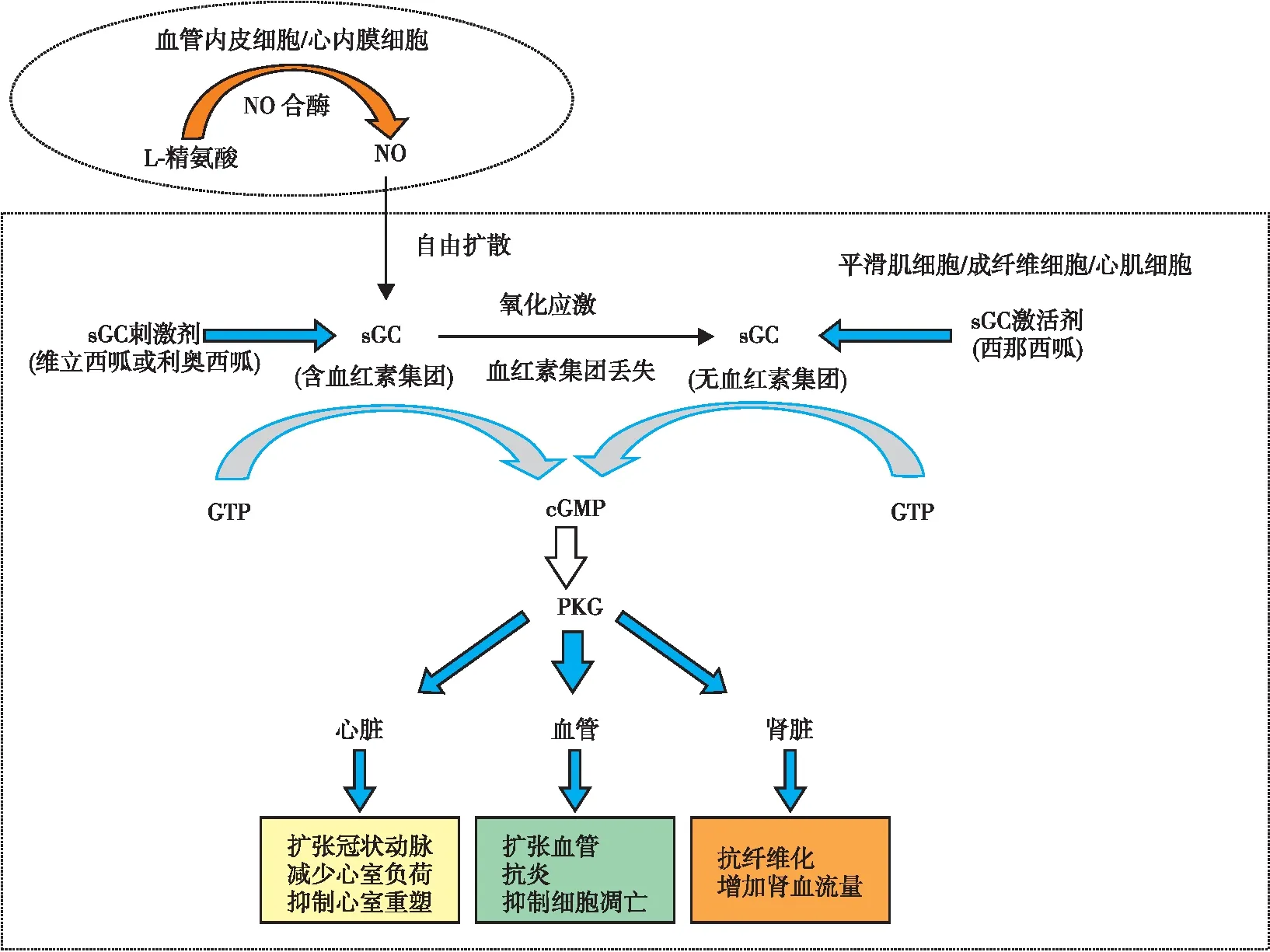
图1 维立西呱的作用机制
2 维立西呱药理学试验及相关临床研究
2.1 维立西呱的药理作用
相关研究显示,0.01~100 μmol/L的维立西呱可将高纯度的sGC激活增加1.7~57.6倍。维立西呱和NO供体对sGC的活性具有协同作用,维立西呱100 μmol/L与NO供体100 nmol/L可使sGC活性较基线提高341.6倍。维立西呱对sGC的激活作用几乎可完全被sGC抑制剂阻断。所以,维立西呱对sGC有很强的选择性,其激活与NO有协同作用,但不依赖于NO[18-19]。大鼠离体心脏研究[20]显示,维立西呱对心率、左心室收缩压和舒张压均无影响,可使冠状动脉血流增加,3 mg/kg和10 mg/kg的剂量可明显抑制心肌肥厚,减少蛋白尿,降低血压等;3 mg/kg和10 mg/kg的治疗组在21 d后的生存率分别是70%和90%,较对照组有显著提升。
2.2 维立西呱的药代动力学和药物相互作用
HF患者常合并多种慢性疾病,如高血压、心律失常、冠心病和糖尿病等,常需多种药物联合治疗,这进一步增加了药物之间相互作用的情况。有3项Ⅰ期临床试验[21]表明,维立西呱与阿司匹林、沙库巴曲缬沙坦和华法林合用耐受性良好,临床上药效学或药代动力学的相互作用未被观察到,维立西呱无需调整剂量。有6项Ⅰ期临床试验[22]显示,与不服用食物相比,在服用食物后,维立西呱的血液浓度曲线下面积和最大血药浓度分别增加了44%和41%,而且健康成年人在禁食条件下联合使用奥美拉唑40 mg/d和氢氧化镁600 mg/d或氢氧化铝900 mg/d时,与单独服用时相比,维立西呱的生物利用度下降了约30%。当健康受试者应用维立西呱联合沙库巴曲缬沙坦、甲芬那酸、咪达唑仑、地高辛、西地那非、阿司匹林、酮康唑、华法林和利福平时,未观察到临床上明显的药代动力学差异。因此,维立西呱的药代动力学在体内和体外相互作用较弱,适用于多种药物合并治疗的HF患者。
2.3 维立西呱在HF领域的相关临床研究
2.3.1 维立西呱在HFpEF患者中的临床研究
SOCRATES-PRESERVED试验[23]是一项针对LVEF≥45%患者的Ⅱb期临床试验,共纳入477例患者,随机分为口服4种不同剂量的维立西呱(1.25、2.5、5、10 mg)和安慰剂。治疗12周后与安慰剂相比,两个主要终点左心房容积和对数转换N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)与基线之间无明显统计学差异。原因可能是观察时间太短,或维立西呱的试验剂量太小,从而无法观察到其降低。与此同时,所有试验组停药率均较低,药物耐受性良好。但在探索性试验[24]中发现,维立西呱10 mg治疗组在欧洲五维健康量表(EuroQol five dimensions questionnaire)和特定疾病的堪萨斯市心肌病调查问卷(Kansas City Cardiomyopathy Questionnaire,KCCQ)上的评分较安慰剂组有显著改善,有统计学差异(P=0.046 1),表明维立西呱在特定剂量下可提高HFpEF患者的生活质量。
鉴于其在生活质量方面取得了令人鼓舞的结果,在SOCRATES-PRESERVED试验的基础上进行了VITALITY-HFpEF试验[25],本试验拥有更大的样本量、更长的治疗时间以及更高的目标剂量。该试验结果表明经过24周治疗,在KCCQ身体限制评分和6分钟步行试验方面,慢性失代偿期HFpEF患者与安慰剂组相比无明显改善[26]。可能与纳入较多症状较轻、KCCQ身体限制评分较高的HFpEF人群相关。因此,维立西呱在HFpEF患者中的疗效需进一步证实。
2.3.2 维立西呱在HFrEF患者中的临床研究
SOCRATES-REDUCED试验[27]主要探索维立西呱在慢性HF患者中的最佳剂量和耐受性,随机纳入456例近期HF恶化的HFrEF患者(纽约心功能分级Ⅱ~Ⅳ级),目标剂量分别为口服1.25、2.5、5、10 mg的维立西呱和安慰剂。在主要终点方面,治疗12周后维立西呱在对数转换NT-proBNP上与安慰剂相比无明显统计学差异。但探索性发现表明存在剂量-反应关系,即应用维立西呱的剂量越高,NT-proBNP的降幅越明显(P<0.02)。同时该试验还证明维立西呱的耐受性良好,未出现过多的不良反应。
为进一步研究维立西呱对HFrEF和近期失代偿期患者的疗效和安全性,开展了针对近期HF恶化的Ⅲ期VICTORIA临床试验[28]。本试验纳入5 050例年龄>18岁、LVEF<45%,且符合纽约心功能分级Ⅱ~Ⅳ级的慢性HF患者,分别接受维立西呱治疗(n=2 526,起始剂量为2.5 mg,随后增加至5 mg和10 mg,目标剂量为10 mg)或安慰剂(n=2 524),两组均接受目前指南推荐的标准药物治疗。主要终点是首次因HF住院或心血管死亡事件的复合终点,次要终点是主要终点的各个组成部分,包括首次和随后因HF住院、全因死亡事件,以及全因死亡或因HF住院的复合终点。中位随访时间为10.8个月,研究结果显示,与安慰剂组相比,维立西呱组降低首次因HF住院和因心血管事件死亡复合终点发生率的10%(HR=0.90,95%CI0.82~0.98,P=0.02),在次要终点方面,维立西呱组因HF住院总人数显著减少(HR=0.91,95%CI0.84~0.99,P=0.02),因HF住院或全因死亡的复合终点显著减少(HR=0.90,95%CI0.83~0.98,P=0.02)[29]。总之,在高危HF患者中,维立西呱可降低因HF住院或因心血管原因死亡的发生率[30]。
3 维立西呱在HF合并症中的临床研究
3.1 维立西呱在HF合并肾功能不全中的临床研究
慢性HF的现有治疗药物在面对肾功能不全的患者时,常会因肌酐升高、LVEF<35%、肾脏灌注不足等原因,致使血管紧张素转化酶抑制剂、β受体阻滞剂、螺内酯等药物的使用受到约束,甚至出现治疗停止的现象,这些都会对HF患者的预后和病情造成不良影响。VICTORIA的亚组试验[31]分析了维立西呱的疗效与HFrEF患者肾功能之间的关系,结果表明治疗期间维立西呱组和安慰剂组的肾功能变化轨迹相似(P>0.05),维立西呱对主要转归的有益作用在有效肾小球滤过率的全部范围内是一致的(P=0.48)。此外,无证据表明维立西呱增加或降低血清钾水平。因此,其可安全地用于血清钾浓度增加的患者,包括禁用肾素-血管紧张素-醛固酮系统阻滞剂的高钾血症患者。
3.2 维立西呱在HF合并心房颤动中的临床研究
一项VICTORIA的亚组试验[32]按照患者的基线资料,分为无心房颤动(房颤)、有房颤病史(目前无房颤)和随机心电图提示房颤3组。该研究发现在HF恶化的高危人群中,近一半存在房颤。与无房颤的患者相比,既往有房颤病史(目前无房颤)可增加心血管疾病死亡的风险,预后更差。随机分组后房颤的发生与心血管死亡和因HF住院率的增加相关,但均不受维立西呱治疗的影响(P=0.51)。无论基线时房颤状态如何,维立西呱对主要终点事件都有明显益处。
3.3 维立西呱在HF合并贫血中的临床研究
在VICTORIA试验[33]中,维立西呱组贫血的发生率(7.6%)高于安慰剂组(5.7%),有关试验进一步探索了维立西呱和贫血之间的关系。维立西呱在最初16周内轻度降低了血红蛋白,贫血的发生率也更高(P<0.001),但这种效果在96周的随访中并未进一步发展,且与维立西呱的治疗益处无关。因此,贫血或血红蛋白水平的下降不影响维立西呱在HFrEF患者中的使用。
3.4 维立西呱在HF合并冠状动脉疾病中的临床研究
VICTORIA试验[34]表明,在近期发生恶化的HFrEF患者中,合并冠状动脉疾病增加了心血管疾病死亡或因HF住院的风险。但无论是否合并冠状动脉疾病,维立西呱的治疗都是有益的,冠状动脉疾病和非冠状动脉疾病患者对维立西呱均拥有较好的耐受性和较低的不良反应。
3.5 维立西呱在HF合并不同NT-proBNP水平中的临床研究
NT-proBNP是对HF患者诊断、风险分层和随访的基础,相关研究探索了在VICTORIA试验[35]中,维立西呱针对不同NT-proBNP水平患者的疗效。在近期接受因HF住院或静脉利尿剂治疗的HFrEF高危患者中,与安慰剂相比,维立西呱对NT-proBNP<8 000 pg/mL的患者,其主要复合终点事件(因HF住院和心血管疾病死亡)发生率明显下降,若NT-proBNP<4 000 pg/mL,则疗效进一步增加。这为维立西呱对高危风险患者的获益提供了新的思路。
4 维立西呱的安全性和耐受性
经典的VICTORIA试验[12]表明维立西呱具有良好的安全性和耐受性,可明显改善HF患者的预后和生活质量。一项研究将健康受试者平均分为5组,分别口服不同剂量(1.25、2.5、5、7.5、10 mg)的维立西呱,随着剂量的增加,受试者血药浓度-时间曲线下面积的增加不呈正比,表明口服维立西呱具有良好的安全性和耐受性。但维立西呱与其他sGC激动剂或5型磷酸二酯酶抑制剂联合使用会引起血压明显下降,故禁止同时使用。与此同时,目前尚未确定其对儿科患者是否安全有效。且维立西呱具有胎儿和胚胎毒性,建议对有生殖能力的女性至少在服药期间使用有效避孕措施,并在最后一次服药后1个月内进行避孕[27]。
5 维立西呱的未来和展望
细胞信号转导功能障碍是HF进展的关键机制之一,同时也是治疗的潜在靶点。维立西呱作为第一个用于HF患者的sGC刺激剂,通过改善NO-sGC-cGMP信号通路,从而在抑制心脏重构、抗血管增生、增加肾脏血流量等方面进行保护,并且已于2022年5月18日在中国被批准上市,用于经静脉药物治疗后病情相对稳定以及近期失代偿的症状性慢性HFrEF(LVEF<45%)成人患者。
尽管目前维立西呱对高危HF患者提供了新的治疗方案,但仍有许多相关问题亟待解决:(1)维立西呱可否与“新四联”药物联合或单独使用,组成HF治疗的新方案;(2)维立西呱的治疗效果是否同样适用于急性HF;(3)维立西呱在人群中易发生症状性低血压和晕厥的相关原因。以上均有待后续相关研究进一步解决。