GC-MS/MS 法测定药品中N-亚硝胺类化合物的含量★
王明明,彭雪琦,葛晓晓,庄件兵,张维祥
(江苏省生产力促进中心,江苏 南京 210000)
0 引言
从2018 年7 月开始,FDA 宣布召回缬沙坦,因为这种药物中含有N-亚硝基二甲胺(NDMA)。对所有制造商的血管紧张素受体阻滞剂(ARB)类活性药物成分(API)和成品药的后续调查也导致了缬沙坦、厄贝沙坦和氯沙坦被额外召回。已发现这些药品中含有NDMA 和N-亚硝基二乙胺(NDEA),两者均为已知动物致癌物和疑似人类致癌物。随后,N-亚硝基异丙胺(NEIPA)、N-亚硝基二异丙胺(NDIPA)、N-亚硝基二丁胺(NDBA)和N-亚硝基甲基-4-氨基丁酸(NMBA)等其他杂质均被标记为潜在的亚硝胺杂质。迄今为止,1 100 多个不同批次的沙坦类药物(缬沙坦、氯沙坦和厄贝沙坦)已被召回,因为其中所含的这些杂质已超过了临时限值[1]。
1 亚硝胺类杂质的来源
在药品的生产过程中,在特定工艺条件下,使用到某些起始物料、原料和中间体,在API 生产过程中可能会形成亚硝胺杂质。这些亚硝胺杂质在后续的API 生产工艺步骤中可能无法全部清除。
胺类物质和亚硝酸盐的反应。使用亚硝酸钠(NaNO2),或其他亚硝酸盐,当存在仲胺或叔胺时,可能会形成亚硝胺物质。仲胺可能会在试剂和溶剂中以杂质或降解物出现。它们可能是试剂、溶剂、API、其降解产物和前体结构的一部分[2]。
2 实验部分
2.1 仪器和试剂
气相色谱-三重四极杆串联质谱联用仪;Agilent7890B-7000D 气质联用仪,安捷伦;聚乙二醇石英毛细管柱HP-INNOWAX,色谱柱(30 m×0.25 mm,0.25 μm);旋涡混匀仪WH-3,上海沪西分析仪器厂有限公司;分析天平,BSA224S-CW,赛多利斯;飞鸽牌台式高速离心机,上海安亭科学仪器厂;KQ-400KDE型高功率数控超声波清洗器,昆山市超声仪器有限公司;超纯水,色谱纯乙腈,Honeywell 公司;色谱纯甲醇,Honeywell 公司;N-亚硝基二乙胺(NDEA)标准品,100μg/mL,DR 公司;N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIA)标准品,质量浓度均为100 μg/mL,ANPEL 公司;奥美沙坦酯片,20 mg/片,北京福元医药公司。
2.2 实验方法
2.2.1 色谱条件
毛细管柱:HP-INNOWAX,30 m×0.25 mm,0.25 μm;检测器:安捷伦7000D;进样口温度:250 ℃;检测器温度:280 ℃;模式:不分流;恒流模式,流量:1 mL/min;载气:He;进样量:2 μL;柱箱温度:起始温度40 ℃,维持0.5 min,再以20 ℃/min 的速率升温至200 ℃,再以60 ℃/min 的速率升温至250 ℃,维持15 min。
2.2.2 质谱条件
电子轰击(EI)离子源;电离电压70 eV;离子源温度280 ℃;四极杆温度Q1和Q2为150 ℃。采用选择离子监测模式定量分析;碰撞气体流速:氮气,1.5 mL/min;猝灭气体流速:氦气,4 mL/min 溶剂延迟3 min。
3 种亚硝胺类物质特征离子参数为N-亚硝基二乙 胺(NDEA)(102,85,56)、N-亚硝基二甲胺(NDMA)(74,44,42)、N-亚硝基二异丙胺(NDIPA)(130,88,42)。
2.3 样品前处理
2.3.1 供试品溶液
精密称取0.5 g 奥美沙坦片样品并转移到10 mL容量瓶中,用甲醇溶解并稀释定容,超声15 min,取出摇匀。将溶液转移至10 mL 离心管中,放入离心机,以4 000 r/min 的转速离心2.5 min,取适量上清液过0.45 μm 尼龙过滤器过滤,转移至GC 样品瓶中待分析。
2.3.2 储备溶液(10 μg/mL)
精密移取质量浓度均为100 μg/mL 的N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)各1mL 于3 个不同的10 mL容量瓶中,用甲醇定容至刻度,配制成质量浓度为10 μg/mL 的各标准储备液。
2.3.3 混合标准中间液(1 μg/mL)
分别移取N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)的储备液各1 mL 至10 mL 容量瓶中,用甲醇定容至刻度,配制成质量浓度为1 μg/mL 的混合标准中间液。
2.3.4 标准曲线溶液
用甲醇逐级稀释该混合标准中间液,配制质量浓度为1.25、2.5、5、10、20、40、80、100 μg/L 标准曲线溶液。
3 结果与讨论
3.1 提取试剂的选择
比较了乙腈和甲醇的提取效果,两者回收率均达到了95%以上。但是用乙腈作为提取试剂时会有明显的杂质峰(见图1),而用甲醇提取则没有(见图2)。因此选择甲醇作为提取试剂。
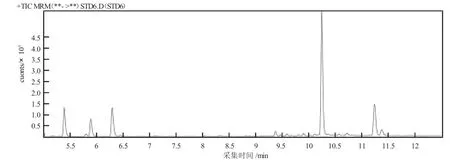
图1 乙腈作为提取试剂的加标回收图
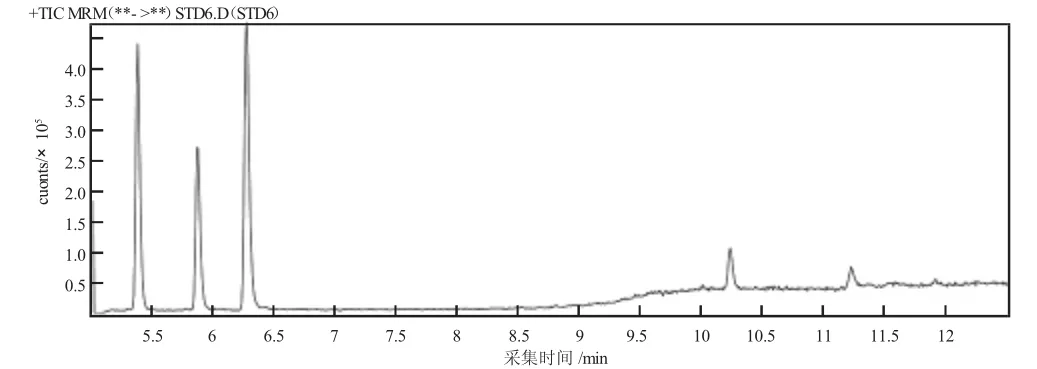
图2 甲醇作为提取试剂的加标回收图
3.2 专属性试验
建立的色谱/质谱分析方法能够准确定量各潜在杂质,杂质与杂质之间、杂质与主峰、杂质与溶剂之间不存在相互干扰。
3.2.1 空白溶液
取空白溶液(10 mL 甲醇)、NDMA、NDEA、NDIPA混合标准溶液、奥美沙坦供试品溶液各进一针,确保各潜在杂质,杂质与杂质之间、杂质与主峰、杂质与溶剂之间不存在相互干扰。
3.2.2 验证结果(表1)
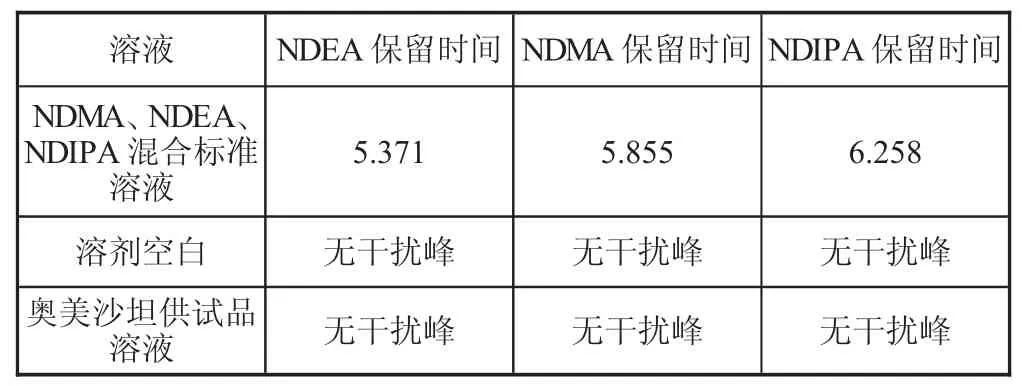
表1 3 种化合物保留时间 单位:min
溶剂空白,奥美沙坦供试品溶液在NDEA,NDMA,NDIPA 色谱峰位置无干扰色谱峰,该分析方法专属性良好。
3.3 线性范围和检出限及定量限
在上述色谱质谱条件下,分别取2 μL N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)混合标准系列溶液进行分析,以待测物色谱峰面积和对应其质量浓度进行线性回归,绘制标准曲线。以3 倍信噪比确定方法的检出限,以10 倍信噪比确定方法的定量限,相应结果见表2。
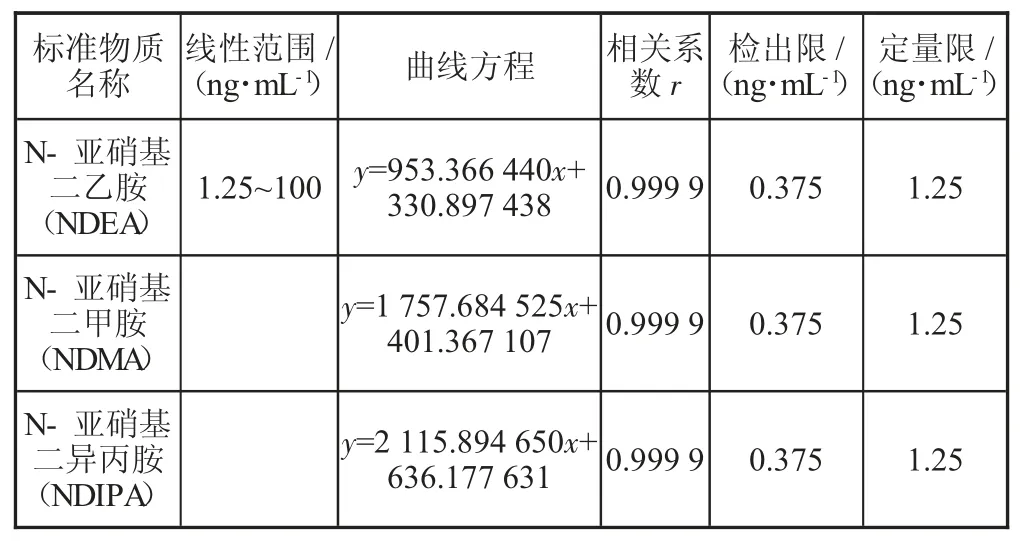
表2 线性参数和检出限及定量限
3.4 加标回收率与精密度测试
在上述气质色谱条件下,按本方法对一种降压药奥美沙坦片进行提取分析,实验结果表明该药品中未检出N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)。在该样品中加入不同浓度的3 种亚硝胺类标准品,加标量分别为为20 ng、200 ng,每个浓度平行测定6 次,考察方法的加标回收率和精密度,结果见表3。
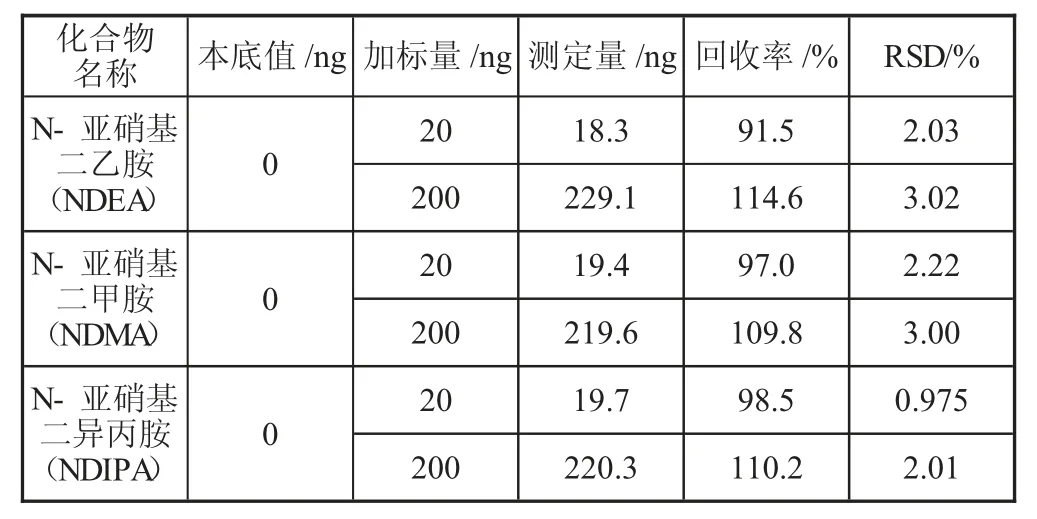
表3 加标回收率与精密度结果
由表3 可见,N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)的平行加标回收率为91.5%~114.6%,相对标准偏差为0.975%~3.02%(n=6),满足分析测试要求。
3.5 溶液稳定性
配制质量浓度为20 ng/mL 杂质限度浓度的奥美沙坦溶液作为溶液稳定性测试溶液。在室温下,分别于0、15、18、23、43 h 进样分析,统计3 种化合物的峰面积,RSD 应小于10%。验证结果见表4。
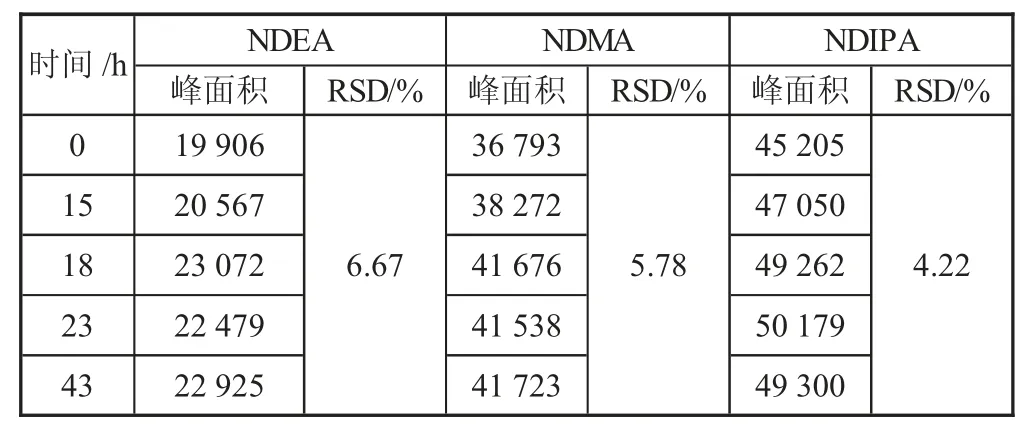
表4 三种化合物不同时间进样分析的峰面积和RSD 值
不同时间点供试品溶液的N-亚硝基二甲胺(NDMA)峰面积的RSD 为5.78%,N-亚硝基二乙胺(NDEA)峰面积的RSD 为6.67%,N-亚硝基二异丙胺(NDIPA)峰面积的RSD 为4.22%,均小于10%,符合要求。
3.6 耐用性
改变色谱条件,配制加标质量浓度为20 ng/mL的供试品溶液,改动条件下的3 种化合物色谱峰面积与原条件下的峰面积比值均应在80%~120%。
标准条件:见2.2 色谱条件。
1)柱箱温度:起始温度38 ℃,维持0.5 min,再以20 ℃/min 的速率升温至200 ℃,再以60 ℃/min 的速率升温至250 ℃,维持15 min。
2)柱箱温度:起始温度42 ℃,维持0.5 min,再以20 ℃/min 的速率升温至200 ℃,再以60 ℃/min 的速率升温至250 ℃,维持15 min。
3)进样口温度:248 ℃。
4)进样口温度:252 ℃。
验证结果见表5。
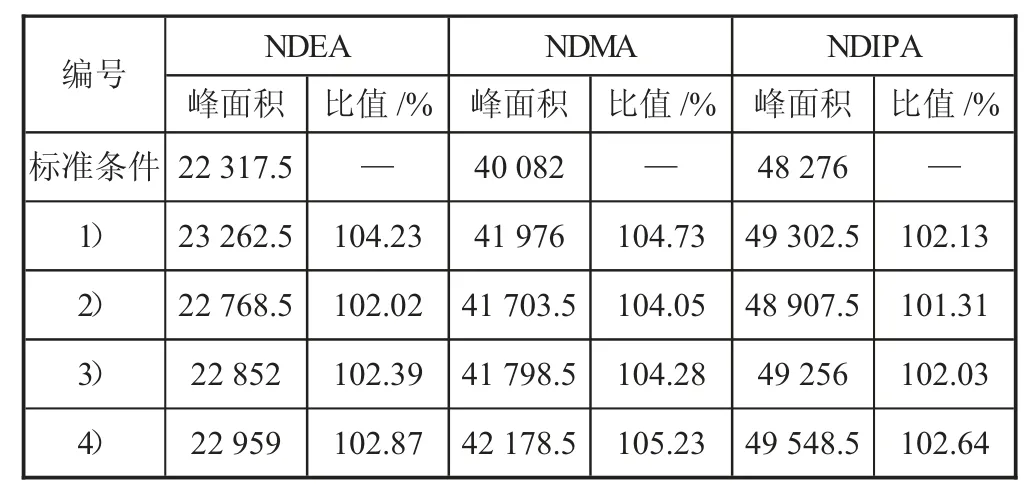
表5 3 种化合物不同条件下进样分析的峰面积和比值
条件变动后测试结果与原条件测试结果相比,NDMA 峰面积的比值在104.05%~105.23%之间,NDEA 峰面的比值在102.02%~104.23%,NDIPA 峰面的比值在101.31%~102.64%,符合要求。
4 结论
本文建立气相色谱质谱法测定药品中N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)3 种亚硝胺类化合物含量的分析方法。本实验对方法的提取试剂进行了确定,考察了方法的线性、检出限等参数。实验结果表明,本方法操作步骤简单,检出限低,加标回收率和精密度满足分析测试要求,适用于N-亚硝基二乙胺(NDEA)、N-亚硝基二甲胺(NDMA)、N-亚硝基二异丙胺(NDIPA)3 种亚硝胺类化合物含量的分析。

