超声引导下射频消融联合点式剥脱术及泡沫硬化剂对原发性小隐静脉曲张的治疗效果
李井荣,荣智华,张望德,李春民
1 首都医科大学附属北京朝阳医院血管外科,北京 100069
2 中国医学科学院北京协和医学院北京协和医院血管外科,北京 100032
慢性下肢静脉功能不全(chronic venous insufficiency,CVI)是一种常见的临床疾病,下肢静脉曲张是CVI的主要临床表现,研究显示,CVI患病率为10%~25%[1]。虽然小隐静脉曲张较大隐静脉曲张少见,仅占静脉曲张的15%[2],但由于小隐静脉注入腘静脉的位置变异较多,小隐静脉曲张的手术治疗较大隐静脉曲张更具有挑战性[3]。19世纪末到20世纪初,高位结扎剥脱术是治疗小隐静脉曲张的唯一治疗方式[4],然而,此手术方式复发率较高[5],而且由于小隐静脉与腓肠神经伴行,增加了神经损伤的风险。在小隐静脉曲张的开放手术中,约26%的患者可并发腓肠神经病变[6-7],由于其解剖结构的变化,即使术前通过超声确定位置,约22%的患者术中也不能充分识别近端小隐静脉或隐腘窝交界处[8]。由于高危结扎剥脱术创伤较大,并发症较多,故不利于患者的术后恢复。近年来,随着静脉血管超声成像技术的发展,超声引导下射频消融术逐渐被广泛应用于小隐静脉曲张的治疗中,与常规手术方式相比,射频消融术对大隐静脉曲张的侵入性更小,更安全有效[9],但对小隐静脉曲张的安全性和有效性的研究并不多。泡沫硬化剂通过破坏静脉血管内的表皮细胞,促使相关静脉闭塞,可处理射频消融未消除的浅静脉团。因此,本研究旨在探讨超声引导下射频消融联合点式剥脱及泡沫硬化剂治疗原发性小隐静脉曲张的临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
收集2019年1月至2022年1月于首都医科大学附属北京朝阳医院与中国医学科学院北京协和医学院北京协和医院接受超声引导下射频消融联合点式剥脱及泡沫硬化剂治疗的小隐静脉曲张患者的临床资料。纳入标准:经彩色多普勒超声证实下肢静脉曲张源于小隐静脉反流,小隐静脉主干直径>5.0 mm,反流时间>1.0 s;小腿沉重、酸胀感等静脉曲张症状或小腿可见迂曲扩张的浅静脉。排除标准:凝血功能障碍;肝肾功能不全;长期卧床史;伴严重的心、肺功能疾病,全身情况差;深静脉血栓形成继发的下肢静脉曲张,静脉曲张合并浅静脉炎;并发大隐静脉曲张;对硬化剂过敏。根据纳入与排除标准,最终共纳入24例小隐静脉曲张患者,其中,男性14例,女性10例;年龄25~78岁,平均(60.54±7.15)岁;平均身高(165.78±8.25)cm;平均体重(73.06±10.87)kg;共30条患肢,其中,双下肢6例,左下肢10例,右下肢8例;高血压13例,糖尿病7例,手术史10例,吸烟史12例,饮酒史9例,均控制较稳定;临床表现-病因学-解剖学-病理生理学(clinical etiology anatomy pathophysiology,CEAP)分级[10]中,C2级患肢18条,C3级7条,C4级5条。
1.2 方法
术前使用彩色多普勒超声评估下肢静脉情况,嘱患者取站立位,将患肢外展外旋,从腹股沟处开始向下探查,并测量股静脉、大隐静脉、腘静脉、小隐静脉的直径,应用挤压法检查各段静脉瓣膜功能,明确所有可能引起静脉曲张的深浅静脉瓣膜功能不全的部位及程度,最后探查小隐静脉管腔内的血流信号、瓣膜的反流时间、小腿交通支静脉的开放程度,监测生命体征及实验室检查结果(血常规、肝功能、肾功能等)。手术过程中,患者取俯卧位,在超声引导下沿小隐静脉的走行区皮下注入2%利多卡因,局部麻醉后于小隐静脉踝关节处切开,定位小隐静脉,导入射频导丝及导管鞘。在超声监测下,将射频导管置于隐腘静脉1~2 cm处并固定导管位置,然后在小隐静脉主干周围分段向筋膜组织内注入麻醉肿胀液,之后在18 W的功率下启动射频缓慢回撤完成双极射频诱导热能(radiofrequencyinduced thermotherapy,RFITT)治疗。射频消融小隐静脉主干后,超声引导下对交通支静脉行点式剥脱及泡沫硬化剂处理浅静脉团,注入泡沫硬化剂后注意行局部压迫。微小切口均无需缝合,术后用弹力绷带加压包扎患肢,鼓励患者下地行走运动。术后3 d换药,拆除绷带。出院后,根据患者病情穿戴医用梯度弹力袜3~6个月。
1.3 观察指标及判定标准
记录患者的术后住院时间、下床活动时间、视觉模拟评分法(visual analogue scale,VAS)评分,统计患者术后并发症发生情况,包括血肿、淤血、皮下硬结等。术后2周、1个月、3个月复查彩色多普勒超声,观察小隐静脉是否完全闭锁,治疗有效定义为术后3个月复查超声显示小隐静脉完全闭锁或形成血栓样物质,无交通支及浅静脉迂曲扩张;复发定义为术后3个月仍有小腿沉重等症状及可见浅静脉迂曲扩张,彩色多普勒超声下见小隐静脉或交通支静脉再通。术前、术后1个月记录静脉临床严重程度评分表(venous clinical severity score,VCSS)、阿伯丁静脉曲张问卷(Aberdeen varicose vein questionnaire,AVVQ)、慢性静脉疾病生活质量量表(chronic venous insufficiency quality of life,CIVIQ)。VCSS包括疼痛、静脉性水肿、色素沉着等10个项目,总分为30分,评分越高提示病情越严重。AVVQ是针对下肢静脉曲张患者的生活质量量表,与CEAP分级、VCSS具有较高的一致性[11]。CIVIQ包括社会活动、精神心理、体能、疼痛4个方面,总分为20~100分,评分越高提示生活质量越好。
1.4 统计学方法
应用SPSS 25.0软件对数据进行统计分析,符合正态分布且方差齐性的计量资料以(±s)表示,组间比较采用两独立样本t检验;计数资料以n(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
24例患者平均手术时间为(50±24)min,平均射频消融时间为(2.31±0.12)min,平均射频功率为18 W,每个患者平均有2个点式剥脱切口,术后住院时间为(2.00±1.00)d,下床活动时间为(3.34±1.20)h,术后VAS 评分为0~2分。术后2周、1个月、3个月进行彩色多普勒超声随访,90%(27/30)患肢治疗有效;术后3个月超声检查提示小隐静脉几乎无血流,10%(3/30)患肢复发。术后,3例患肢血肿,4例淤血,1例皮下硬结,并发症总发生率为33.33%(8/24)。术后1个月VCSS、AVVQ、CIVIQ评分均明显低于术前,差异均有统计学意义(P<0.01)(表1)。
表1 手术前后VCSS、AVVQ、CIVIQ评分的比较(±s)
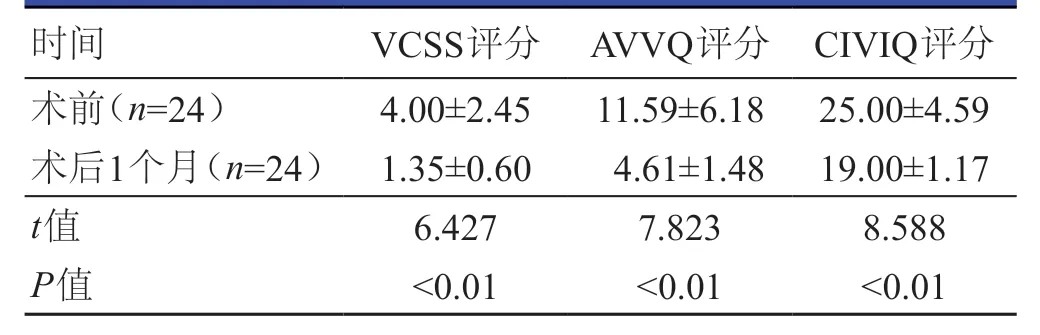
表1 手术前后VCSS、AVVQ、CIVIQ评分的比较(±s)
时间 VCSS评分 AVVQ评分 CIVIQ评分术前(n=24) 4.00±2.45 11.59±6.18 25.00±4.59术后1个月(n=24) 1.35±0.60 4.61±1.48 19.00±1.17 t值 6.427 7.823 8.588 P值 <0.01 <0.01 <0.01
3 讨论
与传统的小隐静脉高位结扎剥脱术相比,超声引导下射频消融联合手术具有恢复时间快、并发症少、安全性高等优点。由于隐腘窝连接处解剖复杂,开放手术对外科技术的要求较高,可能与较高的复发率和并发症相关[12]。目前,越来越多的患者更倾向于接受超声引导下的微创手术,如射频消融术、腔内激光消融术等[13]。Park等[14]研究也发现射频消融术后小隐静脉的1年闭塞率为93.5%(43/46),所有患者的CEAP分级和CIVIQ评分均显著改善,表明通过射频消融术治疗小隐静脉曲张安全、有效。一项纳入49篇文献的Meta 分析结果显示,手术对小隐静脉曲张的解剖成功率为58.0%,射频消融术的解剖成功率为97.1%,超声引导下泡沫硬化剂治疗的解剖成功率为63.6%,提示联合应用射频消融技术和泡沫硬化剂治疗小隐静脉曲张会取得较好的疗效[5]。超声引导下泡沫硬化剂处理交通支静脉是一种安全有效的治疗中小静脉曲张的方法[15],利用超声可观察泡沫硬化剂的流动情况以及分布情况,从而提高手术的治疗效果。
本研究结果显示,超声引导下射频消融联合点式剥脱及泡沫硬化剂治疗小隐静脉曲张可对90%的患肢有效,术后3个月复查超声小隐静脉完全闭锁或形成血栓样物质,无交通支及浅静脉迂曲扩张。Helmy ElKaffas 等[16]研究发现,90例患者射频消融术后24个月的血管闭塞率为94.5%(84/89),其他研究也发现射频消融术的血管闭塞率较高,均为90%以上[9,14,17]。研究显示,与腔内激光消融术相比,射频消融术围手术期疼痛程度较低,淤血等并发症的发生率也较低[18-19]。本研究结果显示,射频消融联合点式剥脱及泡沫硬化剂术后并发症的发生率较低,术后VAS 疼痛评分仅为0~1分,与上述研究结果相符。本研究结果显示,术后1个月VCSS、AVVQ、CIVIQ 评分均明显低于术前,差异均有统计学意义,提示射频消融联合点式剥脱及泡沫硬化剂术后患者的满意度较高。Choi 等[9]研究也发现射频消融术对小隐静脉曲张的疗效较好,CEAP 分级及VCSS 评分均优于术前,差异均有统计学意义。然而,目前关于小隐静脉曲张的研究较少,且大部分研究随访期间小于1年,因此,需要更多前瞻性研究并延长随访时间,进一步深入探讨小隐静脉曲张的治疗及其预后情况。
综上所述,超声引导下射频消融联合点式剥脱术及泡沫硬化剂对原发性小隐静脉曲张的治疗效果较好,安全性较高,值得在临床推广应用。

