老年病人非心脏手术全麻苏醒延迟风险预测模型的建立与验证
沈 俊,李德奎,李晓明,杨 洋,丁少成
苏醒是全身麻醉(全麻)的一个重要阶段,其特征是病人从无意识状态恢复觉醒和意识。这个复杂的过程有着不同于诱导的精确的神经生物学机制[1]。全麻结束后90 min内病人仍然不能自主睁眼或唤醒睁眼称之为苏醒延迟(delayed emergence,DE)[2-3],尽管全麻药物可以在几分钟内代谢清除,但部分病人仍然存在DE。目前,我国人口老龄化趋势越加明显,老年病人接受手术逐年增多,老年病人各系统功能呈退行性变化,对全麻药物敏感性高,内环境易紊乱,导致老年病人更易发生DE,也是麻醉医生面临的严峻挑战。研究[4]发现,未区分年龄时DE发生率为0.5%,而老年病人非心脏手术DE发生率目前尚无真实确切数据。随着精确麻醉理念和快速康复理念的不断深入,提高老年病人麻醉复苏质量对于促进老年病人围术期快速康复,减少相关并发症发生具有重要意义。DE的影响因素较多[5],本研究通过筛选老年病人非心脏手术全麻DE的危险因素,构建DE的预测体系并对其效能进行验证,为临床预防DE提供参考,现作报道。
1 资料与方法
1.1 一般资料 本研究查阅相关研究文献,并实施预实验,结果表明100例老年病人非心脏手术发生DE 9例,发生率为9%,初步纳入6项可能与DE发生相关的危险因素,每项危险因素纳入10项结局事件,计算出样本量需要667(6×10/0.09)例,假设脱落率为15%,故需要样本778例。本研究方案经皖西卫生职业学院附属医院伦理委员会批准,选择2021年1月至2022年3月计划接受非心脏手术的老年病人778例作为研究对象,均与病人或病人家属签署研究知情同意书。纳入标准:年龄≥65岁,性别不限;美国麻醉师协会分级(ASA)Ⅱ~Ⅲ级;气管插管全麻;能够配合研究。
1.2 方法 本研究由受过专门训练的研究人员进行术前访视与数据的收集,入组病人的特征信息通过皖西卫生职业学院附属医院麦迪斯顿手术麻醉信息系统收集,包括(1)一般资料:年龄、性别、ASA分级、体质量指数(BMI)、术前MMSE量表评分、术前Fried表型(Fried′s phenotype,FP)衰弱评分≥3分例数(FP量表由体质量变化、握力、疲乏、步速、身体活动量5个项目组成,评分标准:0分为无衰弱,1~2分为衰弱前期,≥3分为衰弱)[6]、吸烟史、饮酒史、基础疾病史[高血压、糖尿病、冠心病、慢性阻塞性肺部疾病(COPD)]、术前血红蛋白、术前总蛋白、白细胞、总胆红素、谷氨酸氨基转移酶、肌酐、血糖;(2)术中资料:手术类型、麻醉时间、全凭静脉麻醉、舒芬太尼用量、输液总量、出血量、术中血压降低(术中低血压定义:收缩压低于术前基准状态20%)、术中血压升高(术中高血压定义:收缩压高于术前基准状态20%)、术中低脑电双频指数(BIS)(BIS值<45)、术中平均体温。剔除标准:(1)心肺功能严重障碍、脑缺血性疾病;(2)视听力障碍;(3)合并精神分裂症,抑郁症;(4)行心血管手术以及神经外科手术;(5)术后转入ICU;(6)病人麻醉单缺失本研究所需的数据。
1.3 DE的评估 病人麻醉停止即视为复苏开始,期间麻醉医生每隔10 min采用Steward 评分对病人进行评估,评分结果记录于手术麻醉系统中。其中Steward 评分总分0~6分,<4分为未苏醒,≥4分为苏醒。在麻醉停止后90 min时Steward 评分<4分,定义为DE。
1.4 统计学方法 采用t检验、χ2检验或Fisher精确概率法、ROC曲线、多因素logistic回归分析、Nomogram模型和决策曲线分析 ( decision curve analysis,DCA ) 。
2 结果
2.1 老年病人非心脏手术全麻DE发生的单因素分析 本研究共对778例全身麻醉非心脏手术老年病人进行回顾性分析,其中自愿退出本研究18例,术后转入ICU 12例,资料不全30例,最终纳入718例,全身麻醉后共发生66例DE,发生率为9.2%。DE的发生与年龄增加、术前MMSE评分减低、术前FP评分增加、合并COPD、术前血红蛋白浓度减低、麻醉时间延长、术中发生低血压、术中BIS值<45有关(P<0.05~P< 0.01)(见表1 )。
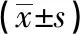
表1 老年病人非心脏手术全麻DE发生的单因素分析
2.2 DE相关因素的ROC分析 将表1结果中差异有统计学意义的计量资料进行 ROC 曲线分析,计算最佳截断值。结果显示:年龄、术前MMSE评分、术前血红蛋白水平、麻醉时间的AUC分别为0.823、0.725、0.673、0.609;最佳截断值分别为:>74岁、≤25分、≤103.7 g/L、>142 min(见图1、表2)。
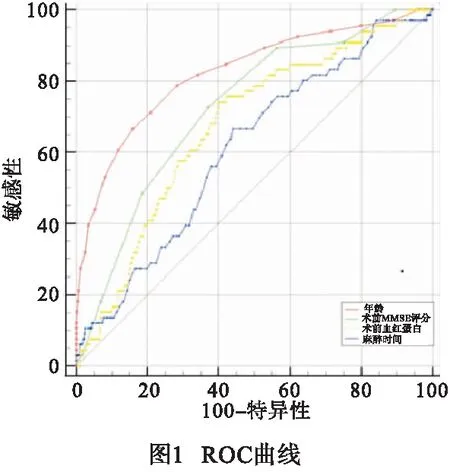
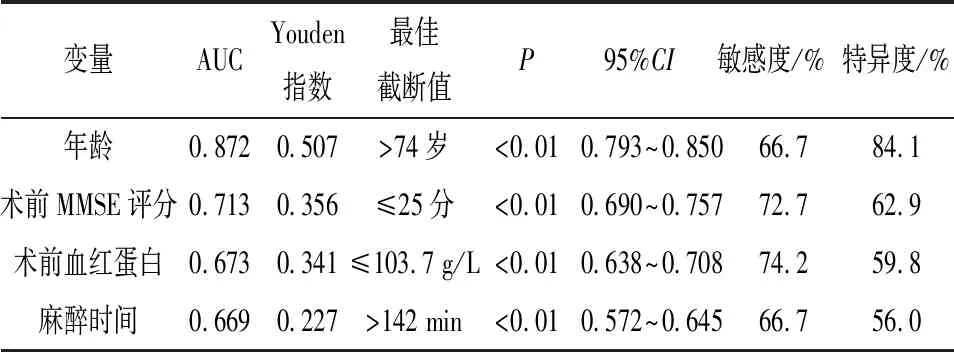
表2 老年病人非心脏手术全麻DE相关变量 ROC曲线分析
2.3 DE发生风险因素的多因素logistic 回归分析 将表1中有统计学意义的计数资料指标以及表2中的变量转化为二分类计数资料进行多因素 logistic 回归分析,采用逐步回归法,Hosmer-Lemeshow模型拟合度有统计学意义(χ2=1.69,P>0.05),结果表明:年龄 (>74岁)、术前MMSE 评分 (≤25分)、术前FP评分 (≥3分)、合并COPD(是)、术中低血压(是)、术中BIS<45(是)是老年病人非心脏手术全麻DE发生的危险因素(P<0.01)(见表3)。
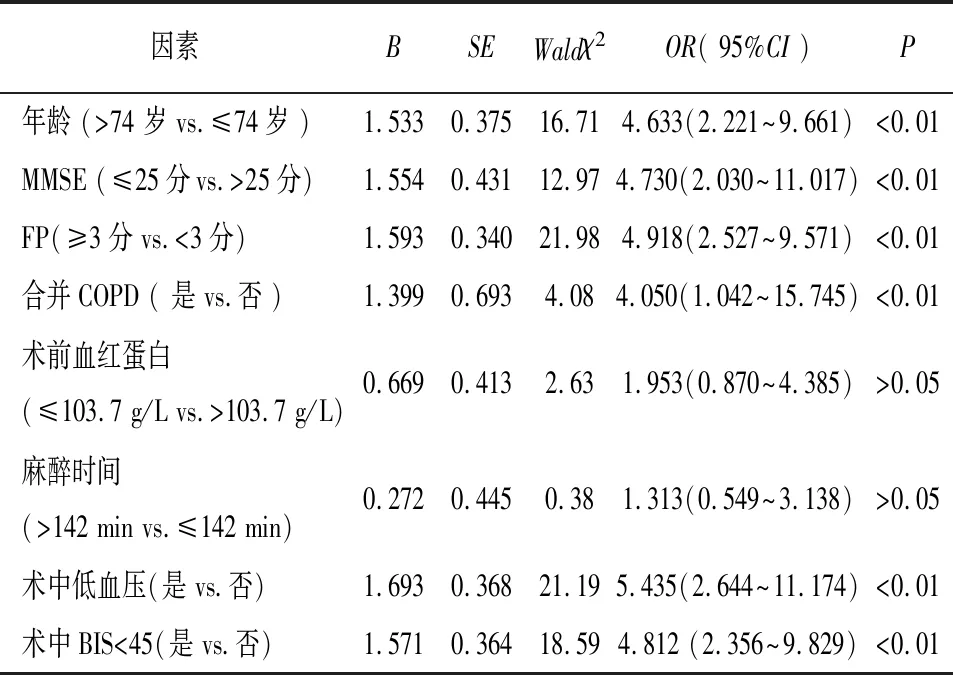
表3 老年病人非心脏手术发生DE的多因素 logistic 回归分析
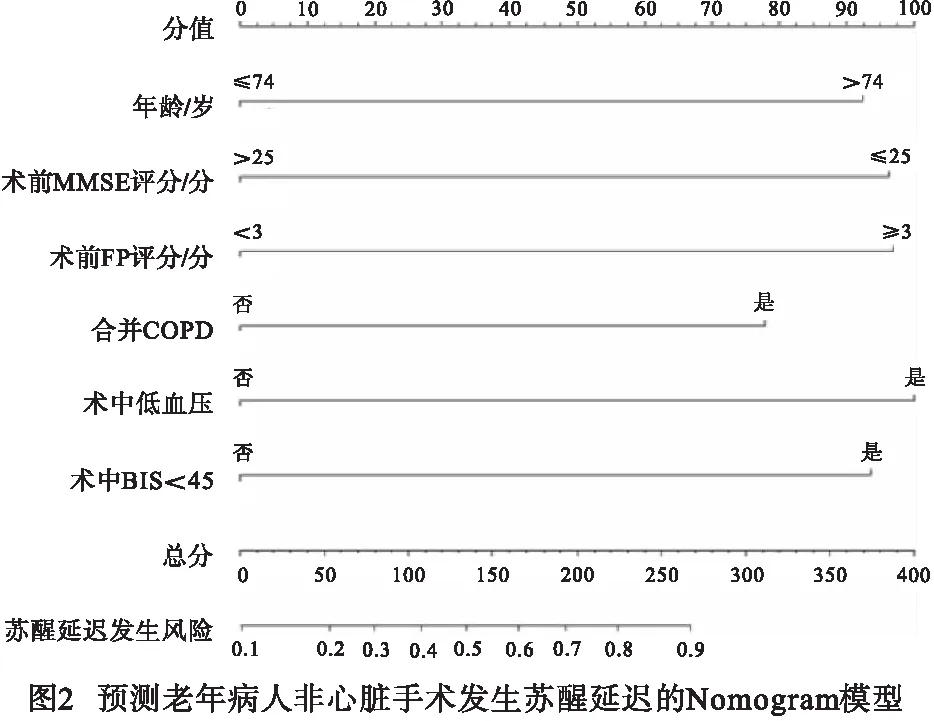
2.4 DE的Nomogram模型构建 将年龄>74岁、术前MMSE 评分≤25分、术前FP评分≥3分、合并COPD、术中低血压、术中BIS<45作为构建预测老年病人非心脏手术发生DE的预测因子,绘制Nomogram模型(见图2)。R语言结果显示 C-index 为 0.750(95%CI:0.679~0.821),内部验证显示校正 C指数为0.743,说明此Nomogram模型具有中等的预测能力。
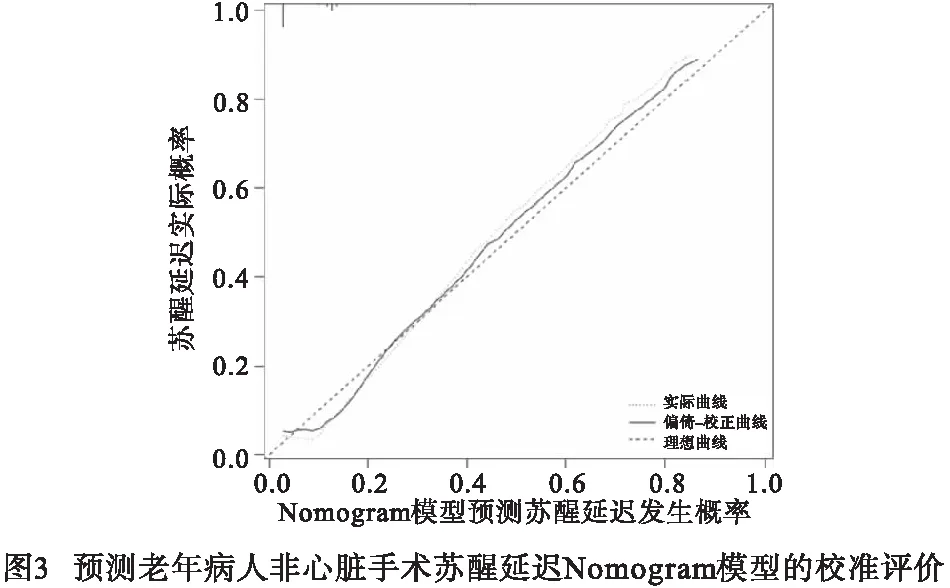
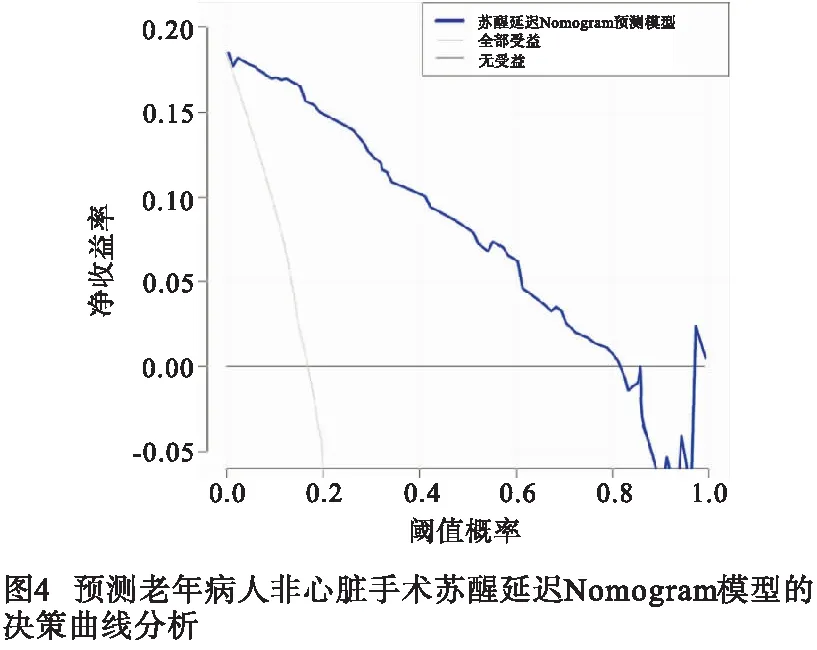
2.5 Nomogram模型的校正与决策曲线评价 首先绘制预测老年病人非心脏手术发生DE的Nomogram模型的校准曲线(见图3),对角线虚线代表理想模型的预测,虚点线表示本研究构建的Nomogram性能,实线表示对构建的Nomogram的校正曲线,其越接近对角线虚线表示预测性能越佳。使用“rmda”包进行DCA分析评估本研究构建的Nomogram模型临床收益,结果表明Nomogram模型预测DE风险阈值为2.0%~81.5%,此时能为临床增加预测收益 (见图4)。
3 讨论
本队列研究结果显示:老年病人非心脏手术全身麻醉DE发生率为9.2%,既往对老年病人非心脏手术DE的临床研究数据很少,大多数可获得的公开材料由病例报告组成[7]。ZELCER等[8]报道443例混合类型手术病人在全麻后15~90 min内无反应的发生率为9.46%,本研究结果与其相近。DE临床上表现为镇静、缺乏主动性和对刺激缺乏足够的反应。其影响因素众多,大部分是可逆转的因素,很小部分可能是脑缺血缺氧性损伤或卒中等器质性疾病导致[9]。本研究针对影响老年病人DE的因素进行筛查,对于有意义的计量资料进行ROC分析,计算其AUC和最佳截断值,并根据最佳截断值将有意义的计量资料转变为二分类计数资料,多因素logistic回归分析结果表明,年龄>74岁、术前MMSE评分≤25分、术前FP评分≥3分、合并COPD、术中低血压、术中BIS<45是老年病人非心脏手术发生DE的危险因素。
为了直观地将影响DE的因素展现出来,我们构建预测老年病人非心脏手术全麻DE的Nomogram模型。列线图在医学中被广泛用作预测预后的工具,具有用户友好的数字界面,更容易理解,帮助临床做出决策。本研究构建的预测DE Nomogram模型的C指数为0.750,队列的内部验证得出校正C指数为0.743,显示出该模型具有良好的辨别力。校正曲线与决策曲线分析均证实该DE Nomogram模型具有较好的准确性,预测DE风险阈值为2.0%~81.5%,能够为临床预测DE的发生提供决策支持。
研究[10]发现随着年龄的增加大脑微血管再生机制受损,微血管血供能力降低,导致神经元供血减少,血脑屏障的完整性及功能受损可导致神经元过度氧化应激反应,导致神经退行性变。神经系统退行性变导致病人对全身麻醉剂、阿片类药物和苯二氮卓类的敏感性增加[11]。老年人麻醉后的脑电波与年轻人明显不同,主要以δ波为主,同时脑电爆发性抑制的发生明显增加,这同样增加了对麻醉药的敏感性[12]。老年人体内的分布体积、清除率和血浆蛋白结合的减少导致药物的游离血浆浓度增高。以上的因素共同导致了老龄化病人麻醉药物产生的效应更加持久而代谢相对减缓,从而导致DE的发生增加。
MMSE评分是评测认知功能常用量表,既往研究表明术前认知功能降低是老年病人非心脏手术术后谵妄发生的独立危险因素[13],使用MMSE评分来预测老年病人非心脏手术DE发生的风险同样也是可行的[14],值得注意的是相当部分的谵妄发生在复苏室内,它可能是DE的一种原因,主要表现为睡眠增多,表情淡漠、语速及动作缓慢等活动受抑表现[15],此外认知功能减退也是中枢神经系统退行性变的一种表现。
衰弱是老龄化人口最重要的特征之一,衰弱病人的生活自理能力明显降低,同时增加术后不良事件发生率[16]。研究[17]发现,75 岁及以上社区老年人中 55.7%存在身体衰弱,40.3%合并有轻度认知障碍,故麻醉医生对“衰弱及其对围手术期的影响”的关注度越来越高,但目前术前衰弱与DE的研究较少。还有研究[18]发现术前身体衰弱是老年病人行非心脏手术发生术后谵妄的危险因素;黄煦晨[19]发现合并衰弱的老年病人行无痛胃肠镜检查时的苏醒时间明显延长。衰弱导致DE发生率增加可能与以下因素有关:(1)肌肉组织萎缩,脂肪相对增多,会使亲脂性的麻醉药物作用时间更长;(2)肾脏萎缩,麻醉药物在肾脏的排泄速度降低;(3)肺实质弹性逐渐减低,功能性肺泡表面积减少,呼吸肌功能降低,导致通气/血流灌注比例失调,拔管后低氧血症和肺不张发生风险增加[20]。笔者强调,迫切需要将术前虚弱评估作为接受手术的老年人的风险分层工具,以弥补常用的风险预测工具,如年龄、美国麻醉医师协会(ASA)分级、代谢当量评分(METS)等无法衡量到的麻醉风险,做到针对性地预防,改善老年病人的预后与康复。COPD的最主要特征是气流的不可逆受阻、肺泡通气量不足以及通气/血流比例失调[21],合并COPD导致DE发生率增加可能与以下因素有关:(1)肺泡通气量不足导致残留的吸入麻醉药排泄减缓;(2)麻醉机械通气后通气/血流比例进一步失衡,肺通气和肺换气受限,进一步损害 COPD病人的气体交换,导致高碳酸血症进而影响麻醉复苏[22]。术中低血压在老年病人非心脏手术期间较为常见,研究[23]表明,术中低血压可能导致术后30 d内重要器官缺血和术后死亡率增加。术中低血压可导致脑缺血缺氧,即使一过性的缺氧也可能造成脑组织不可逆性的水肿和坏死,这种改变在老年人中更加明显。此外老年人的脑血管自动调节能力受损,对低血压的代偿作用减弱,导致脑低灌注,使大脑功能恶化,这种影响主要表现为术后认知功能改变以及脑卒中的发生[24],这些改变也会导致病人的苏醒时间延长,是否能够通过预防术中低血压的发生减少老年病人术后DE的发生值得进一步研究。BIS能够较好地反映大脑皮层的功能状态,减少全麻药用量,研究[25]发现使用BIS进行监测,能够缩短病人拔管时间、睁眼时间以及定向力恢复时间。亦有研究[26]发现,老年病人胃肠道手术术中维持较低的BIS(40~49)导致术后意识恢复时间明显延长。临床上将BIS值<45作为深麻醉状态的标准[27],术中BIS值<45导致DE发生可能与深麻醉状态下脑电爆发性抑制增加,脑灌注减少对麻醉药物敏感性增加有关[12,28]。
针对本研究发现的影响老年病人非心脏术的危险因素,我们应该做到有的放矢,有针对性地干预,积极制定术前、术中、术后各项有力措施。DE的发生是多种因素导致的,也可能是其他术后不良转归的结果,当出现DE时应该维持病人血流动力学、内环境稳定,积极纠正可逆因素,减少并发症发生。但本研究具有一定的局限性:(1)既往鲜见针对老年病人的DE研究,DE的发生率无法参考;(2)预测模型为单中心研究,DE的发生率以及预测模型的准确性有待多中心研究验证;(3)影响DE的因素可能纳入不全,可能遗漏一部分有意义因素(如苏醒时的体温保护、术后疼痛控制、神经阻滞的应用、术中输血等)。

