人工肝治疗肝衰竭病人医院感染调查及危险因素分析
乔 艳,刘传苗,汪小玲,张 妹,李冬冬,郭 普
肝衰竭(liver failure,LF)是由各种因素引起的肝细胞严重损害,病情危重,并发症多,临床治疗困难,单纯内科治疗效果不理想,病死率高[1]。人工肝治疗能够有效清除肝衰竭病人体内有害物质,改善内环境,暂时替代肝脏部分功能,为肝细胞再生创造条件,明显降低肝衰竭病人死亡率,已广泛应用于临床[2]。然而,肝衰竭病人免疫功能低下、肠道菌群易位、人工肝治疗及各种侵袭性操作等诸多因素导致病人易发生医院感染,严重影响治疗效果和预后[3]。本研究回顾性分析了207例人工肝治疗肝衰竭病人的临床资料,探讨人工肝治疗肝衰竭病人发生医院感染的危险因素,为制定预防措施,降低医院感染发生率提供参考。现作报道。
1 资料与方法
1.1 一般资料 选择2018-2021年在蚌埠医学院第一附属医院感染病科住院接受人工肝治疗的且符合纳入标准的207例肝衰竭病人为研究对象,其中发生医院感染的病人有46例。纳入标准:(1)病人的诊断均符合《肝衰竭诊治指南(2018年版)》[4];(2)病人均接受人工肝治疗;(3)病历资料完整;(4)医院感染符合《医院感染诊断标准》[5]。排除标准:(1)病人同时合并严重心、脑、肾脏疾病及恶性肿瘤;(2)伴有肺部疾病病史;(3)伴有泌尿系统疾病病史;(4)临床资料不完整。
1.2 研究方法 通过医院信息系统回顾性收集病人临床资料,包括性别、年龄、住院时间、人工肝导管留置时间、是否合并糖尿病等。分析实验室检查结果包括病人白细胞计数、总胆红素浓度(TBil)、血浆白蛋白、凝血酶原时间、凝血酶原活动度、国际标准化比值(INR)、血肌酐(Cr)及细菌培养。对病人进行终末期肝病模型(MELD)评分[6],计算公式:9.57×(Cr mg/mL)+ 3.78×(TBil mg/mL)+ 11.2 ×(INR)+ 6.4(病因:胆汁淤积性或酒精性肝硬化为0,其他为1)。高危:>18 分,中危:15~18 分,低危:≤14分。
1.3 统计学方法 采用t检验、χ2检验和二元logistic回归分析。
2 结果
2.1 人工肝治疗肝衰竭病人发生医院感染的情况 本研究纳入的207例人工肝治疗肝衰竭病人中,46例病人(22.22%)发生医院感染,其中呼吸道感染病人29例,自发性腹膜炎10例,血流感染4例,穿刺伤口感染1例,泌尿系统感染1例,肠道感染1例。病人各类标本中共分离出48株病原菌,革兰阴性菌占56.25%,革兰阳性菌占25.00%,真菌占18.75%。痰等呼吸道标本中主要分离菌为肺炎克雷伯菌、金黄色葡萄球菌和白念珠菌、曲霉菌。自发性腹膜炎主要病原菌为大肠埃希菌和粪肠球菌。分布见表1。
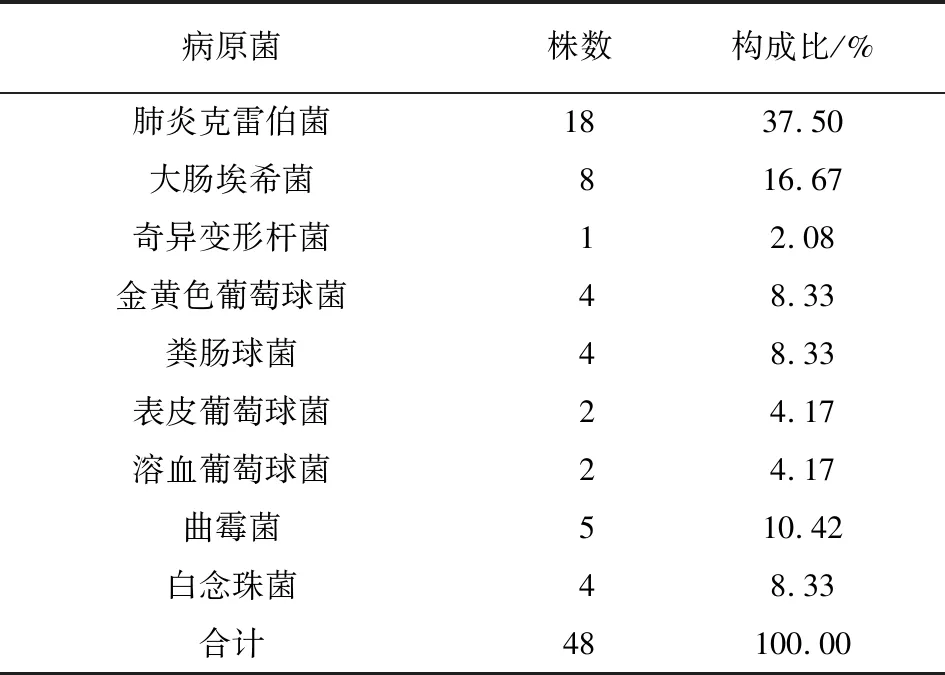
表1 人工肝治疗肝衰竭病人医院感染病原菌分布
2.2 人工肝治疗肝衰竭病人发生医院感染的单因素分析 感染组和非感染组病人在年龄、是否合并糖尿病、人工肝导管留置时间、血清白蛋白、MELD评分等指标比较差异均有统计学意义(P<0.05~P<0.01)(见表2)。
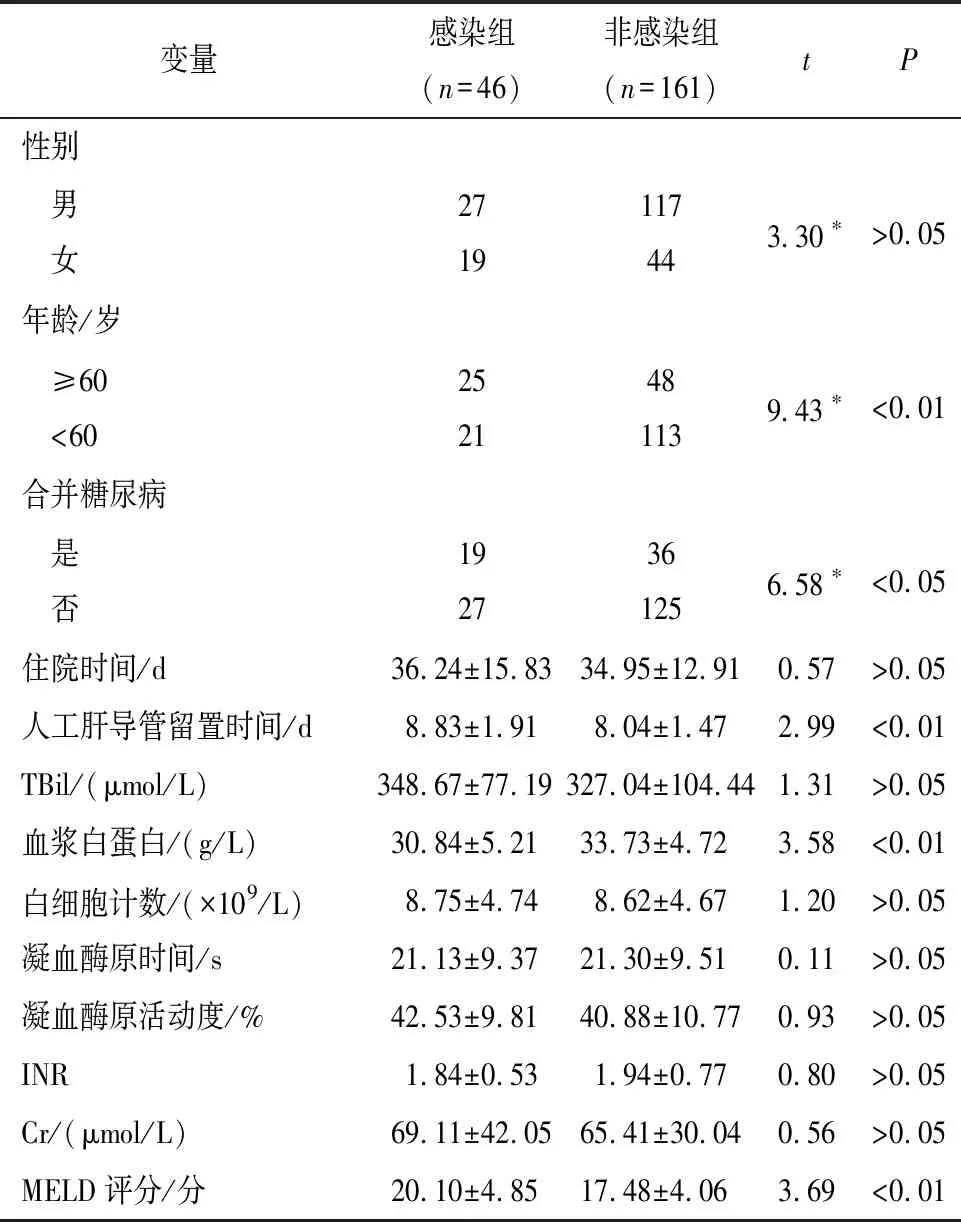
表2 人工肝治疗肝衰竭病人发生医院感染的单因素分析
2.3 人工肝治疗肝衰竭病人发生医院感染的logistic 回归分析 以是否发生医院感染为因变量,将单因素分析中有统计学意义的变量纳入二元logistic回归分析,结果显示合并糖尿病、病人年龄≥60岁、人工肝导管留置时间、血浆白蛋白、MELD评分是人工肝治疗肝衰竭病人发生医院感染的独立危险因素(P<0.05~P<0.01)(见表3、4)。
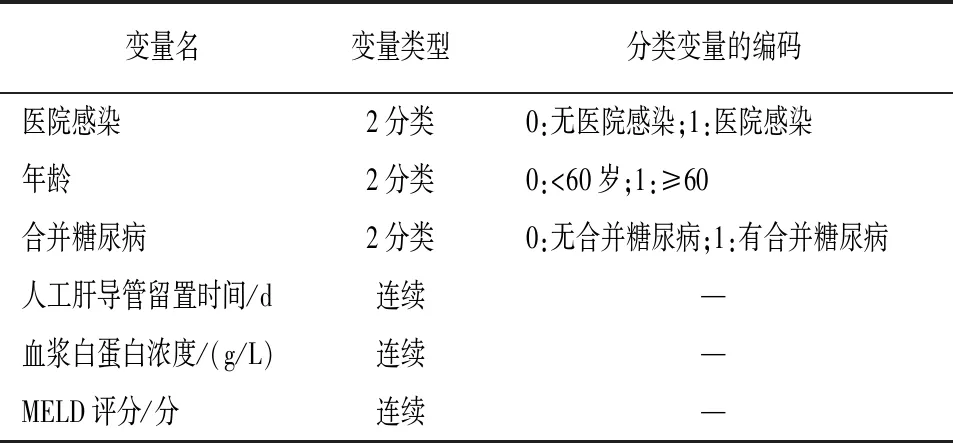
表3 人工肝治疗肝衰竭病人医院感染相关变量赋值
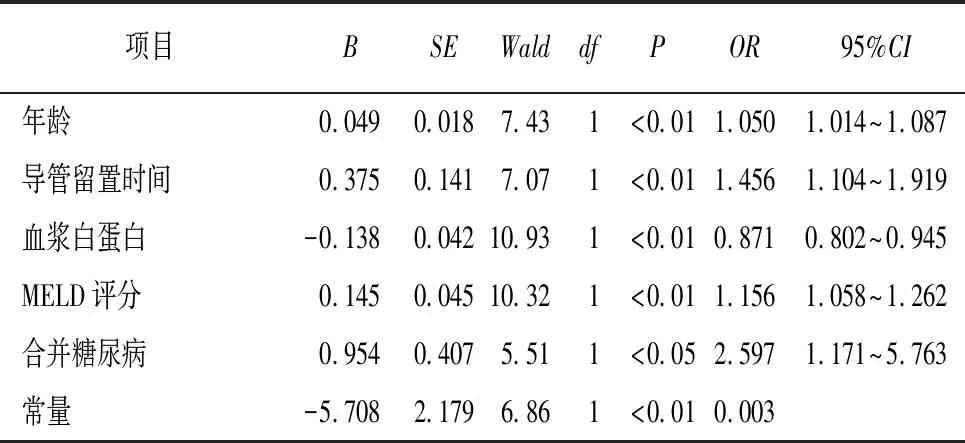
表4 人工肝治疗肝衰竭病人医院感染的logistic 回归分析
3 讨论
肝衰竭病人因肝细胞大面积坏死,导致肝脏合成、解毒及代谢功能障碍,机体血浆纤维结合蛋白和补体功能缺陷等原因导致机体免疫功能低下,肠道菌群紊乱及移位易发生医院感染。一旦发生医院感染,常导致病人病情加重,延长住院时间,增加医疗费用,是引起死亡的危险因素[7-8]。本研究调查了207例人工肝治疗肝衰竭病人临床资料,46例病人发生医院感染,医院感染发生率为22.22%。高于董方红等[3]报道的11.4%和胡世云等[8]报道的13.77%。
本研究中,人工肝治疗肝衰竭病人发生感染以呼吸道感染为主,其次是自发性腹膜炎,与文献[3]报道结果相近。胡正翠等[9]对238例肝衰竭病人进行调查显示肺部感染发生率为22.70%,本研究组肺部感染发生率为14.01%。人工肝治疗期间,病人卧床时间长导致气道分泌物清除能力下降,抗生素和激素的不规范应用增加了肺部感染的风险。另外,高龄病人的气道和肺组织生理结构发生了退行性改变,降低了防御功能,使得空气中的真菌孢子、口腔内定植真菌易进入肺部而发生感染[10-11]。本研究组病人呼吸道主要的分离菌为肺炎克雷伯菌、金黄色葡萄球菌以及白念珠菌、曲霉菌,与相关报道[11-13]一致。自发性细菌性腹膜炎(spontaneous bacterial peritonitis,SBP)也是肝衰竭病人常见并发症之一。研究显示SBP发生的机制主要是肠源性、非肠源性以及一些诱发因素共同作用。肠源性因素包括肝脏单核吞噬细胞系统功能受损,毒素清理能力下降引起肠道菌群过度繁殖,肠壁黏膜通透性增加,大量病原微生物移位至腹腔繁殖;非肠源性因素是指致病菌从皮肤、呼吸道、泌尿道等入侵,同时侵袭性操作破坏人体自然屏障,给病原菌入侵提供条件。另外,低白蛋白血症可诱发腹水产生,腹水中的蛋白质为细菌的生长繁殖提供了营养成分[14-15]。JAIN等[16]研究显示肝衰竭病人的SBP总发生率为20%,而其中医院获得性自发性腹膜炎占16.5%,高于本研究报道。本研究中有10例病人发生了医院获得性自发性腹膜炎,占4.83%,病原菌以肠道菌群大肠埃希菌和粪肠球菌为主。
logistic回归分析显示高龄(年龄≥60岁)、人工肝导管留置时间、血浆白蛋白浓度、合并糖尿病、MELD评分是人工肝治疗肝衰竭病人发生医院感染的危险因素。随着年龄增长,机体的器官功能发生退行性改变,防御功能逐渐下降,高龄病人基础疾病多,营养状态差,免疫力低下,抵御病原菌能力明显下降,研究显示老年住院病人更容易并发医院感染[17]。本调查中感染组高龄病人占54.35%高于非感染组29.81%(P<0.01)。中心静脉置管是人工肝治疗期间必备的血管通路,治疗操作时和导管留置期间,细菌易通过皮肤置管部位或导管开口处进入血液循环引发导管相关性感染,此外,置管24~48 h后导管内纤维蛋白逐渐沉积,可以保护病原微生物免受抗菌药物和吞噬细胞的侵害增加感染风险,多项研究显示中心静脉导管感染发生率与导管留置时间呈正相关[18]。本研究中感染组导管留置时间(8.83±1.91)d,高于非感染组(8.04±1.47)d (P<0.01),与文献[19]报道一致。肝衰竭病人因蛋白质合成障碍、摄入不足、人工肝治疗后血浆白蛋白丢失等因素极易出现低蛋白血症。低蛋白血症可引起机体有效血浆胶体渗透压下降,组织间隙水肿产生腹水和胸水,胸、腹水中的蛋白质利于细菌的生长繁殖,同时病人血浆白蛋白浓度降低提示营养不良,导致机体免疫力下降易诱发感染。本研究中感染组血浆白蛋白浓度低于非感染组病人,2组比较差异有统计学意义(P<0.01)。血糖平稳是维持生理平衡、保证机体正常代谢的关键。血糖水平升高可刺激血管内皮细胞活化后收缩,毛细血管通透性增加,大量液体渗出导致器官和组织灌注不足,引起细胞功能受损及水、电解质紊乱,进而降低中性粒细胞趋化作用及免疫细胞的吞噬功能,导致机体抵抗力下降;同时,高血糖状态利于病原微生物的入侵、定植和繁殖,研究显示糖尿病病人合并感染的发生率可达到25.8%~57.5%[20]。本调查中感染组合并糖尿病病人19例,占41.30%,非感染组合并糖尿病病人36例,占22.36%(P<0.05)。MELD评分作为肝衰竭病人预后的预测指标,具有数据客观、重复性好且涵盖了病人肾功能指标等优点,广泛应用于临床,分值越高提示预后越差,研究证实MELD评分是肝衰竭病人发生医院感染的独立危险因素,本研究中感染组与非感染组MELD评分比较差异有统计学意义(P<0.01),与相关研究[21]结果一致。
医院感染在人工肝治疗肝衰竭病人中发生率较高,是影响病人治疗效果和预后的重要因素。临床治疗过程中,要合理安排人工肝治疗时间,尽量缩短中心静脉导管留置时间,监测病人血浆白蛋白、血糖值变化,对于低蛋白血症病人早期补充白蛋白,糖尿病病人控制血糖在稳定范围,动态评估病人营养状况,制定个性化营养供给方案;关注年龄≥60岁、MELD评分中高危病人,指导病人有效咳嗽,提高机体免疫功能,尽量减少不必要的侵袭性操作,做好各项院感防控措施,预防医院感染的发生。

