稳定同位素技术在水体硝酸盐污染源解析中的研究进展
张列宇,马阳阳*,李国文,唐文忠,杜彩丽,3
1.中国环境科学研究院
2.中国科学院生态环境研究中心
3.同济大学环境科学与工程学院
氮(N)是地球大气中含量最丰富的化学元素(几乎占80%),也是许多关键生物分子(如氨基酸、核苷酸)的基本成分之一。早在20 世纪50年代,人类活动造成的氮负荷已经改变了全球氮循环,比自然来源的氮负荷高出近30%[1]。氮在自然水体中的形态包括有机氮和无机氮,其中硝酸盐()是最稳定的形态,对溶解性无机氮的贡献超过80%[2-4]。硝酸盐以各种方式进入水体,对饮用水造成不利影响,直接威胁人体健康,增加罹患如高铁血红蛋白症、糖尿病、致畸形及非霍奇金淋巴瘤、膀胱癌和卵巢癌等疾病的风险[5-9]。根据世界卫生组织(WHO)发布的最大污染物水平,饮用水中硝酸盐的安全浓度应小于10 mg/L[10]。此外,硝酸盐还会对水生态系统健康造成不利影响,导致水生态系统酸化,刺激初级生产者生长增殖,使水生态系统富营养化,甚至达到损害水生动物生存的毒性水平[11-12]。为减少硝酸盐输入,改善受污染水体的水生态系统状况,准确识别硝酸盐污染来源至关重要。
水体中硝酸盐来源复杂多样,可分为自然源和人为源[13]。目前暴露在地球表面的岩石中,有75%是沉积岩,这些岩石含有全球氮储量的20%左右[14]。Holloway 等[15]在研究加利福尼亚地区某些流域地表水硝酸盐污染与周边含有较高浓度固定氮的基岩的联系发现,地质氮的释放有助于生态系统中氮饱和,导致河水中硝酸盐浓度升高,是地表水中硝酸盐的重要自然来源。在过去的几十年里,剧烈的人类活动,如化肥的使用、化石燃料的燃烧、汽车尾气和生活污水排放等,极大地改变了全球氮循环过程,成为水体硝酸盐源中的主要人为源[16-17]。识别硝酸盐来源最传统的方法是通过调查污染区土地利用类型,并结合水化学特征进行分析,但硝酸盐多样的来源和复杂的氮循环过程使结果具有较大不确定性[18]。20 世纪70年代,有学者开始通过对比潜在来源和水体中的氮同位素对硝酸盐进行源解析[19]。随着同位素检测技术的不断发展,氧(O)同位素也应用于其中。然而在以往的研究中,针对水体中硝酸盐在不同时空条件下参与氮转化过程的综合分析不够清楚,定量解析模型常忽略同位素分馏的影响,不同硝酸盐来源间的混合及其氮氧同位素特征值(δ15N-和δ18O-)范围重叠等问题依旧影响源解析的准确性[20]。为弥补氮氧同位素法的不足,多同位素和稳定同位素联用其他技术开始应用于水体硝酸盐污染源解析,为解释硝酸盐来源特征提供了额外信息。同时通过各种源解析模型量化不同污染源对水体中硝酸盐的贡献率,进一步提高了稳定同位素在硝酸盐源解析中的准确性和适用性。目前大部分研究中的定量解析模型所采用的端元数据,即水体硝酸盐潜在来源的δ15N-和δ18O-常引用已有文献数据,而水体硝酸盐潜在来源的δ15N-和δ18O-受同位素分馏影响存在时空差异,直接引用端元数据使得定量研究在场景适用性中存在局限性。因此,笔者综合阐述了稳定同位素分析技术与其在水体硝酸盐污染源解析中的影响因素,分别从定性和定量研究2 个维度,总结了稳定同位素在水体硝酸盐污染源解析中的发展与应用,以及稳定同位素模型在水体硝酸盐污染源解析中存在的问题,并对未来研究方向进行展望,以期为水体中硝酸盐污染控制提供理论依据。
1 稳定同位素分析技术及应用
稳定同位素研究最早源于20 世纪40年代的地球化学领域,Nier 型质谱仪的应用标志着稳定同位素地球化学的诞生,随后研究人员在Nier 型质谱仪的基础上迅速发展出同位素比值质谱仪(IRMS)[21]。双通道同位素比值质谱仪(DI-IRMS)是20 世纪50—80年代使用最多的稳定同位素分析仪器,后来连续流同位素比值质谱仪(CF-IRMS)以在线进行样品制备、样品体积小、分析速度快、成本效益高等特点占领优势地位[22]。根据用途和样品状态不同,CF-IRMS 还可与元素分析仪(EA)、气相色谱(GC)、液相色谱(LC)等仪器联用。热电离质谱仪(TIMS)是与IRMS 同时期出现的另一种较为常用的稳定同位素质谱分析仪器。稳定同位素质谱分析技术已经进入更多研究领域,涵盖从最初的应用领域到与生命科学和环境科学相关的广泛领域[22-23]。
同位素质谱分析技术的进步为水体中硝酸盐氮氧同位素检测提供了有利条件,目前氮氧同位素已广泛应用于水体硝酸盐污染源解析研究[10,24-25]。硝酸盐中氮和氧元素在生物地球化学循环过程中因同位素分馏而产生丰度变化,使得不同来源的硝酸盐具有不同的氮氧同位素组成[26],因此可以通过对比水体与硝酸盐潜在来源中的硝酸盐氮氧同位素组成来定性确定水体硝酸盐污染来源[27-30]。实际工作中常采用δ表示样品的同位素组成,样品δ计算公式如下:
水体中复杂的硝酸盐来源和氮循环过程导致的同位素分馏,改变了硝酸盐的初始氮同位素和氧同位素,这对于准确识别硝酸盐污染源有一定的影响[31]。为提高污染源分析结果的准确性,逐渐发展出多同位素结合其他技术的方法,用于追踪硝酸盐污染来源和氮转化过程中的更多细节。同时,多种稳定同位素模型也被用于硝酸盐来源的定量计算。
2 稳定同位素在水体硝酸盐污染源解析中的影响因素
2.1 同位素分馏
同位素分馏是指因同位素中子数的差异使其质量与原子间结合力不同,导致生物地球化学循环过程中扩散和反应速率的差异,即一种元素的同位素以不同比例在不同物相中分配。生物体内的新陈代谢反应和自然界的物理化学过程均会造成同位素分馏[24]。水体中硝酸盐来源及氮转化机制和同位素分馏如图1 所示。同位素分馏是利用氮、氧稳定同位素识别水体中硝酸盐污染来源和去向的关键因素,不同来源的δ15N-和δ18O-主要受氮在迁移转化过程中同位素分馏的影响[32]。同位素分馏主要有同位素交换反应和动力学过程2 个原因,其中同位素交换反应可以看作是动力学过程的一部分。稳定同位素受到动力学同位素分馏作用,轻同位素优先参与反应,使得剩余底物中重同位素逐渐富集[33]。同位素分馏系数(α)表示同位素分馏的程度,可以通过式(2)计算得出。同位素富集因子(ε)反映2 种物质之间同位素相对富集或亏损的程度,可以通过式(3)计算得出。
式中:α为同位素分馏系数,α越大同位素分馏程度越大;K为变换过程中的速率常数;ε为同位素富集因子,‰。
水体中发生的生化反应可导致不同程度的氮氧同位素分馏,改变δ15N-和δ18O-,从而影响对硝酸盐来源的判断[34]。在整个氮循环过程中,硝化、反硝化和同化作用中的氮同位素α范围分别为-29‰~-12‰、-40‰~-5‰、-27‰~1‰[32],这表明α在不同氮转化过程中存在显著差异。因此,在与硝酸盐相关的氮迁移转化过程中,同位素分馏对δ15N-和δ18O-的影响成为限制准确识别硝酸盐污染来源研究的难题之一。相比氮同位素分馏,氧同位素分馏对于区分除大气沉降外其他来源的影响很小[10],所以本研究主要探讨氮同位素分馏的影响。改变水体δ15N-的主要生化反应过程包括土壤、粪肥和污水中的硝化作用,厌氧环境中的反硝化作用以及光合作用中的同化作用[35]。目前在水体硝酸盐源解析研究中,有关硝化和反硝化作用对同位素分馏影响的讨论较多,而厌氧氨氧化和硝酸盐异化还原为铵(NH4+)等反应过程中的分馏机制尚不清楚[36],且大部分研究侧重于对比不同时空变化下硝酸盐污染源的差异,忽略了不同时空变化对同位素分馏和δ15N-的影响,通过解析氮转化在不同时空变化下对δ15N-的影响将有助于准确识别硝酸盐污染来源。
2.2 氮转化中δ15N-NO3-的时间差异性
硝化作用是微生物将氨氧化成亚硝酸盐、硝酸盐的过程。Huang 等[37]研究发现水体中硝酸盐主要来源于春季和夏季的硝化作用,而外部贡献(如大气沉降)对秋冬季的同位素组成影响较大;Ji 等[38]研究也得出硝化过程在农业活动密集的雨季和暖季对水体硝酸盐贡献更为显著的结论。相比春夏季,秋冬季水体呈低温、低流量的特征,生物转化较弱,外源污染加重,所以硝化作用在春夏季比秋冬季对水体中δ15N-和δ18O-的影响更大。因此,在研究外部来源对水体中硝酸盐的贡献时,冬季采样有助于减小水体自身硝化作用对源解析结果的影响。
微生物反硝化作用是导致δ15N-和δ18O-变化的另一个过程,确定反硝化作用的发生是判断硝酸盐污染来源的重要前提[39]。在反硝化过程中,硝酸盐通过反硝化细菌依次转化为亚硝酸盐、一氧化氮和一氧化二氮,最终被还原为气态氮。Wong等[40]在澳大利亚流域研究中发现反硝化作用在雨季比旱季表现得更为活跃,对水体δ15N-和δ18O-的影响更大;相反,Yi 等[41]研究结果表明,相对于雨季,反硝化作用在旱季对水体δ15N-和δ18O-的影响更大。可见,反硝化作用对水体δ15N-和δ18O-的影响在相同季节下并不一致。
2.3 氮转化中δ15N-NO3-的空间差异性
理论上水体NO3-中的氧分子大约有1/3 来自空气氧,2/3 来自环境水,通过对比硝化作用产生硝酸盐δ18O 的理论值和实测值可以判断水体中是否因硝化作用产生硝酸盐[42]。Zhang 等[43]通过该方法得出硝化作用在研究区域氮转化过程中对δ15N-NO3-的影响最大;Yang 等[44]研究得出重庆市某郊区水体中硝酸盐主要通过硝化作用产生。微生物反硝化作用是水体中导致残留硝酸盐重同位素积累的重要自净化过程,将提高水体中δ15N-和δ18O-,且δ15N-和δ18O-的比值为1.3~2.1[45]。Zhang等[43]在滹沱河冲积扇区研究发现,大部分地表水水样δ15N-和δ18O-的比值在旱季高于1.3~2.1,在雨季低于1.3~2.1,得出反硝化作用对研究区域内硝酸盐同位素组成无显著影响。Yang 等[44]在解析重庆城市区域硝酸盐来源时,测得δ15N-和δ18O-的比值为1.8,表明在城市厌氧管道流中有反硝化作用发生。另有一些研究在解析硝酸盐污染源时重点对比了时空差异下水体中δ15N-和δ18O-的差异,如Zhao 等[35]对漓江水样硝酸盐同位素数据进行分析,得出δ15N-具有雨季低旱季高的变化特征,而δ18O-并无明显的季节变化特征,且二者空间变化均不大;Ye 等[46]对不同土地利用区流域中无机氮的来源和转化机制进行研究得出,δ15N-存在明显的季节和空间差异,农村地区的δ15N-雨季高于旱季,而城市地区则相反,且农村地区δ15N-均低于城市地区。
除了硝化和反硝化过程等生物反应过程,也有研究表明当硝酸盐浓度较高时,水生植物吸收和矿化作用中的分馏效应会导致硝酸盐同位素略有富集;土壤中的阴离子交换位点也会不断地保留和释放硝酸盐,从而引起氧氮同位素的一小部分分离[47]。相比硝化和反硝化作用,硝酸盐在水生植物吸收和矿化作用过程中发生的同位素交换反应对于同位素分馏的影响较小,但对硝酸盐在水体中迁移转化的判断依然有影响。
根据GB/T50801.2013中规定地源热泵系统能效的测试时要考虑到热源侧流量,而在深一步的探究时发现,地下水热泵系统在实际的工作中,当机组功率一定时,热源侧流量与热源侧的进出水温度是一一对应的,所以在构建该模型时不考虑热源侧流量。同时,考虑到天气变化可能会导致室外温度对系统的EER产生一定影响,所以将室外温度也作为输入参数之一[4]。
3 稳定同位素在硝酸盐污染源解析中的发展与应用
3.1 稳定同位素在硝酸盐污染源解析中的研究热点
同位素技术在硝酸盐污染源解析方面的研究已有40 多年的历史。研究初期受技术限制,学者们只能通过与几种潜在硝酸盐来源的氮同位素(δ15N)进行比较,定性确定水体中硝酸盐污染的主要来源。虽然不同硝酸盐来源的δ15N 不同,但其范围仍存在重叠。此外,硝酸盐来源广泛且相互间混合过程复杂,硝化反硝化等氮相关生物地球化学循环都会改变δ15N-,仅用δ15N 来确定硝酸盐的来源和迁移转化规律的应用较为有限。随着研究方法不断进步,氧同位素(δ18O)开始应用于源解析,不同硝酸盐来源的δ18O-NO3-范围不同,可为硝酸盐来源的识别提供更多信息。氮氧双同位素方法已广泛用于定性识别和追踪水体中的硝酸盐来源及其迁移转化过程[48-50]。采用Web of Science 引文数据库,以nitrate sources* and stable isotope* and water* or river*作为检索主题词,以Environmental Science or Engineering Environmental or Water Resources 为检索精炼类别,检索时间跨度为2011—2021年,共查到6 430 篇相关文献。采用VOSviewer 对以上检索的文献关键词进行共现性分析(图2),得出近10年与水体硝酸盐污染来源相关的热点研究主要包括稳定同位素在地下水和地表水硝酸盐污染源解析中的应用、硝酸盐在水体中的迁移转化特征和土地利用类型对源解析结果的影响等。其中,稳定同位素在水体硝酸盐污染源解析中的应用主要集中在对地下水的研究,硝酸盐在水体中的迁移转化特征主要以硝化与反硝化作用对硝酸盐浓度的影响研究为主,对比不同土地利用类型下的硝酸盐污染来源也是硝酸盐源解析中常见的研究方法,这为不同类型水体硝酸盐污染治理提供了针对性的科学依据。

图2 2011—2021年稳定同位素技术识别水体中硝酸盐污染来源相关文献关键词共现聚类分析Fig.2 Co-occurrence cluster analysis of keywords related to the identification of sources of nitrate pollution in water bodies using stable isotope techniques from 2011 to 2021
3.2 稳定同位素在硝酸盐污染源解析中的定性研究
3.2.1 双同位素技术
双同位素技术即利用不同硝酸盐来源中δ15N-和δ18O-差异来识别水体中硝酸盐来源。Kohl 等[19]在1971年调查了美国伊利诺伊州桑加蒙河排水系统中硝酸盐的来源,这是首次利用氮同位素确定硝酸盐污染来源的研究。但由于不同硝酸盐潜在来源的δ15N-范围部分重叠,使其难以准确区分不同硝酸盐潜在来源[10]。随着20 世纪80年代同位素分析技术的进步,开始有学者同时使用δ15N-和δ18O-识别硝酸盐污染来源[51-52]。δ18O-可以很好地区分大气沉降和其他硝酸盐污染来源,从而弥补了利用氮同位素溯源的不足。通常认为水体中硝酸盐有4 种来源:大气沉降、土壤氮、化学肥料和粪污(粪便和污水通常归为一类)[10]。大气沉降源是由闪电、化石燃料燃烧产生的氮氧化物作为硝化/反硝化的副产物,被大气中的光化学自由基氧化成硝酸盐而形成;土壤、粪肥和污水中的氨(NH3)发生硝化作用是水体中硝酸盐污染的主要来源;化学肥料是硝酸盐的另一个主要来源,它既直接来源于肥料中所含的硝酸盐,也来源于施肥后土壤中NH3发生的硝化作用[27]。这4 种来源的δ15N-和δ18O-范围在不同研究中有所差异,表1 描述了文献中对不同硝酸盐来源δ15N-和δ18O-范围的报道,大部分文献采用在Xue 等[10]研究基础上修正后的δ15N-和δ18O-范围,部分文献采用在Kendall 等[53]研究基础上修正后的δ15N-和δ18O-范围[54-55],不同文献中对相同硝酸盐来源δ15N-和δ18O-范围的描述有2‰~35‰的差距,这可能与样品采集、预处理和检测方法以及环境背景差异有关[56-57]。
表1 定性研究中不同硝酸盐来源δ15N-NO3-和δ18O-NO3-范围Table 1 Range of δ15N- and δ18O- values from different nitrate sources in qualitative research

表1 定性研究中不同硝酸盐来源δ15N-NO3-和δ18O-NO3-范围Table 1 Range of δ15N- and δ18O- values from different nitrate sources in qualitative research
硝酸盐来源δ15N-NO-3/‰δ18O-NO-3/‰文献来源大气沉降-13~1325~75[31,35,37,58-60]-5~525~75[56]-15~1560~98[57]土壤氮0~8-10~10[31,35,37,58-60]3~8-5~15[56]0~8-10~10[57]无机肥料-6~617~25[31, 35, 37, 58-60]-4~4-5~15[56]-4~417~25[57]粪便和污水4~25-5~10[31, 35, 37, 58-60]8~25-5~15[56]5~20-5~15[57]
δ18O-可帮助识别单独使用δ15N-无法区分的硝酸盐来源,双同位素方法可以提高源识别的准确性。但如果在氮转化过程中发生了复杂的分馏过程(如硝化、反硝化或同化作用等),同位素组成可能会被修改[10,34],所以有必要在硝酸盐源解析前掌握其迁移转化规律。此外,人类粪便污染对人类的风险高于动物粪便污染[10]。利用氮氧同位素技术将粪便和污水划分为同一种硝酸盐来源对于准确溯源仍具有局限性,研究人员已尝试引入其他方法来改善这种情况[61-64]。
3.2.2 多同位素技术
多同位素法是利用δ15N-和δ18O-以外的额外同位素,如D-H2O、18O-H2O、δ17O-和δ11B 等来追踪硝酸盐的来源和转化,弥补了双同位素法的不足。
δ15N-范围的重叠使得大气源识别较为困难,由于大气臭氧(O3)在形成过程中会出现非质量分馏(MIF),MIF 的程度可以用Δ 来表示:
大气硝酸盐的Δ17O 较高,不受反硝化、同化等生物地球化学过程的影响,所以Δ17O 可以作为大气沉降在地表水中的示踪剂来区分大气沉降和其他陆源[52]。Hundey 等[61]利用δ15N 和Δ17O 得出Uinta 山脉湖泊水体中至少70%的硝酸盐由大气输送。Liu等[66]首次将三重硝酸盐同位素(δ15N-、δ18O-NO3-和Δ17O-)应用于大型河流,并建立三重同位素混合模型来确定大气氮沉降对河水的贡献情况,结果表明大气沉降对河流硝酸盐贡献率为0~7%,而粪肥、污水和化肥对黄河中下游河流硝酸盐的贡献也相当。
硼(B)是硝酸盐来源在水中固有的共迁移示踪剂,不受迁移和反硝化作用的影响[10]。δ11B 随污染源的变化而变化,据相关研究,粪肥δ11B 为6.9‰~42.1‰,化肥δ11B 为8‰~17‰,污水δ11B 为-7.7‰~12.9‰,雨水δ11B 为13‰~48‰[67-69]。Xue 等[70]基于δ15N、δ18O 和δ11B 结果识别了地表水中硝酸盐来源。但矿物沉淀和黏土矿物的吸附与解吸作用仍会影响δ11B,一定程度上也限制了硼同位素在识别硝酸盐来源应用中的适用性[71]。
多同位素可以为水体中硝酸盐污染源解析提供更多信息,借助D-H2O 和18O-H2O 研究水体的混合、供应和蒸发为了解硝酸盐的来源提供了补充,δ17O-和δ11B 以不受反硝化等作用影响的特征体现出额外优势。多同位素的应用需从实际问题出发,根据污染源的构成和环境特征选择与之相匹配的稳定同位素技术。
3.2.3 稳定同位素联合其他技术
某些离子、分子和微生物可提供与氮相关生物地球化学循环过程中硝酸盐迁移转化的额外信息。Yuan 等[62]由同位素解析模型得出水体硝酸盐污染源包括粪肥、污水和土壤氮,而对理化参数进行主成分分析得出水体硝酸盐污染源包括粪肥、污水、氮肥、铵肥和土壤氮。Bu 等[63]通过分析河流水体中氮与其他理化参数之间的关系表明,在不同采样周期内,河流氮污染主要由硝化和反硝化过程驱动,而不是由季节性生物需求驱动。Ren 等[64]通过对比分析地表水和地下水的pH、NH3-N 和COD,得出再生水在入渗过程中的生化反应可能在河水补充地下水时起作用,研究区地下水中NO3-的最大贡献者是污水处理厂的入渗排放。因此,水体理化参数为解释硝酸盐在水体中的迁移转化和来源贡献补充了信息。
粪便和污水中某些特定的微生物或化学物质使它们有别于其他来源,例如人类产生的化学标记物,包括病原体、粪便指示菌、粪便甾醇、药物和食品添加剂等;与污水系统相关的化学标记物,如洗涤剂和咖啡因等[72-74]。所以化学标记物可以在一定程度上解决稳定同位素技术在硝酸盐源解析中无法区分粪便和污水来源的局限性。为了进一步区分人类和动物粪便,未来有必要对动物相关化学标记物进行研究。
3.3 同位素模型在硝酸盐污染源解析中的定量研究
在早期研究中,通常采用基于质量平衡的线性混合模型对硝酸盐来源进行量化。根据标准双同位素三元线性混合模型,可确定不超过3 个源的贡献:
式中:δ15N 和δ18O 分别为混合物的硝酸盐氮、氧同位素组成,‰;fi为污染源i占混合物的比例,i取1、2、3;δ15Ni和δ18Oi分别为污染源i的硝酸盐氮、氧同位素组成。
线性混合模型在解析少量硝酸盐来源的应用中具有一定优势,Yang 等[75]通过线性混合模型成功得出基于盐度的各硝酸盐来源贡献率,但当硝酸盐来源超过3 个,线性混合模型会变得不再适用而使得解析结果存在不确定性[76]。表2 总结了应用于硝酸盐来源解析的各种同位素模型优缺点,其中IsoError模型可以包含可变性,但是不适用3 个以上源的情况[77];IsoSource 模型可以用来处理多个源[78],如徐璐等[56]利用IsoSource 模型定量分析得出研究区域地下水中硝酸盐来源贡献率,但该模型无法考虑不确定性和变异系数。Moore 等[79]提出了MixSIR 模型,该模型使用贝叶斯框架来确定混合物中不同来源贡献的概率分布。贝叶斯统计可以整合先验信息和不确定性来源,为数据解释提供了强大的工具[80]。
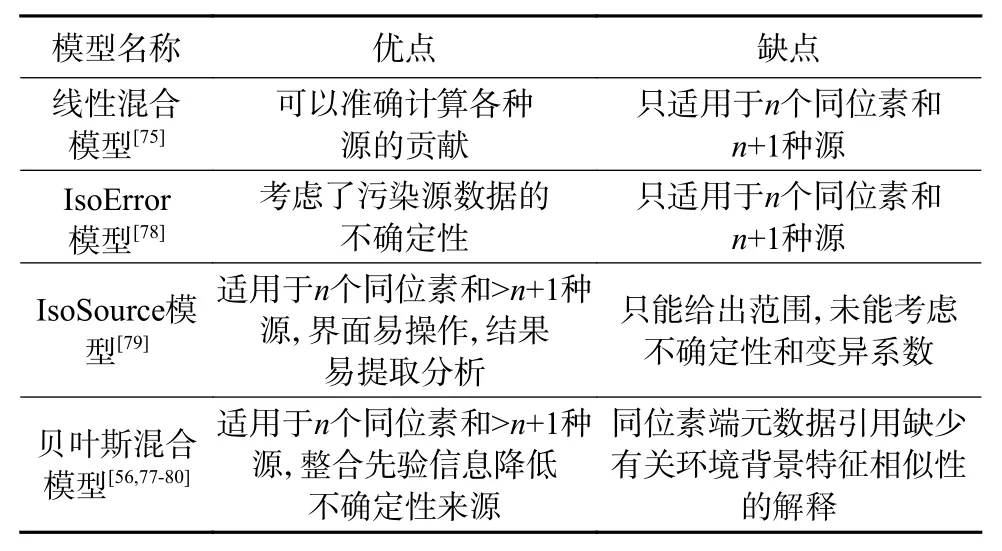
表2 各模型优缺点比较Table 2 Comparison of advantages and disadvantages of each model
Parnell 等[76]基于R 统计软件开发了SIAR 模型,其将马尔可夫链蒙特卡罗抽样与贝叶斯更新相结合,建立混合分数的后验分布,公式如下:
式中:pi为模型估计的源i的比例;qji为同位素j在源i中的丰度;Sji为源i中同位素j的丰度,呈正态分布,平均值为µji,方差为ω2ji。cji为同位素j在源i中的营养富集因子,呈正态分布,平均值为λji,方差为τ2ji。εji为残差,呈正态分布,均值为0,方差为σ2ji,σ2ji由模型估计得到。
目前SIAR 模型在地表水和地下水硝酸盐源识别方面有许多应用[81-84]。有研究分别采用IsoSource、IsoError 和SIAR 模型分析水体中硝酸盐来源,结果表明污染源和受纳水体较大的δ15N-NO3-和δ18ONO3-范围使得IsoSource 和IsoError 模型结果不确定性较高,而SIAR 模型由于考虑到同位素空间差异性使结果的不确定性最低[85]。尽管如此,不同地区应用SIAR 模型解析硝酸盐污染源时(表3),输入端的4 个潜在来源的δ15N-和δ18O-有很大差异,而且由于研究过程中面临的采样检测成本等问题,只有少数研究采用实测值[84],大部分研究中所用均值和标准差主要参考已有文献,忽略了时空变化等环境条件对δ15N-和δ18O-的影响,这使得SIAR 模型在有关同位素分馏问题中的不确定性依旧不可避免。因此,在利用氮氧同位素模型解析硝酸盐污染来源时,有必要调查研究区域内不同时空变化特征下的环境背景值,即本土硝酸盐输入端4 个潜在来源的δ15N-NO3-和δ18O-。通过对研究区域内环境背景值进行整理归纳,形成属于本地的硝酸盐端元数据库对未来污染溯源研究意义重大[55]。

表3 定量研究中SIAR 模型所使用的端元同位素组成Table 3 Endmember isotope values used by SIAR models in quantitative studies‰
4 结语
稳定同位素为水体硝酸盐污染源从定性到定量解析研究提供了新方法,并得到广泛应用。然而,在定性和定量研究中,很少考虑不同环境条件下参与硝酸盐迁移转化的相关微生物对同位素分馏的影响。时空差异性间接影响着水样和潜在来源的δ15N-NO3-和δ18O-,不同环境背景条件下的相关生化反应对硝酸盐迁移转化和同位素分馏的影响还需展开深入研究。未来有必要通过分析微生物参与氮转化的相关基因来认识硝酸盐在迁移和转化过程中的足迹,为水体污染源控制提供科学依据;土壤层或者地下水硝酸盐的输入应成为地表水体硝酸盐污染源解析的重点考察端元;通过对大量不同时期样品的采集和分析,结合机器学习发展出适应研究区域地理气候特征的稳定同位素模型,从而更加准确地解析水体中硝酸盐污染来源。

