富马酸替诺福韦二吡呋酯片联合胸腺法新治疗慢性乙型肝炎的效果
李秋霞 ,贾超,白艳,陈佩
(郑州市第一人民医院 a.全科医学科;b.消化内科 河南 郑州 450000)
慢性乙型肝炎(chronic hepatitis B,CHB)为临床常见的病毒性感染疾病,其发病与环境、饮食、病毒感染、免疫功能低等因素明显相关,患者常出现不同程度的无力、恶心、腹胀、肝区疼痛等症状[1-2]。CHB主要经血液、破损皮肤黏膜及性接触传播,具有发病率高、潜伏期长的特点,可导致人体免疫功能下降,若不及时治疗,可进展为肝硬化或肝癌,严重威胁患者生命安全[3]。因此,需早期开展治疗以控制疾病进展。富马酸替诺福韦二吡呋酯片常用于对抗病毒感染,可抑制乙肝病毒复制,防止病毒在人体内大量繁殖,但该药物无法彻底清除病毒[4]。胸腺法新属于胸腺肽类药物,具有抗病毒和免疫调节的作用,能刺激外周血液免疫细胞,增强机体免疫力,提高抗病毒能力[5]。本研究选取98例CHB作为研究对象,探讨富马酸替诺福韦二吡呋酯片联合胸腺法新在CHB中的应用效果。
1 对象与方法
1.1 研究对象
本研究选取2021年1月至2022年9月郑州市第一人民医院98例CHB患者,按照随机数字表法分为单一组和联合组,各49例。单一组男27例,女22例;年龄19~65(39.52±9.18)岁;病程6~35(21.03±6.47)个月;体重指数19~27(23.06±2.07)kg·m-2。联合组男25例,女24例;年龄19~66(35.43±9.24)岁;病程5~35(20.96±6.51)个月;体重指数19~28(23.11±2.05)kg·m-2。两组患者一般资料均衡可比(P>0.05)。
1.2 选取标准
(1)纳入标准:①符合中华医学会肝病学分会制定的《慢性乙型肝炎治疗指南》[6]中的相关诊断标准;②伴有不同程度的无力、恶心、腹胀、肝区疼痛等症状;③近6个月未接受过免疫刺激因子、胸腺肽、免疫调节剂等抗病毒治疗;④无其他严重疾病;⑤乙型肝炎核心抗体、乙型肝炎表面抗原、乙型肝炎e抗原(hepatitis Be antigen,HBeAg)转阴率均呈阳性。(2)排除标准:①有药物滥用史;②伴有严重心肌梗死或心律失常;③长期接受雌激素或孕激素治疗;④对本研究药物过敏;⑤合并甲状腺功能障碍;⑥伴有其他肝炎病毒感染。
1.3 方法
单一组接受营养支持,口服富马酸替诺福韦二吡呋酯片(珠海联邦制药股份有限公司中山分公司,国药准字H20213059),每次300 mg,每日1次。持续治疗6个月。
联合组在单一组基础上接受胸腺法新(海南双成药业股份有限公司,国药准字H20030407)皮下注射,每次1.6 mg,每日1次,4 d后改为每周2次。持续治疗6个月。
1.4 疗效评估标准
显效:治疗6个月后,患者无力、恶心、腹胀、肝区疼痛等症状基本消失,肝功能恢复正常。缓解:治疗6个月后,患者无力、恶心、腹胀、肝区疼痛等症状有所改善,肝功能有所恢复。无效:治疗6个月后,未达显效和缓解。将显效、缓解计入总有效。
1.5 观察指标
(1)疗效。(2)载体转阴率。记录对比两组HBV-DNA、HBeAg转阴率。(3)肝功能。治疗前后天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、总胆红素(total bilirubin,TBIL)水平。具体操作如下:清晨抽取患者空腹状态下静脉血4 mL,放于抗凝管中抗凝,离心处理,设置离心机转速为3 000 r·min-1,离心10 min后取上层血清。采用AU2700全自动生化分析仪检测患者的ALT、AST、TBIL水平,试剂盒均由北京普利莱基因技术有限公司提供。(4)肝纤维化指标水平。记录对比两组治疗前后Ⅳ型胶原蛋白(type Ⅳ collagen,C-Ⅳ)、透明质酸(hyaluronic acid,HA)、Ⅲ型前胶原蛋白(type Ⅲ procollagen,PCⅢ)水平。具体操作如下:清晨抽取所有患者空腹状态下静脉血4 mL,离心后取上层血清。采用放射免疫法检测C-Ⅳ、HA、PCⅢ水平,试剂盒均由上海白益生物科技有限公司提供。(5)不良反应发生率。
1.6 统计学方法
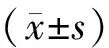
2 结果
2.1 疗效
联合组总有效率高于单一组(P<0.05)。见表1。

表1 两组疗效比较(n,%)
2.2 载体转阴情况
联合组HBV-DNA转阴率、HBeAg转阴率高于单一组(P<0.05)。见表2。

表2 两组载体转阴率比较[n(%)]
2.3 肝功能
两组AST、ALT、TBIL水平差异无统计学意义(P>0.05)。治疗后,联合组AST、ALT、TBIL水平低于单一组(P<0.05)。见表3。
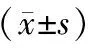
表3 两组肝功能比较
2.4 肝纤维化指标
两组治疗前C-Ⅳ、HA、PCⅢ水平差异无统计学意义(P>0.05)。治疗后,联合组C-Ⅳ、HA、PCⅢ水平低于单一组(P<0.05)。见表4。

表4 两组肝纤维化指标比较
2.5 不良反应发生率
联合组不良反应发生率与单一组对比,差异无统计学意义(P>0.05)。见表5。

表5 两组不良反应发生率比较(n,%)
3 讨论
CHB是由乙型肝炎病毒持续性感染引发的肝脏慢性疾病,具有病程长、难根治、易反复等特点,乙型肝炎病毒抵抗力强,能通过血液制品、母婴等途径进行传播,导致病毒性肝炎[7-8]。CHB患者早期症状轻微,仅表现为头晕、乏力、食欲不振等症状,如不及时治疗,可引发蜘蛛痣、肝掌、肝脾肿大等症状,病情进展至失代偿期,还会造成肝功能损伤及肝纤维化,严重影响患者生活质量[9-10]。临床对抗CHB常采用抗病毒、抗纤维化、保护肝脏、增强机体免疫功能等手段,虽能在一定程度上改善肝功能损伤,控制疾病进展,但远期疗效不理想。
富马酸替诺福韦二吡呋酯片能经过二酯水解转变为替诺福韦,再通过细胞酶的磷酸化形成二磷酸替诺福韦,进而抑制乙型肝炎病毒反转录酶和艾滋病病毒反转录酶活性,可用于治疗CHB[11-12]。胸腺法新属于一种免疫增强药物,可促进淋巴细胞成熟、γ-干扰素、白细胞介素等细胞因子分泌,增强机体抗病毒、抗细菌、抗肿瘤的免疫活性,起到对抗病毒感染的效果[13-14]。本研究结果显示,联合组总有效率、HBV-DNA转阴率和HBeAg转阴率高于单一组。分析原因,富马酸替诺福韦二吡呋酯片的水溶性和抗病毒功效较强,能快速抑制病毒聚合酶合成,与脱氧核糖底物竞争性结合,提升机体抗病毒能力。该药物口服后,能被人体快速吸收和降解,且不良反应小,治疗安全性较高,有利于抑制病毒链延长,防止病毒在人体中大量繁殖。但单独使用该药物,难以完全清除乙肝病毒,需与其他药物联合使用。胸腺法新是一种细胞免疫增强药物,可促进细胞毒性T细胞及自然杀伤细胞成熟、分化,有效抑制HBV-DNA在人体中复制,从而提升肝炎病毒清除率,与富马酸替诺福韦二吡呋酯片联合使用能起到协同作用,促进HBV-DNA、HBeAg转阴,改善患者病情。
ALT在肝细胞中的水平最高,是评判肝功能的重要指标,肝功能损伤及破裂会导致ALT升高,该指标水平升高往往预示着肝功能异常。AST主要分布在心肌和肝组织内,可反映肝疾病进展,正常情况下,人体血清中的AST水平较低,但当肝细胞出现损伤时,细胞膜通透性会进一步增加,从而使胞腔内的AST释放入血,该指标水平上升说明肝功能降低。TBIL是直接胆红素和间接胆红素的总和,肝脏在胆红素代谢中具有摄取、结合和排泄功能,若肝功能障碍,可引起TBIL升高,同时该指标也是临床上判断黄疸症状的重要依据。本研究结果显示,治疗后,联合组AST、ALT、TBIL水平较单一组低,充分佐证二者联合能改善患者肝功能。富马酸替诺福韦二吡呋酯片对病毒DNA的抑制作用较强,能有效抑制HBV-DNA复制,阻断肝细胞间各种病毒相互传播的途径,降低肝细胞膜上靶抗原的表达,减轻肝脏损伤,从而改善患者肝功能。胸腺法新能促进T淋巴细胞成熟,快速清除人体中的肝炎病毒,抑制病毒蔓延,与富马酸替诺福韦二吡呋酯片联合使用能彻底清除乙型肝炎病毒,改善患者肝功能。C-Ⅳ是构成基底膜的主要成分,能反映基底膜胶原的更新率,正常情况下在肝脏中的水平较低,C-Ⅳ水平增加可反映肝纤维化过程,常作为肝纤维化的早期监测指标。HA广泛分布于结缔组织、上皮组织和神经组织中,并能在肝脏内形成肝脏基质,填充在肝细胞周围,该指标水平能反映肝细胞功能及肝纤维化,预测肝硬化,当出现乙型肝炎病毒感染时,肝组织纤维化变性严重,常导致HA水平升高。此外,该水平与肝组织病理变化程度存在明显关联性,肝组织损伤会导致肝内皮细胞数量大幅减少,代谢功能下降,引发HA水平升高。PCⅢ是由3个相同的肽链组成的蛋白质,能反映人体胶原代谢情况及组织纤维增生情况,该指标水平偏高提示肝脏存在炎症或肝纤维化趋势。研究数据显示,治疗后,联合组C-Ⅳ、HA、PCⅢ水平较单一组低,提示二者联合能改善患者肝纤维化指标。这一结果与王佩龙等[15]的研究结果一致。富马酸替诺福韦二吡呋酯片与胸腺法新联合能提升机体免疫力,有效抑制肝细胞增生,防止胶原蛋白过度表达,降低病毒复制和繁殖速度,最大程度上减轻肝细胞炎症反应及肝纤维化,延缓疾病进展,避免肝脏失代偿、肝硬化等不良事件的发生。实验结果显示,联合组不良反应发生率与单一组对比差异无统计学意义,说明二者联合治疗安全性较高。
4 结论
富马酸替诺福韦二吡呋酯片联合胸腺法新治疗CHB效果确切,能促进HBV-DNA、HBeAg转阴,改善患者肝功能和肝纤维化指标,且治疗安全性较高。

