肉豆蔻化学成分和药理作用研究进展及其质量标志物(Q-Marker)预测分析
刘润润,孙爱清,于小钧,贺梦媛,谢和兵,高 鹏,丛竹凤, *
肉豆蔻化学成分和药理作用研究进展及其质量标志物(Q-Marker)预测分析
刘润润1,孙爱清2,于小钧1,贺梦媛1,谢和兵3,高 鹏4*,丛竹凤1, 2*
1. 山东中医药大学药学院,山东 济南 250355 2. 山东第一医科大学附属肿瘤医院,山东 济南 250117 3. 西藏神猴药业有限责任公司,西藏 日喀则 330006 4.山东中医药大学药物研究院,山东 济南 250355
肉豆蔻是常用药食同源中药,具有温中行气、涩肠止泻的功效,主要包括木脂素类、挥发油类和多酚类等化学成分,具有调节消化系统、抗癌、抗炎镇痛、抗菌、抗氧化等药理作用。通过对肉豆蔻化学成分、药理作用、毒性和临床应用进行综述,根据中药质量标志物(quality marker,Q-Marker)理念,从植物亲缘、采收时期和炮制方法、药效、药性、配伍、化学成分可测性等方面对肉豆蔻的Q-Marker进行预测分析,初步预测去氢二异丁香酚、肉豆蔻醚、安五脂素、甲氧基丁香酚、榄香素、丁香酚和α-蒎烯等为其可能的Q-Marker,为肉豆蔻质量评价和药品研发提供参考。
肉豆蔻;质量标志物;去氢二异丁香酚;肉豆蔻醚;安五脂素;甲氧基丁香酚;榄香素;丁香酚;α-蒎烯
肉豆蔻是肉豆蔻科植物肉豆蔻Houtt的干燥种仁,始载于《雷公炮炙论》[1],性辛、温,归脾、胃、大肠经。肉豆蔻具温中行气、涩肠止泻之功效,可用于脾胃虚寒、久泻不止、脘腹胀痛、食少呕吐[2]。近年来,大量研究者对肉豆蔻化学成分与临床应用进行研究,但现行质量控制指标仅为挥发油和去氢二异丁香酚,且挥发油为含量测定项,未明确化学成分,质量控制与评价仍有待商榷。为确保中药质优效佳,刘昌孝院士[3-6]针对中药生物属性、制造过程及配伍理论等自身医药体系的特点,提出中药质量标志物(quality marker,Q-Marker)的概念,有利于建立中药全过程质量评价体系,确保其规范化和标准化。本文对肉豆蔻的化学成分、药理作用、毒性及临床应用进行综述,对其Q-Marker进行预测分析,为肉豆蔻的质量控制和品质评价提供参考。
1 化学成分
肉豆蔻含有多种化学成分,包括木脂素、挥发油、多酚类和其他类成分,目前研究集中于木脂素类和挥发油类成分。
1.1 木脂素
肉豆蔻中木脂素结构类型多样,主要有二苄基丁烷类(1~9)、芳基萘类(10~12)、四氢呋喃类(13~27)、苯骈呋喃类(28~45)和8--4型新木脂素类(46~58)、二芳基丙烷类(59~63)、非环丙醇新木脂素类(64)和其他类(65~69),其中去氢二异丁香酚(32)[7]具有多种药理活性。化合物信息及结构见表1和图1。
1.2 挥发油
挥发油是肉豆蔻的主要生物活性成分,以苯丙素类(70~94)、单萜类(95~151)和倍半萜类(152~176)为主[27],其中肉豆蔻醚(81)约占挥发油总量的12.45%,为主要成分[28]。脂肪酸酯类(177~192)、脂肪酸类(193~201)、烷烃类(202~214)及其他类(215~239)等,化合物信息及结构见表2和图2。
表1 肉豆蔻中木脂素类成分
Table 1 Lignans in Myristicae Semen
编号化合物文献编号化合物文献 1(8R,8′S)-7-(3,4-亚甲基二氧苯基)-8-甲基-8′-亚甲基二羟基–7′-(3′,4′-亚甲二氧基苯基)-丁醇 819甘密树皮素A14 20肉豆蔻素C114 2(8R,8′S)-7′-(3′,4′-亚甲基二氧苯基)-8,8′-二甲基-7-(3,4-二羟基苯基)-丁烷 821verrucosin14 22四氢呋喃愈创木酚B14 3消旋-甲基二氢愈创木酸 823肉豆蔻素B15 47-(4-羟基-3-甲氧基苯基)-7′-(3′,4′-亚甲基二氧基苯)-8,8′-木脂素-7-甲基醚 824肉豆蔻素A215 25(−)-(7S,7′R,8S,8′R)-4,4′-二羟基-3,5,3′-三甲氧基-7,7′-环氧木脂素16 5(8R,8′S)-7-(3,4-亚甲基二氧苯基)-8-甲基-8′-羟基甲基-7′-(3′,4′-亚甲基二甲基苯基)-丁醇 8 26肉豆蔻素B316 6肉豆蔻醇A 927肉豆蔻素B116 7桢楠素A 928(7R,8R)-7,8-二氢-7-(3,4-二羟基苯基)-3′-甲氧基-8-甲基-1′-(E-丙烯基)苯骈呋喃13 8安五脂素 9 9内消旋-二氢愈创木酸1029肉豆蔻酚A15 10(+)-myrisfragransin1130fragnasol A15 11(+)-二甲基吡喃肉豆蔻素1131fragnasol C15 12愈创木脂素1232去氢二异丁香酚17 13machilin F 9335′-甲氧基去氢二异丁香油酚17 14nectandrin B10342,3-二氢-7-甲氧基-3-甲基-2-[3,4-(亚甲基二氧基)-5-甲氧苯基]-5-丙烯基苯骈呋喃17 15(7S,8′R,7′R)-4,4′-二羟基-3,3′-二甲氧基-7′,9-环氧基苯胺13 16(7S,8S,7′R,8′S)-4,5′-二羟基-3,3′-二甲氧基-7,7′-环氧基木脂素1335利卡灵B17 36accuminatin18 17花叶松苷醇14377-甲氧基-3-甲基-5-(E)-丙烯基-2-(3,4,5-三甲氧基苯基)-2,3-二氢苯骈呋喃18 18日本楠脂素14

续表1
1.3 多酚类
肉豆蔻中的多酚类包括酚酸类(240~242)和黄酮类(243~248),已从中分离出邻苯二甲酸(240)[12]、原儿茶酸(242)[51]等化合物。具体化合物信息及结构见表3和图3。
1.4 其他类
除上述成分外,肉豆蔻还含有二苯基烷烃类(1,2)-1-(4-hydroxy-3-methoxyphenyl)-1,2- propanediol[13]、马拉巴酮B和C[52],甾体类化合物如β-谷甾醇[53],其他成分皮蝇磷[44]等。
2 药理作用
肉豆蔻不仅在消化系统疾病的治疗中发挥效用,还具有调节神经系统和心脑血管、降血糖、抗癌、抗炎镇痛等药理作用,活性成分主要为木脂素类、苯丙素类及挥发油类。
2.1 对消化系统的作用
肉豆蔻在消化系统疾病中主要发挥保肝护肠、抗胃溃疡及止泻等作用,活性成分为木脂素类和苯丙素类等,代表性成分为安五脂素(8)、nectandrin B(14)、甲氧基丁香酚(94)、肉豆蔻醚等,具体作用机制见图4。
2.1.1 保肝 肉豆蔻可治疗化学性肝损伤。肉豆蔻提取物及肉豆蔻木脂素(58)可通过上调过氧化物酶体增殖物激活受体α(peroxisome proliferator activated receptor α,PPARα)通路,减弱氧化应激,改善硫代乙酰胺引起的小鼠肝损伤[54]。肉豆蔻醇提物通过激活腺苷酸活化蛋白激酶α(adenosine monophosphate activated protein kinase α,AMPKα)磷酸化,抑制脂肪酸合成酶及调节元件结合蛋白的表达,从而减少体内外脂肪酸合成,缓解脂毒性大鼠肝细胞损伤[55]。Poorbagher等[56]发现肉豆蔻酚类化合物可降低-天门冬酰胺酶致肝毒性小鼠的肝酶活性、炎症反应,增强抗氧化活性,改善肝细胞崩解和空泡化等现象。安五脂素通过抑制c-Jun氨基末端蛋白激酶的磷酸化、细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)的活化,降低丙氨酸氨基转移酶和谷氨酸转移酶活性,减轻顺铂诱导的小鼠肝损伤[57]。nectandrin B可增强叔丁基过氧化氢诱导的肝损伤小鼠的ERK磷酸化水平,激活核因子E2相关因子2(nuclear factor E2 related factor 2,Nrf2)抗氧化通路,改善肝细胞氧化损伤[58]。甲氧基丁香酚通过抑制促肝纤维化基因mRNA和核因子-κB(nuclear factor-κB,NF-κB)信号通路表达,减缓四氯化碳诱导的小鼠肝损伤[59]。综上,肉豆蔻提取物、木脂素类和苯丙素类可通过抑制氧化应激、肝脏炎症、脂肪堆积及肝纤维化来保护肝脏。

图1 肉豆蔻中木脂素类成分化学结构
表2 肉豆蔻中挥发油类成分
Table 2 Classification of volatile oils in Myristicae Semen
编号化合物文献编号化合物文献 702-羟基-3-甲氧基-5-(2-丙烯基)苯酚12862,3-二氢-2-甲氧苯并呋喃32 713-(3,4-二甲氧基苯基)-1,2-丙二醇1287细辛醚33 72反式-3,4-二甲氧基肉桂酸1288异萎叶酚34 73(2R)-3-(5-methoxy-3,4-methylenedioxyphenyl)-1,2-propanediol1389异丁香酚34 90反式-o-甲基异丁香酚34 74(2R)-3-(3,4-methylenedioxyphenyl)-1,2-propanediol1391反式-异榄香脂素34 75(2R)-3-(3,4,5-三甲氧基苯基)-1,2-丙二醇16922-甲氧基-3-(2-丙烯基)-苯酚35 763-甲氧基-4,5-亚甲二氧基肉桂酸1693甲基胡椒酚36 77胡椒基丙酮2894甲氧基丁香酚37 78黄樟醚2995α-水芹烯28 79甲基丁香酚2996β-侧柏烯28 80反式甲基异丁香酚2997α-蒎烯29 81肉豆蔻醚2998β-蒎烯29 82榄香素29993-蒈烯29 83丁香酚29100松油烯-4-醇30 84胡椒醇30101香桧烯31 85异香兰素31102(+)-4-蒈烯31
续表2

编号化合物文献编号化合物文献 103邻伞花烃31144顺式-3-甲基-6-异丙基-2-环己烯-1-醇40 1044-甲基-1-异丙基-双环[3.1.0]-己烷双脱氢衍生物31145(+)-柠檬烯41 1462-茨醇41 105莰烯31147茴香脑41 106桉叶油素31148(S)-顺式-马鞭草烯醇41 107龙脑31149δ-樟脑41 108香橙醇31150马苄烯酮41 109芳樟醇32151薄荷-2-烯-1-醇(顺-对)42 110反式-对-薄荷烷-2-烯-1-醇32152β-檀香烯30 1112,6-二甲基-2,6-辛二烯32153β-榄香烯31 112γ-焦烯32154(−)-匙叶桉叶油烯醇31 113醋酸异胡薄荷醇33155愈创木醇32 114β-水芹烯34156荜澄茄苦素33 115对-聚伞花烃34157γ-杜松烯34 1168-羟基-对-伞花烃34158杜松烯34 1171-萜品烯醇34159反式-α-金合欢烯34 118β-萜品醇34160左旋匙叶桉叶油烯醇34 119小茴香烯34161反式-α-佛手柑油烯34 120反式-α-罗勒烯34162吉马烯D34 1211,3,8-对-薄荷三烯34163α-古巴烯37 122波斯菊萜34164α-荜澄茄烯38 1233-甲基莰尼醇34165α-蛇麻烯39 124反式-胡椒醇34166可巴烯40 125异麝香草酚34167β-荜澄茄苦素40 126对-薄荷烷-1,4-二烯-7-醇34168β-没药烯40 1274-亚甲基-1-(1-甲基乙基)-环己烯35169β-杜松烯40 128对-薄荷烷-1-烯-8-醇35170naphthalene,1,2,4a,5,6,8a-hexahydro-4,7-dimeth-yl-1-(1-methylethyl)41 129伪柠檬烯37 130bicyclo[2.2.1]hept-2-ene,1,7,7-trimethyl38171naphthalene,1,2,3,4,4a,7-hexahydro-1,6-dimeth-yl-4-(1-methylethyl)41 131右旋桃金娘烯醇38 132α-侧柏烯38172去氢白菖烯41 1334-松油醇39173氧化石竹烯41 134(E)-异柠檬烯39174δ-荜澄茄烯43 1351,4-桉叶素39175顺-丁香烯43 1361,8-桉叶素39176(Z,E)-α-金合欢烯44 137香茅醇39177香草酸16 138葑醇39178肉豆蔻酸27 139松香芹醇39179肉豆蔻酸甲酯28 140α-松油烯40180α-萜品醇乙酯31 141柠檬烯40181顺式香叶醇乙酸酯31 142反式-1-甲基-4-异丙基-2-环己烯-1-醇401822-氨基苯甲酸-3,7-二甲基-1,6-辛二烯-3-醇酯32 143顺式-1-甲基-4-异丙基-2-环己烯-1-醇40183龙脑乙酯34
续表2
2.1.2 护肠 肉豆蔻护肠功能主要表现为缓解肠道痉挛和保护肠黏膜。Prashant等[60]发现肉豆蔻水提物可阻断乙酰胆碱受体和组胺受体松弛豚鼠的离体回肠,缓解肠痉挛。肉豆蔻挥发油通过抑制肠组织白细胞介素-8(interleukin-8,IL-8)和NF-κB p65蛋白表达,降低炎症水平,从而改善放射性肠炎小鼠的肠黏膜损伤[61]。肉豆蔻醚可上调直肠灌注乙酸诱导的结肠炎大鼠的Nrf2及血红素加氧酶-1的水平,降低结肠髓过氧化物酶活性及mRNA表达,通过抗氧化、抗炎活性治疗溃疡性结肠炎及其黏膜损伤[62]。综上,肉豆蔻挥发油及苯丙素类成分通过调控神经递质、炎症因子和抗氧化酶的活性保护肠道。
2.1.3 抗胃溃疡 肉豆蔻中马拉巴酮B和马拉巴酮C可通过上调黏蛋白含量,提高前列腺素E2水平,增加表皮细胞生长因子受体和环氧合酶表达,促进吲哚美辛诱导的胃溃疡小鼠伤口愈合[52]。Sattar等[63]研究推测肉豆蔻中改善乙醇致胃溃疡小鼠的主要活性成分为黄酮类化合物,其具体机制仍需进一步研究。以上表明肉豆蔻通过增加血管愈合相关激素和抗氧化改善胃部损伤。
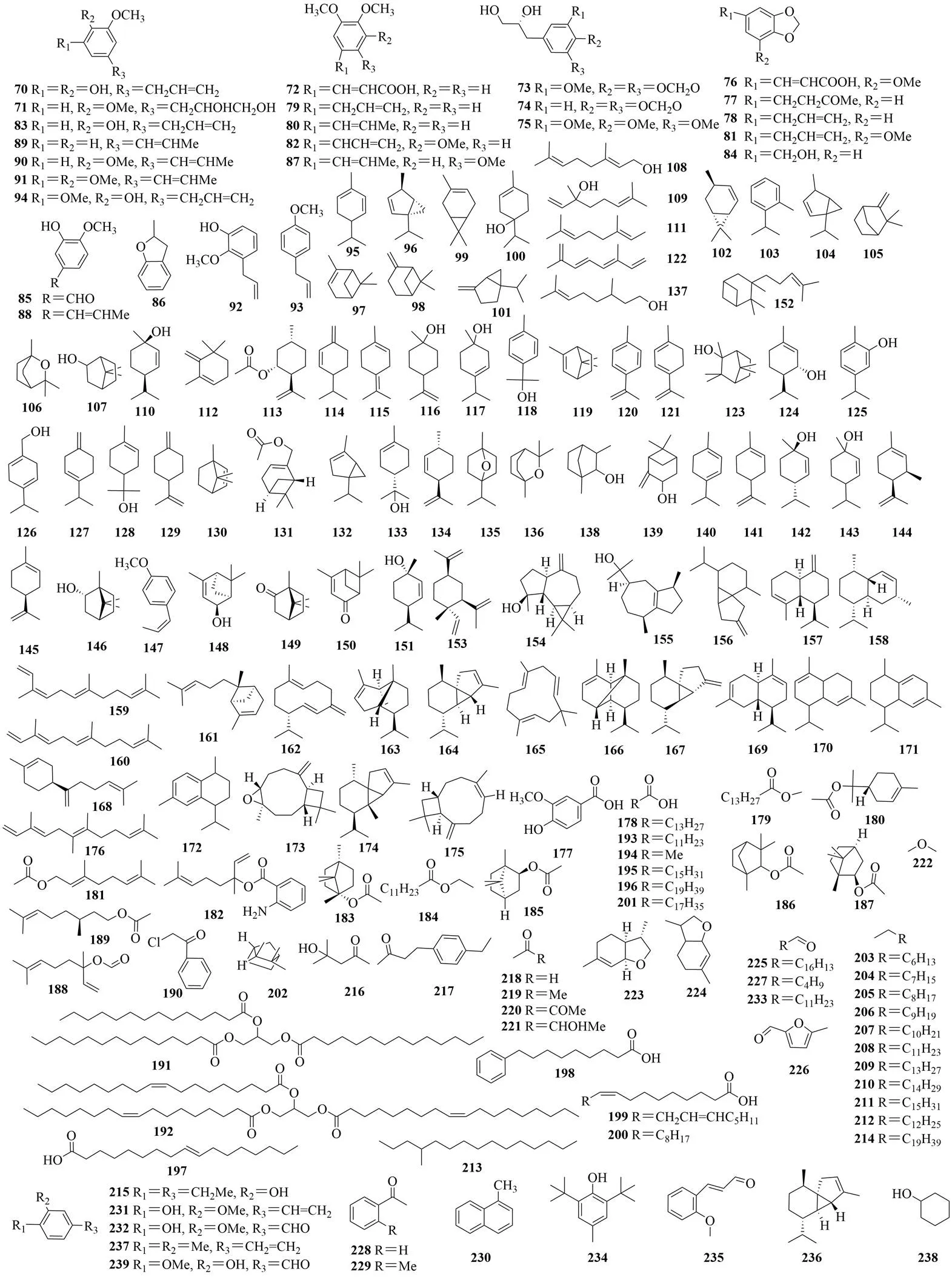
图2 肉豆蔻中挥发油成分化学结构
表3 肉豆蔻中多酚类成分
Table 3 Classification of polyphenols in Myristicae Semen
编号化合物文献编号化合物文献 240邻苯二甲酸122457,3′,4′-三羟基黄酮16 241virolane222467-羟基色原酮16 242原儿茶酸512475,7-diacetyl chrysin48 243紫铆因16248异甘草素51 244硫磺菊素16

图3 肉豆蔻中多酚类的化学结构

图4 肉豆蔻对消化系统的药理作用机制
2.1.4 止泻 肉豆蔻的原油悬浮液和石油醚提取物可分别通过增加豚鼠肠道张力和抑制回肠收缩发挥止泻作用[64]。
2.2 对神经系统的作用
肉豆蔻具有抗痴呆、抗抑郁、抗帕金森和抗癫痫等药理作用,主要以苯丙素类和挥发油类成分发挥作用。
2.2.1 抗痴呆 肉豆蔻醇提物具有较高的体外抗丁酰胆碱酯酶的活性和金属螯合能力,减缓H2O2诱导的大鼠肾上腺嗜铬PC12细胞神经元氧化损伤,预防阿尔茨海默病(Alzheimer’s disease,AD),其物质基础可能为三肉豆蔻酸甘油酯(191)和5,7- diacetyl chrysin(247)[48]。安五脂素防治AD的机制为通过降低p21、p27蛋白表达、磷脂酰肌醇-3-激酶(phosphatidylinositol-3-kinase,PI3K)及蛋白激酶B(protein kinase B,Akt)等的磷酸化水平,从而提高小鼠小胶质细胞及海马神经元的生存率[65-66]。肉豆蔻提取物可增强大鼠海马组织抗衰老因子Klotho水平,降低PI3K和Akt等磷酸化,改善慢性脑低灌注大鼠的空间认知能力,预防血管性痴呆[67]。肉豆蔻中甲基丁香酚(79)、丁香酚(83)、肉豆蔻酸(178)和β-谷甾醇经鉴定,可抑制东莨菪碱诱导的失忆大鼠体内外乙酰胆碱酯酶(acetylcholinesterase,AchE)活性,从而治疗痴呆和AD[68]。综上,肉豆蔻及其活性成分通过增强抗氧化抗炎能力,调节胆碱酯酶活性预防痴呆。
2.2.2 抗抑郁 肉豆蔻正己烷提取物可通过增加5-羟色胺(5-hydroxytryptamine,5-HT)受体(5-HT2A/2C、5-HT3及5-HT1A等)及去甲肾上腺素(norepinephrine,NE)的释放,降低小鼠悬尾不动时间发挥抗抑郁活性,其原因可能是肉豆蔻醚抑制单胺氧化酶活性[69]。肉豆蔻挥发油抗抑郁机制为提高小鼠脑内5-HT、多巴胺、NE的含量[70]。王锐等[33]发现肉豆蔻挥发油β-环糊精包合物可显著改善慢性温和不可预知性应激抑郁大鼠的自主活动状况,其抗抑郁活性成分可能为肉豆蔻醚、黄樟醚(78)等。李明慧等[71]基于网络药理学与分子对接发现,肉豆蔻抗抑郁机制可能为β-谷甾醇下调AchE和一氧化氮合酶的水平。综上,肉豆蔻挥发油等主要通过神经递质和内分泌途径来抗抑郁。
2.2.3 抗帕金森病 肉豆蔻中的安五脂素通过激活新生大鼠中脑中PPARγ和提高精氨酸酶-1表达水平为多巴胺能神经提供保护作用,防止炎症变性,进而改善帕金森病[72]。
2.2.4 抗癫痫 肉豆蔻乙醇提取物可通过减少戊四氮诱导癫痫小鼠的神经元损失,改善胶质细胞活化,其抗癫痫物质基础可能为肉豆蔻酸、榄香素(82)和肉豆蔻醚[73]。具体机制见图5。
2.3 对心脑血管的作用
2.3.1 血液系统药理学活性 肉豆蔻中-(7, 8)-7-acetoxy-3,4,3,5-tetramethoxy-8--4-neolignan(55)可通过降低5-HT、三磷酸腺苷(adenosine triphosphate,ATP)的释放,抑制血栓素B2的形成,增加环磷酸腺苷水平,减弱细胞内Ca2+交换,从整体上抑制凝血酶和血小板活化因子诱导的血小板聚集,从而预防心血管疾病和脑卒中[23]。长期服用肉豆蔻醇提物可促进大鼠红细胞和血小板的生成,对肝酶活性、尿素氮和肌酐水平无影响,可预防贫血、血小板减少等疾病[74]。
2.3.2 调血脂 肉豆蔻可通过提高抗氧化酶及其受体的活性来调节血脂水平。不含黄樟醚的肉豆蔻醇提物可提高PPARα和PPARγ活性,降低血糖和三酰甘油水平,从而对2型糖尿病大鼠的高脂血症起治疗作用[75]。肉豆蔻挥发油可增加高胆固醇血症大鼠超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶、谷胱甘肽过氧化物酶和谷胱甘肽的活性,降低脂质过氧化水平[76]。

图5 肉豆蔻对神经系统的药理作用机制
2.3.3 保护心脏 肉豆蔻挥发油可通过提高心肌组织SOD含量,减少丙二醛含量,抗脂质过氧化保护大鼠缺血再灌注离体心脏;也可通过增加冠脉流量和负性传导等改善心律失常[77-79]。
2.4 降血糖
肉豆蔻可调节血糖水平,预防心血管疾病。肉豆蔻通过激活GATA结合蛋白3/肝X受体α通路,上调ATP结合盒转运蛋白家族A亚家族成员1基因的表达,促进胆固醇外排和抗炎因子IL-10的产生,从而预防动脉粥样硬化等心血管疾病[80]。Yoshioka等[24]研究发现肉豆蔻提取物的正己烷部位可显著降低ig葡萄糖溶液小鼠的血糖水平,其活性成分为肉豆蔻醚、-2-(4-allyl- 2,6-dimethoxy-phenoxy)-1-(3,4-dimethoxyphenyl)-propan-1-ol(ADDP,56)、(7,8)-2-(4-allyl-2,6- dimethoxyphenoxy)-1-(3,4,5-trimethoxyphenyl)-propan-1-ol(ADTP,57)和利卡灵B(35),均可促进大鼠骨骼肌L6细胞中葡萄糖转运蛋白4的易位,从而抑制餐后高血糖,其中ADDP和ADTP的混合物可通过促进AMPK磷酸化发挥作用。利卡灵B通过激活PPARγ,上调胰岛素受体底物1、Akt和PI3K的磷酸化水平,作用于胰岛素信号通路,从而改善分化细胞中葡萄糖转运;诱导小鼠前脂肪3T3-L1细胞分化,增加三酰甘油的积累,促进脂联素分泌,从而改善体内血糖血脂,治疗糖尿病[81]。综上,肉豆蔻降血糖的机制涉及提高抗炎能力、改善葡萄糖转运、调节胰岛素通路和促进脂质代谢等。
2.5 抗癌
肉豆蔻通过调节信号通路、ATP水平、DNA复制或改变线粒体功能等途径抑制癌细胞增殖。肉豆蔻醚可通过下调靶向表皮生长因子受体/ERK信号通路抑制体内外实验中胃癌细胞生长[82];体外实验证明其对人结肠癌HCT116和LOVO细胞具有抗增殖作用,其机制为下调丝裂原活化细胞外信号调节激酶/ERK信号通路[83];Seneme等[84]发现肉豆蔻醚还可通过结合多药耐药蛋白P-糖蛋白,协同化疗药物发挥抗癌作用。甲氧基丁香酚可通过上调p53/p21通路,损伤线粒体功能,进而抑制人子宫内膜癌细胞生长[85]。去氢二异丁香酚可通过抑制癌细胞DNA的复制与生长,使细胞周期滞留,诱发自噬效应等抗结肠癌[86]。Chumkaew等[19]研究表明myticaganal C(40)对口腔癌和小细胞肺癌具有显著疗效,myticaganal A和B(38、39)及myrisfrageal A和B(41、42)对以上2种癌及乳腺癌具有中等细胞毒性,4者对口腔癌的半抑制浓度(median inhibition concentration,IC50)分别为17.9、20.3、20.6、15.9 μmol/L,对小细胞肺癌的IC50分别为24.4、45.6、29.7、27.3 μmol/L,对乳腺癌的IC50分别为17.1、22.7、21.4、14.3 μmol/L。
2.6 抗炎镇痛作用
肉豆蔻主要通过调节免疫及神经系统发挥抗炎镇痛作用。当机体免疫功能下降时,往往会引发炎症反应,从而导致相关疾病[87],肉豆蔻醇提物可增强鲤鱼免疫应答[88]。宗伟英等[89]发现肉豆蔻醇提物还可通过抑制黄嘌呤氧化酶和肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)活性,降低高尿酸血症小鼠的血尿酸水平,从而改善痛风性急性关节炎。肉豆蔻中1-(3,4-dihydroxyphenyl)-3-(4- methoxyphenyl)-propane(59)[26]及利卡灵B[20]可抑制小鼠RAW264.7巨噬细胞一氧化氮的生成,从而降低炎性介质刺激水平。肉豆蔻醚可降低RAW264.7细胞中TNF-α、粒细胞集落刺激因子、IL-1α等细胞因子水平,通过下调细胞内钙水平抑制一氧化氮的产生,从而发挥抗炎作用[90]。Checker等[91]研究发现肉豆蔻木脂素类成分可增加哺乳动物脾细胞中伴刀豆球蛋白A刺激的淋巴细胞数量,增强免疫反应抑制炎症反应。安五脂素可通过抑制PI3K/Akt通路,呈剂量相关性抑制一氧化氮的产生,改善小胶质细胞炎症[66]。Qiburi等[92]发现去氢二异丁香酚可通过下调小胶质细胞的促炎因子和提高抗氧化基因的表达治疗神经炎症。在镇痛方面,肉豆蔻主要通过抑制慢性炎性疼痛模型小鼠中神经激肽1受体、环氧合酶-2及P物质减缓注射完全弗氏佐剂诱导的肿胀、机械性和高温诱发痛[93]。肉豆蔻中生物碱类成分可显著缓解乙酸所致小鼠内脏疼痛[94]。
2.7 抗菌
肉豆蔻提取物、苯丙素类等是肉豆蔻抗菌作用的物质基础。肉豆蔻氯仿提取物对革兰阳性菌、白色念珠菌和耐甲氧西林金黄色葡萄球菌的最低抑菌浓度分别为1.56、25和3.12 μg/mL[95]。肉豆蔻提取物(榄香素、肉豆蔻醚、甲氧基丁香酚等)可作为外排泵抑制剂抗耐甲氧西林金黄色葡萄球菌[96]。肉豆蔻挥发油对细菌的抑制效果优于真菌,抑菌效果如下:金黄色葡萄球菌>大肠杆菌>枯草杆菌>酿酒酵母菌>黄曲霉[97]。肉豆蔻醚、丁香酚、α-蒎烯(97)对金黄色葡萄球菌、大肠杆菌、志贺氏菌、霍乱弧菌均有一定的抑菌活性,肉豆蔻醚、丁香酚还具有抗伤寒杆菌活性[98]。丁香酚可通过改变奇异假单胞菌细胞膜的完整性发挥杀菌作用[99],还可通过下调半胱氨酸和蛋氨酸代谢-核糖同型半胱氨酸酶基因、上调精氨酸和脯氨酸代谢-乙酰-γ-谷氨酰磷酸脱氢酶基因抑制耐甲氧西林金黄色葡萄球菌活性[100]。
2.8 抗氧化

2.9 其他
此外,肉豆蔻正己烷提取物可抑制黑色素生成[105],肉豆蔻醚和甲基丁香酚可通过抑制下丘脑神经肽Y mRNA表达来增强大鼠食欲[106],利卡灵B可抗寄生虫[107],肉豆蔻还具有壮阳、防龋齿、调节脂肪代谢[108]、防辐射[109]、保肾[110]、保护男性生育能力[111]等功能。
3 毒性研究
随着对肉豆蔻药理作用的深入研究,其毒性与不良反应也引起广泛关注。《中药大辞典》中肉豆蔻的毒性成分为肉豆蔻醚和榄香素,具有致幻作用。Duarte等[112]通过临床研究发现一次性摄入18~28 g肉豆蔻,患者可出现焦虑、谵语、幻觉等神经系统异常的中毒行为,其机制可能为肉豆蔻醚和榄香素代谢为具有兴奋神经系统作用的3-甲氧基-4,5-甲氧基-5-苯乙胺。研究发现,小鼠吸入肉豆蔻精油0.5 mL抑制其运动能力率可达68.62%,对吸入肉豆蔻精油1 mL的小鼠2.0 h后进行活性成分鉴定得知,肉豆蔻醚、4-松油醇(133)和黄樟醚血药浓度可达7.1、6.28和1.28 g/mL,含量较高,故推测以上成分具有毒性[113]。除此之外,肉豆蔻醚代谢生成可与-乙酰半胱氨酸共价结合的1-羟基肉豆醚,在250 μmol/L时表现为对小鼠原代肝细胞显著的细胞毒性[114]。Demetriades等[115]发现服用50 g肉豆蔻后患者出现心跳过速、心悸、口干、面部潮红等心血管异常症状,可能是由于类似血清素激动剂的丁香酚、异丁香酚(89)、黄樟醚和芳樟醇(109)发挥作用。目前对于肉豆蔻毒性反应的临床研究较少,从药食同源安全性角度出发可在后续研究中加强对该方面的研究。
4 临床应用
肉豆蔻在临床上广泛应用,古今方剂中多与性味辛温,主入胃、大肠经的中药(丁香、补骨脂等)进行配伍,用于消化系统疾病的治疗。但随着现代药理作用的拓展,现代中药复方制剂不仅剂型多样,其也用于神经系统及心血管疾病的治疗,主要与性味苦酸平的诃子、广枣配伍。
4.1 在古代方剂中的临床应用
肉豆蔻的临床应用在《圣济总录》《内科摘要》《普济方》《局方》等本草典籍中均有记载。配伍温补药,如补骨脂,可以脾肾双补、化湿止泻;配伍温阳散寒药,如附子,可以温中健脾、固肠止泻。主要用于治疗久泻不止、虚寒气滞、脘腹胀痛、食少呕吐等症状。本草典籍记载的肉豆蔻在古代方剂中的部分临床应用见表4。
表4 肉豆蔻在古代方剂中的临床应用
Table 4 Clinical applications of Myristicae Semen in ancient prescriptions
出处配伍药物功能与主治 《圣济总录》附子治脾脏久冷、滑泻不止 半夏、茱萸、巴豆治留饮宿食不消 《内科摘要》五味子、吴茱萸、生姜等治脾胃虚弱、大便不实、饮食不思 《普济方》缩砂、羊肝治休息痢、羸瘦 《局方》丁香、甘草、白面治一切冷气、心腹胀满、胸膈痞滞、哕逆呕吐、泄泻虚滑等 《圣惠方》附子、白石脂治妇人白带下、腹内冷痛 藿香治小儿霍乱不止 人参、厚朴、生姜、粟米治霍乱呕吐不止
4.2 在现代中药复方制剂中的应用
含肉豆蔻的传统中成药剂型主要有丸剂、膏剂、散剂等,现代主要有片剂、冲剂、颗粒剂等。《校注妇人良方》收录的四神丸,肉豆蔻为臣药,具有温脾暖胃、涩肠止泻之功,助君药补骨脂温肾暖脾、固涩止泻。四神片收载于《中国药典》2020年版,其联合兰美沙拉嗪可治疗溃疡性结肠炎[116],与双歧三联活菌胶囊联用治疗慢性功能性便秘[117],与匹维溴铵联合可治疗肠易激综合征[118]。在民族用药方面,肉豆蔻粉剂脐敷可用于治疗骨科患者术后腹胀便秘[119];藏医含肉豆蔻的煳儿灸联合油脂涂擦可用于治疗神经性呕吐[120];金诃愈心冲剂可用于治疗血栓和冠心病[121]。此外,肉豆蔻复方制剂在临床上可用于治疗心脏疾病,巴亚玛等[122]对30例窦性心动过缓患者进行口服肉豆蔻五味丸治疗,结果显示治疗组总有效率为66.67%,心律失常疗效较好。索朗平措[123]使用三味肉豆蔻汤剂治疗50例隆思型心绞痛患者,其中40例治愈,8例好转,2例无效,总有效率高达96%,尤其对情绪紧张和过劳诱因的心绞痛疗效显著。经药智网检索含肉豆蔻的中成药方剂共155种,对处方药物(频次≥10)进行关联规则分析。由图6可见,在临床应用中成药处方中,与肉豆蔻高频配伍的药材有丁香、木香、红花、诃子和沉香等。
5 Q-Marker预测分析
5.1 植物亲缘学及化学成分特有性
肉豆蔻科植物全球约16属380余种,在我国有3属15种,产自台湾、广东、海南等地区,尤以云南南部为主[124]。目前已从中分离出木脂素、挥发油、多酚等化学成分,挥发油作为其化学结构多样的主要次生代谢产物,具有抗癌、抗炎镇痛等多种药理活性,可为Q-Marker的筛选提供参考。苯丙素类化合物肉豆蔻醚、榄香素和黄樟醚含量较高[27],是肉豆蔻的主要药效成分。徐杨斌等[39]通过气相色谱-飞行时间质谱法分析英国、中国云南和印尼3个产地肉豆蔻油中的挥发性成分,结果表明不同产地成分组成无较大差别,主要为肉豆蔻醚和α-蒎烯等化合物,但云南肉豆蔻油中1,8-桉叶素含量较高。此外,挥发油成分在其混伪品中也具有明显差异。王远志等[125]采用气相色谱-质谱测定肉豆蔻与长形肉豆蔻中的挥发油成分,二者生品成分差异显著,前者α-蒎烯含量远高于后者,黄樟醚含量远低于后者,含量差异可应用于其真伪鉴别。综上,苯丙素类成分肉豆蔻醚、榄香素、黄樟醚和挥发油成分α-蒎烯、1,8-桉叶素在不同地区和不同品种肉豆蔻中的含量差别较大,具有特异性,可作为其Q-Marker的参考。
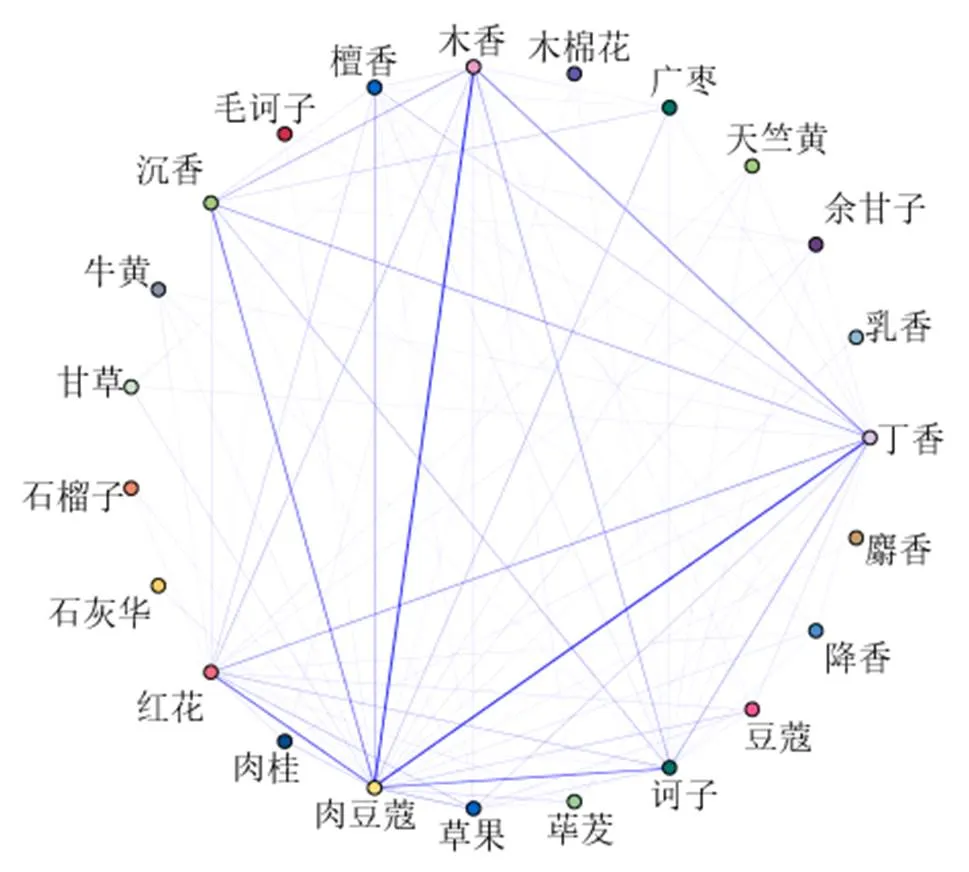
图6 含肉豆蔻的中成药处方中高频用药关联网络
5.2 不同采收时期和炮制方法
中药采收时期及炮制工艺等因素影响其化学成分与疗效,可为其质量控制提供一定参考。林杰等[126]采用气相色谱-质谱法对春冬2季采收的肉豆蔻挥发性成分进行对比分析,二者组成差异显著,前者含双戊烯(141),常作香料;而后者含右旋萜二烯(145)、甲基丁香酚及肉豆蔻醚,更适宜药用。药材加工方法也会影响品质优劣,肉豆蔻常用煨法、炒法及制霜进行炮制。煨制和炒制后α-蒎烯等相对含量显著提高[127],而麸煨和制霜后去氢二异丁香酚[128]和毒性成分黄樟醚[129]、肉豆蔻醚[130]等显著降低。综上,表明生态因子与炮制工艺可影响肉豆蔻中木脂素类、苯丙素类及萜烯类成分。去氢二异丁香酚、甲基丁香酚、肉豆蔻醚、黄樟醚、双戊烯、右旋萜二烯和α-蒎烯等,可为其资源利用和质量控制提供参考,作为Q-Marker的来源。
5.3 成分与功效相关性
基于化学成分的多样性,中药的药理作用多元化,结合肉豆蔻的成分与功效进行Q-Marker的预测分析。肉豆蔻传统功效为温中行气、涩肠止泻,中医常用温中理气治疗脾胃虚寒的病证。肉豆蔻中木脂素类和挥发油类成分具有止泻功效[131]。脾胃虚寒可能会导致结肠炎和胃溃疡,肉豆蔻醚可抗结肠炎[62],马拉巴酮B和C可抗胃溃疡[52]。因此,可考虑将以上3种成分作为肉豆蔻Q-Marker的参考。
现代研究表明,肉豆蔻具有调节神经系统、抗癌、抗炎、抗菌、抗氧化等药理作用,尤其是木脂素类安五脂素、苯丙素类丁香酚、肉豆蔻醚具有多种生物活性。肉豆蔻中的安五脂素[65-66]、丁香酚[68]、β-谷甾醇[71]、肉豆蔻醚[69]及榄香素[73]等通过不同作用机制治疗中枢神经系统疾病。甲氧基丁香酚[85]、去氢二异丁香酚[86],肉豆蔻醚[83-84]等可对多种癌细胞发挥抑制作用。利卡灵B[20]、安五脂素[66]、肉豆蔻醚[90]等可作为抗炎镇痛的物质基础。丁香酚、肉豆蔻醚、α-蒎烯[98]等为肉豆蔻的主要抗菌化合物。去氢二异丁香酚和马拉巴酮B[104]等具有显著抗氧化活性。安五脂素[58]和甲氧基丁香酚[59]等可作为保肝药效物质基础。以上化学成分与肉豆蔻扩展功效息息相关,综上,木脂素类去氢二异丁香酚、安五脂素、利卡灵B,苯丙素类肉豆蔻醚、甲氧基丁香酚、丁香酚、榄香素和α-蒎烯等可作为Q-Marker的参考。
5.4 传统药性
四气五味作为中药药性的重要组成部分,性味合参从不同角度反映并指导药物配伍应用,可作为Q-Marker的参考依据。肉豆蔻性辛温,根据中药药性理论,辛味药归肝、脾、肺和胃,主发散、行气血,其化学成分主要为挥发油[132-133]。温性是反映药物作用性质的重要概念之一,在《神农本草经》《本草衍义》《本草品汇精要》中皆有提到,挥发油、木脂素等成分是温性药物的化学成分[134]。因此,肉豆蔻中挥发油、木脂素类等成分可为其Q-Marker的选择提供参考。
5.5 复方配伍环境
肉豆蔻基于不同配伍环境发挥不同疗效,治疗相关疾病。蒙古族和藏族验方中,肉豆蔻中的榄香素、肉豆蔻醚可治疗心血管系统疾病[135]。蒙药额尔敦-乌日勒复方中肉豆蔻中的肉豆蔻醚具有抗炎作用,去氢二异丁香酚具有抗炎抗氧化活性,可用于缺血性脑卒中后神经损伤的恢复[136]。八味沉香散系藏族验方,始载于《四部医典》,由沉香、肉豆蔻、广枣等8味药组成,方中肉豆蔻具有调节心脑血管系统的功效[137]。含肉豆蔻的中成药如肠舒止泻胶囊、九味沉香胶囊、止泻保童冲剂和四神片等用于治疗消化系统疾病,与其传统功效一致。肉豆蔻与补骨脂配伍可促进肉豆蔻中去氢二异丁香酚的溶出,提高肉豆蔻辛温的疗效,常作为温肾暖脾、涩肠止泻药对[138-139]。仁增加等[140]利用网络药理学和分子对接等技术,分析藏药五味肉豆蔻方干预新型冠状病毒肺炎的机制,发现肉豆蔻中的β-谷甾醇和myrrhanol C可能是其关键活性成分。因此,在复方配伍环境中,榄香素、肉豆蔻醚、去氢二异丁香酚和myrrhanol C主要发挥温中行气、涩肠止泻等功用,与现代药理学调节消化系统、神经系统、心脑血管系统、抗炎、抗氧化研究一致,可将上述成分作为肉豆蔻相关复方的Q-Marker。
5.6 化学成分可测性
Q-Marker的基本条件包括可定性鉴别和定量测定。目前可通过薄层鉴别法、高效液相色谱法及指纹图谱的建立等方法对肉豆蔻化学成分进行分析,为可测性的Q-Marker提供参考依据。《中国药典》2020年版规定了肉豆蔻中挥发油和去氢二异丁香酚的含量测定方法及其限度要求,其中以挥发油测定法甲法测定,规定挥发油不得少于6.0%;采用反相高效液相色谱法测定去氢二异丁香酚,规定干燥品中去氢二异丁香酚不得少于0.10%[2]。
挥发油是肉豆蔻的主要活性成分,约占其成分总质量的8%~15%。黄樟醚、甲基丁香酚、榄香素、肉豆蔻醚等苯丙素类化合物占肉豆蔻精油总峰面积的6.2%[106]。采用气相色谱-质谱法定性分析肉豆蔻中挥发油成分,共分离得到80个化学成分,匹配度达87%的有63个[27]。贾天柱等[130]利用薄层扫描法测定出生品肉豆蔻中肉豆蔻醚和黄樟醚占挥发油含量的26.25%和3.52%。李力等[36]和赵祥升等[141]采用气相法定量测定肉豆蔻成分,结果显示含量较高的挥发油成分为松油烯-4-醇(100)和β-蒎烯(98),苯丙素类成分含量由高到低为榄香素、肉豆蔻醚、异丁香酚、丁香酚。王晶等[15]通过超高效液相色谱-四极杆飞行质谱技术鉴定得补骨脂-肉豆蔻药对入血成分中有10个来源于肉豆蔻,包含去氢二异丁香酚和肉豆蔻酚A(29)等。李志平等[142]采用一测多评法测定九味沉香胶囊中的安五脂素和去氢二异丁香酚的含量。
肉豆蔻醚、榄香素、黄樟醚、丁香酚等苯丙素类成分具有毒性[108],主要表现为中枢神经系统及心血管系统的不良反应,不利于其抗抑郁、抗癌及抗氧化等药理作用的发挥。因此应考虑化学成分的安全性,黄樟醚大小鼠的半数致死量为1950、2350 mg/kg,肉豆蔻醚与之相当[143],但控制用量在10 g以下一般不会引起不良反应。上述成分的药理活性可代表肉豆蔻的主要适应证与生物活性,毒性可控,且均可定性定量分析,故可作为肉豆蔻质量的反映指标。因此,肉豆蔻醚、黄樟醚、松油烯-4-醇、β-蒎烯、榄香素、异丁香酚、丁香酚、安五脂素、肉豆蔻酚A及去氢二异丁香酚可作为肉豆蔻的潜在Q-Marker。
6 结语与展望
肉豆蔻为历史悠久的药食同源中药,含有木脂素、挥发油等多种化学成分,疗效丰富,应用领域不断扩大。现代学者对其木脂素类和苯丙素类成分开展了一系列研究,但肉豆蔻醚等活性成分的毒性作用不容小觑。随其种类增多,药材质量参差不齐,临床疗效也存在一定差异,加之毒效兼具,目前单一测定指标已无法满足其质量控制需求。本文在对肉豆蔻化学成分、药理作用、毒性研究及临床应用进行归纳总结的基础上,以Q-Marker为指导,进行了植物亲缘学和化学成分特有性、不同采收时期和炮制方法、成分与功效相关性、传统药性、复方配伍环境及化学成分可测性等分析。选取肉豆蔻特有的、可测定的、含量较高的药效活性成分,结合毒性研究筛选影响传统药性及复方配伍的有效成分,结果表明,肉豆蔻中的木脂素类、苯丙素类成分是其发挥临床疗效的代表性成分。故推测肉豆蔻内去氢二异丁香酚、肉豆蔻醚、安五脂素、甲氧基丁香酚、榄香素、丁香酚及α-蒎烯等成分可作为肉豆蔻的潜在Q-Marker,见图7。

图7 肉豆蔻Q-Marker预测分析
肉豆蔻自古被誉为治疗虚寒性泻利之要药,但目前对其“止泻”单体活性成分及作用机制研究尚有欠缺,可结合肠道菌群与止泻中药具有双向调节的机制,对该疗效进行针对性研究。其次,主要成分肉豆蔻醚、榄香素、丁香酚等苯丙素类不仅具有广泛的药理活性,也会产生幻觉等中毒反应。与上述成分结构相关的黄樟醚和甲基丁香酚等已被定义为遗传毒性致癌物,故推测成分结构与药效、毒性间存在联系,但上述成分致癌性及基因毒性尚不明确,缺乏结构毒性研究和毒理学数据,有待深入探究。现代肉豆蔻研究主要集中于化学成分的提取分离,其单体成分研究以木脂素和挥发性成分为主,但定量测定方法仍有待提升,且不同产地基原对比研究较少,肉豆蔻内黄酮等其他成分的研究也有待补充。基于其质量控制和临床疗效等方面的研究探索,更多的生物活性成分可作为其Q-Marker的备选,为肉豆蔻的质量控制体系提供参考,积极推进其应用与发展。
利益冲突 所有作者均声明不存在利益冲突
[1] 雷斅. 雷公炮炙论 [M]. 张骥补, 施仲安辑校. 南京: 江苏科学技术出版社, 1985: 46.
[2] 中国药典 [S]. 一部. 2020: 141.
[3] 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物 (Q-Marker): 中药产品质量控制的新概念 [J]. 中草药, 2016, 47(9): 1443-1457.
[4] 刘昌孝. 中药质量标志物 (Q-Marker) 研究发展的5年回顾 [J]. 中草药, 2021, 52(9): 2511-2518.
[5] Liu C X, Cheng Y Y, Guo D A,. A new concept on quality marker for quality assessment and process control of Chinese medicines [J]., 2017, 9(1): 3-13.
[6] Wang Y L, Cui T, Li Y Z,. Prediction of quality markers of traditional Chinese medicines based on network pharmacology [J]., 2019, 11(4): 349-356.
[7] Godínez C B, Pérez G S, Pérez R J,. Synthesis and biological activities of dehydrodiisoeugenol: A review [J]., 2022, 15(11): 1351.
[8] Cuong T D, Hung T M, Han H Y,. Potent acetylcholinesterase inhibitory compounds from[J]., 2014, 9(4): 499-502.
[9] Lee S U, Shim K, Ryu S,. Machilin A isolated fromstimulates osteoblast differentiation [J]., 2009, 75(2): 152-157.
[10] Cho J Y, Choi G J, Son S W,. Isolation and antifungal activity of lignans fromagainst various plant pathogenic fungi [J]., 2007, 63(9): 935-940.
[11] Miyazawa M, Kasahara H, Kameoka H. A new lignan (+)-myrisfragransin from[J]., 1996, 8(1): 25-26.
[12] 张蕾, 徐云峰, 沈硕, 等. 肉豆蔻的化学成分研究 [J]. 中国现代中药, 2010, 12(6): 16-19.
[13] Duan L, Tao H W, Hao X J,. Cytotoxic and antioxidative phenolic compounds from the traditional Chinese medicinal plant,[J]., 2009, 75(11): 1241-1245.
[14] Nguyen P H, Van Thu Le T, Kang H W,. AMP-activated protein kinase (AMPK) activators from(nutmeg) and their anti-obesity effect [J]., 2010, 20(14): 4128-4131.
[15] 王晶, 韩燕全, 魏良兵, 等. 补骨脂-肉豆蔻配伍前后血中移行成分的UPLC-Q-TOF/MS分析 [J]. 中草药, 2018, 49(22): 5264-5270.
[16] 季霄, 吴士龙, 贾天柱, 等. 肉豆蔻的化学成分研究 [J]. 中草药, 2014, 45(23): 3367-3372.
[17] Yang X W, Huang X, Ma L A,. The intestinal permeability of neolignans from the seeds ofin the Caco-2 cell monolayer model [J]., 2010, 76(14): 1587-1591.
[18] Kruakaew S, Singha S, Sangvichien E,. Neolignans fromseeds, revision of their absolute configurations, reduction products and biological activities [J]., 2022, 199: 113174.
[19] Chumkaew P, Srisawat T. New neolignans from the seeds ofand their cytotoxic activities [J]., 2019, 73(1): 273-277.
[20] Cao G Y, Yang X W, Xu W,. New inhibitors of nitric oxide production from the seeds of[J]., 2013, 62: 167-171.
[21] 杨秀伟, 黄鑫, 艾合买提·买买提. 肉豆蔻中新的新木脂素类化合物 [J]. 中国中药杂志, 2008, 33(4): 397-402.
[22] Francis K S, Suresh E, Nair M S. Chemical constituents fromfruit [J]., 2014, 28(20): 1664-1668.
[23] Kang J W, Min B S, Lee J H. Anti-platelet activity of erythro-(7,8)-7-acetoxy-3,4,3′,5′-tetramethoxy-8--4′-neolignan from[J]., 2013, 27(11): 1694-1699.
[24] Yoshioka Y, Kono R, Kuse M,. Phenylpropanoids and neolignans isolated fromenhance glucose uptake in myotubes [J]., 2022, 13(7): 3879-3893.
[25] 袁子民, 王静, 胡娜, 等. 肉豆蔻中总木脂素的提取工艺优化研究 [J]. 中成药, 2014, 36(2): 420-421.
[26] 李大山, 曾天艳, 马莎, 等. 肉豆蔻中二芳基丙烷类抗炎活性成分 [J]. 天然产物研究与开发, 2021, 33(5): 779-783.
[27] 张根荣, 胡静, 丁斐, 等. 肉豆蔻挥发性成分的气相色谱/质谱分析 [J]. 时珍国医国药, 2016, 27(11): 2596-2598.
[28] 秦宇仙, 徐琳, 余冯萍, 等. 纤维素酶辅助水蒸气蒸馏提取肉豆蔻挥发油的品质及其活性评价 [J]. 食品与发酵工业, 2022, 48(10): 112-118.
[29] Lima R K, das Graças Cardoso M, Andrade M A,. Bactericidal and antioxidant activity of essential oils fromhoutt andH. B. K [J]., 2012, 89(3): 523-528.
[30] 贾天柱, 傅宝庆, 袁昌鲁. 肉豆蔻不同炮制品挥发油含量及其化学成分比较 [J]. 中药材, 1992, 15(1): 27-29.
[31] 王莹, 杨秀伟, 陶海燕, 等. 商品肉豆蔻挥发油成分的GC-MS分析 [J]. 中国中药杂志, 2004, 29(4): 339-342.
[32] 江欣禅, 钮彪, 卢金清. 顶空-固相微萃取/气相色谱-质谱法分析肉豆蔻中挥发性成分 [J]. 中国医院药学杂志, 2013, 33(18): 1546-1548.
[33] 王锐, 潘贝, 赵华伟, 等. 肉豆蔻挥发油β-CD包合物GC-MS成分分析及其抗抑郁活性物质研究 [J]. 世界中医药, 2018, 13(4): 785-789.
[34] 王莹, 杨秀伟. 印度尼西亚产肉豆蔻挥发油成分的GC-MS分析 [J]. 中华中医药杂志, 2007, 22(9): 603-606.
[35] 卢金清, 李雨玲, 李婷, 等. 肉豆蔻挥发油化学成分的GC-MS分析 [J]. 西北药学杂志, 2012, 27(3): 202-204.
[36] 李力, 潘倩雯, 郭偲, 等. 不同方法提取肉豆蔻挥发油成分的气相色谱-质谱法分析 [J]. 医药导报, 2019, 38(12): 1630-1634.
[37] 杨晓东, 何广铭, 彭娇, 等. 肉豆蔻饮片及其标准汤剂中挥发性成分差异分析 [J]. 江西中医药, 2021, 52(7): 65-68.
[38] 田卉玄, 杨瑞琦, 邹慧琴, 等. 电子鼻与HS-GC-MS技术快速鉴别肉豆蔻霉变过程中气味变化及其物质基础 [J]. 中国中药杂志, 2021, 46(22): 5853-5860.
[39] 徐杨斌, 王德懿, 冒德寿, 等. 不同产地肉豆蔻油中挥发性成分的GC-TOF/MS分析 [J]. 香料香精化妆品, 2018(1): 31-36.
[40] 赵祥升, 黄立标, 陈宏降, 等. 肉豆蔻叶和种仁挥发油GC-MS分析 [J]. 现代中药研究与实践, 2012, 26(3): 69-72.
[41] 林霜霜, 邱珊莲, 郑开斌, 等. 5种精油的化学成分及对番茄早疫病的抑菌活性研究 [J]. 中国农学通报, 2017, 33(31): 132-138.
[42] Adiani V, Gupta S, Chatterjee S,. Activity guided characterization of antioxidant components from essential oil of Nutmeg () [J]., 2015, 52(1): 221-230.
[43] 李铁林, 周杰, 徐植灵, 等. 炮制对肉豆蔻挥发油含量的影响及肉豆蔻挥发油化学成分的研究 [J]. 中国中药杂志, 1990, 15(7): 21-23.
[44] 席小辉, 宋欠欠, 江雨彤, 等. 盐析辅助水蒸气蒸馏法提取肉豆蔻精油及其抗氧化和清除亚硝酸盐作用研究 [J]. 东北农业大学学报, 2021, 52(8): 57-68.
[45] 赖闻玲, 曾志, 陈亿新, 等. 中药复方中后下组份化学成分研究 (II) 肉豆蔻挥发油 [J]. 中草药, 2002, 33(7): 596-598.
[46] 杨瑞琦, 李佳慧, 陈慧荣, 等. 肉豆蔻药材霉变前后挥发油成分的GC-MS分析 [J]. 中华中医药杂志, 2019, 34(10): 4812-4815.
[47] 刘博, 陈开勋, 陈渭萍, 等. 肉豆蔻超临界二氧化碳萃取工艺及其精油的GC-MS分析研究 [J]. 香料香精化妆品, 2003(4): 17-19.
[48] Omidpanah S, Vahedi-Mazdabadi Y, Manayi A,. Phytochemical investigation and anticholinesterase activity of ethyl acetate fraction ofHoutt. seeds [J]., 2022, 36(2): 610-616.
[49] 邱琴, 张国英, 孙小敏, 等. 超临界CO2流体萃取法与水蒸气蒸馏法提取肉豆蔻挥发性化学成分的研究 [J]. 中药材, 2004, 27(11): 823-826.
[50] 郑国平, 李东星. 肉豆蔻和肉豆蔻衣脂肪酸成分的比较研究 [J]. 石河子科技, 2013(4): 16-18.
[51] 李秀芳, 吴立军, 贾天柱, 等. 肉豆蔻的化学成分 [J]. 沈阳药科大学学报, 2006, 23(11): 698-701.
[52] Banerjee D, Bauri A K, Guha R K,. Healing properties of malabaricone B and malabaricone C, against indomethacin-induced gastric ulceration and mechanism of action [J]., 2008, 578(2/3): 300-312.
[53] Hou J P, Wu H, Wang Y,. Isolation of some compounds from nutmeg and their antioxidant activities[J]., 2012, 36(2): 164-170.
[54] Yang X N, Liu X M, Fang J H,. PPARα mediates the hepatoprotective effects of nutmeg [J]., 2018, 17(5): 1887-1897.
[55] Zhao W Y, Song F F, Hu D G,. The protective effect ofHoutt. extracts against obesity and inflammation by regulating free fatty acids metabolism in nonalcoholic fatty liver disease [J]., 2020, 12(9): 2507.
[56] Poorbagher M R M, Karimi E, Oskoueian E. Hepatoprotective effect of nanoniosome loadedphenolic compounds in mice-induced hepatotoxicity [J]., 2022, 26(21): 5517-5527.
[57] Sohn J H, Han K L, Kim J H,. Protective effects of macelignan on cisplatin-induced hepatotoxicity is associated with JNK activation [J]., 2008, 31(2): 273-277.
[58] Song J S, Kim E K, Choi Y W,. Hepatocyte-protective effect of nectandrin B, a nutmeg lignan, against oxidative stress: Role of Nrf2 activation through ERK phosphorylation and AMPK-dependent inhibition of GSK-3β [J]., 2016, 307: 138-149.
[59] de Souza Basso B, Haute G V, Ortega-Ribera M,. Methoxyeugenol deactivates hepatic stellate cells and attenuates liver fibrosis and inflammation through a PPAR-γ and NF-κB mechanism [J]., 2021, 280: 114433.
[60] Prashant B, Yogesh P, AgrawalMona Y. Antispasmodic effect offragrance [J]., 2013, 6: 1094-1096.
[61] 曹阳, 于明新. 肉豆蔻有效成分对急性放射性肠炎肠黏膜保护作用及相关机制研究 [J]. 辽宁中医药大学学报, 2019, 21(1): 43-46.
[62] Ismail Abo El-Fadl H M, Mohamed M F A. Targeting endoplasmic reticulum stress, Nrf-2/HO-1, and NF-κB by myristicin and its role in attenuation of ulcerative colitis in rats [J]., 2022, 311: 121187.
[63] Sattar A, Abdo A, Mushtaq M N,. Evaluation of gastro-protective activity ofon ethanol-induced ulcer in albino rats [J]., 2019, 91(2): e20181044.
[64] Grover J K, Khandkar S, Vats V,. Pharmacological studies onAntidiarrheal, hypnotic, analgesic and hemodynamic (blood pressure) parameters [J]., 2002, 24(10): 675.
[65] 宗堪堪, 刘鑫, 玄延花, 等. 肉豆蔻木酚素对脂多糖激活的小胶质细胞条件培养基对海马神经元损伤的保护作用 [J]. 中国临床药理学杂志, 2019, 35(6): 528-531.
[66] Zong K K, Liu X, Sun Z,. Macelignan inhibits the inflammatory response of microglia and regulates neuronal survival [J]., 2020, 339: 577123.
[67] 邱新茹, 宗堪堪, 孙周, 等. 肉豆蔻提取物改善缺血缺氧大鼠脑损伤的作用机制 [J]. 医学研究生学报, 2022, 35(2): 125-130.
[68] Khan M A, Srivastava V, Kabir M,. Development of synergy-based combination for learning and memory using,and TLC-MS-bioautographic studies [J]., 2021, 12: 678611.
[69] Iwata N, Kobayashi D, Kawashiri T,. Mechanisms and safety of antidepressant-like effect of nutmeg in mice [J]., 2022, 45(6): 738-742.
[70] 孙婷婷, 崔瑛, 汪晶, 等. 肉豆蔻挥发油对行为绝望抑郁小鼠的影响 [J]. 中华行为医学与脑科学杂志, 2014, 23(6): 534-536.
[71] 李明慧, 陈卓, 杨霞, 等. 基于网络药理学与分子对接研究肉豆蔻治疗抑郁症的作用机制 [J]. 湖南中医杂志, 2022, 38(5): 156-164.
[72] Kiyofuji K, Kurauchi Y, Hisatsune A,. A natural compound macelignan protects midbrain dopaminergic neurons from inflammatory degeneration via microglial arginase-1 expression [J]., 2015, 760: 129-135.
[73] Ghorbanian D, Ghasemi-Kasman M, Hashemian M,.houtt extract attenuates neuronal loss and glial activation in pentylenetetrazol-induced kindling model [J]., 2019, 18: 812-825.
[74] Khoshvaghti A, Hashemian M, Dehghan V,. Toxicological and biochemical studies ofhydroalcoholic extracts in albino rats [J]., 2015, 6(3): 154-166.
[75] Lestari K, Diantini A, Barliana M,. Potential natural dual agonist PPARα/γ-induced antidiabetic and antidyslipidemic properties of safrole-free nutmeg seed (Houtt) extract [J]., 2019, 9(3): 248-253.
[76] Hassanen N H M. Protective effect of nutmeg and rosemary on oxidative stress in hypercholesterolemic rats [J]., 2015, 4(4): 465.
[77] 张子英, 伊乐, 爱民, 等. 蒙药肉豆蔻挥发油对大鼠心律失常的作用 [J]. 中国民族医药杂志, 2013, 19(1): 41-43.
[78] 张子英, 伊乐, 爱民, 等. 肉豆蔻挥发油对大鼠心肌的保护作用 [J]. 内蒙古中医药, 2013, 32(13): 123-124.
[79] 宣丽颖, 汤文莉, 刘月英, 等. 蒙药肉豆蔻对大鼠心律失常的作用 [J]. 大家健康: 学术版, 2015, 9(4): 34.
[80] Liu S M, Gao J H, He L H,.promotes ABCA1expression and cholesterol efflux in THP-1-derived macrophages [J]., 2021, 53(1): 63-71.
[81] Shyni G L, Sasidharan K, Francis S K,. Licarin B fromimproves insulin sensitivity via PPARγ and activation of Glut4 in the IRS-1/PI3K/Akt pathway in 3T3-L1 adipocytes [J]., 2016, 6(83): 79859-79870.
[82] Song J H, Xu X L, He S S,. Myristicin suppresses gastric cancer growth via targeting the EGFR/ERK signaling pathway [J]., 2023, 16(7): 712-724.
[83] 段春燕, 何娜娜, 朱蕾, 等. 肉豆蔻醚抑制结肠癌细胞增殖、迁移和侵袭的作用及机制研究 [J]. 世界科学技术—中医药现代化, 2020, 22(4): 907-913.
[84] Seneme E F, dos Santos D C, de Lima C A,. Effects of myristicin in association with chemotherapies on the reversal of the multidrug resistance (MDR) mechanism in cancer [J]., 2022, 15(10): 1233.
[85] Costa B P, Nassr M T, Diz F M,. Methoxyeugenol regulates the p53/p21 pathway and suppresses human endometrial cancer cell proliferation [J]., 2021, 267: 113645.
[86] 李昌红. 去氢二异丁香酚抗结肠癌的作用及机制研究 [D]. 重庆: 西南大学, 2021.
[87] 刘军. 正确理解危重病免疫功能障碍免疫与炎症的关系 [A] // 第十一届全国免疫学学术大会摘要汇编 [C]. 合肥: 中国免疫学会, 2016: 114.
[88] Rashidian G, Shahin K, Elshopakey G E,. The dietary effects of nutmeg () extract on growth, hematological parameters, immunity, antioxidant status, and disease resistance of common carp () against[J]., 2022, 10(3): 325-325.
[89] 宗伟英, 肖功胜, 李世升, 等. 肉豆蔻提取物的抗痛风作用研究 [J]. 世界最新医学信息文摘, 2016, 16(12): 124-125.
[90] Lee J Y, Park W. Anti-inflammatory effect of myristicin on RAW264.7 macrophages stimulated with polyinosinic-polycytidylic acid [J]., 2011, 16(8): 7132-7142.
[91] Checker R, Chatterjee S, Sharma D,. Immunomodulatory and radioprotective effects of lignans derived from fresh nutmeg mace () in mammalian splenocytes [J]., 2008, 8(5): 661-669.
[92] Qiburi Q, Temuqile T, Baigude H. Synergistic regulation of microglia gene expression by natural molecules in herbal medicine [J]., 2021, 2021: 9920364.
[93] 肖俊勇, 李力, 从仁怀, 等. 多指标综合评定肉豆蔻挥发油缓解慢性炎性疼痛的谱效关系 [J]. 医药导报, 2019, 38(10): 1264-1271.
[94] Hayfaa A A S, Sahar A M A S, Awatif M A S. Evaluation of analgesic activity and toxicity of alkaloids inseeds in mice [J]., 2013, 6: 611-615.
[95] Abutaha N, Al-Keridis L A, Ali El Hadi Mohamed R,. Potency and selectivity indices ofHoutt. mace chloroform extract against non-clinical and clinical human pathogens [J]., 2021, 19(1): 1096-1107.
[96] Oo T, Saiboonjan B, Srijampa S,. Inhibition of bacterial efflux pumps by crude extracts and essential oil fromHoutt. (nutmeg) seeds against methicillin-resistant[J]., 2021, 26(15): 4662.
[97] 蒋鸣. 肉豆蔻挥发油抑菌作用研究 [J]. 中国调味品, 2021, 46(1): 63-66.
[98] Nu T T, Htun A A, Ngwe D H,. Evaluation of antibacterial activity and isolation of some organic constituents from seed ofHott. (ZADEIK-PO) [J]., 2020, 1A(XVIII): 293-301.
[99] Devi K P, Sakthivel R, Nisha S A,. Eugenol alters the integrity of cell membrane and acts against the nosocomial pathogen[J]., 2013, 36(3): 282-292.
[100] Buru A S, Neela V K, Mohandas K,. Microarray analysis of the genomic effect of eugenol on methicillin-resistant[J]., 2022, 27(10): 3249.
[101] Veerendrakumar S P, Gayathri R, Priya V V,. Evaluation of antioxidant and protease-inhibitory potential of ethanolic extract of(nutmeg) [J]., 2021: 263-270.
[102] 马可, 南星梅, 苏姗姗, 等. 肉豆蔻挥发油对低氧诱导肺动脉平滑肌细胞增殖的抑制作用及其抗氧化活性 [J]. 中国药理学与毒理学杂志, 2018, 32(7): 535-542.
[103] 卓微伟, 李凤, 胡君. 响应面法优化超声辅助提取肉豆蔻总黄酮工艺及其抗氧化活性研究 [J]. 食品研究与开发, 2021, 42(19): 126-133.
[104] Li C W, Chu Y C, Huang C Y,. Evaluation of antioxidant and anti-α-glucosidase activities of various solvent extracts and major bioactive components from the seeds of[J]., 2020, 25(21): 5198.
[105] Shanu H, Maansi V, Joshi Rajesh K,. Anti-melanogenic activity ofextract againstusing phenotypic based screening [J]., 2020, 20(1): 67.
[106] Ogawa K, Ito M. Appetite-enhancing effects of nutmeg oil and structure-activity relationship of habituation to phenylpropanoids [J]., 2019, 73(3): 513-522.
[107] Zhang J L, Si H F, Lv K,. Licarin-B exhibits activity against theRH strain by damaging mitochondria and activating autophagy [J]., 2021, 9: 684393.
[108] 马可, 南星梅, 赵婧, 等. 肉豆蔻的药理和毒理作用研究进展 [J]. 中药药理与临床, 2022, 38(1): 218-224.
[109] 张勇, 张娟娟, 康文艺, 等. 肉豆蔻属植物化学成分和药理活性研究进展 [J]. 中国中药杂志, 2014, 39(13): 2438-2449.
[110] Oseni O, Olagboye S, Idowu A. Potassium bromate induced renal toxicity in wistar albino rats: Effects of aqueous extract of nutmeg (Houtt) [J]., 2015, 5(12): 1547-1556.
[111] Khalil A S M, Giribabu N, Yelumalai S,. Myristic acid defends against testicular oxidative stress, inflammation, apoptosis: Restoration of spermatogenesis, steroidogenesis in diabetic rats [J]., 2021, 278: 119605.
[112] Duarte D, Mendonça M, Ramos L. The psychoactive power of foods: A case of acute nutmeg intoxication [J]., 2021, 34(4): 298-300.
[113] Muchtaridi, Subarnas A, Apriyantono A,. Identification of compounds in the essential oil of nutmeg seeds (Houtt.) that inhibit locomotor activity in mice [J]., 2010, 11(11): 4771-4781
[114] Zhu X, Wang Y K, Yang X N,. Metabolic activation of myristicin and its role in cellular toxicity [J]., 2019, 67(15): 4328-4336.
[115] Demetriades A K. Low cost, high risk: Accidental nutmeg intoxication [J]., 2005, 22(3): 223-225.
[116] 宋祖强, 仝巧云, 龚勇. 联合应用美沙拉嗪和四神片治疗溃疡性结肠炎的疗效分析 [J]. 中国社区医师: 医学专业, 2013, 29(19): 73.
[117] 查列. 双歧三联活菌胶囊联合四神片治疗慢性功能性便秘87例 [J]. 中国乡村医药, 2013, 20(1): 41.
[118] 王晶晶, 覃红英, 宋晓东. 匹维溴铵联合四神片治疗肠易激综合征的临床观察 [J]. 中国民族民间医药, 2009, 18(17): 131.
[119] 张君芳. 肉豆蔻粉敷脐治疗骨科患者术后腹胀便秘效果观察 [J]. 中国乡村医药, 2014, 21(16): 56-57.
[120] 多杰措, 杨桑加. 藏医煳儿灸联合油脂涂擦治疗神经性呕吐的临床体会 [J]. 中国民族医药杂志, 2014, 20(1): 8-9.
[121] 张光茹, 陈秋红. 金诃愈心冲剂防治高脂血症的实验研究 [J]. 上海中医药杂志, 2003, 37(9): 59-60.
[122] 巴亚玛, 纳顺达来. 蒙药肉豆蔻五味丸治疗窦性心动过缓临床疗效观察 [J]. 中国民族医药杂志, 2015, 21(8): 8-10.
[123] 索朗平措. 藏药三味肉豆蔻汤剂治疗50例隆思病临床疗效分析 [J]. 中国民族医药杂志, 2015, 21(6): 16.
[124] 中国科学院中国植物志编辑委员会. 中国植物志-第二十七卷 [M]. 北京: 科学出版社, 1979: 194.
[125] 王远志, 李坤, 贾天柱. 肉豆蔻与长形肉豆蔻挥发油成分GC-MS比较分析 [J]. 吉林医药学院学报, 2008, 29(2): 85-87.
[126] 林杰, 卢金清, 江汉美, 等. 春、冬季采收肉豆蔻中挥发性成分分析 [J]. 中国调味品, 2017, 42(3): 118-120.
[127] 黄鑫, 杨秀伟. 不同炮制品肉豆蔻挥发油成分的GC-MS分析 [J]. 中国中药杂志, 2007, 32(16): 1669-1675.
[128] 耿媛媛, 胡昌江, 潘新, 等. GC-MS分析炮制对二神丸中挥发性成分的影响 [J]. 中成药, 2014, 36(10): 2148-2151.
[129] 胡娜, 刘欢, 袁子民, 等. 肉豆蔻制霜新工艺优选及质量评价 [J]. 中国实验方剂学杂志, 2013, 19(21): 10-12.
[130] 贾天柱, 袁昌鲁, 曹克慧, 等. 肉豆蔻不同炮制品挥发油中肉豆蔻醚、黄樟醚的薄层扫描测定 [J]. 中国中药杂志, 1991, 16(5): 275-278.
[131] 袁子民, 刘欢, 王静. 肉豆蔻及炮制品醇提取物的止泻及抗炎作用研究 [J]. 时珍国医国药, 2015, 26(12): 2910-2911.
[132] 傅睿. 中药药性理论辛味功效及物质基础研究思路初探 [J]. 亚太传统医药, 2014, 10(9): 55-56.
[133] 周复辉, 易增兴, 罗亨凡. 辛味中药化学成分的分析 [J]. 安徽农业科学, 2006, 34(12): 2760.
[134] 李瑞奇, 苗明三. 药性温的现代研究及相互关系 [J]. 中医学报, 2012, 27(11): 1456-1459.
[135] 朱琳, 李永芳, 李向阳. 藏药八味沉香散的有效成分及药理作用研究进展 [J]. 中国民族民间医药, 2019, 28(14): 73-76.
[136] 其布日. 额尔敦-乌日勒的活性成分分析及其对小胶质细胞基因调控作用的研究 [D]. 呼和浩特: 内蒙古大学, 2021.
[137] 朱琳. 藏药八味沉香散抗心肌缺血再灌注损伤作用的药效物质基础研究 [D]. 西宁: 青海大学, 2020.
[138] 高家荣, 杨晓旭, 魏良兵, 等. 补骨脂、肉豆蔻配伍前后特征指纹图谱及指标成分含量变化研究 [J]. 中药材, 2014, 37(10): 1873-1876.
[139] 高家荣, 徐双枝, 韩燕全, 等. 补骨脂-肉豆蔻药对配伍前后主要成分的UPLC-MS/MS测定及药代动力学研究 [J]. 中国中药杂志, 2017, 42(9): 1782-1786.
[140] 仁增加, 万玛措, 李啟恩, 等. 基于网络药理学和分子对接的藏药五味肉豆蔻方干预新型冠状病毒肺炎(COVID-19) 的作用机制研究 [J]. 高原科学研究, 2020, 4(3): 71-83.
[141] 赵祥升, 黄立标, 杨海建, 等. GC法同时测定肉豆蔻中丁香酚、异丁香酚、肉豆蔻醚和榄香脂素的含量 [J]. 药物分析杂志, 2012, 32(9): 1569-1573.
[142] 李志平, 王加良, 张艳丽, 等. 一测多评法同时测定九味沉香胶囊中9种成分 [J]. 中成药, 2020, 42(5): 1129-1134.
[143] Götz M E, Sachse B, Schäfer B,. Myristicin and elemicin: Potentially toxic alkenylbenzenes in food [J]., 2022, 11(13): 1988.
Research progress on chemical composition and pharmacological effects ofand predictive analysis on its quality marker
LIU Run-run1, SUN Ai-qing2, YU Xiao-jun1, HE Meng-yuan1, XIE He-bing3, GAO Peng4, CONG Zhu-feng1,2
1. College of Pharmacy, Shandong University of Traditional Chinese Medicine, Jinan 250355, China 2. The Affiliated Cancer Hospital, Shandong First Medical University, Jinan 250117, China 3. Tibet God Monkey Pharmaceutical Co., Ltd., Shigatse 330006, China 4. Institute of Pharmaceutical Research, Shandong University of Traditional Chinese Medicine, Jinan 250355, China
Roudoukou () is a commonly used medicine and food homologous traditional Chinese medicine, which has the effects of warming the middle and moving, astringing the intestines and checking diarrhea. Its chemical components mainly include lignans, volatile oils and polyphenols.has the pharmacological effects of regulating the digestive system, anti-cancer, anti-inflammatory and analgesic, antibacterial and antioxidant, etc. This paper reviews its chemical constituents, pharmacological effects, toxicity studies and clinical applications. According to the concept of quality marker (Q-Marker) of traditional Chinese medicine, Q-Markers ofwas predicted from plant affinity, collecting periods and processing methods, efficacy, medicinal properties, compatibility, and chemical component measurability. It was preliminarily predicted that dehydrodiisoeugenol, myristicin, macelignan, methoxyeugenol, elementin, eugenol and α-pinene were the possible Q-Marker, to provid a reference for the quality evaluation and drug development of.
; quality marker; dehydrodiisoeugenol; myristicin; macelignan; methoxyeugenol; elementin; eugenol; α-pinene
R285
A
0253 - 2670(2023)14 - 4682 - 19
10.7501/j.issn.0253-2670.2023.14.029
2022-12-02
中央引导地方科技发展专项:二十味肉豆蔻丸品质提升及二次开发研究(YDZX2021083-04)
刘润润(1999—),女,硕士研究生,研究方向为中药制剂学。E-mail: liurunrun2022@163.com
高 鹏(1978—),教授,博士生导师,从事中药创新药物现代研究。E-mail: gaopeng@sdutcm.edu.cn
丛竹凤(1978—),医学硕士,副主任药师,执业药师,从事创新药物开发研究。E-mail: congzhufeng@163.com
[责任编辑 赵慧亮]

