洋紫荆的化学成分研究
梁 蒙,王亚凤,李小梅,何瑞杰,谢桃结,阳丙媛,朱鸿杰,黄永林*
洋紫荆的化学成分研究
梁 蒙1, 2,王亚凤1,李小梅1,何瑞杰1,谢桃结3,阳丙媛1,朱鸿杰3,黄永林1*
1. 广西壮族自治区中国科学院广西植物研究所,广西植物功能物质与资源持续利用重点实验室,广西 桂林 541006 2. 桂林医学院药学院,广西 桂林 541004 3. 柳州市园林科学研究所,广西 柳州 545005
对洋紫荆的化学成分进行研究。综合利用Sephadex LH-20、Chromatorex C18、Diaion HP20SS等柱色谱分离技术进行分离纯化,并综合应用HR-ESI-MS、NMR、ECD等多种波谱方法鉴定化合物结构。从洋紫荆花的甲醇提取物中分离得到8个化合物,分别鉴定为4,6-二羟基亚环己基乙腈-8-β--葡萄糖苷(1)、-色氨酸(2)、咖啡酸甲酯(3)、对羟基苯甲酸β--吡喃葡萄糖酯苷(4)、山柰酚-3--α--鼠李糖苷(5)、山柰酚-3--β-芸香苷(6)、山柰酚-5--[α--鼠李糖基-(1→6)-β--吡喃葡萄糖苷](7)、kaempferol 3--β-glucopyranosyl (1→2)[α-rhamnopyranosyl(1→6)]- β-glucopyranoside(8)。化合物1为新化合物,命名为蝙蝠葛氰苷G,化合物2~6、8为首次从洋紫荆中分离得到。
洋紫荆;生物碱;蝙蝠葛氰苷G;咖啡酸甲酯;山柰酚-3--α--鼠李糖苷;山柰酚-3--β-芸香苷
洋紫荆L. 为豆科羊蹄甲属植物。羊蹄甲属植物全世界约600种,遍布于世界热带地区,我国有40种、4亚种、11变种,主产南部和西南部[1-2]。洋紫荆因花大而艳丽,在许多城市作为绿化树种大量栽种[3-4]。在民间,洋紫荆的根、茎皮、叶和花均有悠久的民间药用历史,茎皮可以用于治疗消化不良和急性肠胃炎,花具有清热解毒、止咳平喘、消炎等功效[5],洋紫荆花又名老白花,云南普洱当地人常采食老白花[6]。目前,对于洋紫荆花的化学成分研究相对较少,仅有廖云等[6]对洋紫荆花的化学成分进行了研究,共分离鉴定了8个化合物,以及本课题组对洋紫荆的化学成分进行了研究,共分离鉴定了14个化合物,并对部分化合物的酪氨酸酶抑制活性进行了测试,发现原儿茶酸、咖啡酸具有较好的酪氨酸酶抑制活性[7]。为了更进一步掌握洋紫荆花的物质基础,为其开发利用提供技术支撑,本实验对洋紫荆花的甲醇提取物部位进行了化学成分研究,从中分离鉴定了8个化合物,分别为4,6-二羟基亚环己基乙腈-8-β--葡萄糖苷(4,6-dihydroxycyclohexylideneacetonitrile-8-β-- glucoside,1)、-色氨酸(-tryptophan,2)、咖啡酸甲酯(methyl caffeate,3)、对羟基苯甲酸-β--吡喃葡萄糖酯苷(-hydroxybenzoyl-β-- glucopyranoside,4)、山柰酚-3--α--鼠李糖苷(kaempferol-3--α--rhamnoside,5)、山柰酚-3--β-芸香苷(kaempferol-3--β-rutidine,6)、山柰酚-5--[α--鼠李糖基-(1→6)-β--吡喃葡萄糖苷](kaempferol-5--[α--rhamnol-(1→6)-β--glucuro- noside],7)、山柰酚-3--β-葡萄糖基(1→2)[α-鼠李糖基(1→6)]-β-葡萄糖苷(kaempferol 3--β- glucopyranosyl(1→2)[α-rhamnopyranosyl(1→6)]-β- glucopyranoside,8)。化合物2~6、8均为首次从洋紫荆中分离得到,其中化合物1为新化合物,命名为蝙蝠葛氰苷G。
1 仪器与试药
Brucker Avance 500 MHz超导核磁共振波谱仪(瑞士Bruker公司);LC-MS/IT-TOF液相色谱-质谱仪(日本岛津公司);CA-1111型冷却水循环(东京理化公司);EYELAN-1300型旋转蒸发仪(东京理化公司);自动接收仪(日本Advantec公司);BS400S型精密电子天平(上海菁海仪器有限公司);电热鼓风干燥箱(上海一恒科学仪器有限公司);Sephadex LH-20(25~100 μm;GE Healthcare Bio-Science AB,Uppsala,瑞士);Chromatorex C18(Fuji Silysia Chemical公司,日本);Diaion HP20SS(Mistubishi Chemical,Tokyo,日本);MCI gel CHP 20P(75~150 μm;Mitsubishi Chemical,Tokyo,日本);GF254薄层色谱硅胶(Merck KGaA,德国);所用试剂甲醇、乙腈等均为分析纯(AR),水为纯净水。
洋紫荆花于2020年3月采自广西柳州市,经柳州市园林科学研究所刘思高级工程师鉴定为洋紫荆L.的花,凭证样品(20200318A)存放于广西植物功能物质研究与资源持续利用重点实验室。
2 提取与分离
取新鲜洋紫荆花33.1 kg,纯甲醇室温浸提3次,每次5 d,提取液滤过后合并,减压浓缩得到洋紫荆花浸膏1 344.9 g。洋紫荆花浸膏加水溶解后用石油醚反复萃取至无色,水溶液部分经Diaion HP20SS柱色谱(10 cm×65 cm)分离,甲醇-水(0→100%,每10%为1梯度,每梯度500 mL)为洗脱剂梯度洗脱,得到Fr. 1~7共7个组份。Fr. 3(17.7 g)经Sephadex LH-20柱色谱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱,得到8个组份Fr. 3.1~3.8。Fr. 3.1(4.7 g)经Diaion HP20SS柱色谱分离,甲醇-水(0→80%,每10%为1梯度)为洗脱剂梯度洗脱得到化合物1(43 mg)。Fr. 4(63.7 g)经MCI色谱柱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱,得到Fr. 4.1~4.5共5个组份。Fr. 4.2(7.5 g)经Chromatorex C18、Diaion HP20SS柱色谱分离,甲醇-水(0→80%,每10%为1梯度)为洗脱剂梯度洗脱得到化合物8(28 mg)。Fr. 4.3(3.4 g)经Chromatorex C18、Diaion HP20SS柱色谱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱、Sephadex LH-20柱色谱分离,乙醇-水(100%→0,每10%为1梯度)为洗脱剂梯度洗脱分离纯化得到化合物2(78 mg)、4(22 mg)。Fr. 7(4.2 g)经Sephadex LH-20柱色谱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱,得到Fr. 7.1~7.3共3个组份。Fr. 7.1(2.5 g)经Diaion HP20SS、Sephadex LH-20柱色谱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱,经过TLC检测,分别合并相同流分得到化合物3(32 mg)、5(34 mg)。Fr. 7.3(0.4 g)经Diaion HP20SS柱色谱分离,甲醇-水(0→100%,每10%为1梯度)为洗脱剂梯度洗脱,经过TLC检测,分别合并相同流分得到化合物6(42 mg)、7(42 mg)。
3 糖绝对构型的确定
参照Tanaka等[8]的方法对化合物1中糖的绝对构型进行确定。精确称取样品1.0 mg,加入0.6 mL 0.5 mol/L盐酸,在90 ℃下反应2 h使其充分水解,加入阴离子交换树脂IRA 400调至中性,过滤除去树脂,将滤液减压浓缩后真空干燥,向滤液残渣中加入含有1.0 mg-半胱氨酸甲酯盐酸盐的吡啶溶液0.2 mL,在60 ℃下反应1 h,再向反应物中加入含有1.0 mg邻甲苯异硫氰酸酯的吡啶溶液0.2 mL,于60 ℃下反应1 h,即得到样品中糖部分的衍生物,糖标准品以相同条件衍生化。分别取相同体积的样品糖部分的衍生物与对照品衍生物,在柱温箱温度40 ℃下,以25%乙腈-水作为流动相,254 nm作为检测波长,0.8 mL/min的体积流量于高效液相色谱进行分析,通过对比保留时间,确定糖的绝对构型。
4 计算ECD
对化合物1的ECD计算实验包括构象分析、计算和图谱拟合3个步骤。首先利用ChemDraw 3D对化合物进行能量最小化操作,得到初始构象;接着采用Spartan's 10软件进行优势构象搜索,选取玻尔兹曼-总体大于5%的构象进行ECD计算,然后利用CPCM极化导体计算模型对MeOH中B3LYP/6-31+g(d,p)水平的构象进行初始优化;采用时间依赖密度泛函理论(TD-DFT)对化合物18b的所有构象在B3LYP/6-311+g(d,p)水平在MeOH中进行ECD的理论计算,共计算了50种激发态的旋转强度,再使用程序SpecDis 1.6(维尔茨堡大学,德国)和GraphPad Prism 5(加利福尼亚大学圣迭戈分校,美国)从偶极长旋转强度中应用sigma=0.3 eV的高斯带形状生成ECD光谱图,生成图谱与化合物的实验图谱比较,确定化合物的绝对构型。
5 结构鉴定
化合物1:白色粉末,易溶于甲醇;根据高分辨率质谱HR-ESI-MS显示分子离子峰为/: 376.124 4 [M+HCOO]−(计算值376.124 9),化合物分子式为C14H21NO8,不饱和度为5。化合物1的13C-NMR谱显示出特征性的α, β-不饱和丁腈信号[C117.5(C-1)][9]。在化合物1的1H-和13C-NMR谱中显示1个六碳糖并通过β-糖苷键连接到苷元上[H4.35 (1H, d,= 7.8 Hz, H-1′);C104.3 (C-1′),77.9 (C-2′),77.4 (C-3′),74.6 (C-4′),71.1 (C-5′), 62.2 (C-6′)]。通过衍生化反应,将化合物1糖部分的衍生物与-葡萄糖标准品衍生物通过高效液相色谱检测,出峰时间一致(R=18.76 min),从而确定化合物中葡萄糖的绝对构型为构型。在化合物的1H-NMR中,除糖基外,还存在3个次甲基氢信号H4.82 (1H, m, H-4), 4.14 (1H, m, H-6), 4.91 (1H, m, H-8),2个亚甲基氢信号H2.16 (1H, brd,= 11.8 Hz, H-5a), 1.56 (1H, brt,= 11.8 Hz, H-5b), 2.26 (1H, brd,= 14.9 Hz, H-7a), 1.77 (1H, brd,= 14.9 Hz, H-7b),通过1H-1H COSY及HSQC谱图分析可知,C-4至C-8的链接方式为-CH(O)-CH2-CH(O)- CH2-CH(O)-。剩下的次甲基信号[H5.56 (1H, s, H-2),C92.7 (C-2)] 和季碳[C169.5 (C-32)] 类似于menisdaurin的氰乙烯基[10]。经与文献对比,化合物1与从木榄属木榄植物中分离得到的menisdaurin D核磁共振数据非常相似,与化合物menisdaurin D相比,化合物1少了1个亚甲基质子信号,多了1个连氧次甲基碳氢信号[C66.5 (C-4),H4.82 (1H, m, H-4)],推测该化合物可能为menisdaurin D中的亚甲基被氧化成连氧次甲基,HMBC谱图中显示H-2与[C169.5 (C-3)、C66.5 (C-4) 和C78.5 (C-8)] 之间存在显著的长程偶联,确定了4位亚甲基被氧化成连氧次甲基,以及β-不饱和腈的位置。
最终化合物1的结构借助于二维NMR技术进行了确定,见图1。在HMBC图谱中可以观察到H-1′ (H4.35) 与C-8 (C78.5)、H-8 (H4.91) 与C-1′ (C104.3)/C-2 (C92.7)/C-3 (C169.5)/C-6 (C67.2)/C-7 (C38.2)、H-2 (H5.56) 与C-1 (C117.5)/C-3 (C169.5)/C-4 (C66.5)/C-8 (C78.5)、H-4 (H4.82) 与C-2 (C92.7)/C-3 (C169.5)/C-5 (C44.5) 远程相关,提示化合物的平面结构见图1。

图1 化合物1的结构及关键HMBC (→) 和1H-1H COSY (▬) 相关图谱
在NOESY谱图中发现H-4、H-6和H-8相互间均存在NOE相关信号,说明H-4、H-6和H-8在同侧,进一步通过计算ECD的方法,确定化合物1的绝对构型为4, 6,8(图2)。最终化合物1的结构鉴定为4,6-二羟基亚环己基乙腈-8-β--葡萄糖苷(图1),经Sci-finder检索为1个新化合物,命名为蝙蝠葛氰苷G。核磁数据见表1。
化合物2:白色结晶(甲醇);1H-NMR (500 MHz, DMSO-6): 11.08 (1H, s, NH), 7.58 (1H, d,= 8.0 Hz, H-4), 7.35 (1H, d,= 8.0 Hz, H-7), 7.24 (1H, s, H-2), 7.06 (1H, t,= 7.6 Hz, H-6), 6.96 (1H, t,= 7.6 Hz, H-5), 3.51 (1H, dd,= 4.0, 8.7 Hz, H-11), 3.31 (1H, dd,= 4.0, 15.0 Hz, H-10a), 2.99 (1H, dd,= 8.7, 15.0 Hz, H-10b);13C-NMR (125 MHz, DMSO-6): 124.3 (C-2), 109.5 (C-3), 118.3 (C-4), 118.5 (C-5), 120.9 (C-6), 111.4 (C-7), 136.4 (C-8), 127.4 (C-9), 27.1 (C-10), 54.8 (C-11), 170.6 (COOH)。以上数据与文献报道基本一致[11],鉴定化合物2为-色氨酸。
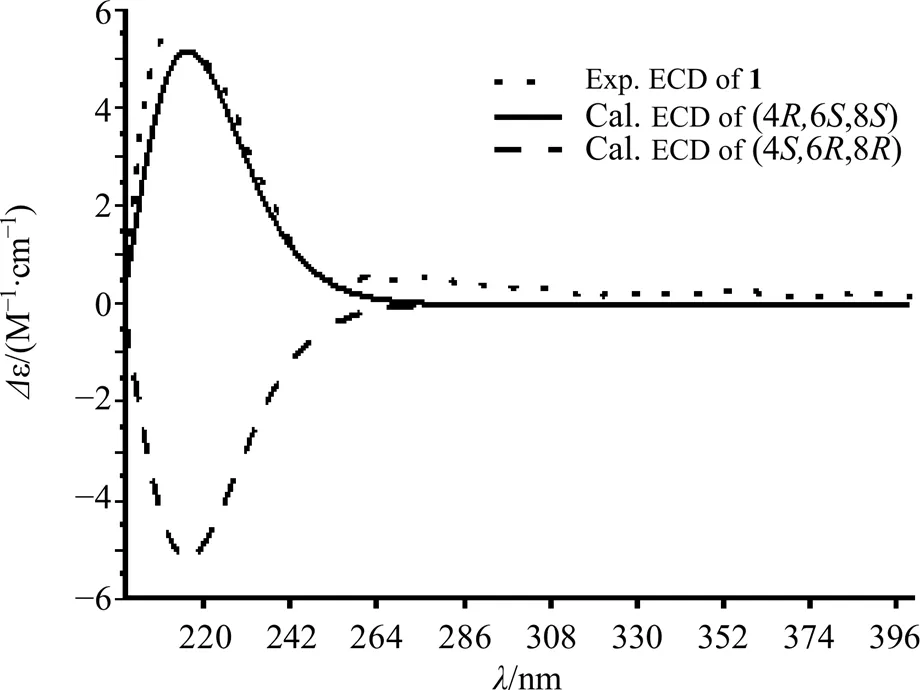
图2 化合物1的实验ECD和计算ECD图谱
表1 化合物1的1H-NMR (500 MHz) 和13C-NMR (125 MHz) 数据(CD3OD)
Table 1 1H-NMR (500 MHz) and 13C-NMR (125 MHz) data of compound 1 (CD3OD)
碳位δHδC 1 117.5 25.56 (1H, s)92.7 3 169.5 44.82 (1H, m)66.5 52.16 (1H, brd, J = 11.8 Hz)44.5 1.56 (1H, brt, J = 11.8 Hz) 64.14 (1H, m)67.2 72.26 (1H, brd, J = 14.9 Hz)38.2 1.77 (1H, brd, J = 14.9 Hz) 84.91 (1H, m)78.5 Glu-1′4.35 (1H, d, J = 7.8 Hz)104.3 2′3.16 (1H, m)74.6 3′3.31 (1H, m)77.4 4′3.30 (1H, m)71.1 5′3.19 (1H, m)77.9 6′3.77 (1H, d, J = 11.8 Hz)62.2 3.64 (1H, dd, J = 11.8, 4.3 Hz)
化合物3:白色针晶(甲醇);1H-NMR (500 MHz, CD3OD): 7.52 (1H, d,= 16.0 Hz, H-7), 7.03 (1H, d,= 2.0 Hz, H-2), 6.94 (1H, dd,= 2.0, 8.2 Hz, H-6), 6.76 (1H, d,= 8.2 Hz, H-5), 6.24 (1H, d,= 16.0 Hz, H-8), 3.75 (3H, s, -OCH3);13C-NMR (125 MHz, CD3OD): 127.7 (C-1), 115.1 (C-2), 146.8 (C-3), 149.5 (C-4), 122.9 (C-5), 116.5 (C-6), 146.9 (C-7), 114.8 (C-8), 169.8 (C-9), 52.0 (-OCH3)。与文献报道对照基本一致[12-13],故鉴定化合物3为咖啡酸甲酯。
化合物4:白色无定形粉末;1H-NMR (500 MHz, CD3OD): 8.04 (2H, d,= 8.9 Hz, H-2, 6), 6.99 (2H, d,= 8.9 Hz, H-3, 5), 5.69 (1H, t,= 7.5 Hz, H-1′), 3.87 (1H, dd,= 2.1, 12.1 Hz, H-6′a), 3.86 (3H, s, -OCH3), 3.71 (1H, dd,= 4.9, 12.1 Hz, H-6′b), 3.42~3.52 (4H, m, H-2′~5′);13C-NMR (125 MHz, CD3OD): 167.5 (C-1), 114.9 (2C, C-2, 6), 133.1 (2C, C-3, 5), 122.7 (C-4), 96.0 (C-1′), 74.0 (C-2′), 78.0 (C-3′), 71.1 (C-4′), 78.7 (C-5′), 62.3 (C-6′), 166.7 (-COO)。以上数据与文献报道基本一致[14],鉴定化合物4为对羟基苯甲酸β--吡喃葡萄糖酯苷。
化合物5:浅黄色无定形粉末;1H-NMR (500 MHz, CD3OD): 7.76 (2H, d,= 8.4 Hz, H-2′, 6′), 6.94 (2H, d,= 8.4 Hz, H-3′, 5′), 6.37 (1H, d,= 2.0 Hz, H-8), 6.20 (1H, d,= 2.0 Hz, H-6), 5.39 (1H, d,= 1.6 Hz, H-1′′), 4.25 (1H, s, H-2′′), 3.74 (1H, m, H-3′′), 3.33~3.35 (2H, m, H-4′′, 5′′), 0.94 (3H, d,= 5.8 Hz, H-6′′);13C-NMR (125 MHz, CD3OD): 158.5 (C-2), 136.2 (C-3), 179.5 (C-4), 161.5 (C-5), 99.8 (C-6), 165.8 (C-7), 94.7 (C-8), 163.1 (C-9), 105.9 (C-10), 122.6 (C-1′), 131.9 (2C, C-2′, 6′), 116.5 (2C, C-3′, 5′), 159.2 (C-4′), 103.4 (C-1′′), 71.9 (C-2′′), 72.2 (C-3′′), 73.2 (C-4′′), 72 (C-5′′), 17.6 (C-6′′)。以上数据与文献报道基本一致[15],鉴定化合物5为山柰酚- 3--α--鼠李糖苷。
化合物6:浅黄无定形粉末;1H-NMR (500 MHz, CD3OD): 8.10 (2H, d,= 8.8 Hz, H-2′, 6′), 6.89 (2H, d,= 8.8 Hz, H-3′, 5′), 6.39 (1H, d,= 2.0 Hz, H-8), 6.20 (1H, d,= 2.0 Hz, H-6), 5.05 (1H, d,= 7.8 Hz, H-1′′), 4.54 (1H, brs, H-1′′′), 1.14 (1H, d,= 6.5 Hz, H-6′′′);13C-NMR (125 MHz, CD3OD): 158.5 (C-2), 135.7 (C-3), 179.6 (C-4), 162.9 (C-5), 100.0 (C-6), 166.0 (C-7), 94.9 (C-8), 159.4 (C-9), 105.6 (C-10), 122.6 (C-1′), 132.5 (2C, C-2′, 6′), 116.1 (2C, C-3′, 5′), 161.5 (C-4′), 105.5 (C-1′′), 75.0 (C-2′′), 77.2 (C-3′′), 70.1 (C-4′′), 75.3 (C-5′′), 67.4 (C-6′′), 101.9 (C-1′′′), 72.3 (C-2′′′), 72 (C-3′′′), 73.9 (C-4′′′), 69.7 (C-5′′′), 18.0 (C-6′′′)。以上数据与文献报道基本一致[15],鉴定化合物6为山柰酚-3--β-芸香苷。
化合物7:浅黄无定形粉末;1H-NMR (500 MHz, CD3OD): 8.07 (2H, d,= 8.9 Hz, H-2′, 6′), 6.89 (2H, dd,= 8.9 Hz, H-3′, 5′), 6.39 (1H, dd,= 2.0 Hz, H-8), 6.20 (1H, d,= 2.0 Hz, H-6), 5.13 (1H, d,= 7.5 Hz, H-1′′), 4.54 (1H, brs, H-1′′′), 1.20 (1H, d,= 6.5 Hz, H-6′′′);13C-NMR (125 MHz, CD3OD): 159.4 (C-2), 135.5 (C-3), 179.4 (C-4), 166.0 (C-5), 100.0 (C-6), 163.0 (C-7), 94.9 (C-8), 158.5 (C-9), 105.6 (C-10), 122.6 (C-1′), 132.4 (2C, C-2′, 6′), 116.1 (2C, C-3′, 5′), 161.5 (C-4′), 104.6 (C-1′′), 75.0 (C-2′′), 78.1 (C-3′′), 71.4 (C-4′′), 75.7 (C-5′′), 68.7 (C-6′′), 101.9 (C-1′′′), 72.0 (C-2′′′), 72.3 (C-3′′′), 73.9 (C-4′′′), 69.7 (C-5′′′), 17.9 (C-6′′′)。以上数据与文献报道基本一致[16-17],鉴定化合物7为山柰酚-5--[α--鼠李糖基-(1→6)-β--吡喃葡萄糖苷]。
化合物8:浅黄色无定形粉末;1H-NMR (500 MHz, CD3OD): 8.02 (2H, d,= 8.6 Hz, H-2′, 6′), 6.92 (2H, d,= 8.6 Hz, H-3′, 5′), 6.38 (1H, d,= 2.1 Hz, H-8), 6.17 (1H, d,= 2.1 Hz, H-6), 5.35 (1H, d,= 7.6 Hz, H-1″), 4.83 (1H, d,= 7.8 Hz, H-1″′), 4.50 (1H, d,= 1.4 Hz, H-1″″), 1.11 (2H, d,= 6.5 Hz, H-6″″);13C-NMR (125 MHz, CD3OD): 159.3 (C-2), 134.7 (C-3), 179.3 (C-4), 162.3 (C-5), 99.9 (C-6), 165.7 (C-7), 94.9 (C-8), 158.3 (C-9), 105.6 (C-10), 122.9 (C-1′), 132.3 (2C, C-2′, 6′), 116.1 (2C, C-3′, 5′), 161.2 (C-4′), 101.1 (C-1′′), 81.5 (C-2′′), 77.7 (C-3′′), 71.1 (C-4′′), 76.6 (C-5′′), 68.2 (C-6′′′), 104.1 (C-1′′′), 75.1 (C-2′′′), 77.6 (C-3′′′), 71.3 (C-4′′′), 78.1 (C-5′′′), 62.4 (C-6′′′), 102.0 (C-1′′′′), 71.9 (C-2′′′′), 72.2 (C-3′′′′), 73.8 (C-4′′′′), 69.6 (C-5′′′′), 17.8 (C-6′′′′)。以上数据与文献报道基本一致[18],鉴定化合物8为kaempferol 3--β-glucopyranosyl(1→2)[α-rhamno- pyranosyl(1→6)]-β-glucopyranoside。
6 讨论
洋紫荆在民间药用历史悠久,具有清热解毒、止咳平喘、消炎等功效,值得进行深入研究。本研究从洋紫荆花甲醇提取物中分离得到8个化合物,化合物2~6、8均为首次从洋紫荆中分离得到,其中化合物1为新化合物,结构类型涉及生物碱、酚酸和黄酮类。研究为洋紫荆花的进一步开发利用奠定了基础,同时也增加了对洋紫荆所含物质基础的认知。
利益冲突 所有作者均声明不存在利益冲突
[1] Huang P L, Sun Y, Chen H C,. Proteolytic fragments of anti-HIV and anti-tumor proteins MAP30 and GAP31 are biologically active [J]., 1999, 262(3): 615-623.
[2] Jyoti, Samant S S, Kamal K,. Diversity, distribution, indigenous uses and conservation prioritization of the economically important floristic diversity in Nadaun Block of Hamirpur District, Himachal Pradesh [J]., 2014, 6(7): 522-540.
[3] Sahu G, Gupta P K. A review onLinn [J]., 2012, 3 (1): 48-51.
[4] Singh K, Singh D, Singh V. Multidimensional uses of medicinal plant kachnar (linn.) [J]., 2016, 4: 58-72.
[5] Katre N V. Immunogenicity of recombinant IL-2 modified by covalent attachment of polyethylene glycol [J]., 1990, 144(1): 209-213.
[6] 廖云, 李蓉涛. 洋紫荆(L.) 花的化学成分研究 [J]. 天然产物研究与开发, 2013, 25(5): 634-636.
[7] 梁蒙, 王亚凤, 谢桃结, 等. 洋紫荆粉色花的化学成分及其酪氨酸酶抑制活性研究 [J]. 林产化学与工业, 2022, 42(4): 68-74.
[8] Tanaka T, Nakashima T, Ueda T,. Facile discrimination of aldose enantiomers by reversed-phase HPLC [J]., 2007, 55(6): 899-901.
[9] Ueda K, Yasutomi K, Mori I. Structure of a new cyanoglucoside fromLoesn. [J]., 1983, 12(1): 149-150.
[10] Yi X X, Deng J G, Gao C H,. Four new cyclohexylideneacetonitrile derivatives from the hypocotyl of mangrove () [J]., 2015, 20(8): 14565-14575.
[11] 李国强, 邓志威, 李军, 等. 海星的化学成分研究(英文) [J]. 中国药学: 英文版, 2004, 13(2): 81-86.
[12] 宋亚玲, 王红梅, 倪付勇, 等. 金银花中酚酸类成分及其抗炎活性研究 [J]. 中草药, 2015, 46(4): 490-495.
[13] 林建斌, 赵立春, 郭建忠, 等. 金荞麦地上部分化学成分的研究 [J]. 中草药, 2016, 47(11): 1841-1844.
[14] 尚小雅, 李冲, 张承忠, 等. 藏药五脉绿绒蒿中非生物碱成分 [J]. 中国中药杂志, 2006, 31(6): 468-471.
[15] 方伟, 阮金兰, 王仲, 等. 斜方复叶耳蕨的化学成分研究 [J]. 中国中药杂志, 2008, 33(6): 649-650.
[16] Siddiqui B S, Khatoon N, Begum S,. Flavonoid and cardenolide glycosides and a pentacyclic triterpene from the leaves ofand evaluation of cytotoxicity [J]., 2012, 77(1): 238-244.
[17] Kazuma K, Noda N, Suzuki M. Malonylated flavonol glycosides from the petals of[J]., 2003, 62(2): 229-237.
[18] Kite G C, Veitch N C, Boalch M E,. Flavonol tetraglycosides from fruits of(Leguminosae) and the authentication ofand[J]., 2009, 70(6): 785-794.
Chemical constituents from
LIANG Meng1, 2, WANG Ya-feng1, LI Xiao-mei1,HE Rui-jie1, XIE Tao-jie3, YANG Bing-yuan1,ZHU Hong-jie3, HUANG Yong-lin1
1. Guangxi Key Laboratory of Plant Functional Phytochemicals and Sustainable Utilization, Guangxi Institute of Botany, Guangxi Zhuang Autonomous Region and Chinese Academy of Sciences, Guilin 541006, China 2. Guilin Medical University, School of Pharmacy, Guilin 541004, China 3. Liuzhou Institute of Gardening, Liuzhou 545005, China
To investigate the chemical constituents ofThe methanol extract of flowers ofwas isolated and purified by column chromatographies with Sephadex LH-20, Chromatorex C18, Diaion HP20SS. And their structures were identified by various spectroscopic methods, such as HR-ESI-MS, NMR, ECD, et al.A total of eight compounds were isolated from the extract of flowers ofTheir structures were identified as4,6- dihydroxycyclohexylideneacetonitrile-8-β--glucoside (1),-tryptophan (2), methyl caffeate (3),-hydroxybenzoyl-β-- glucopyranoside (4), kaempferol-3--α--rhamnoside (5), kaempferol-3--β-rutidine (6), kaempferol-5--[α--rhamnol-(1→6)- β--glucuronoside] (7), kaempferol 3--β-glucopyranosyl(1→2)[α-rhamnopyranosyl(1→6)]-β-glucopyranoside (8).Compound 1 is a new compound named menisdaurin G. Compounds 2—6 and 8 were obtained from the plant for the first time.
L.; alkaloids; menisdaurin G; methyl caffeate; kaempferol-3--α--rhamnoside; kaempferol-3--β- rutidine
R284.1
A
0253 - 2670(2023)14 - 4427 - 06
10.7501/j.issn.0253-2670.2023.14.003
2023-03-16
柳州市科技攻关项目(2019B0801b006);国家自然科学基金项目(82060764);广西科学院基本科研业务费项目(CQZ-C-1901);桂林市创新平台与人才计划项目(20210102-3)
梁 蒙,硕士研究生。E-mail: 532226735@qq.com
黄永林,研究员,博士,研究方向为天然产物化学及开发利用研究。E-mail: hyl@gxib.cn
[责任编辑 王文倩]

