猫爪草中的1个新呋喃倍半萜
张露丹,龙玉娇,王瑞沣,曹亚男,范小勇,邹 坤,王 慧*
•化学成分 •
猫爪草中的1个新呋喃倍半萜
张露丹1,龙玉娇1,王瑞沣1,曹亚男1,范小勇2,邹 坤1,王 慧1*
1. 三峡大学生物与制药学院 天然产物研究与利用湖北省重点实验室,湖北 宜昌 443002 2. 复旦大学附属公共卫生临床中心,上海 201508
研究猫爪草的化学成分及其体外抗结核杆菌活性。综合运用正相硅胶柱色谱、大孔树脂柱色谱、薄层色谱和高效液相色谱等多种色谱技术对猫爪草醇提物进行分离纯化,根据化合物的理化性质及其波谱数据鉴定其结构,并采用微量肉汤二倍稀释法对所得到的单体化合物进行体外抗结核杆菌活性评价。从猫爪草醇提物中分离鉴定了11个单体化合物,分别为(5)-5-[5-(furan-3-yl)-2-methyl-5-oxopentyl]-3-methylfuran-2(5)-one(1)、棕榈酸乙酯(2)、邻苯二甲酸二丁酯(3)、反式-4-羟基-2-壬烯酸(4)、亚油酸甲酯(5)、亚油酸乙酯(6)、亚油酸(7)、1--(9, 12-octadecadienoyl) glycerol(8)、烟酰胺(9)、腺苷(10)和邻苯二甲酸二甲酯(11)。体外抗结核杆菌实验结果表明,化合物1、2、4~8和10对牛型分枝杆菌BCG有较弱抑制活性,其最低抑菌浓度均为100 μg/mL。化合物1为新的呋喃倍半萜,命名为猫爪草呋喃倍半萜A,化合物4、8~11为首次从该植物中分离得到。化合物1、2、4~8和10对牛型分枝杆菌BCG有较弱抑制活性。
猫爪草;猫爪草呋喃倍半萜A;结核杆菌;烟酰胺;反式-4-羟基-2-壬烯酸;腺苷
结核病(tuberculosis,TB)是一种古老的、经空气传播的慢性感染性疾病,由结核分枝杆菌(mycobacterium tuberculosis,Mtb)引起,最常见的患病部位是肺部(即肺结核)。据世界卫生组织(World health organization,WHO)最新数据显示,2021年全球约有1060万个结核病新发病例,导致约160万人死亡,目前全球约有1/4的人口感染Mtb,结核病是严重危害人类健康的传染性疾病之一,是全球单一传染病致死的十大死亡原因之一[1]。
猫爪草是毛茛科毛茛属一年生草本植物小毛茛Thunb.的干燥块根,始载于《中药材手册》,1977年开始收载于《中国药典》,现被列为国家重点发展的3类中药材之一[2]。猫爪草的块根为主要入药部分,民间用其治疗淋巴结核。临床上猫爪草也用于治疗结核病、肿瘤和咽炎[3]。国内已有猫爪草胶囊获得生产批准,还有益肺止咳胶囊、仙鱼汤、养金护肺汤等包含猫爪草在内的复方药剂[4]。经文献调研,国内外学者已从猫爪草中分离鉴定出有机酸类、酯类、黄酮类、生物碱类、糖苷类等多种化学成分,且对猫爪草及其制剂进行了抗结核活性和临床疗效的研究[5-12]。
本研究前期采用微量肉汤二倍稀释法评价了猫爪草醇提物石油醚、醋酸乙酯和正丁醇萃取部位的体外抗结核杆菌活性,结果表明其萃取部位均对牛型分枝杆菌BCG均具有一定抑制活性,最低抑菌浓度(minimal inhibitory concentration,MIC)分别为200、100和200 μg/mL。为明确其抗结核杆菌活性成分,本课题组对猫爪草醇提物石油醚、醋酸乙酯及正丁醇萃取部位化学成分进行了系统分离,共分离得到11个化合物,分别鉴定为(5)-5-[5-(furan- 3-yl)-2-methyl-5-oxopentyl]-3-methylfuran-2(5)-one(1)、棕榈酸乙酯(ethyl palmitate,2)、邻苯二甲酸二丁酯(dibutyl phthalate,3)、反式-4-羟基-2-壬烯酸(-4-hydroxy-2-nonenoic acid,4)、亚油酸甲酯(methyl linoleate,5)、亚油酸乙酯(ethyl linoleate,6)、亚油酸(linoleic acid,7)、1--(9,12- octadecadienoyl) glycerol(8)、烟酰胺(niacinamide,9)、腺苷(β-adenosine,10)和邻苯二甲酸二甲酯(dimethyl phthalate,11),结构见图1。化合物1为新的呋喃倍半萜,命名为猫爪草呋喃倍半萜A;化合物4、8~11为首次从该植物中分离得到。对单体化合物进行体外抗结核杆菌活性评价,实验结果显示,化合物1、2、4~8和10对牛型分枝杆菌BCG有较弱抑制活性,其MIC均为100 μg/mL。
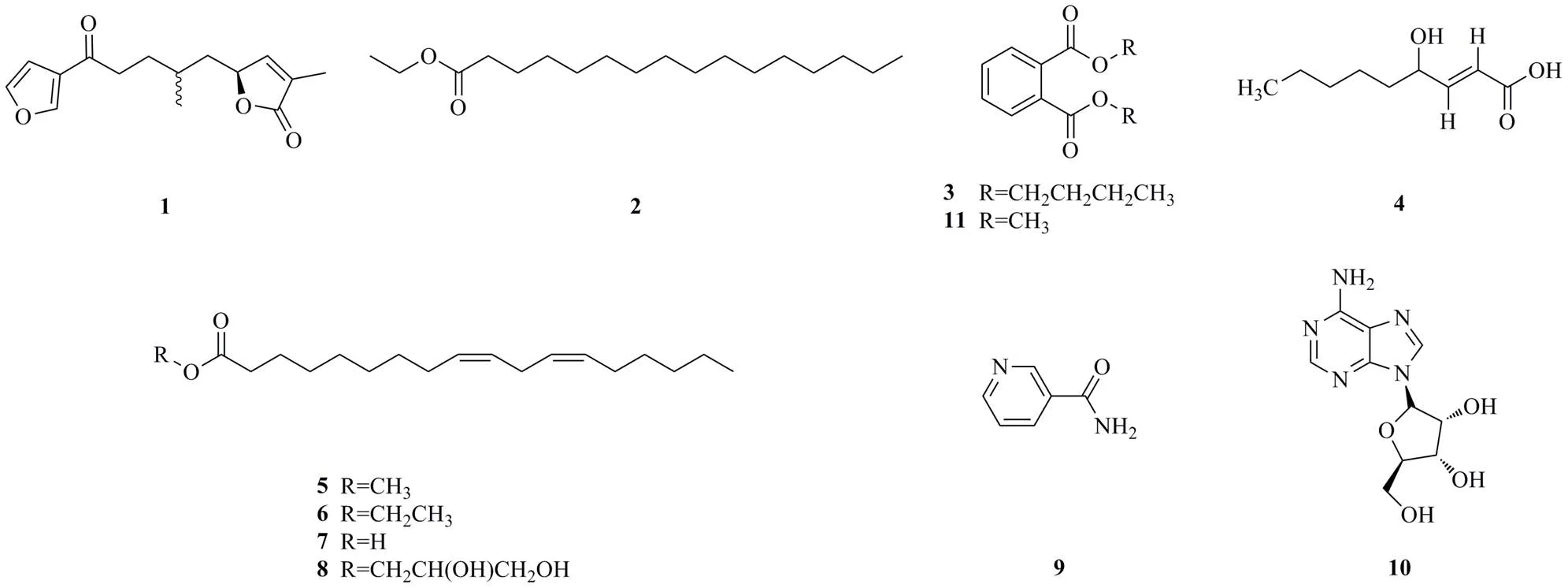
图1 化合物1~11的化学结构
1 仪器与材料
Dionex Ultimate 3000型高效液相色谱仪(美国戴安公司);LC-2010型高效液相色谱仪(北京清博华科技有限公司);分析型色谱柱YMC-Pack ODA-A(250 mm×4.6 mm,5 μm,日本 YMC 公司);半制备型色谱柱Daisogel-10μ-100A(250 mm×10 mm,10 μm,日本DAISO公司);半制备型色谱柱Positisil ODS-P(250 mm×10 mm,5 μm,北京英莱克科技发展有限公司);AV 400型核磁共振波谱仪(瑞士布鲁克公司);solariX型FT-ICR MS/MRMS(德国布鲁克道尔顿公司);Acquity QDa型质谱检测器(美国Waters公司);Chirascan型圆二色光谱仪(英国应用光物理公司);GLH-100C型恒温恒湿培养箱(德国BINDER公司);Haier HR40-ⅡA2型生物安全柜(上海恒勤仪器设备有限公司);UV-5900型紫外可见分光光度计(上海元析仪器有限公司);TOMY SX-700型蒸汽灭菌器(北京久航润达科技有限公司);200~300、300~400目正相柱色谱硅胶、薄层色谱硅胶板GF254(青岛海洋化工有限公司);HP-20大孔吸附树脂(日本三菱公司);色谱甲醇、色谱乙腈(美国TEDIA公司);石油醚、醋酸乙酯、甲醇、二氯甲烷、浓硫酸(天津科密欧化学试剂有限公司);正丁醇、无水乙醇(国药集团);α-萘酚(天津市大茂化学试剂厂);Middlebrook 7H9培养基(美国BD公司);甘油(上海阿拉丁生化科技股份有限公司);聚山梨酯80(生工生物工程股份有限公司);DMSO、异烟肼、乙胺丁醇(美国Sigma-Aldrich公司);利福平(常州制药厂有限公司)。
药材于2021年5月购买自云南省,经三峡大学生物与制药学院王玉兵教授鉴定为小毛茛Thunb.的干燥块根。标本(RT20210001)存放于三峡大学天然产物研究与利用湖北省重点实验室。
标准菌株牛型分枝杆菌BCG由上海公共卫生临床中心提供。
2 提取与分离
猫爪草干燥块根2.19 kg,粉碎后加95%乙醇2.5 L,冷浸提取4次,每次24 h,合并提取液,减压浓缩得浓缩液。浓缩液用水分散后,依次用石油醚、醋酸乙酯及正丁醇各1.5 L萃取4次,各部分萃取液减压浓缩至干,得到石油醚萃取部位(18.7 g),醋酸乙酯萃取部位(3.9 g)及正丁醇萃取部位(20.6 g)。
石油醚部位(18.7 g)经正相硅胶柱色谱(200~300目)分离,石油醚-丙酮(100∶0→1∶2)梯度洗脱,得到122个流分。TLC及HPLC分析后,合并Fr. 66~71(236.4 mg),经半制备型HPLC分离纯化(甲醇-水47∶53,3 mL/min),得到化合物1(2.2 mgR=25.7 min)。合并Fr. 25~30(R1,4.6 g),经正相硅胶柱色谱(300~400目)进一步分离,石油醚-醋酸乙酯(50∶1→1∶1)梯度洗脱,得到106个流分,TLC及HPLC分析后,合并亚流分Fr. R1-7~11(143.2 mg),经半制备HPLC分离纯化(乙腈-水73∶27,3 mL/min),得到化合物2(6.4 mg,R=29.7 min);合并亚流分Fr. R1-39~42(401.4 mg),经半制备HPLC分离纯化(甲醇-水66∶34,3 mL/min),得到化合物3(4.5 mg,R=39.8 min)。合并Fr. 52~60(R2,2.9 g),经正相硅胶柱色谱(300~400目)进一步分离,二氯甲烷-甲醇(100∶0→2∶1)梯度洗脱,得到96个流分,TLC及HPLC分析后,合并亚流分Fr. R2-67~73(197.1 mg),经半制备HPLC分离纯化(乙腈-0.1%乙酸水29∶71,3 mL/min),得到化合物4(4.3 mg,R=21.9 min)。
醋酸乙酯部位(R3,3.9 g)经正相硅胶柱色谱(200~300目)分离,石油醚-醋酸乙酯(100∶0→1∶3)梯度洗脱,得到200个流分。TLC及HPLC分析后,合并Fr. R3-33~40(176.5 mg),经半制备HPLC分离纯化(乙腈-水79∶21,3 mL/min),得到化合物5(11.6 mg,R=67.5 min)和6(17.6 mg,R=80.2 min);合并Fr. R3-79~80(115.3 mg),经半制备HPLC分离纯化(乙腈-水75∶25,3 mL/min),得到化合物7(48.4 mg,R=38.8 min);合并Fr. R3-135~148(65.7 mg),经半制备HPLC分离纯化(乙腈-水65∶35,3 mL/min),得到化合物8(13.5 mg,R=57.4 min)。
正丁醇部位(R4,20.6 g)经HP-20大孔吸附树脂柱色谱分离,纯水洗脱至Molish试剂对洗脱液无紫环反应,后续以(30%、60%、100%)乙醇-水梯度洗脱,得到26个流分。经TLC及HPLC分析后,合并Fr. R4-5~6(583.2 mg),经半制备HPLC分离纯化(甲醇-0.1%乙酸水4∶96,3 mL/min),得到化合物9(2.9 mg,R=17.2 min)和10(21.6 mg,R=62.6 min);合并Fr. R4-20~26(313.3 mg),经半制备HPLC分离纯化(甲醇-0.1%乙酸水28∶72,3 mL/min),得到化合物11(4.9 mg,R=37.2 min)。
3 结构鉴定
化合物1:淡黄色油状物,HR-ESI-MS给出准分子离子峰/: 263.127 7 [M+H]+(理论值263.127 8);285.109 7 [M+Na]+(理论值285.109 7);547.230 1 [2M+Na]+(理论值547.230 2),由此可知,化合物1的分子式为C15H18O2,不饱和度为7。从碳谱和氢谱数据(表1)可知,化合物含有3个碳碳双键和2个羰基碳,由此推测,该化合物含有2个环系。
结合1H-NMR、13C-NMR和HSQC谱可知,该化合物有2个CH3,3个CH2,6个CH以及4个季碳。1H-NMR谱中,低场区给出5个质子信号H8.05 (1H, brs, H-4), 7.45 (1H, t,= 1.6 Hz, H-1), 7.04 (1H, 的质子;高场区在H2.77 (2H, t,= 7.2 Hz, H2-6), 1.88 (1H, m, H-7a), 1.78 (1H, m, H-8), 1.64 (1H, m, H-10a), 1.57 (1H, m, H-7b) 和1.52 (1H, m, H-10b) 处给出6个连在脂肪碳上的质子信号;在H1.92 (3H, t,= 1.6 Hz, Me-15) 处给出1个连在烯碳上的甲基质子信号和H1.02 (3H, d,= 7.2 Hz, Me-9) 处1个连在次甲基上的甲基质子信号。
表1 化合物1的核磁数据(400/100 MHz, CDCl3)
Table 1 NMR data of compound 1 (400/100 MHz, CDCl3)
碳位δCδH 1144.47.45 (1H, t, J = 1.6 Hz) 2108.86.76 (1H, d, J = 1.6 Hz) 3127.8 4147.28.05 (1H, brs) 5195.0 637.92.77 (1H, t, J = 7.2 Hz) 2.77 (1H, t, J = 7.2 Hz) 7a30.71.88 (1H, m) 7b 1.57 (1H, m) 830.01.78 (1H, m) 920.11.02 (3H, d, J = 7.2 Hz) 10a40.91.64 (1H, m) 10b 1.52 (1H, m) 1179.74.98 (1H, m) 12149.17.04 (1H, t, J = 1.6 Hz) 13130.0 14174.4 1510.81.92 (3H, t, J = 1.6 Hz)
1H-1H COSY谱(图2)中,H7.45 (1H, t,=1.6 Hz, H-1) 和6.76 (1H, d,= 1.6 Hz, H-2) 存在明显相关;H2.77 (2H, t,= 7.2 Hz, H2-6) 和1.88 (1H, m, H-7a) 以及1.57 (1H, m, H-7b) 存在明显相关;H1.78 (1H, m, H-8) 和1.57 (1H, m, H-7b), 1.52 (1H, m, H-10b), 1.02 (3H, d,= 7.2 Hz, Me-9) 均存在明显相关;H1.52 (1H, m, H-10b) 和4.98 (1H, m, H-11) 存在明显相关;H4.98 (1H, m, H-11) 和7.04 (1H, t,= 1.6 Hz, H-12) 存在明显相关。HMBC谱(图2)中H8.05 (1H, brs, H-4) 和c 144.4 (C-1), 127.8 (C-3), 108.8 (C-2) 存在明显相关;H7.45 (1H, t,=1.6 Hz, H-1) 和C147.2 (C-4), 127.8 (C-3), 108.8 (C-2) 存在明显相关;H6.76 (1H, d,= 1.6 Hz, H-2) 和c 144.4 (C-1), 147.2 (C-4) 存在明显相关,提示分子中存在呋喃环单元;HMBC谱(图2)中H7.04 (1H, t,= 1.6 Hz, H-12) 和C79.7 (C-11) 存在明显相关;H2.77 (2H, t,= 7.2 Hz, H2-6) 和Ct,= 1.6 Hz, H-12), 6.76 (1H, d,= 1.6 Hz, H-2) 和4.98 (1H, m, H-11),推测为连在烯碳或者连氧碳上195.0 (C-5), 30.7 (C-7) 存在明显相关;H1.92 (3H, t,= 1.6 Hz, Me-15) 和C174.4 (C-14), 149.1 (C-12), 130.0 (C-13) 存在明显相关,提示该甲基连在C-13位;H1.02 (3H, d,= 7.2 Hz, Me-9) 和C40.9 (C-10), 30.7 (C-7), 30.0 (C-8) 存在明显相关,提示该甲基连在C-8位;H1.64 (1H, m, H-10a), 1.52 (1H, m, H-10b) 和C79.7 (C-11) 存在明显相关;H1.64 (1H, m, H-10a) 和C149.1 (C-12) 存在明显相关。NOESY谱(图3)中,H1.02 (3H, d,= 7.2 Hz, Me-9) 和H1.57 (1H, m, H-7b), 1.52 (1H, m, H-10b)存在明显相关,表明其位于同侧;而H1.02 (3H, d,= 7.2 Hz, Me-9) 和H4.98 (1H, m, H-11) 没有明显相关,表明其位于异侧。
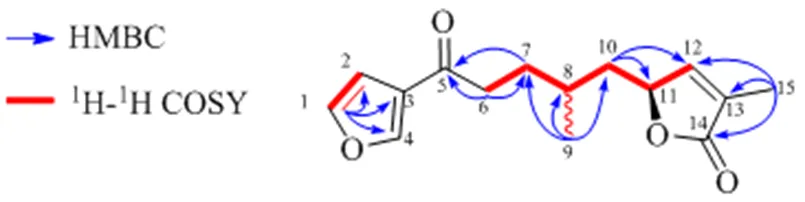
图2 化合物1的主要HMBC和1H-1H COSY相关
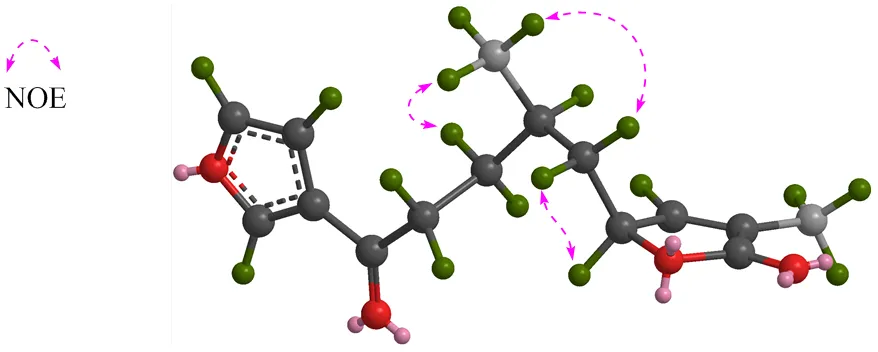
图3 化合物1的主要NOESY相关
化合物1的绝对构型通过圆二色散光谱(circular dichroism,CD)的量子化学计算所确定。黑色曲线部分为该化合物的实测CD曲线,黑色虚线分别对应其2种互为镜像的立体构型的计算CD曲线。将实测CD曲线和计算CD曲线比对,根据匹配度确定该化合物的绝对构型为11(图4)。经Sci-finder检索,化合物1为新化合物,命名为猫爪草呋喃倍半萜A(ranunculifuran A)。
化合物2:白色固体。HR-ESI-MS/: 285.278 8 [M+H]+(理论值285.278 8),确定分子式为C18H36O2,计算不饱和度为1。1H-NMR (400 MHz, CDCl3): 0.88 (3H, t,= 7.2 Hz, H-16), 1.26 (27H, m, H-4~15, 18), 1.61 (2H, m, H-3), 2.29 (2H, t,= 7.6 Hz, H-2), 4.13 (2H, dd,= 14.0, 7.2 Hz, H-17);13C-NMR (100 MHz, CDCl3): 14.3 (CH3), 14.4(CH3), 22.8 (C-15), 25.1 (C-3), 29.3~29.8 (C-4~13), 32.1 (C-14), 34.6 (C-2), 60.3 (C-17), 174.1 (C-1)。以上数据与文献报道的数据基本一致[13],故鉴定化合物2为棕榈酸乙酯。
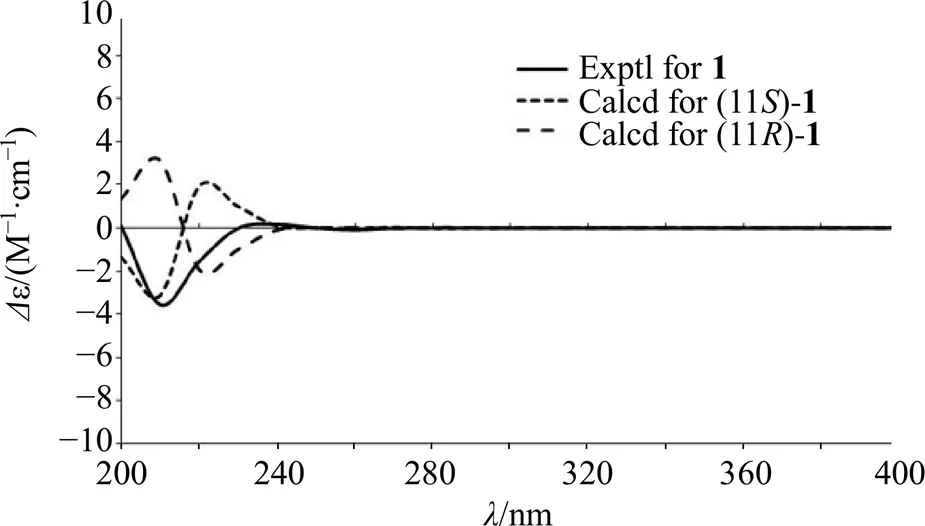
图4 化合物1的计算ECD曲线和实测ECD曲线
化合物3:无色油状物。HR-ESI-MS/: 279.159 1 [M+H]+(理论值279.159 1),确定分子式为C16H22O4,计算不饱和度为6。1H-NMR (400 MHz, CDCl3): 0.96 (6H, t,= 7.6 Hz, H-4′), 1.44 (4H, m, H-3′), 1.72 (4H, m, H-2′), 4.31 (4H, t,= 6.8 Hz, H-1′), 7.53 (2H, dd,= 5.6, 3.6 Hz, H-1, 2), 7.72 (2H, dd,= 5.6, 3.6 Hz, H-3, 6);13C-NMR (100 MHz, CDCl3): 13.9 (C-4′), 19.3 (C-3′), 30.7 (C-2′), 65.7 (C-1′), 129.0 (C-3, 6), 131.1 (C-4, 5), 132.5 (C-1, 2), 167.9 (C=O)。以上数据与文献报道的数据基本一致[14],故鉴定化合物3为dibutyl phthalate。
化合物4:无色油状物。ESI-MS/: 171.1 [M-H]−(理论值171.1),分子式C9H16O3。1H-NMR (400 MHz, CDCl3): 0.89 (3H, t,= 6.0 Hz, H-9), 1.29~1.47 (6H, m, H-6~8), 1.57 (2H, m, H-5), 4.31 (1H, s, H-4), 6.04 (1H, s, H-2), 6.99 (1H, m, H-3);13C-NMR (100 MHz, CDCl3): 14.2 (C-9), 22.7 (C-8), 25.1 (C-7), 31.8 (C-6), 36.6 (C-5), 71.2 (C-4), 120.2 (C-2), 152.1 (C-3), 171.5 (C-1)。以上数据与文献报道的数据基本一致[15],故鉴定化合物4为-4-hydroxy- 2-nonenoic acid。
化合物5:无色油状物。HR-ESI-MS/: 295.263 2 [M+H]+(理论值295.263 2),确定分子式为C19H34O4,计算不饱和度为3。1H-NMR (400 MHz, CDCl3): 0.88 (3H, t,= 6.8 Hz, H-18), 1.25~1.39 (14H, m, H-4~7, 15~17), 1.63 (2H, m, H-3), 2.04 (4H, dd,= 14.0, 7.2 Hz, H-8, 14), 2.30 (2H, t,= 7.6 Hz, H-2), 2.77 (2H, t,= 7.2 Hz, H-11), 3.66 (3H, s, -OCH3), 5.29~5.40 (4H, m, H-9, 10, 12, 13);13C-NMR (100 MHz, CDCl3): 14.2 (C-18), 22.7 (C-17), 25.1 (C-3), 25.8 (C-11), 27.3 (C-8), 27.3 (C-14), 29.2 (C-6), 29.3 (C-5), 29.3 (C-4), 29.5 (C-15), 29.7 (C-7), 31.7 (C-16), 34.2 (C-2), 51.6 (C-OCH3), 128.0 (C-12), 128.2 (C-10), 130.2 (C-9), 130.4 (C-13), 174.5 (C-1)。以上数据与文献报道的数据基本一致[16],故鉴定化合物5为methyl linoleate。
化合物6:无色油状物。HR-ESI-MS/: 309.278 8 [M+H]+(理论值309.278 8),确定分子式为C20H36O2,计算不饱和度为3。1H-NMR (400 MHz, CDCl3): 0.88 (3H, t,= 6.8 Hz, H-18), 1.25 (3H, t,= 7.2 Hz, H-20), 1.27~1.34 (14H, m, H-4~7, 15~17), 1.61 (2H, m, H-3), 2.04 (4H, dd,= 14.0, 7.2 Hz, H-8, 14), 2.28 (2H, t,= 7.2 Hz, H-2), 2.76 (2H, t,= 7.2 Hz, H-11), 4.11 (2H, dd,= 14.0, 7.2 Hz, H-19), 5.35 (4H, m, H-9, 10, 12, 13);13C-NMR (100 MHz, CDCl3): 14.2 (C-18), 14.4 (C-20), 22.7 (C-17), 25.1 (C-16), 25.7 (C-6), 27.3 (C-7), 27.3 (C-15), 29.2 (C-8), 29.2 (C-14), 29.3 (C-5), 29.5 (C-11), 29.7 (C-4), 31.6 (C-3), 34.5 (C-2), 60.3 (C-19), 128.0 (C-10), 128.1 (C-12), 130.2 (C-9), 130.3 (C-13), 174.1 (C-1)。以上数据与文献报道基本一致[17],故鉴定化合物6为ethyl linoleate。
化合物7:无色油状物。HR-ESI-MS/: 281.247 6 [M+H]+(理论值为281.247 5),确定分子式为C18H32O2,计算不饱和度为3。1H-NMR (400 MHz, CDCl3): 0.89 (3H, t,= 6.8 Hz, H-18), 1.25~1.39 (14H, m, H-4~7, 15~17), 1.65 (2H, m, H-3), 2.05 (4H, dd,= 13.6, 6.8 Hz, H-8, 14), 2.35 (2H, t,= 7.6 Hz, H-2), 2.77 (2H, t,= 6.8 Hz, H-11), 5.35 (4H, m, H-9, 10, 12, 13);13C-NMR (100 MHz, CDCl3): 14.2 (C-18), 22.7 (C-17), 24.8 (C-3), 25.8 (C-11), 27.3 (C-6), 27.3 (C-14), 29.2 (C-5), 29.2 (C-6), 29.3 (C-4), 29.5 (C-15), 29.7 (C-7), 31.7 (C-16), 34.2 (C-2), 128.0 (C-12), 128.2 (C-10), 130.1 (C-9), 130.3 (C-13), 180.7 (C-1)。以上数据与文献报道一致[18],故鉴定化合物7为linoleic acid。
化合物8:无色油状物。HR-ESI-MS/: 355.284 3 [M+H]+(理论值355.284 3),确定分子式为C21H38O4,计算不饱和度为3。1H-NMR (400 MHz, CDCl3): 0.88 (3H, t,= 6.8 Hz, H-18), 1.26~1.36 (14H, m, H-4~7, 15~17), 1.62 (2H, m, H-3), 2.04 (4H, dd,= 13.6, 6.8 Hz, H-8, 14), 2.34 (2H, t,= 7.6 Hz, H-2), 2.76 (2H, t,= 6.4 Hz, H-11), 3.59 (1H, dd,= 11.6, 6.0 Hz, H-3′b), 3.69 (1H, dd,= 11.6, 4.0 Hz, H-3′a), 3.91 (1H, m, H-2′), 4.11~4.20 (2H, m, H-1′), 5.28~5.41 (4H, m, H-9, 10, 12, 13);13C-NMR (100 MHz, CDCl3): 14.2 (C-18), 22.7 (C-17), 25.0 (C-3), 25.7 (C-11), 27.3 (C-8), 27.3 (C-14), 29.2 (C-6), 29.3 (C-5), 29.5 (C-4), 29.7 (C-15), 31.6 (C-16), 34.3 (C-2), 63.4 (C-3′), 65.3 (C-1′), 70.4 (C-2′), 128.0 (C-10), 128.2 (C-12), 130.1 (C-9), 130.4 (C-13), 174.5 (C-1)。以上数据与文献报道的数据基本一致[19],故鉴定化合物8为1-- (9,12-octadecadienoyl) glycerol。
化合物9:无色针状结晶(甲醇)。ESI-MS/: 123.1 [M+H]+(理论值123.1),分子式C6H6N2O。1H-NMR (400 MHz, CD3OD): 7.55 (1H, ddd,= 8.0, 4.8, 0.8 Hz, H-5), 8.29 (1H, dt,= 8.0, 2.0 Hz, H-4), 8.69 (1H, dd,= 4.8, 1.6 Hz, H-6), 9.02 (1H, d,= 1.6 Hz, H-2);13C-NMR (100 MHz, CD3OD): 125.1 (C-5), 131.4 (C-3), 137.4 (C-4), 149.5 (C-2), 152.8 (C-6), 169.8 (C=O)。以上数据与文献报道的数据基本一致[20],故鉴定化合物9为烟酰胺。
化合物10:白色固体粉末。ESI-MS/: 268.1 [M+H]+(理论值268.1),分子式C10H13N5O4。1H-NMR (400 MHz, DMSO-6): 3.61 (2H, m, H-5′), 3.96 (1H, m, H-4′), 4.14 (1H, m, H-3′), 4.59 (1H, m, H-2′), 5.88 (1H, d,= 6.0 Hz, H-1′), 8.14 (1H, s, H-2), 8.36 (1H, s, H-8);13C-NMR (100 MHz, DMSO-6): 61.7 (C-5′), 70.6 (C-3′), 73.5 (C-2′), 85.9 (C-4′), 88.0 (C-1′), 119.3 (C-5), 140.0 (C-8), 149.1 (C-4), 152.4 (C-2), 156.1 (C-6)。以上数据与文献报道的数据基本一致[21],故鉴定化合物10为β-adenosine。
化合物11:淡黄色油状物。ESI-MS/: 195.1 [M+H]+(理论值195.1),分子式C10H10O4。1H-NMR (400 MHz, CDCl3): 3.92 (6H, s, -OCH3), 7.55 (2H, dd,= 6.0, 3.6 Hz, H-3, 4), 7.73 (2H, dd,= 6.0, 3.6 Hz, H-2, 5);13C-NMR (100 MHz, CDCl3): 52.8 (-OCH3), 129.0 (C-3, 6), 131.3 (C-4, 5), 132.0 (C-1, 2), 168.2 (C=O)。以上数据与文献报道的数据基本一致[22],故鉴定化合物11为dimethyl phthalate。
4 体外抗结核杆菌活性
采用微量肉汤二倍稀释法考察猫爪草醇提物石油醚、醋酸乙酯和正丁醇萃取部位,以及所有化合物对BCG的抑制活性。试验菌株BCG培养至对数生长期,用培养物和培养基稀释成菌悬液供检测用。试验在96孔平底细胞培养板中进行,设置空白、阳性对照、阴性对照和给药组,各萃取部位、单体化合物和阳性对照药平行检测3次。加200 μL无菌蒸馏水到微板的外围孔中,于第2列孔中加200 μL Middlebrook 7H9肉汤,继续向第2列孔中注入2 μL各化合物溶液、阳性药物(利福平、异烟肼、乙胺丁醇)、阴性对照物(DMSO),剩余孔中都增补100 μL Middlebrook 7H9肉汤,留1行作空白对照,不加任何物质只加培养基,对每列进行系列二倍稀释,100 μL菌悬液加到所有检测孔中。被检测化合物溶液的最终质量浓度200~0.78 μg/mL,阳性药物质量浓度50~0.1 μg/mL。平板套上封闭的塑料袋在37 ℃的培养箱中孵育7~9 d,而后观察浊度。无混浊现象的最低浓度定义为MIC。
体外抗结核杆菌活性实验结果显示猫爪草醇提物石油醚、醋酸乙酯和正丁醇萃取部位对牛型分枝杆菌BCG有不同程度的抑制活性,其MIC分别为200、100和200 μg/mL;化合物1、2、4~8和10对牛型分枝杆菌BCG有较弱抑制活性,其MIC均为100 μg/mL;阳性对照药利福平、异烟肼和乙胺丁醇的MIC分别为0.2、0.4、12.5 μg/mL。
5 讨论
猫爪草有机酸部位是其抗结核有效部位之一,且猫爪草中有机酸的含量较高,其中长链脂肪酸占大多数[23-25]。本研究从猫爪草中分离鉴定了11个化合物,包括1个呋喃倍半萜、5个长链有机酸类化合物、2个邻苯二甲酸酯、2个生物碱和1个非长链有机酸,其中化合物1为新的呋喃倍半萜,将其命名为猫爪草呋喃倍半萜A;化合物4、8~11均为首次从猫爪草中分离得到。
人型分枝杆菌H37Rv、H37Ra和牛型分枝杆菌BCG被广泛用作研究结核致病性机制的参比菌株[26]。本研究从猫爪草中分离鉴定的5个长链有机酸类化合物(化合物2、5~8)和1个非长链有机酸(化合物4)对牛型分枝杆菌BCG具有较弱抑制活性,其MIC均为100 μg/mL[27]。化合物2为棕榈酸的衍生物,化合物5~8为亚油酸或其衍生物,据报道,亚油酸和棕榈酸对结核分枝杆菌H37Rv及3种多药耐药结核分枝杆菌菌株的MIC分别为50~100 μg/mL和25~50 μg/mL[28-29],化合物2、5~8对结核分枝杆菌H37Rv以及耐药结核分支杆菌是否具有抑制活性,其抗菌作用机制如何均有待进一步研究。
本研究成果丰富了猫爪草的化学成分多样性,为猫爪草中抗结核杆菌活性先导化合物的发现提供了实验依据。
利益冲突 所有作者均声明不存在利益冲突
[1] World Health Orgnization. Global Tuberculosis Report 2020 [R/OL]. [2022-10-27]. https://www.who.int/teams/ global-tuberculosis-programme/tb-reports/global-tuberculosis-report-2022.
[2] 黄华靖, 江洁怡, 肖观林, 等. 猫爪草的化学成分、药理作用研究进展及其质量标志物的预测分析 [J]. 中药材, 2022, 45(3): 752-759.
[3] Wang C L, Wang J Q, Gao M Z,.: Review of its chemical constituents, pharmacology, quality control and clinical applications [J]., 2022, 74(7): 930-952.
[4] 刘芊伊. 猫爪草醇类提取物对小鼠骨髓来源巨噬细胞极化的影响 [D]. 遵义: 遵义医学院, 2018.
[5] 熊英, 邓可众, 郭远强, 等. 猫爪草中黄酮类与苷类化学成分的研究 [J]. 中草药, 2008, 39(10): 1449-1452.
[6] Xiong Y, Deng K Z, Gao W Y,. A novel alkenoic acid ester and a new benzophenone from[J]., 2007, 18(11): 1364-1366.
[7] Deng K Z, Xiong Y, Zhou B,. Chemical constituents from the roots ofand their inhibitory effects on[J]., 2013, 18(10): 11859-11865.
[8] Zhan Z L, Feng Z M, Yang Y N,. Ternatusine A, a new pyrrole derivative with an epoxyoxepino ring from[J]., 2013, 15(8): 1970-1973.
[9] Feng Z M, Zhan Z L, Yang Y N,. New heterocyclic compounds fromThunb [J]., 2017, 74: 10-14.
[10] Zhang L, Li R Y, Li M Z,.andstudy of anti-tuberculosis effect of extracts isolated from[J]., 2014, 31(4): 336-342.
[11] 周勇, 程芳. 猫爪草对肺结核患者外周血淋巴细胞颗粒裂解肽表达及其T淋巴细胞杀菌能力的影响 [J]. 中国药学杂志, 2017, 52(18): 1629-1632.
[12] 夏露, 卢水华, 刘平. 中药对结核病免疫调控机制的研究进展 [J]. 中国防痨杂志, 2020, 42(2): 168-172.
[13] 熊英, 苌美燕, 章常华, 等. 猫爪草中的脂肪酸类化合物 [J]. 热带亚热带植物学报, 2016, 24(3): 348-351.
[14] Li J T, Yin B L, Liu Y,. Mono-aromatic constituents of[J]., 2009, 45(2): 234-236.
[15] Mu L H, Ju Q F, Liu P,. Chemical constituents of the roots of[J]., 2013, 48(6): 1004-1007.
[16] He W J, Zhou X J, Qin X C,. Quinone/hydroquinone meroterpenoids with antitubercular and cytotoxic activities produced by the sponge-derived fungussp. ZSDS1-F7[J]., 2017, 31(5): 604-609.
[17] Aidarhan N, Guoruoluo Y, Liu Z S,. Chemical constituents of the petroleum-ether fraction from seeds of[J]., 2020, 56(2): 358-360.
[18] Nakano H, Cantrell C L, Mamonov L K,. Echinopsacetylenes A and B, new thiophenes from[J]., 2011, 13(23): 6228-6231.
[19] Kim D G, Kang M J, Hong S S,. Antiinflammatory effects of functionally active compounds isolated from aged black garlic [J]., 2017, 31(1): 53-61.
[20] 晁凌会, 彭治添, 任易, 等. 紫堇的化学成分研究 [J]. 中草药, 2018, 49(7): 1508-1512.
[21] 旷敏, 彭伟伟, 许立, 等. 植物根际土壤真菌的化学成分研究 [J]. 中南药学, 2022, 20(9): 1975-1981.
[22] Khusnutdinov R I, Shchadneva N A, Mayakova Y Y,. Methylation of mono- and dicarboxylic acids with dimethyl carbonate catalyzed with binder-free zeolite NaY [J]., 2017, 53(2): 163-168.
[23] 池玉梅, 杨毅琴, 于生. 中药材猫爪草有机酸部位药效及组成的研究 [J]. 南京中医药大学学报, 2007, 23(6): 365-367.
[24] 何潇. 猫爪草多糖理化性质及抗肝损伤活性的研究 [D]. 长沙: 湖南中医药大学, 2019.
[25] 黄华靖, 江洁怡, 肖观林, 等. UPLC-Q-TOF-MS法分析猫爪草化学成分 [J]. 中成药, 2022, 44(7): 2405-2409.
[26] Xiao G H, Zhang S, Zhang L,. Untargeted metabolomics analysis revealsstrain H37Rv specifically induces tryptophan metabolism in human macrophages [J]., 2022, 22(1): 249-258.
[27] Gibbons S. Plants as a source of bacterial resistance modulators and anti-infective agents [J]., 2005, 4(1): 63-78.
[28] Choi W H. Evaluation of anti-tubercular activity of linolenic acid and conjugated-linoleic acid as effective inhibitors against[J]., 2016, 9(2): 125-129.
[29] Sandoval-Montemayor N E, García A, Elizondo-Treviño E,. Chemical composition of hexane extract ofand anti-activity of some of its constituents [J]., 2012, 17(9): 11173-11184.
A new furanosesquiterpenoid from
ZHANG Lu-dan1, LONG Yu-jiao1, WANG Rui-feng1, CAO Ya-nan1, FAN Xiao-yong2, ZOU Kun1, WANG Hui1
1. Hubei Key Laboratory of Natural Products Research and Development, College of Biological and Pharmaceutical Sciences, China Three Gorges University, Yichang 443002, China 2. Shanghai Public Health Clinical Center, Fudan University, Shanghai 201508, China
To investigate the chemical constituents from Maozhaocao() and their activities against.Various chromatographic techniques, including silica gel column chromatography, macroporous resin column chromatography, TLC and HPLC, were used to separate and purify the ethanol extracts from. The structures of isolates were elucidated by physicochemical properties and spectral analyses. The activity of all compounds againstwas tested by microbroth double dilution method.Eleven compounds were isolated fromand identified as (5)-5-(5-(furan-3-yl)-2-methyl-5-oxopentyl)-3-methylfuran-2(5)-one (1), ethyl palmitate (2), dibutyl phthalate (3),-4-hydroxy-2-nonenoic acid (4), methyl linoleate (5), ethyl linoleate (6), linoleic acid (7), 1--(9,12-octadecadienoyl) glycerol (8), niacinamide (9), β-adenosine (10), dimethyl phthalate (11), respectively. Compounds 1, 2, 4—8 and 10 had mild inhibitory activities againstBCG, all with a minimum inhibitory concentration (MIC) value of 100 μg/mL, respectively.Compound 1 is a new furanosesquiterpenoid, named ranunculifuran A. Compounds 4, 8—11 were isolated fromfor the first time. Compounds 1, 2, 4—8 and 10 had mild inhibitory activities againstBCG.
; ranunculifuran A;; niacinamide;-4-hydroxy-2-nonenoic acid; β-adenosine
R284.1
A
0253 - 2670(2023)14 - 4413 - 07
10.7501/j.issn.0253-2670.2023.14.001
2023-04-15
国家自然科学基金资助项目(22207063);高等学校学科创新引智计划(D20015);湖北省教育厅科学技术研究项目(Q20161207);天然产物研究与利用湖北省重点实验室(三峡大学)开放基金(2022NPRD07)
张露丹,硕士研究生,研究方向为天然产物化学。E-mail: zhangld27@126.com
王 慧,博士,副教授,研究方向为天然产物化学。E-mail: alice0507@yeah.net
[责任编辑 王文倩]
——青蒿素

