3D 打印耳廓模型在耳廓再造软骨支架雕刻成形中的应用
李腾海, 杨田野, 彭维海
(吉林大学第一医院整形外科,吉林 长春 130021)
小耳畸形是颌面部最常见的先天畸形之一,耳廓再造术是治疗小耳畸形的主要方法之一。外耳廓是体表最复杂的三维立体器官,在截面积上展现出外耳轮廓高低错落的14 个解剖结构,因此耳廓再造术被认为是整形外科最复杂和最具挑战性的手术之一。耳廓再造术的关键是耳廓支架的精细雕刻。传统耳廓支架雕刻模型的制作方法是参照健侧耳廓,以X 线胶片为材料临摹成二维平面耳廓模型。但耳廓是三维立体器官,胶片耳模是二维平面的,因此与3D 耳廓模型(3D 耳模)比较,胶片耳模缺乏精确度和立体感,尤其是耳甲腔、耳舟和三角窝的曲面度及深度导致再造耳廓的精确性较差。数字化3D 打印技术在颅颌面和骨关节外科领域的广泛应用为3D 耳模在耳廓再造术中的应用提供了可能[1-4]。1993 年KANEKO[5]首次在耳廓再造术中采用3D 耳模。随着3D 打印技术应用的深入,目前较多临床医生采用3D 打印耳模指导耳廓支架的雕刻成形,并取得了良好的疗效[6-13]。然而关于3D耳模的量化指标尚不完善,目前的量化指标尚无法精确评估3D 耳模的临床应用。本研究回顾性分析3D 耳模应用于耳廓再造术患者的临床资料,对患者术后再造耳廓的量化指标进行精细化评估,旨在为评价3D 耳模的临床应用提供依据。
1 资料与方法
1.1 研究对象回顾性分析2018 年2 月—2021 年2 月于吉林大学第一医院整形外科行Nagata 法耳廓再造术76 例先天性单侧小耳畸形患者的临床资料。男性41 例,女性35 例,年龄8~36 周岁,平均年龄(12.0±1.5)周岁。右侧耳畸形46例,左侧30例。依据Nagata 耳分型分为耳垂型36 例、小耳甲腔型25 例和耳甲腔型15 例。纳入标准:①单侧小耳畸形,对侧耳廓正常;②8 周岁以上或胸围>68 cm;③患者及其家属支持3D 打印耳模;④能够完成术后半年以上随访;⑤所有手术均由同一手术团队完成。排除标准:①双侧小耳畸形;②既往有精神疾病或认知障碍者;③严重的半侧颜面短小症患者。本研究经吉林大学第一医院伦理委员会备案(伦理备案号2020-704),与所有患者及其家属进行沟通,并签署知情同意书。
1.2 3D 耳模制备患者取平卧位,采用256 排电子计算机断层扫描(computed tomography,CT)(德国西门子股份公司)进行健侧耳廓数据采集,图像层厚 1 mm,层间隔 1 mm,扫描范围为整个头面部,数据格式为DICOM。将选取的健侧耳廓及其邻近的耳廓周围颞区结构采用Mimics 19.0 软件进行三维重建,以光固化立体造型术(stereolithography,STL)格式存储,并采用Cura 3D 打印切片软件将STL 文件作镜像及平滑处理,将重建耳廓边缘缩小2 mm,耳甲腔缩小1 mm,获得与健侧耳廓形态相同的三维解剖图像,导入A8S3D 打印机(深圳市极光尔沃科技股份有限公司),打印层厚0.1 mm,精度0.2 mm,喷头流速约为24 cc·h-1,喷头温度为200 ℃,热床温度为60 ℃,打印原料为聚乳酸,打印出3D 耳模,见图1。术前参照3D 耳模与患者及其家属充分沟通再造耳廓的形态。
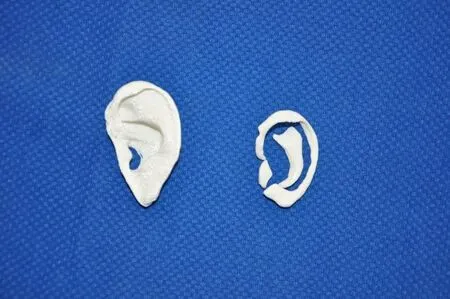
图1 3D 打印耳廓模型Fig.1 3D printing auricle model
1.3 手术方法所有患者均采用Nagata 法耳廓再造术,所有手术均由同一术者和团队完成。第一期手术依据术前肋软骨三维成像评估,适当截取第6~8 肋软骨。术中参照已消毒的3D 耳模进行耳廓支架雕刻。将第6 和第7 肋的联合部及部分第7 肋设计为耳廓支架基底,精细雕刻出对耳轮及其上下脚、耳舟、对耳屏和三角窝等结构。将第8 肋精细雕刻成耳轮和耳轮脚,若第8 肋长度不够,将部分第7 肋用作耳轮的拼接,耳轮脚延伸至耳甲腔。根据3D 耳模对耳轮的长度、锐度和曲线变化,取部分第7 肋修剪成对耳轮,叠加在耳廓支架基底相应位置上。若为耳垂型小耳畸形,则利用剩余的第6 和7 肋软骨精细雕刻成耳屏及耳屏切迹;若为小耳甲腔型或耳甲腔型,则无需雕刻耳屏及耳屏切迹。将第6 肋近胸骨端一条形软骨埋置在胸部皮下,以备二期手术使用。最后参照3D 耳模将各结构边缘打磨光滑,力求耳廓支架形态自然和精确。所有软骨的拼接和固定均采用钢丝及可吸收缝线固定。依据残耳和乳突区皮肤条件及雕刻的耳廓支架制备乳突区皮瓣,并保留一筋膜蒂,将耳廓支架放置于乳突皮瓣下,同时行耳垂转位,观察耳廓形态,位置良好后,放置1~2 根负压引流管。术后6 个月以后行第二期耳廓提升术,参照3D 耳模,将第一期保留的肋软骨雕刻成底座,垫高耳廓,形成与健侧耳廓一致的耳颅角。
1.4 评价指标所有病例随访6~12 个月,平均随访8 个月,分别测量再造耳廓和健侧耳廓的长度和宽度,耳甲腔长度、宽度和深度,三角窝深度和耳颅角。见图2。测量采用同一工具,由3 名观察员进行数据测量,将再造耳廓数据与健侧耳廓数据进行比较。依据ZHANG 等[14]和BAUER[15]提出的良好再造耳廓标准制定调查问卷。术后6 个月后对76 例患者或患者家属进行满意度调查,分析患者及其家属对再造耳廓位置、大小、耳颅角、对称性和稳定性的满意度,设为非常满意、满意、尚可和不满意4 项,非常满意和满意均计为患者满意,计算患者满意率。满意率=满意患者数/患者总数×100%。
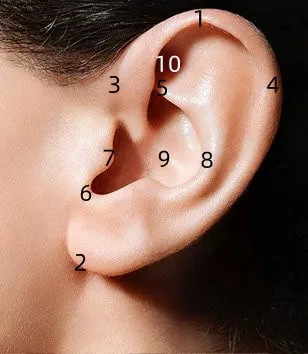
图2 耳廓测量点Fig.2 Measured sites of auricle
1.5 统计学分析采用 SPSS 19.0 统计软件进行统计学分析。再造耳廓和健侧耳廓的长度和宽度,耳甲腔长度、宽度和深度,三角窝深度和耳颅角均符合正态分布,以±s 表示,样本均数比较采用配对t检验。以P<0.05 为差异有统计学意义。
2 结 果
2.1 患者满意率术后随访76 例患者。所有再造耳廓均成活;8 例患者术后出现皮瓣尖端血运差,部分结痂,未有支架软骨外露,后经清创和局部换药后愈合;3 例患者出现术后血肿,及时发现清除血肿后,正常愈合。患者满意度调查结果显示:患者及其家属对再造耳廓的对称性满意率为85.5%,对再造耳廓大小、位置和稳定性满意率均>90%,对耳颅角的满意率为68.4%,平均满意率为87.4%。见表1。

表1 再造耳廓患者满意率Tab.1 Satisfaction rates of patients with reconstructive auricles
2.2 一般资料[病例1]患儿,男性,10 岁,右侧小耳甲腔型小耳畸形。采用Nagata 法耳廓再造术,术中采用3D 耳模辅助耳廓支架雕刻,术后各亚单位结构清晰,外形良好,患儿及其家属满意。再造耳廓和健侧耳廓长度为60.5 和60.6 mm,宽度分别为33.1 及33.2 mm。再造耳廓和健侧耳廓的耳甲腔长度、宽度和深度分别为22.6 和23.5 mm,13.5 和13.9 mm,13.8 和14.0 mm。再造耳廓和健侧耳廓的三角窝深度分别为6.5 和6.6 mm。再造耳廓和健侧耳廓耳颅角分别39°和42°。见图3。
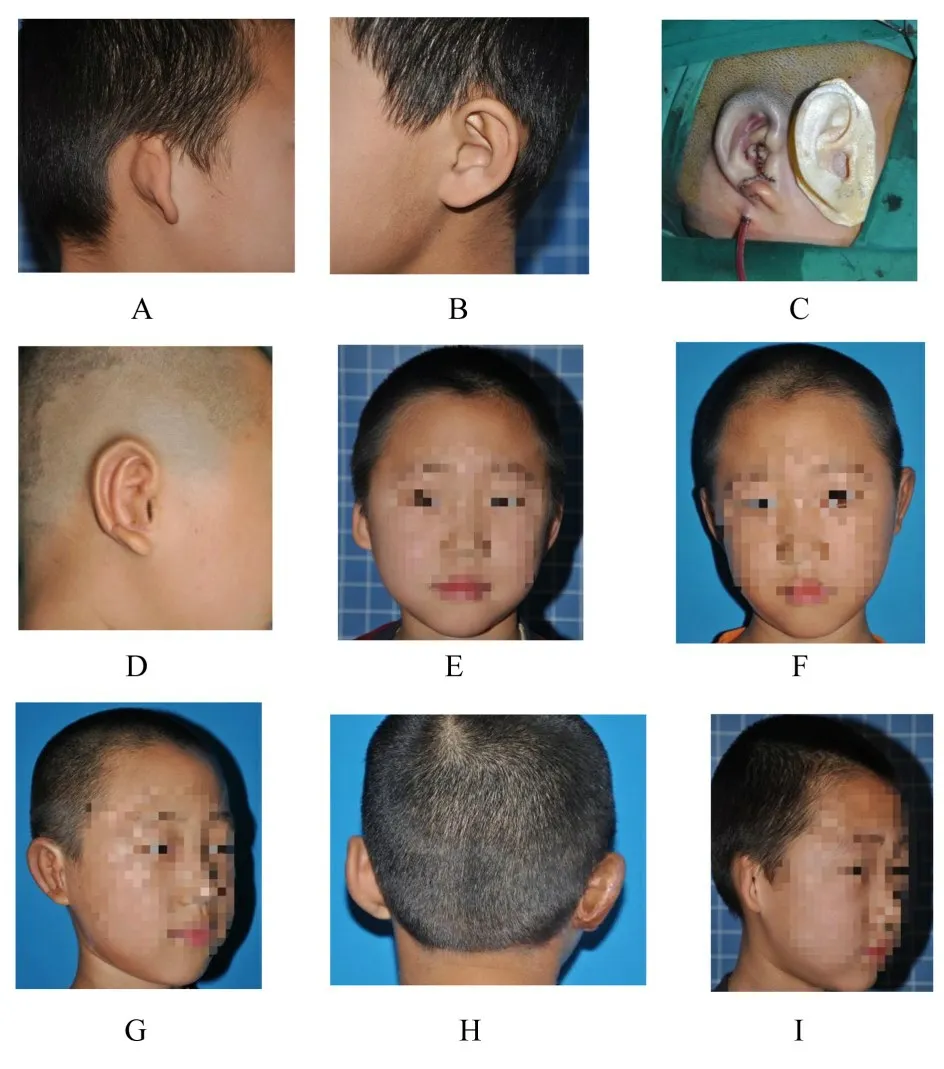
图3 3D 打印耳模治疗小耳畸形示意图(病例1)Fig.3 Sketch map of microtia treated with 3D printing auricular model(Case 1)
[病例2]患儿,女性,15 岁,右侧小耳甲腔型小耳畸形。采用Nagata 法耳廓再造术,术中采用3D 耳模辅助耳廓支架雕刻,术后耳廓外形良好,各亚单位结构清晰,尤其是耳舟、三角窝和对耳轮,患儿及其家属对再造耳廓满意度较高。再造耳廓和健侧耳廓长度为63.8 和64.0 mm,宽度分别为35.1 和35.2 mm。再造耳廓和健侧耳廓的耳甲腔长度、宽度和深度分别为23.9 和23.7 mm,14.2 和14.5 mm,14.3 和14.2 mm。再造耳廓和健侧耳廓的三角窝深度分别为6.8和6.6 mm。再造耳廓和健侧耳廓耳颅角分别44°和45°。见图4。
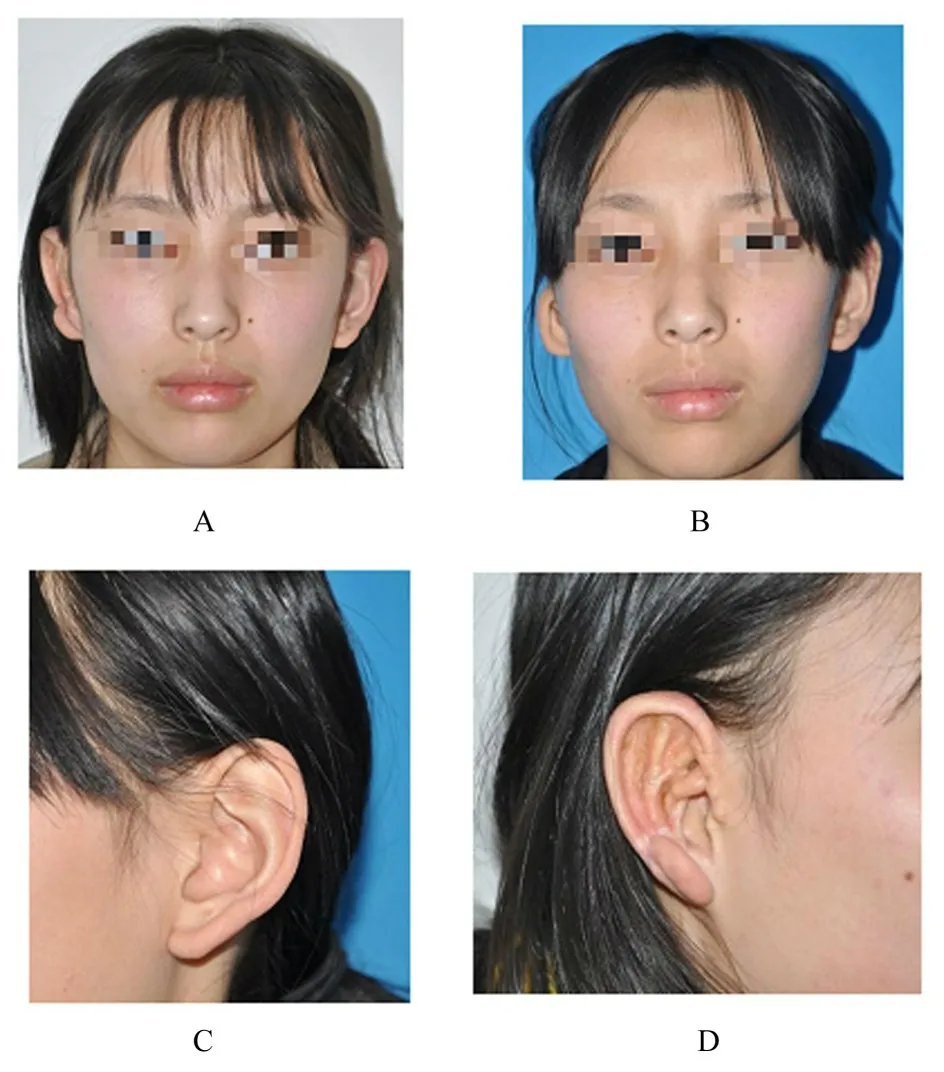
图4 3D 打印耳模治疗小耳畸形示意图(病例2)Fig.4 Sketch map of microtia treated with 3D printing auricular model(Case 2)
2.3 再造耳廓和健侧耳廓测量指标 与健侧耳廓比较,再造耳廓的长度和宽度,耳甲腔长度、宽度和深度,三角窝深度差异均无统计学意义(P>0.05)。证实再造耳廓和健侧耳廓外形相似度较高,耳廓精细结构相似度也较高。与健侧耳廓的耳颅角(38.3°±4.7°)比较,再造耳廓的耳颅角(32.5°±5.2°)缩小(P=0.014 1)。见表2。
表2 健侧耳廓和再造耳廓测量指标Tab.2 Measurment indexes of normal and reconstructive auricles (n=76,±s)
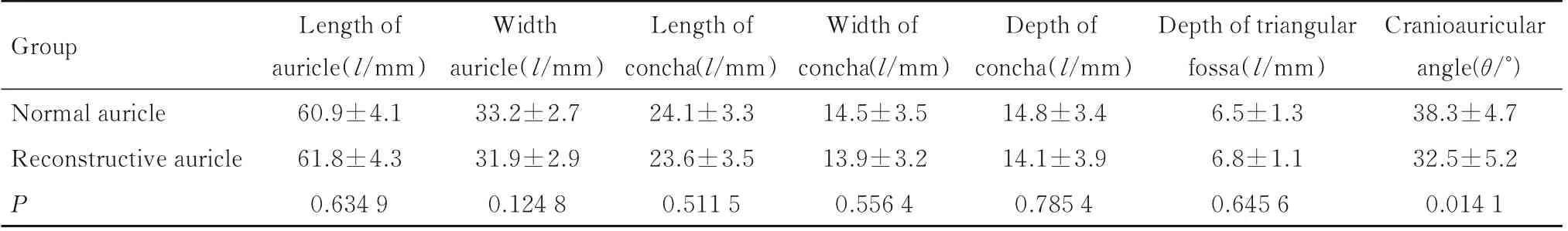
表2 健侧耳廓和再造耳廓测量指标Tab.2 Measurment indexes of normal and reconstructive auricles (n=76,±s)
Group Cranioauricular angle(θ/°)Normal auricle Reconstructive auricle P Length of auricle(l/mm)60.9±4.1 61.8±4.3 0.634 9 Width auricle(l/mm)33.2±2.7 31.9±2.9 0.124 8 Length of concha(l/mm)24.1±3.3 23.6±3.5 0.511 5 Width of concha(l/mm)14.5±3.5 13.9±3.2 0.556 4 Depth of concha(l/mm)14.8±3.4 14.1±3.9 0.785 4 Depth of triangular fossa(l/mm)6.5±1.3 6.8±1.1 0.645 6 38.3±4.7 32.5±5.2 0.014 1
3 讨 论
先天性小耳畸形发病率为0.008%~0.017%,是颌面部发病率排名第二位的先天性畸形。小耳畸形患者除存在外观上的畸形外,还伴有听力下降,部分患者会产生心理方面的障碍,累及双侧的患者甚至会导致言语发育迟缓,严重者会影响智力发育。
耳廓是体表结构最为复杂的器官,尽管其体积较小,但存在14 个解剖结构,因此耳廓再造术被认为是整形外科难度较大的手术之一,需要医生有精湛的技术和良好的艺术审美观[16-18]。再造耳廓的对称性是耳廓再造术成功的决定性因素之一,提高再造耳廓的对称性对整形医生较为重要。耳廓支架的精准成形是再造耳廓对称性的核心要素之一,耳廓支架的雕刻是参照耳模进行的。传统的耳模采用透明的X 线胶片,将胶片置于健侧耳廓上,根据健侧耳廓的形状进行临摹。这种2D 胶片耳模存在一定的局限性:制备胶片耳模的过程中,由于需要将胶片施压在耳廓表面进行临摹,压力会导致耳廓轻微变形,从而产生一定的误差;胶片耳模反映耳廓的二维大体轮廓,正常耳廓是三维立体器官,胶片耳模无法反映真实耳廓的三维解剖结构,尤其是其凹凸结构[19]。
随着科技的进步,3D 打印技术联合数字医学能够将复杂的人体器官数字化并精确打印为实物,并在许多医学领域得到了广泛应用[20]。目前,3D打印技术在整形外科领域,尤其是在小耳畸形的诊治方面应用较多。外耳再造手术中,采用3D 打印耳模可对耳支架雕刻成形进行指导,并对术后效果进行比较,3D 打印耳模可帮助再造耳廓获得更加精确和对称的美观效果[21-26]。采用生物3D 打印技术构建再生耳软骨用于耳廓重建的应用也较为广泛。美国康奈尔大学采用3D 打印技术,以患者耳廓为模板,将异种胶原质和成软骨细胞制备成高密度水凝胶,并通过打印机形成软骨框架,经培育后凝胶中的活细胞逐渐发育成为具有生物活性的耳软骨组织,外形与原始耳廓基本保持一致[27]。研究者[28-29]尝试采用杂交融合技术,将水凝胶与静电纺丝共同形成软骨支架,提高支架稳定性的同时,保证其具有一定的柔韧度,可使人成软骨细胞的生长发育不受影响。LEE 等[30]采用更为轻质的人工材料作为支架,其内填充成软骨细胞后被埋植在患者手臂皮下组织内,经过一段时间的生长,待软骨组织基本成形后,将其取出通过手术移植到患者身上。
以往大部分研究[9-11]采用3D 打印耳模作为耳廓支架雕刻的模板,仅对耳廓长度和宽度及耳颅角进行比较,然而这些指标并不能完全反映耳廓解剖亚单位的精细结构。因此本研究增加了耳甲腔的长度、宽度和深度及三角窝深度等指标,可以有效补充以往指标的不足,更能充分反映健侧耳廓与再造耳廓各解剖结构的相似性。本研究结果显示:耳廓宽度和长度,耳甲腔长度、宽度和深度及三角窝深度均与健侧耳廓各项指标接近,且组间比较差异均无统计学意义。再造耳廓的耳颅角明显缩小,可能是由于植皮区后期瘢痕挛缩,导致再造耳廓耳颅角缩小。因此可以在二期耳廓抬高术时,将耳颅角适当增加5°~10°,以便后期植皮挛缩后可达到理想对称的耳颅角。术后随访结果显示:3D 打印耳模可以精确呈现耳轮和对耳轮的走向、长短、高度、锐度和曲线变化及三角窝的深度、耳甲的深度和耳颅角等解剖结构的细节和空间构造,有利于指导医生利用肋软骨制作精细化和个性化的三维耳廓支架,从而提高再造耳廓与健侧耳廓的对称性和相似程度,使患者及其家属的满意度提高。
本研究通过术前三维肋软骨成像结合3D 打印耳模,可以充分评估所需肋软骨量,适量获取,避免浪费,因此可以最大限度地减轻切取肋软骨所导致的胸廓畸形,该畸形也是耳廓再造术后比较严重的并发症之一,这与其他研究[31]报道的结果一致。
综上所述,基于数字化3D 打印技术的3D 打印耳模可指导医生进行个性化和精准化的耳支架雕刻成形,可使再造耳廓获得良好的对称性和精美性,甚至媲美健侧耳廓,值得临床推广应用。
——护肾

