基于超高效液相色谱-四极杆飞行时间高分辨质谱联用技术的益心舒胶囊化学成分分析与鉴定
张欢,尹德录,路翔宇,苏炳新
作者单位:连云港市第一人民医院心血管内科,江苏 连云港 222000
益心舒胶囊由人参、麦冬、五味子、黄芪、丹参、川芎、山楂7 味中药组成,其中人参细粉入药,五味子、丹参85%乙醇提取入药,麦冬等4 味水煎煮入药;具有益气复脉,活血化瘀,养阴生津的功效,主要用于气阴两虚,瘀血阻脉所致的胸痹,症见胸痛胸闷、心悸气短、脉结代;冠心病心绞痛见上述证候者[1]。临床研究表明,益心舒胶囊单独用药或联合用药对持续性心房颤动、心力衰竭、心绞痛等症均有效[2-5]。益心舒胶囊现收录于2020 年版《中国药典》(一部),作为非处方药品,在心血管疾病中应用广泛。但是其相关物质基础研究薄弱,药物组成复杂,药效成分不清,进而影响了其有效的质量控制和更加广泛的临床应用。
本研究自2021 年9―12 月采用UPLC-Q-TOFMS 技术对益心舒胶囊的化学成分进行系统分析与鉴定,为其药效物质基础研究和临床应用提供参考。
1 材料与方法
1.1 药物与试剂益心舒胶囊(贵州信邦制药股份有限公司,批号20210109);人参皂苷Rg1(批号4318,纯度98.0%)、人参皂苷Rb1(批号2326,纯度98.0%)、人参皂苷Rd(批号3505,纯度98.0%)、丹参素钠(批号6716,纯度98.0%)、丹酚酸B(批号5853,纯度98.0%)、迷迭香酸(批号2886,纯度98.0%)均购自上海诗丹德生物技术有限公司;丹酚酸 A(批号O-011-170607,纯度98.0%)购自成都瑞芬思生物科技有限公司;人参皂苷Ro(批号20120805,纯度98.0%)购自上海源叶生物科技有限公司;人参皂苷Re(批号110754-200320,纯度96.0%)购自中国食品药品检定研究院。
乙腈和甲醇(色谱级,Thermo Fisher Scientific 公司)、甲酸(色谱级,阿拉丁试剂优有限公司),超纯水由纯水仪制备(Milli-Q Integral,Millipore,Bedford,USA)。
1.2 仪器Waters ACQUITY UPLC 超高效液相色谱仪(Waters,USA),Waters Synapt G2-Si Q-TOF 质谱仪(Waters,USA);超声波水浴(德国Elma P180H);电子天平(Quintix 224-1 CN-1,赛多利斯北京有限公司)。
1.3 方法
1.3.1 色谱条件色谱柱Waters Acquity HSS T3(2.1 mm×100 mm,1.8 µm);流动相0.1%甲酸(A)-乙腈(B),梯度洗脱(0~13 min,5%~70% B;13~15 min,70%~95% B;15~17 min,95% B);体积流量0.3 mL/min;柱温30 ℃;进样量2.0 µL。
1.3.2 质谱条件电喷雾离子源(ESI),正离子和负离子模式检测;采集方法:Fast DDA;扫描范围:m/z50~1 500;采集前三强母离子的二级碎片;毛细管喷雾电压离子:2.0 kV;锥孔电压:40 V;源温度:100 ℃;去溶剂气温度:450 ℃;去溶剂气流速:800 L/h,锥孔气流速:50 L/h;负离子碰撞能:低质量端能量设置为20~30 V,高质量端能量设置为60~100 V;正离子碰撞能:低质量端能量设置为10~30 V,高质量端能量设置为40~60 V。
1.3.3 溶液制备
1.3.3.1 供试品溶液精密称取益心舒胶囊粉末20 mg,置于离心管中,加入50%甲醇水溶液1 mL,超声(功率1 130 W,频率37 kHz)提取30 min,冷却至室温后,离心(14 000 r/min,10 min),取上清,即得。
1.3.3.2 对照品溶液分别精密称定对照品人参皂苷Rg1、Rb1、Re、Rd、Ro、丹参素钠、丹酚酸A、丹酚酸B、迷迭香酸各1 mg,分别置于离心管中,加入1 mL 50%甲醇使其溶解,各移取10 µL,再用50%甲醇稀释,将其制成质量浓度为10 mg/L的混标溶液。
1.4 数据分析通过文献检索,归纳总结分离自人参、麦冬、五味子、黄芪、丹参、川芎、山楂等7个益心舒胶囊组成药味的化学成分信息,建立化合物库。数据库中包括各化合物名称、结构、分子式、分子量等信息,数据库采用Progenesis SDF(Waters,USA)进行管理。采用Waters MassLynx V4.1 分析供试品溶液中化合物的保留时间、一级质谱、二级质谱等信息,一级质谱中限定质量偏差(<5 mDa),根据一级质谱推导化合物分子式,分子式输入Progenesis SDF检索自建数据库,并与对照品、文献报道数据进行比对,对化合物进行结构鉴定。
2 结果
在上述实验条件下采集益心舒胶囊的UPLCQTOF 基峰离子流图,见图1。按照“1.3”项下方法,共解析出86 个化合物,见表1。其中9 种化合物经过与对照品比对保留时间及一级、二级质谱图进行鉴定,其余化合物结合数据库及参考文献进行鉴定。
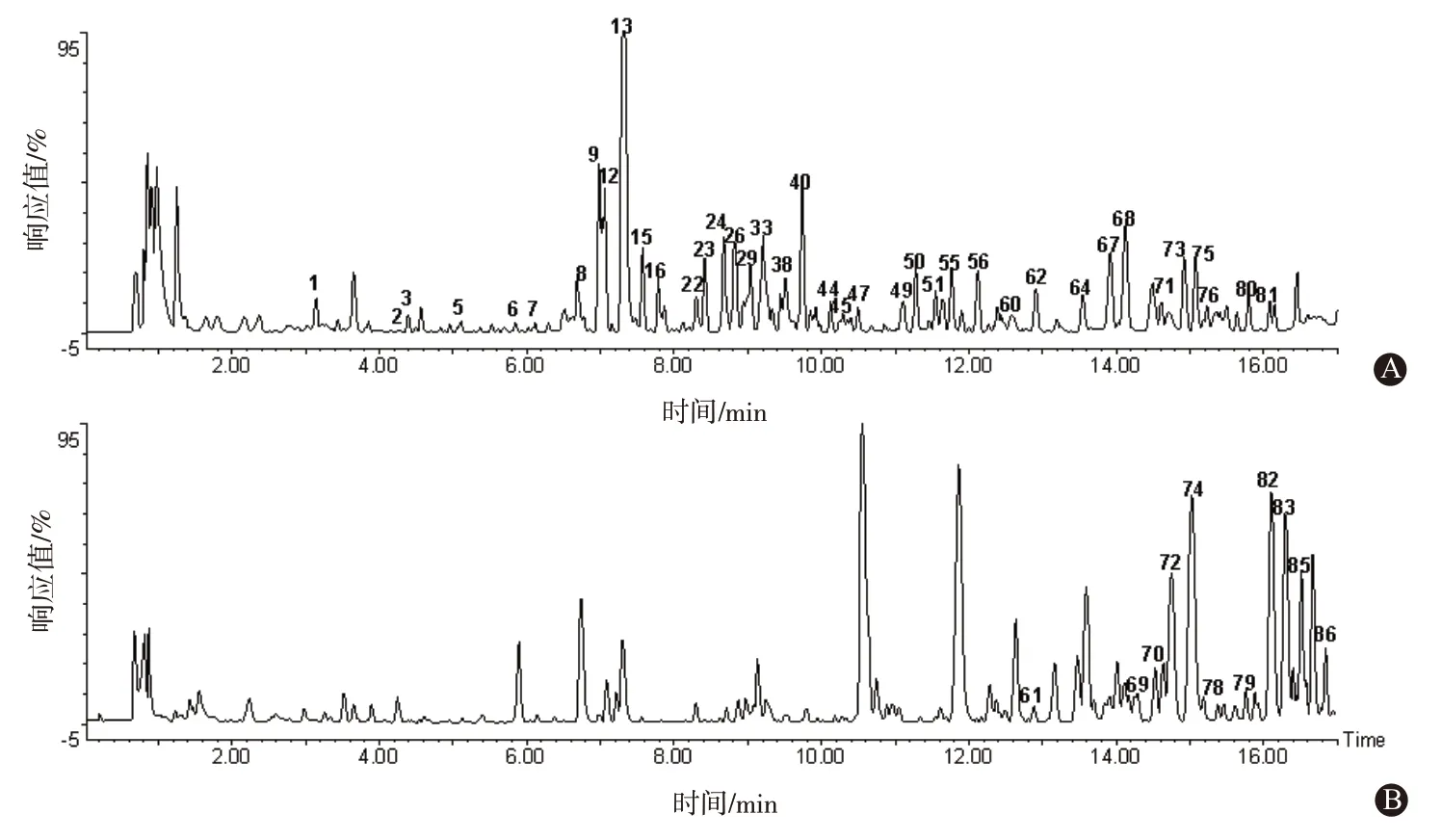
图1 益心舒胶囊正、负离子模式下基峰离子流图:A为负离子模式;B为正离子模式
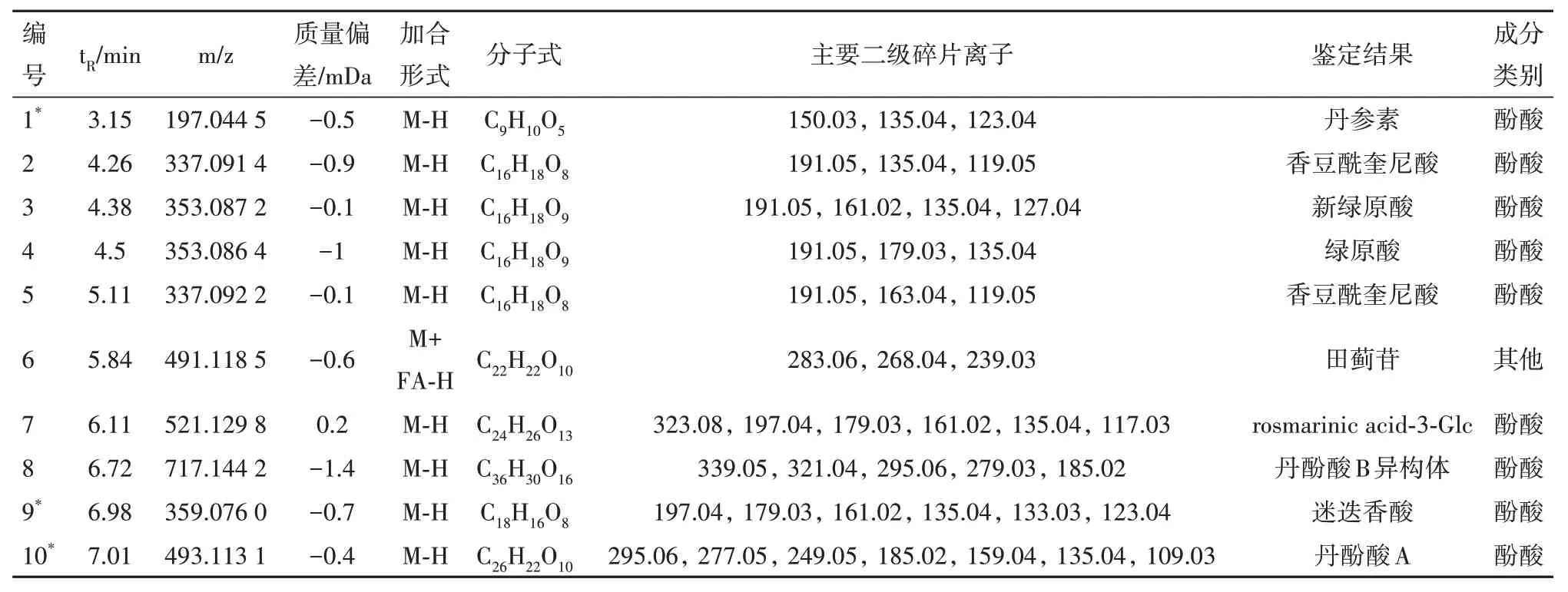
表1 益心舒胶成分鉴定结果
2.1 皂苷类化合物皂苷类成分主要来源于人参,益心舒胶囊中共鉴定了35种皂苷类化合物,包括原人参三醇型(PPT)5 个、原人参二醇型(PPD)12 个、齐墩果酸型(OA)5 个、侧链杂化型6 个以及酰化型7个。
原人参三醇型与原人参二醇型皂苷负离子模式下,大多形成甲酸加合离子,二级裂解时通常优先丢失糖配基,并获得苷元离子信息,其中原人参三醇型皂苷苷元离子为m/z475.38,原人参二醇型皂苷苷元离子为m/z459.38。中性丢失162.05 Da,146.06 Da 和132.04 Da 分别对应葡萄糖、鼠李糖和木糖/阿拉伯糖。以人参皂苷Re(化合物11)为例,一级质谱在m/z991.546 9 处得到加合离子[M+FAH]−,推导分子式为C48H82O18。二级碎片信息:m/z945.54 [M-H]−依次丢失一个葡萄糖(m/z783.49)、一个鼠李糖得到(m/z637.43)、及一个葡萄糖得到苷元离子(m/z475.38),以及苷元离子侧链断裂丢失C6H12产生(m/z391.28)。通过与对照品比对,最终确定11号峰为ginsenoside Re,其质谱裂解途径如图2 所示。化合物44 保留时间为9.73 min,在负离子模式下可见其甲酸加合离子峰m/z991.548 3 [M+FA-H]−,二级质谱可以观察到碎片离子m/z945.54,783.49,621.44,459.38,375.29,分别对应脱氢峰,以及因此丢失三个葡萄糖及苷元离子侧链断裂,因此化合物44为带有三个葡萄糖的原人参二醇型皂苷,通过检索化合物库并与文献[6]对比,化合物44 鉴定为notoginsenoside K。类似地,还鉴定了4 个原人参三醇型皂苷(化合物12,24,32,42)和10个原人参二醇型皂苷(化合物25,26,28,30,34,35,40,51,56,57)。
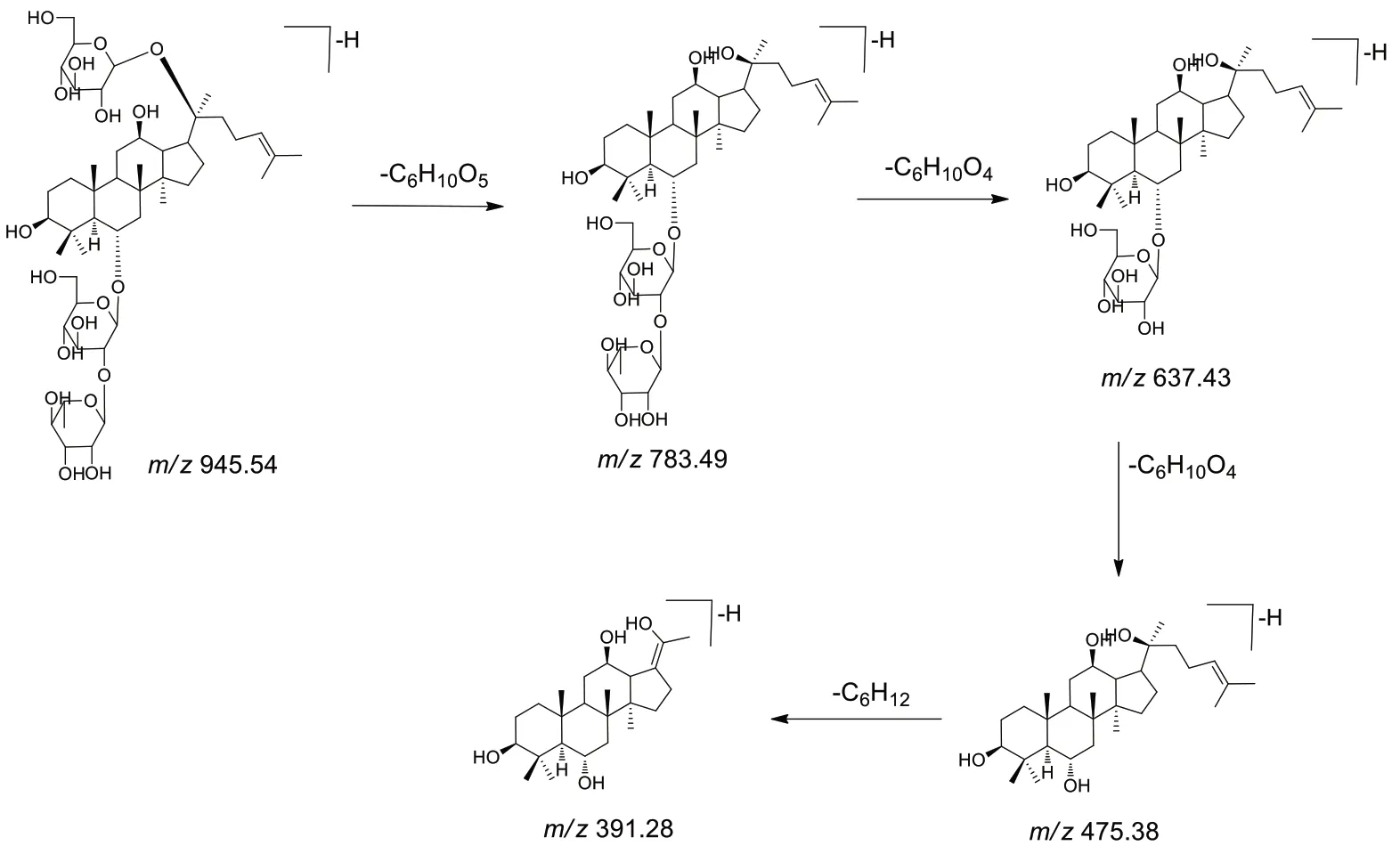
图2 ginsenoside Re负离子下的裂解途径
侧链杂化型皂苷可以通过二级质谱中苷元离子进行鉴别,如化合物49 和50 的苷元离子均为m/z457.37,相比于原人参二醇型皂苷苷元,其在苷元C-20侧链上多一个双键,结合化合物的保留顺序[7],化合物49 和50 分别鉴定为ginsenoside Rg6 和ginsen⁃oside F4。类似地根据文献报道的保留顺序[8],化合物52 和55 分别鉴定为ginsenoside Rk3 和ginsen⁃oside Rh4。
酰化皂苷根据酰化基团中是否含有羧基分别中性皂苷(乙酰化)和酸性皂苷(丙二酰化)。乙酰化取代皂苷与原人参二醇型及原人参三醇型相近,一级质谱主要观察到甲酸加合离子;丙二酰取代皂苷主要形成[M-H]−。以化合物41为例,在一级质谱图中,主要形成[M-H]−以及源内碎裂形成m/z987.55 [M-CO2-H]−,在二级碎片中观察到脱去丙二酰基的m/z945.54 [M-Mal-H]−,以及相应的脱糖碎片m/z783.48,621.44,459.38,因此化合物41 为含有三个葡萄糖基和一个丙二酰基取代的原人参二醇型皂苷,经过数据库比对鉴定为malonyl ginsenoside Rd,与文献报道基本一致[9],其质谱裂解途径如图3所示。
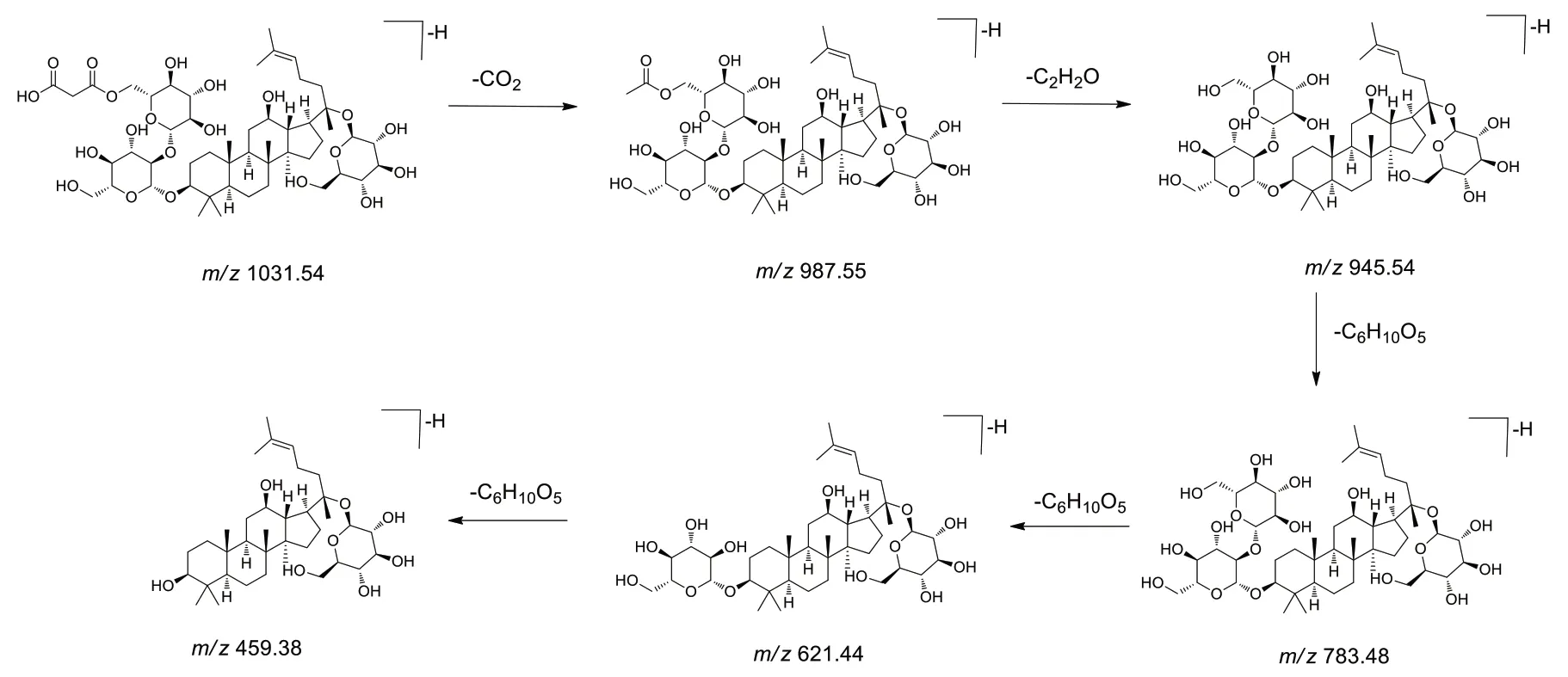
图3 malonyl ginsenoside Rd负离子下的裂解途径
齐墩果酸型皂苷可以通过苷元离子m/z455.35进行鉴定,因为齐墩果酸型皂苷大多含有葡萄糖醛酸取代,在一级质谱中通常形成[M-H]−。以人参皂苷Ro(化合物33)为例,一级质谱在m/z955.4893 观察到准分子离子峰[M-H]-。二级质谱中可以检测到碎片离子m/z793.44,613.37,569.38,469.38,455.35,由脱糖和二氧化碳等产生,通过与对照品比对,最终确定化合物33 为人参皂苷Ro,其质谱裂解途径如图4所示。
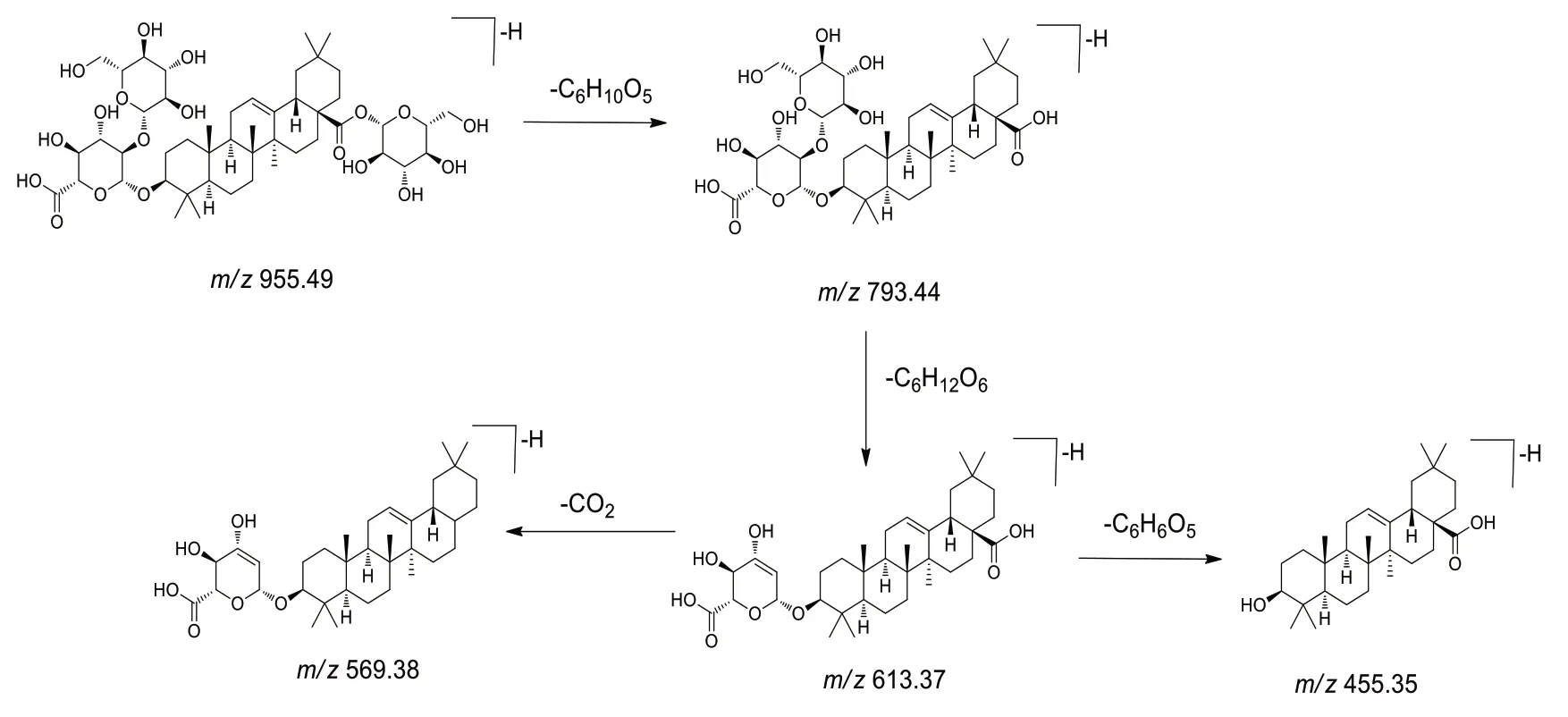
图4 ginsenoside Ro负离子下的裂解途径
2.2 酚酸类化合物酚酸类成分主要为来源于丹参的丹酚酸类化合物,丹酚酸类化合物根据结构类型可以分为单聚体和多聚体(二聚体、三聚体和四聚体),多聚体由多个单聚体通过酯键或者醚键聚合。丹参素(化合物1)为单聚体丹酚酸类成分,其[M-H]-准分子离子峰为m/z197.0443,碎裂主要产生丢失水分子和CO2产生m/z135.04,丹参素通过与对照品比对进行鉴定。化合物9 的母离子为m/z359.076 0,分子式推导为C18H16O8,二级碎片中检测到与丹参素一致的碎片信息(m/z197.04,135.04,123.04),推定为由丹参素组成的二聚体型丹酚酸类化合物,通过数据库检索及对照品比对鉴定为迷迭香酸,其质谱裂解途径如图5 所示。化合物1 由一级质谱图可知,其[M-H]−准分子离子峰为m/z717.144 7,在二级质谱中主要检测到m/z321.04 的碎片及相关离子,其由酯键断裂丢失两个C9H10O5生成,通过对照品比对,化合物1鉴定为丹酚酸B。

图5 迷迭香酸负离子下的裂解途径
2.3 二萜类化合物本品共鉴定二萜类化合物20个,主要为来源于丹参中的二萜醌类化合物及其衍生物。以化合物64为例,正离子模式下拟合分子式为C18H14O3,二级质谱中碎片离子m/z261.09,233.10,205.10,190.08,169.06,141.07,分别对应为[M+H-H2O]+,[M+H-H2O-CO]+,[M+H-H2O-2CO]+,[M+H-CO-C5H6O]+,[M+H-2CO-C5H6O]+,与文献报道二氢丹参酮Ⅰ碎裂行为基本一致[10],由此,推测化合物64 为二氢丹参酮Ⅰ,其质谱裂解途径见图6。
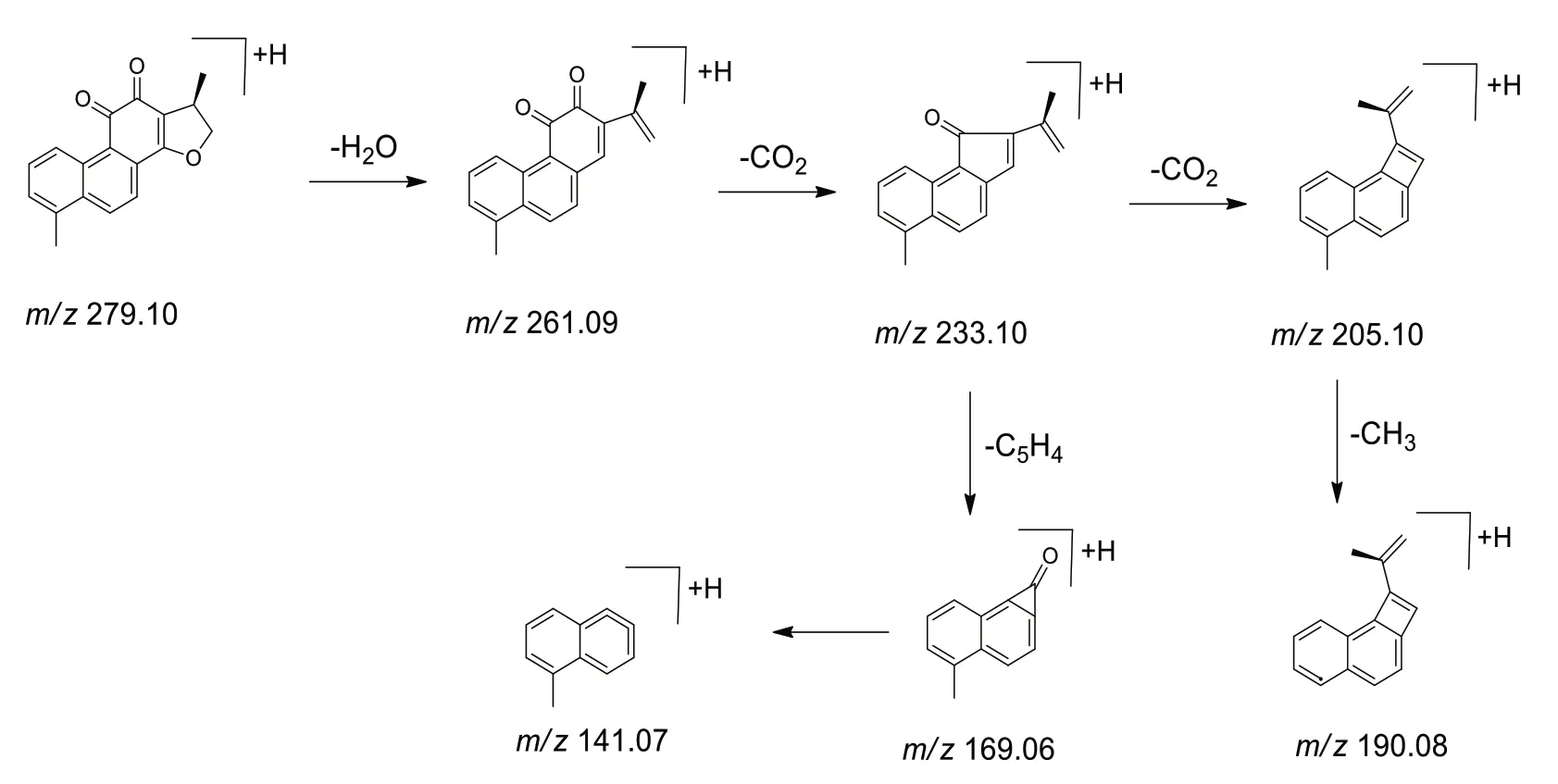
图6 二氢丹参酮I正离子下的裂解途径
2.4 木脂素类化合物本品共鉴定9 个木脂素类化合物,以化合物84 为例,正离子模式下拟合分子式为C23H28O6,二级质谱中碎片离子m/z386.17,370.18,355.15,331.12,316.09,300.10,285.08 分别对应为[M+H-CH3]+,[M+H-OCH3]+,[M+H-CH3-OCH3]+,[M+H-C5H10]+,[M+H-CH3-C5H10]+,[M+HOCH3-C5H10]+,[M+H-OCH3-CH3-C5H10]+,与文献报道五味子乙素碎裂行为基本一致[11],由此,推测化合物84为五味子乙素,其质谱理解途径见图7。

图7 五味子乙素正离子下的裂解途径
2.5 其他除上述化学成分外,本品还检测到黄酮类如田蓟苷、黄芪异黄烷苷、芹菜素-7-O-β-D-吡喃葡萄糖苷、3'-甲氧基大豆黄素,及bornyl 7-O-α-Larabinofuranosyl-(1→6)-β-D-glucopyranoside 与积雪草酸。具体结果见表1。
3 讨论
中药复方制剂对一些疑难病症疗效显著,然而这些中药制剂成分复杂、作用机制不清,不利于临床广泛应用。中药复方制剂的化学物质基础研究是有效性、安全性和质量控制的前提[12-13]。液相色谱串联高分辨质谱具有准确、灵敏、快速等优势,适用于中药复方制剂的化学物质基础研究。本研究将UPLC-QTOF-MS 应用于临床常用复方益心舒胶囊的化学成分分析,最终确定了86个成分。
检测到的成分主要为皂苷类、酚酸类、二萜类及木质素类,主要来源于人参、丹参、五味子等三味药材,可能与益心舒胶囊中各药味入药方式有关。粉末入药的人参及经过乙醇提取五味子、丹参中以次级代谢物为主,而麦冬、黄芪、川芎、山楂等4味药为水煎煮提取,低极性的次级代谢物含量低难以检测。2020 年版《中国药典》(一部)分别以人参皂苷Rg1 和人参皂苷Re、丹酚酸B 为指标对人参和丹参进行质量控制。文献报道[14],五味子甲素和五味子乙素是益心舒胶囊治疗心力衰竭的关键活性成分,他们可以通过减弱内皮素-1 诱导的收缩功能障碍、脑钠肽含量升高和人诱导多能干细胞衍生心肌细胞形态学变化发挥治疗作用。因此,在益心舒胶囊的质量控制中可以进一步考虑对药味五味子的质量控制。
本研究开展了益心舒胶囊的化学物质基础研究,值得注意的是,化学成分并不同等于药效成分。只有吸收入血的成分才可能是发挥药效的直接物质,因此后期还需要进一步开展益心舒胶囊的药代及药动学研究,以及入血成分的活性评价以及分子机制研究,以期更加全面地阐释益心舒胶囊的作用机制。

