养血安神片质量评价方法研究*
杨美丽,张少杰,杨金蕊,王 楠,潘炫屹,付萍萍,徐 彬
(1. 河北省保定市食品药品检验所,河北 保定 071000; 2. 河北大学附属医院,河北 保定 071000)
药品评价研究工作通过标准检验、探索性研究、相关数据分析等手段对药品的质量进行全面分析与评价,给出正确结论[1],旨在促进药品质量的提升,保障人民用药安全。近年来,随着社会压力的不断加大,失眠的发病率呈明显上升趋势。养血安神片由仙鹤草、墨旱莲、鸡血藤、熟地黄、地黄、合欢皮、首乌藤7 味中药组方,临床疗效好,价格低廉,市场占有率很高。其现行质量标准收载于《中华人民共和国卫生部药品标准·中药成方制剂(第六册)》,仅有性状和检查项,真伪优劣不易评判,标准可控性差。为考察该药的整体质量,确保人民用药安全、有效,为行政监管提供技术支持,课题组对其开展质量评价工作,且收集了执行该部颁标准的10 家生产企业的共16 批样品,基于“点-线-面”的全方质量评价模式[2]开展质量评价工作,在法定检验基础上开展了薄层色谱鉴别[3-5]、含量测定[6-8]、指纹图谱鉴定[9-16]、显微检查[17]等探索性研究,进行了样品测定及质量分析评价,以期能促进药品质量的提升。现报道如下。
1 仪器与试药
1.1 仪器
DIONEX Ultimate 3000 型液相色谱仪(赛默飞世尔科技<中国>有限公司),配有二极管阵列检测器;Agilent 1260 型高效液相色谱仪(安捷伦科技<中国>有限公司),配有紫外检测器;Sartorius CPA 225D 型电子天平(德国赛多利斯集团,精度为万分之一/十万分之一);SK7200H 型超声波清洗器(上海科导超声仪器有限公司,功率为350 W,频率为53 kHz);Olympus BX50 型显微镜(奥林巴斯<中国>有限公司)。
1.2 试药
2,3,5,4′ - 四羟基二苯乙烯- 2 -O-β-D- 葡萄糖苷对照品(简称二苯乙烯苷,批号为110844 -202116,含量为94.8%),没食子酸对照品(批号为110831-201906,含量为91.5%),原儿茶酸对照品(批号为110809 - 201906,含量为97.7%),绿原酸对照品(批号为110753-202119,含量为96.3%),旱莲苷A 对照品(批号为111886-201804),大黄素对照品(批号为110756 - 201913,含量为96.0%),大黄素甲醚对照品(批号为110758-201817,含量为99.2%),熟地黄对照药材(批号为121196-202007),墨旱莲对照药材(批号为120958-201708),首乌藤对照药材(批号为120939-201908),均购于中国食品药品检定研究院;乙腈为色谱纯,甲酸、甲醇均为分析纯,水为娃哈哈饮用纯净水;仙鹤草、墨旱莲、鸡血藤、熟地黄、地黄、合欢皮、首乌藤饮片(市售),经河北省保定市食品药品检验所杨美丽高级工程师鉴定均为正品;养血安神片(共16批,编号为1-16,购于河北省内6个市县,涉及10家生产企业)。
2 方法与结果
2.1 薄层色谱鉴别[3-5]
溶液制备:取样品10 片,除去包衣,研细,加水30 mL,加热煮沸10 min,放冷,离心,取上清液,加乙酸乙酯并振摇提取2 次,每次20 mL,合并乙酸乙酯提取液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。取熟地黄对照药材2 g、墨旱莲对照药材2 g、首乌藤对照药材1.5 g,分别加水40 mL,煎煮30 min,放冷,离心,取上清液,加乙酸乙酯并振摇提取2 次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加甲醇1 mL 使溶解,作为对照药材溶液。取旱莲苷A 对照品,加甲醇制成每1 mL 含1 mg 的溶液,作为对照品溶液Ⅰ。取大黄素对照品、大黄素甲醚对照品,加甲醇制成每1 mL 各含0.2 mg 的溶液,作为对照品溶液Ⅱ和对照品溶液Ⅲ。按处方工艺分别制备缺熟地黄、墨旱莲、首乌藤的阴性样品,并按供试品溶液制备方法制备阴性对照品溶液。
熟地黄:吸取供试品溶液5~15 μL,熟地黄对照药材溶液、缺熟地黄的阴性对照品溶液各5 μL,分别点于同一硅胶G 薄层板上,以石油醚(60~90 ℃)- 乙酸乙酯(1∶1,V/V)为展开剂,展开,取出,晾干,喷以二硝基苯肼乙醇试液,置日光下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置显相同颜色的斑点,且阴性对照无干扰。色谱图见图1 A。

1,1′. 对照药材溶液 2 - 9. 供试品溶液 10. 阴性对照品溶液(分别缺熟地黄、墨旱莲、首乌藤) 11,11′. 对照品溶液A. 熟地黄(日光) B. 墨旱莲 C. 首乌藤(365 nm)图1 薄层色谱图1,1′.Reference medicinal material solution 2-9.Test solution 10.Negative reference solution((lacking Rehmanniae Radix Praeparata,Ecliptae Herbs,and Polygoni Multiflori Caulis,respectively) 11,11′.Reference solutionA.Rehmanniae Radix Praeparata(sunlight) B.Ecliptae Herbs C.Polygoni Multiflori Caulis(365 nm)Fig.1 TLC chromatograms
墨旱莲:吸取供试品溶液、墨旱莲对照药材溶液、对照品溶液Ⅰ、缺墨旱莲的阴性对照品溶液各10 μL,分别点于同一硅胶G 薄层板上,以二氯甲烷- 乙酸乙酯- 甲醇- 水(30∶40∶15∶3,V/V/V/V)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,105 ℃加热至斑点显色清晰。供试品溶液色谱中,在与对照药材溶液和对照品溶液色谱相应位置显相同颜色的斑点,且阴性对照无干扰。色谱图见图1 B。
首乌藤:吸取供试品溶液5~10 μL,首乌藤对照药材溶液、缺首乌藤的阴性对照品溶液、对照品溶液Ⅱ、对照品溶液Ⅲ各5 μL,分别点于同一硅胶G 薄层板上,以正己烷- 乙酸乙酯- 甲酸(12∶3∶0.1,V/V/V)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液和对照品溶液色谱相应位置显相同的黄色荧光斑点,且阴性对照无干扰。色谱图见图1 C。
2.2 含量测定[6-8]
2.2.1 色谱条件
色谱柱:Shiseido CAPCELL PAK C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈- 水溶液(17∶83,V/V);流速:10 mL/min;检测波长:320 nm;柱温:30 ℃;进样量:10 μL。
2.2.2 溶液制备
取二苯乙烯苷对照品适量,精密称定,加80%甲醇制成质量浓度为0.1 mg/mL 的溶液,即得对照品溶液。取样品20 片,除去糖衣,研细,取1.0 g,精密称定,置具塞锥形瓶中,精密加入80%甲醇25 mL,称定质量,超声提取(功率为250 W,频率为40 kHz)30 min,放冷,再称定质量,加80%甲醇补足减失的质量,摇匀,用0.45 μm滤膜滤过,取续滤液,即得供试品溶液。按处方工艺制备不含首乌藤的阴性样品,按供试品溶液制备方法制备阴性对照品溶液。
2.2.3 方法学考察
专属性试验:取2.2.2 项下供试品溶液、对照品溶液、阴性对照品溶液及空白溶剂(80%甲醇)各适量,按2.2.1 项下色谱条件进样测定,记录色谱图。供试品溶液色谱中,在与对照品溶液色谱相同保留时间处有相应色谱峰出现,且阴性对照无干扰。色谱图见图2。
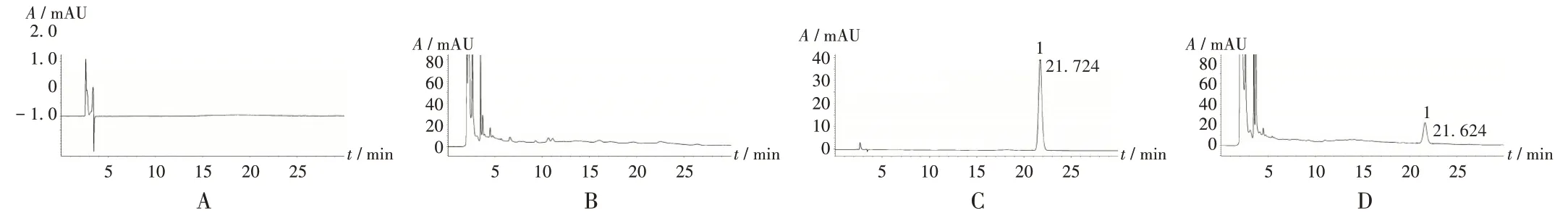
1.2,3,5,4′ - 四羟基二苯乙烯- 2 - O - β - D葡萄糖苷A. 空白溶剂 B. 阴性对照品溶液 C. 对照品溶液 D. 供试品溶液图2 高效液相色谱图1.2,3,5,4′-tetrahydroxy stilbene - 2 - O - β - D - glucosideA.Blank solvent B.Negative reference solution C.Reference solution D.Test solutionFig.2 HPLC chromatograms
线性关系考察:取二苯乙烯苷对照品0.010 50 g,精密称定,加80%甲醇溶解并定容,作为对照品贮备液;精密量取对照品贮备液1,1,2 mL,分别置25,10,10 mL 容量瓶中,加80%甲醇溶解并定容,作为对照品溶液A,B,C;分别精密吸取对照品贮备液3,5,10 μL及对照品溶液A,B,C 各10 μL,按2.2.1 项下色谱条件进样测定,以进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y= 3 411X- 11.98,r=0.999 0(n=6)。结果表明,二苯乙烯苷进样量在0.039 3~0.982 8 μg范围内与峰面积线性关系良好。
检测限与定量限确定:取2.2.2项下对照品溶液适量,加80%甲醇逐级稀释,分别以信噪比(S/N)为10和3的进样量为定量限和检测限。结果定量限为0.001 3 μg,检测限为0.000 4 μg。
精密度试验:精密吸取线性关系考察对照品贮备液5 μL,按2.2.1 项下色谱条件进样测定6 次,记录峰面积。结果二苯乙烯苷峰面积的RSD为0.41%(n=6),表明仪器精密度良好。
稳定性试验:取样品适量,精密称定,按2.2.2项下方法制备供试品溶液,分别于0,4,8,12,20,24 h 时按2.2.1 项下色谱条件进样测定,记录峰面积。结果峰面积的RSD为1.02%(n= 6),表明供试品溶液在24 h 内稳定性良好。
重复性试验:取样品适量,精密称定,共7 份,按2.2.2 项下方法制备供试品溶液,按2.2.1 项下色谱条件进样测定,记录峰面积,并计算含量。结果二苯乙烯苷含量的RSD为1.29%(n=7),表明方法重复性良好。
加样回收试验:取已知含量的样品(0.351 4 mg/g)0.5 g,精密称定,共6 份,精密加入对照品溶液(取二苯乙烯苷0.010 77 g,精密称定,置200 mL 容量瓶中,加80%甲醇溶解并定容,摇匀)5 mL,依法制备供试品溶液,按2.2.1项下色谱条件进样测定,记录峰面积,并计算加样回收率。结果见表1。

表1 加样回收试验结果(n=6)Tab.1 Results of the recovery test(n=6)
2.2.4 样品含量测定
取16 批(编号为1-16)样品,按2.2.2 项下方法制备供试品溶液,按2.2.1 项下色谱条件进样测定,记录峰面积,并计算含量。结果样品中二苯乙烯苷含量为每片0.06~0.57 mg,提示样品间一致性较差;仅9批样品含量测定结果相对集中,为每片0.10~0.20 mg;有4批样品含量测定结果偏低(每片低于0.10 mg),提示首乌藤的质量较差,或存在投料不足的嫌疑。详见表2。
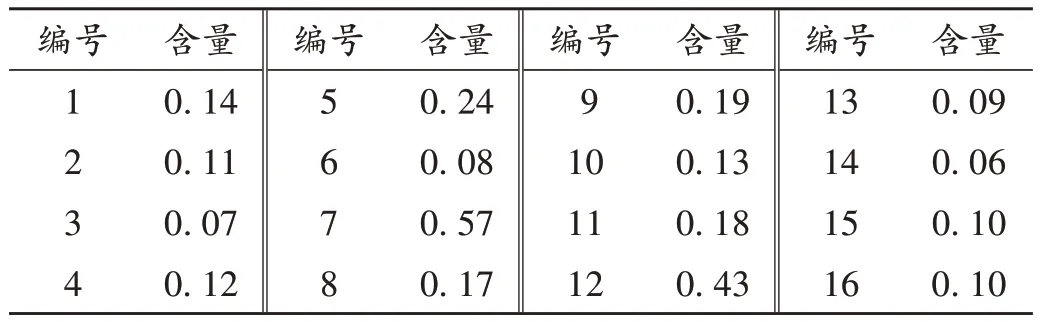
表2 样品中2,3,5,4′-四羟基二苯乙烯-2-O-β-D葡萄糖苷含量测定结果(mg/片)Tab.2 Results of the content determination of 2,3,5,4′-tetrahydroxy stilbene-2-O-β-D-glucoside in samples(mg/tablet)
2.3 指纹图谱鉴定[9-16]
2.3.1 色谱条件
色谱柱:Shiseido CAPCELL PAK C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈(A)-0.1%甲酸水溶液(B),梯度洗脱(0~10 min 时2%A,10~33 min 时2%A →19%A,33~50 min 时19%A →26%A,50~60 min 时26%A →40%A,60~65 min时40%A);流速:1.0 mL/min;检测波长:280 nm(0~28 min),320 nm(28~52 min),280 nm(52~75 min);柱温:30 ℃;进样量:10 μL。
2.3.2 溶液制备
取二苯乙烯苷、没食子酸、原儿茶酸、绿原酸对照品各适量,精密称定,加80%甲醇溶解,制成每1 mL 含0.1 mg 的单一对照品溶液及混合对照品溶液。按2.2.2项下方法制备供试品溶液。按处方工艺取各单一药材适量(相当于成药4片的量),按处方工艺分别制备单一样品,按供试品溶液制备方法制备单一药材溶液。
2.3.3 方法学考察
精密度试验:取2.3.2 项下供试品溶液适量,按2.3.1项下色谱条件连续进样测定6次,记录色谱图。以9 号峰(二苯乙烯苷峰)为参照峰,结果色谱图中1-16号峰相对保留时间和相对峰面积的RSD均低于5.00%(n=6),表明仪器精密度良好。
稳定性试验:取2.3.2 项下供试品溶液适量,分别于0,2.5,5.0,7.5,10.0,15.0,20.0,24.0 h 时按2.3.1项下色谱条件进样测定,记录色谱图。以9号峰(二苯乙烯苷峰)为参照峰,结果色谱图中1-16 号峰相对保留时间和相对峰面积的RSD均低于5.00%(n= 8),表明供试品溶液24 h内稳定性良好。
重复性试验:取样品6 份,按2.3.2 项下方法制备供试品溶液,按2.3.1 项下色谱条件进样测定,记录色谱图。以9 号峰(二苯乙烯苷峰)为参照峰,结果色谱图中1-16 号峰相对保留时间和相对峰面积的RSD均低于5.00%(n=6),表明方法重复性良好。
2.3.4 共有峰及主要色谱峰指认
取16 批(编号为1 - 16)样品,依法制备供试品溶液,按2.3.1 项下色谱条件进样测定,色谱图见图3A。依据测定结果,确定13 个共有峰(8 号峰、10 号峰、12 号峰除外)作为特征峰。
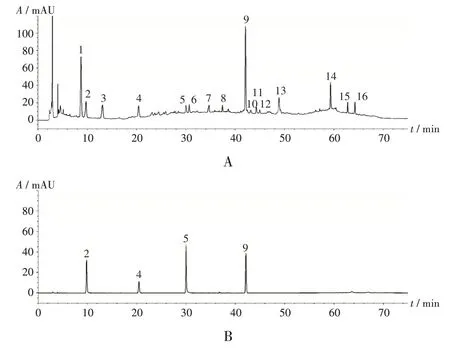
2. 没食子酸 4. 原儿茶酸 5. 绿原酸 9.2,3,5,4′ - 四羟基二苯乙烯- 2 - O - β - D - 葡萄糖苷A. 供试品溶液 B. 混合对照品溶液图3 高效液相色谱图2.Gallic acid 4.Protocatechuic acid 5.Chlorogenic acid 9.2,3,5,4′-tetrahydroxy stilbene-2-O-β-D-glucosideA.Test solution B.Mixed reference solutionFig.3 HPLC chromatograms
分别取2.3.2项下单一对照品溶液各适量,并进样测定,比较色谱峰的保留时间及紫外光谱结果,确定2号峰、4号峰、5号峰、9号峰分别为没食子酸、原儿茶酸、绿原酸、二苯乙烯苷。色谱图见图3 B。结合单一药材溶液在相同条件下的测定图谱及色谱峰的紫外吸收光谱,确认1-3号峰为地黄及熟地黄的特征峰,9号峰为首乌藤的特征峰,13号峰、14号峰主要来源于仙鹤草,4-8号峰为多药味(首乌藤、鸡血藤、墨旱莲等)的共有成分。
2.3.5 指纹图谱测定及相似度评价
对16 批样品进行指纹图谱测定,以9 号峰为参照峰,各峰相对保留时间的RSD均低于5.00%。采用国家药典委员会主持开发的中药色谱指纹图谱相似度评价软件2012A版生成标准谱图,分别对样品与标准谱图进行多点校正、Mark峰匹配,并计算相似度。结果见表3。

表3 样品相似度计算结果Tab.3 Similarity of samples
2.3.6 聚类分析
采用SPSS 18.0 统计学软件中系统聚类法的Ward法,选取平方Euclidean 距离为度量标准,对所测样品与标准谱图的相似度进行系统聚类分析,结果按相似度大小将样品分为五小类。相似度在0.90以上及以下的分别聚为两大类,组间距离最大;2批(编号为6,14)样品的相似度低于0.80,单独聚为一小类,离群明显。详见图4。
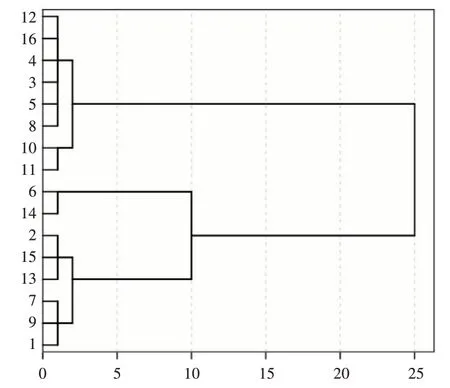
图4 16批样品聚类分析结果Fig.4 Results of the cluster analysis of 16 batches of samples
2.4 显微检查异性有机物
药材被粉碎后的组织细胞特征或内含物依然保留,这是中成药显微鉴定的基础[17]。采用显微检查法筛查制剂中的异性有机物,考察是否存在投料不足、不按工艺生产、非法投料等问题。显微检查结果如下:1)养血安神片为半浸膏制剂,部分首乌藤以原粉入药,显微镜下应仅可见首乌藤的组织特征,若其他药味的专属组织特征有一定镜检率,则提示生产工艺存在问题。16 批样品均能检出首乌藤显微特征,提示无企业为省去首乌藤粉碎工序而将所有药味一起提取制剂。2)1 批样品地黄或熟地黄薄壁组织特征及仙鹤草非腺毛组织特征镜检率较高,1 批样品仙鹤草非腺毛组织特征镜检率较高,提示有地黄、熟地黄及仙鹤草原粉入药。3)2 批样品淀粉粒甚多,且粉末颜色偏浅,提示提取出膏量可能偏少,添加了较多辅料才能按标准每片芯0.25 g 进行压片,存在投料不足或工艺不合理等嫌疑。指纹图谱显示,上述2 批样品多种成分含量较低,与该项检验结果具有相关性。可见,16 批样品中有4 批样品的显微特征提示生产工艺存在问题,应引起重视。
2.5 安全性考察
参考原国家食品药品监督管理局批准的药品检验补充检验方法和检验项目批准件2009024,2012004,2013002,筛查样品中是否添加艾司唑仑、阿普唑仑、三唑仑、劳拉西泮、硝西泮、地西泮、苯巴比妥、异戊巴比妥、延胡索乙素(罗通定)、青藤碱及氯苯那敏11种化学成分。结果16批样品中均未检出相应成分,不存在非法添加的情况。
3 讨论
3.1 薄层色谱鉴别
由图1 可知,薄层色谱图中斑点虽均有检出,但不同厂家斑点强弱不同,5 批样品增大点样量也仅是略显,提示单药味质量差异较大,存在以次充好投料、少投料、不按工艺生产等嫌疑。
仙鹤草为蔷薇科植物龙芽草的干燥地上部分,主要含有黄酮、三萜、异香豆素、有机酸类成分[13]。其相关研究多以黄酮类成分为主,但黄酮类成分并非仙鹤草的专属性成分,含量较低,且产地、采收加工等因素对药材的含量影响较大,不利于质量控制[18-19]。方中,仙鹤草经水煮浓缩入药,在尝试对仙鹤草进行薄层色谱鉴别时,采用水提醇沉及70%乙醇直接超声提取2种方法,再用乙醚萃取除杂,正丁醇萃取浓缩的方式净化样品,分别采用硅胶G 薄层板,聚酰胺薄膜经多种展开系统展开,但仙鹤草对照药材斑点较多,阴性干扰严重,经多次调整仍不理想,故未能建立仙鹤草的专属薄层鉴别方法。鸡血藤亦因阴性干扰未制订适宜的方法。
3.2 含量测定
在方法的建立过程中发现,样品中二苯乙烯苷的含量显著高于其他组分的特征成分,由于指纹图谱中大部分样品色谱图中没食子酸、原儿茶酸、绿原酸的色谱峰峰高及峰面积均较小,相对二苯乙烯苷峰含量低很多,为保证方法的准确性,尤其是低浓度成分的准确性,指纹图谱测定时未进行多成分的含量测定,仅以流动相乙腈- 水溶液测定二苯乙烯苷,该体系下检出干扰成分少,分析时间短,专属性更强,且方法学考察符合要求。经测定,16 批样品每片含二苯乙烯苷0.06~0.57 mg,相差近10倍,4批含量低于每片0.10 mg,初步推测部分企业可能存在首乌藤饮片质量较差或投料不足的嫌疑,提示应制订相关限度。
3.3 指纹图谱
参考2020 年版《中国药典(一部)》,地黄、合欢皮、墨旱莲等药材均采用低波长测定相关成分含量,但养血安神片在低波长处的色谱图基线漂移严重。采用二极管阵列检测器进行全波长扫描,发现低波长附近成分异常复杂,无法理想分离,且含量低的成分采集效果很差。3D 光谱图显示,280 nm 及320 nm 波长附近均有较理想的紫外吸收峰,为使指纹图谱中呈现较多色谱信息且响应值适宜,最终采用280 nm →320 nm →280 nm的切换波长法测定。
相似度测定结果显示,1)16 批样品的相似度为0.771~0.985,发现部分企业的样品离散较远。通过色谱图对比,发现这些企业的样品的色谱图差异性较大,如编号为6 和14 样品的相似度均低于0.80,聚类分析也将其聚为一类。指纹图谱显示,18~50 min 范围内色谱峰个数和峰面积与标准谱图均有较大差异,尤其是9 号峰及13 号峰,表明样品的化学成分差异较大。峰面积小或缺失,提示存在多药味少投或用不合格品替代投料等嫌疑,质量较差。2)相似度在0.80~0.90之间的样品,查看色谱图发现,9 号峰和13 号峰对相似度的贡献较大,其次为1-3 号峰,该区间的样品地黄、熟地黄特征峰与首乌藤特征峰的大小呈现不规律变化,任何药味特征峰明显低于标准谱图均能降低相似度,提示地黄、熟地黄或首乌藤可能存在少投或用不合格品替代投料等嫌疑,质量一般。3)相似度高于0.90 的样品,质量较好。4)供试品溶液的颜色与色谱图也具有一定相关性。颜色浅,色谱图中1-3 号峰的峰面积均较小,指纹图谱相似度低,提示地黄及熟地黄存在不按规定投料的嫌疑。研究中,按处方工艺自制1 份样品平行测定进行验证,溶液颜色较深,指纹图谱与参照图谱相似度为0.966,与样品预期测定结果基本一致。本研究中的样品依据现有质量标准均为合格样品,但指纹图谱体现的差异性表明所建立的指纹图谱更能反映样品的真实性,为其质量控制提供了更有效的技术方法。
3.4 显微鉴别
显微鉴别结果显示,16 批样品中,有4 批样品存在不按工艺生产、饮片未经提取而直接以原粉入药等嫌疑。鉴别用供试品溶液制备时,先经水煮10 min,16 批样品水煮后有2 批呈黏稠状,与其他样品区别明显,推测淀粉类辅料添加量较多,这与植物组织显微筛查中同批样品显微镜下淀粉粒多证据指向相同。指纹图谱显示,上述2 批样品各成分含量相对较低。样品性状按标准应为除去糖衣后显黑棕色,但颜色明显较浅,与标准有一定差异。辅料添加量大,提示工艺中浓缩得到的稠膏量少,存在不按规定投料、以次充好投料、不按工艺生产等多种嫌疑。
方中首乌藤部分以原粉入药,显微镜下草酸钙簇晶特征明显,但方中仙鹤草也含有较多草酸钙簇晶且大小与首乌藤有交叉。若企业不按工艺提取而直接用仙鹤草原粉入药,专属性鉴别不理想,易造成误判,故未制订显微鉴别项。
3.5 方法评价
本研究中建立的方法准确、可靠,可用于养血安神片的质量控制及评价,为其规范生产、质量标准提升提供了有效的技术方法与支持。

